文档内容
素养说明:运用题给陌生的原理和规律进行解题是近几年高考的一大热点,主要
考查考生的迁移运用能力,但得分率极低;今以化学反应速率常数为例进行讲解
拓展,旨在让考生学会灵活变通,做到举一反三,稳取高分。
1.速率常数含义
速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相
同的浓度条件下,可用速率常数大小来比较化学反应的反应速率。
2.速率方程
一定温度下,化学反应速率与反应物浓度以其计量数为指数的幂的乘积成正比。
对于反应:aA+bB===gG+hH
则 =kca(A)·cb(B)(其中k为速率常数)。
v
如:①SO Cl SO +Cl =k c(SO Cl )
2 2 2 2 v 1 2 2
②2NO 2NO+O =k c2(NO )
2 2 v 2 2
③2H +2NO N +2H O =k c2(H )·c2(NO)
2 2 2 v 3 2
3.速率常数的影响因素
温度对化学反应速率的影响是显著的,速率常数是温度的函数,同一反应,温度
不同,速率常数将有不同的值,但浓度不影响速率常数。
[题型专练]
1.(2015·全国卷Ⅰ·28节选)碘及其化合物在合成杀菌剂、药物等方面具有广泛用
途。回答下列问题:
Bodensteins研究了下列反应:
2HI(g) H (g)+I (g)
2 2
在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下
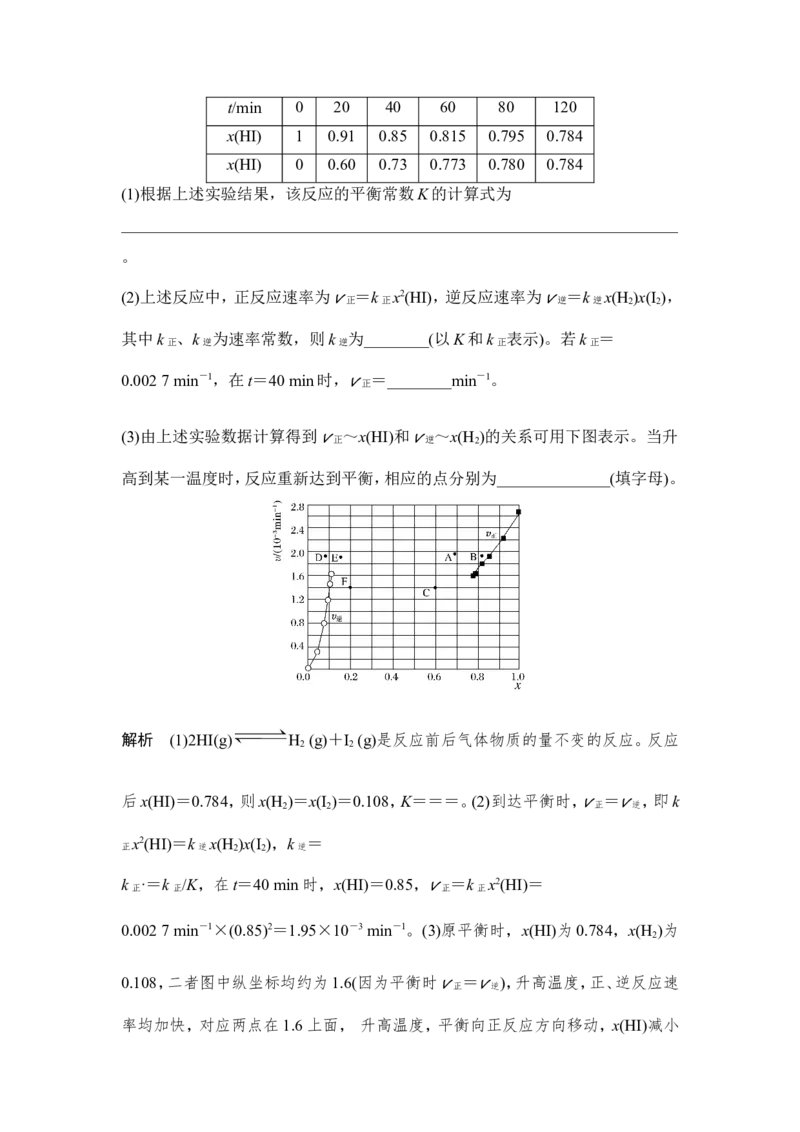
表:t/min 0 20 40 60 80 120
x(HI) 1 0.91 0.85 0.815 0.795 0.784
x(HI) 0 0.60 0.73 0.773 0.780 0.784
(1)根据上述实验结果,该反应的平衡常数K的计算式为
_____________________________________________________________________
。
(2)上述反应中,正反应速率为 =k x2(HI),逆反应速率为 =k x(H )x(I ),
v正 正 v逆 逆 2 2
其中k 、k 为速率常数,则k 为________(以K和k 表示)。若k =
正 逆 逆 正 正
0.002 7 min-1,在t=40 min时, =________min-1。
v正
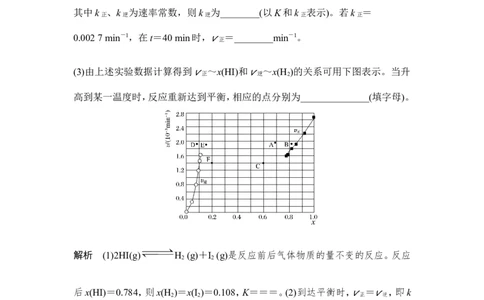
(3)由上述实验数据计算得到 ~x(HI)和 ~x(H )的关系可用下图表示。当升
v正 v逆 2
高到某一温度时,反应重新达到平衡,相应的点分别为______________(填字母)。
解析 (1)2HI(g) H (g)+I (g)是反应前后气体物质的量不变的反应。反应
2 2
后x(HI)=0.784,则x(H )=x(I )=0.108,K===。(2)到达平衡时, = ,即k
2 2 v正 v逆
x2(HI)=k x(H )x(I ),k =
正 逆 2 2 逆
k ·=k /K,在t=40 min时,x(HI)=0.85, =k x2(HI)=
正 正 v正 正
0.002 7 min-1×(0.85)2=1.95×10-3 min-1。(3)原平衡时,x(HI)为0.784,x(H )为
2
0.108,二者图中纵坐标均约为1.6(因为平衡时 = ),升高温度,正、逆反应速
v正 v逆
率均加快,对应两点在1.6上面, 升高温度,平衡向正反应方向移动,x(HI)减小(A点符合),x(H )增大(E点符合)。
2
答案 (1)K= (2)k /K 1.95×10-3
正
(3)A、E
2.(2016·海南高考,16)顺1,2二甲基环丙烷和反1,2二甲基环丙烷可发生如下转
化:
该反应的速率方程可表示为:(正)=k(正)c(顺)和 (逆)=k(逆)c(反),k(正)和k(逆)
v v
在一定温度时为常数,分别称作正、逆反应速率常数。回答下列问题:
(1)已知:t 温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数
1
值K =________;该反应的活化能E (正)小于E (逆),则ΔH________0(填“小
1 a a
于”“等于”或“大于”)。
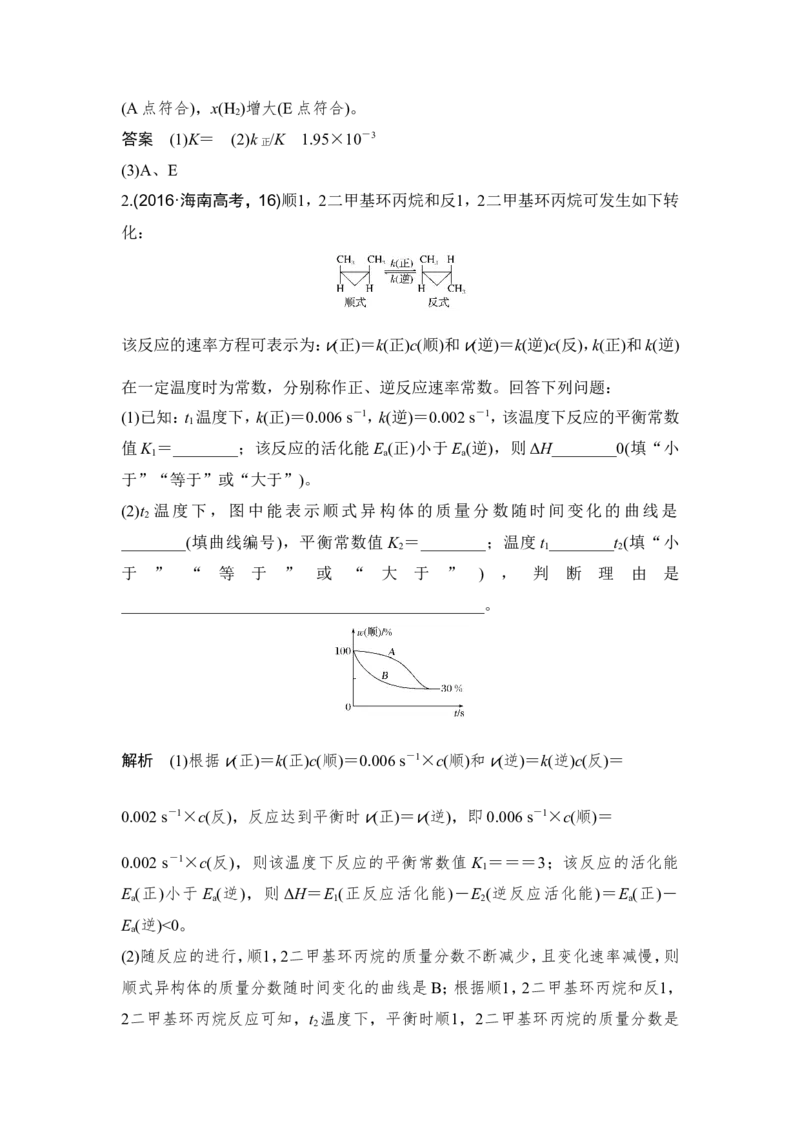
(2)t 温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是
2
________(填曲线编号),平衡常数值 K =________;温度 t ________t (填“小
2 1 2
于 ” “ 等 于 ” 或 “ 大 于 ” ) , 判 断 理 由 是
_____________________________________________。
解析 (1)根据 (正)=k(正)c(顺)=0.006 s-1×c(顺)和 (逆)=k(逆)c(反)=
v v
0.002 s-1×c(反),反应达到平衡时 (正)= (逆),即0.006 s-1×c(顺)=
v v
0.002 s-1×c(反),则该温度下反应的平衡常数值 K ===3;该反应的活化能
1
E (正)小于 E (逆),则 ΔH=E (正反应活化能)-E (逆反应活化能)=E (正)-
a a 1 2 a
E (逆)<0。
a
(2)随反应的进行,顺1,2二甲基环丙烷的质量分数不断减少,且变化速率减慢,则
顺式异构体的质量分数随时间变化的曲线是B;根据顺1,2二甲基环丙烷和反1,
2二甲基环丙烷反应可知,t 温度下,平衡时顺1,2二甲基环丙烷的质量分数是
230%,则反1,2二甲基环丙烷的质量分数是70%,因二者的摩尔质量相同,即反应
平衡时顺1,2二甲基环丙烷的物质的量分数是30%,则反1,2二甲基环丙烷的物
质的量分数是70%,代入平衡常数的表达式K ===;因K 大于K ,此反应为放
2 1 2
热反应,升高温度平衡向逆反应方向移动,得t 大于t 。
2 1
答案 (1)3 小于 (2)B 小于 放热反应升高温度时平衡向逆反应方向移动