文档内容
模板 01 热化学方程式的书写与盖斯定律的应用
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明 ·模板构建 答题模板 + 技巧点拨
技法01 化学反应与焓变 技法02 盖斯定律的应用
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
盖斯定律是指化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。盖斯定律的
应用在于可以根据已准确测定的反应热来求知实验难测或根本无法测定的反应热,可以利用已知的反
应热计算未知的反应热。该类试题主要以生产、生活、科技和能源等社会热点问题为背景,将热化学
方程式的书写与盖斯定律的计算融合在一起进行考查,较好地考查了学生对知识的灵活应用和运算能
力。解答该类题目不仅要清楚书写热化学方程式的要求和注意事项,理解盖斯定律的含义,还要合理
设计反应途径,正确加减热化学方程式。
。
第一步:选唯一作 ①如果是信息类题目,先根据信息写出热化学方程式。
参照物 ②对比已知热化学方程式和目标热化学方程式,若目标热化学方程式中的某
物质只与已知一个已知热化学方程式中共有,则选择该物质作为参照物,依
次参照物在目标热化学方程式中的位置及计量数确定已知热化学方程式的计
量数、ΔH的必变量。
③若目标热化学方程式中某种物质在多个已知热化学方程式中出现,则在计
算确定ΔH时,该物质暂时不作为参照物。
第二步:调整系数 ①调整计量数:将参照物在已知热化学方程式中的计量数调整为与目标热化
学方程式相同,将该已知热化学方程式中的ΔH乘以“+n”倍
②同边相加,异边相减:已知热化学方程式的某个或几个物质与目标热化学方程式中的共有物质在同一边(同为反应物或生成物),直接相加,反之相
减。
第三步:整合关系 将ΔH代入,求出目标热方程式的ΔH。
技法01 化学反应与焓变
1.从两种角度理解化学反应热
微观 宏观
a表示断裂旧化学键吸收的能
a表示反应物的活化能;
量;
图像分析 b表示活化分子形成生成物释放的
b表示生成新化学键放出的能
能量;
量;
c表示反应热
c表示反应热
ΔH的计算 ΔH=H(生成物)-H(反应物) ΔH=∑E(反应物键能)-∑E(生成物键能)
2.热化学方程式的书写
(1)书写热化学方程式的“五环节”
①写方程式:写出配平的化学方程式。
②标状态:用s、l、g、aq标明物质的聚集状态。
③定条件:确定反应的温度和压强(101kPa、25℃时可不标注)。
④标ΔH:在方程式后写出ΔH,并注明ΔH的“+”或“-”。
⑤标数值:根据化学计量数写出ΔH的值。
(2)热化学方程式书写易出现的错误
①未标明反应物或生成物的状态而造成错误。
②反应热的符号使用不正确,即吸热反应未标出“+”号,放热反应未标出“-”号,从而导致错误。
③漏写ΔH的单位,或者将ΔH的单位写为kJ,从而造成错误。
④反应热的数值与方程式的计量数不对应而造成错误。
⑤对燃烧热、中和热的概念理解不到位,忽略其标准是1 mol可燃物或生成1 mol H O(l)而造成错误。
2
⑥对于具有同素异形体的物质,除了要注明聚集状态之外,还要注明物质的名称。
如:①S(单斜,s)+O(g)===SO(g) ΔH=-297.16 kJ·mol-1
2 2 1
②S(正交,s)+O(g)===SO(g) ΔH=-296.83 kJ·mol-1
2 2 2
③S(单斜,s)===S(正交,s) ΔH=-0.33 kJ·mol-1
3(3)燃烧热和中和热应用中的注意事项
①均为放热反应,ΔH<0,单位为kJ·mol-1。
②燃烧热概念理解的三要点:
a.外界条件是25 ℃、101 kPa;
b.反应的可燃物是1 mol;
c.生成物是稳定的氧化物(包括状态),如碳元素生成的是CO ,而不是CO,氢元素生成的是液态水,
2
而不是水蒸气。
③中和热概念理解三要点:
a.反应物酸、碱是强酸、强碱;
b.溶液是稀溶液,不存在稀释过程的热效应;
c.生成物液态水是1 mol。
3.焓变计算
(1)键能公式:ΔH=反应物总键能-生成物总键能
(2)活化能公式:ΔH=正反应活化能-逆反应活化能
(3)总能量公式:ΔH=生成物总能量-反应物总能量(其中能垒图中的相对能量相当于总能量)
技法02 盖斯定律的应用
1.运用盖斯定律的技巧——“三调一加”
一调:根据目标热化学方程式,调整已知热化学方程式中反应物和生成物的左右位置,改写已知的热
化学方程式。
二调:根据改写的热化学方程式调整相应ΔH的符号。
三调:调整中间物质的化学计量数。
一加:将调整好的热化学方程式及其ΔH相加。
2.运用盖斯定律的三个注意事项
(1)热化学方程式乘以某一个数时,反应热的数值必须也乘上该数。
(2)热化学方程式相加减时,物质之间相加减,反应热也必须相加减。
(3)将一个热化学方程式颠倒时,ΔH的“+”“-”随之改变,但数值不变。
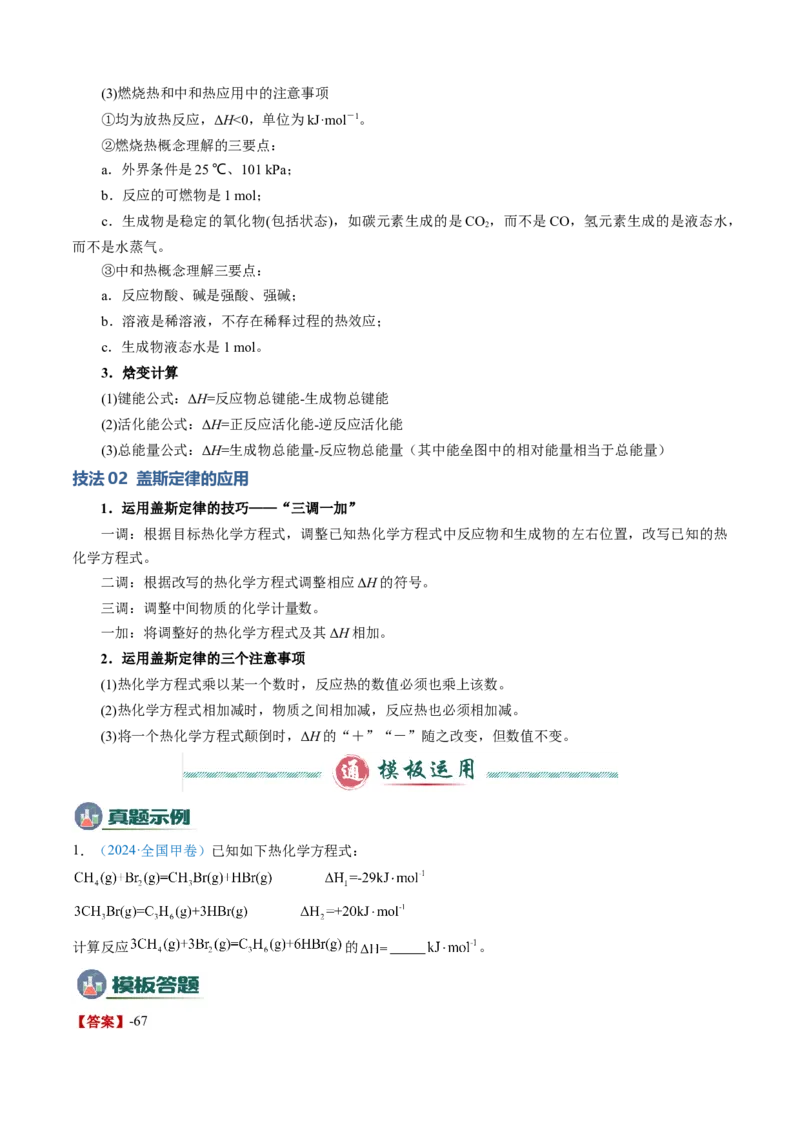
1.(2024·全国甲卷)已知如下热化学方程式:
计算反应 的 。
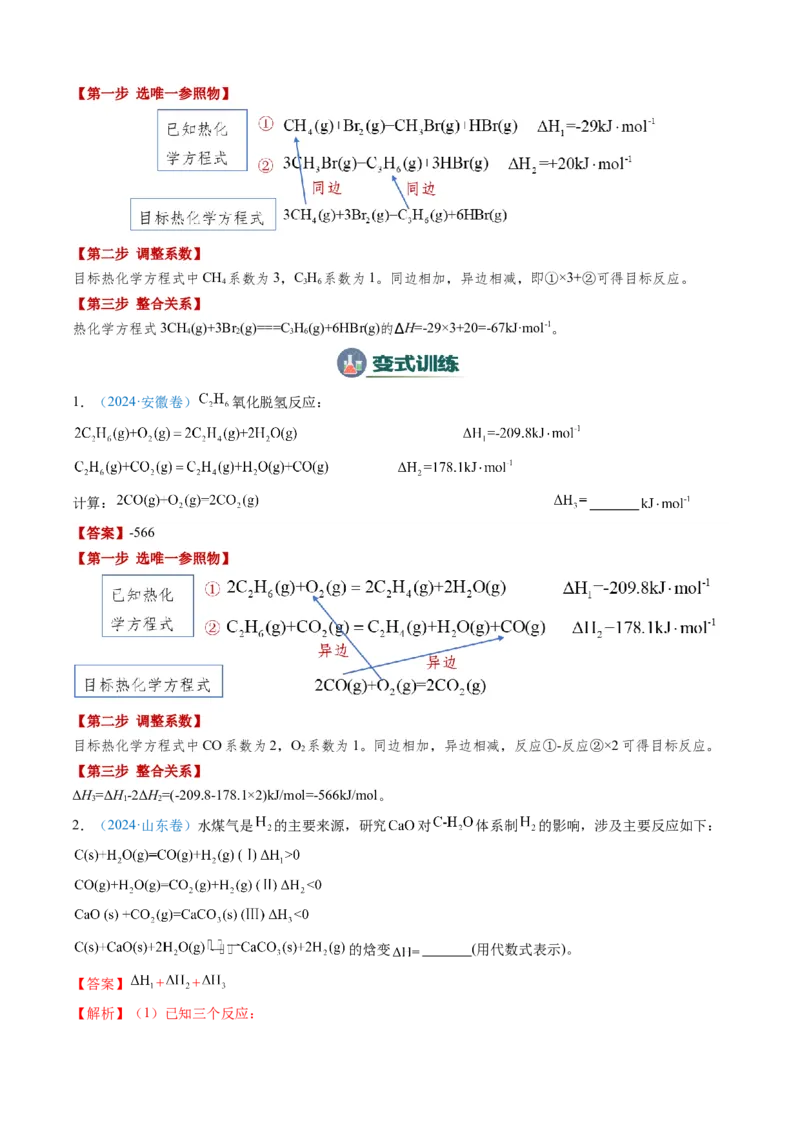
【答案】-67【第一步 选唯一参照物】
【第二步 调整系数】
目标热化学方程式中CH 系数为3,C H 系数为1。同边相加,异边相减,即①×3+②可得目标反应。
4 3 6
【第三步 整合关系】
热化学方程式3CH(g)+3Br (g)===C H(g)+6HBr(g)的∆H=-29×3+20=-67kJ·mol-1。
4 2 3 6
1.(2024·安徽卷) 氧化脱氢反应:
计算:
【答案】-566
【第一步 选唯一参照物】
【第二步 调整系数】
目标热化学方程式中CO系数为2,O 系数为1。同边相加,异边相减,反应①-反应②×2可得目标反应。
2
【第三步 整合关系】
ΔH=ΔH-2ΔH=(-209.8-178.1×2)kJ/mol=-566kJ/mol。
3 1 2
2.(2024·山东卷)水煤气是 的主要来源,研究 对 体系制 的影响,涉及主要反应如下:
的焓变 (用代数式表示)。
【答案】 + +
【解析】(1)已知三个反应:Ⅰ.
Ⅱ.
Ⅲ.
设目标反应 为Ⅳ,根据盖斯定律,Ⅳ=Ⅰ+Ⅱ+Ⅲ,所以
+ + 。
3.(2024·湖南卷)丙烯腈( )是一种重要的化工原料。工业上以 为载气,用 作催化剂
生产 的流程如下:
已知:①反应釜Ⅰ中发生的反应:
ⅰ:
②反应釜Ⅱ中发生的反应:
ⅱ:
ⅲ:
总反应 (用含
、 、和 的代数式表示);
【答案】(1)ΔH+ΔH +ΔH
1 2 3
【解析】(1)根据盖斯定律,总反应HOCH CHCOOC H(g)+NH (g)→CH =CHCN(g)+C HOH(g)
2 2 2 5 3 2 2 5
+2H O(g)可以由反应i+反应ii+反应iii得到,故ΔH=ΔH+ΔH +ΔH ;
2 1 2 3
1.(2024·甘肃卷)由 制备 :
已知
时,由 制备 硅 (填“吸”或“放”)热 。升高温
度有利于制备硅的原因是 。
【答案】吸 587.02 该反应为吸热反应,升高温度,反应正向移动,有利于制备硅
【解析 】由 题给热化学方程式: ① , ;②
, ;则根据盖斯定律可知,①+②,可得热化学方程
式 , ,则制备56gSi,即2molSi,需要吸收热量为 ;该反应为吸热反应,升高温度,
反应正向移动,有利于制备硅。
2.(2024·黑吉辽卷)为实现氯资源循环利用,工业上采用 催化氧化法处理 废气:
。
结合以下信息,可知 的燃烧热 。
【答案】-258.8
【解析】表示氢气燃烧热的热化学方程式为④ ,设①
,② ,③ ,则 ,因
此氢气的燃烧热 -57.2kJ/mol-184.6kJ/mol-44kJ/mol=-258.8
3.(2024·河北卷)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:
。
若正反应的活化能为 ,则逆反应的活化能 (用含 正的代数式表示)。
【答案】
【解析】根据反应热 与活化能E 和E 关系为 正反应活化能-逆反应活化能可知,该反应的
正 逆
。
4.(2024·贵州卷)在无氧环境下,CH 经催化脱氢芳构化可以直接转化为高附加值的芳烃产品。一定温
4
度下,CH 芳构化时同时存在如下反应:
4
ⅰ.
ⅱ.
(1)反应ⅰ在1000K时 (选填“能”或“不能”)自发进行。
(2)已知25℃时有关物质的燃烧热数据如表,则反应ⅱ的 (用含 的代数式表
示)。
物质
【答案】(1)能 (2)6a-b-9c
【解析】(1)反应ⅰ. ,在1000K
时,ΔG=ΔH-TΔS=+74.6 kJ·mol-1-1000K×80.84×10-3kJ·mol-1·K-1=-6.24 kJ·mol-1<0,故反应ⅰ在1000K时能自发进行。
(2)ⅱ.
由题给数据可得出以下热化学方程式:
③CH(g)+2O(g)=CO(g)+2HO(l) ΔH=akJ·mol-1
4 2 2 2
④C H(l)+7.5O(g)=6CO(g)+3HO(l) ΔH=bkJ·mol-1
6 6 2 2 2
⑤H(g)+0.5O (g)=HO(l) ΔH=c kJ·mol-1
2 2 2
依据盖斯定律,将反应③×6-④-⑤×9得,反应ⅱ的 (6a-b-9c) kJ·mol-1。
5.(2023·全国甲卷)已知下列反应的热化学方程式:
①
②
反应③ 的 _______ ,平衡常数 _______(用 表
示)。
【答案】 或
【解析】根据盖斯定律可知,反应③=(反应②-反应①),所以对应
;根据平衡常数表达式与热化学方程式之
间的关系可知,对应化学平衡常数 或 ,故答案为: ; 或 ;
6.(2023·全国乙卷)已知下列热化学方程式:
则 的 _______ 。
【答案】(a+c-2b)
【解析】①
②
③
根据盖斯定律可知,①+③-② 2可得 ,则
(a+c-2b) 。
7.(2023·新课标卷)根据图1数据计算反应 的 _______ 。【答案】
【解析】在化学反应中,断开化学键要消耗能量,形成化学键要释放能量,反应的焓变等于反应物的键能
总和与生成物的键能总和的差,因此,由图1数据可知,反应 的
。
8.(2023·山东卷)一定条件下,水气变换反应 的中间产物是 。为探究该
反应过程,研究 水溶液在密封石英管中的分子反应:
Ⅰ.
Ⅱ.
一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、 ,则该条件下水气变换反应的焓变 _____(用含
的代数式表示)。
【答案】 -
【解析】根据盖斯定律,反应II-反应I=水气变换反应,故水气变换反应的焓变 = - ;
9.已知重整过程中部分反应的热化学方程式为:
①CH(g)===C(s)+2H(g) ΔH=+74.8 kJ·mol-1
4 2 1
②CO(g)+HO(g)===CO (g)+H(g) ΔH=-41.2 kJ·mol-1
2 2 2 2
③C(s)+HO(g)===CO(g)+H(g) ΔH=+131.5 kJ·mol-1
2 2 3
则反应CH(g)+CO(g) 2CO(g)+2H(g)的ΔH=________
4 2 2
【答案】+247.5 kJ·mol-1
【解析】根据盖斯定律,由①-②+③可得:CH(g)+CO(g)2CO(g)+2H(g) ΔH=+74.8 kJ·mol-1-
4 2 2
(-41.2 kJ·mol-1)+131.5 kJ·mol-1=+247.5 kJ·mol-1。
10.已知:①CO(g)+HO(g) HCOOH(g) ΔH=-72.6 kJ·mol-1
2 1
②2CO(g)+O(g) 2CO(g) ΔH=-566.0 kJ·mol-1
2 2 2
则反应2CO(g)+2HO(g) 2HCOOH(g)+O(g)的ΔH=________kJ·mol-1
2 2 2
【答案】+420.8
【解析】根据盖斯定律,由2×①-②,可得2CO(g)+2HO(g) 2HCOOH(g)+O(g) ΔH=-72.6×2
2 2 2
kJ·mol-1+566.0 kJ·mol-1=+420.8 kJ·mol-1。
11.已知:Ⅰ.2NO(g)+O(g) ===2NO(g) ΔH=-113 kJ·mol-1
2 2 1
Ⅱ.NO(g)+O(g) ===NO(g)+O(g) ΔH=-199 kJ·mol-1
3 2 2 2Ⅲ.N O(g) ===2NO(g) ΔH=+55.3 kJ·mol-1
2 4 2 3
Ⅳ.4NO(g)+O(g) ===2N O(g) ΔH=-57 kJ·mol-1
2 2 2 5 4
则反应6NO (g)+O(g) ===3N O(g) ΔH=________ kJ·mol-1
2 3 2 5
【答案】-228
【解析】根据盖斯定律×(Ⅳ×3+Ⅱ×2-Ⅰ)得:6NO (g)+O(g)===3N O(g) ΔH=×[(-57 kJ·mol-1)×3+(-
2 3 2 5
199 kJ·mol-1)×2-(-113 kJ·mol-1)]=-228 kJ·mol-1。
11.已知:N(g)+O(g)===2NO(g) ΔH=+180.5 kJ·mol-1
2 2
C(s)+O(g)===CO (g) ΔH=-393.5 kJ·mol-1
2 2
2C(s)+O(g)===2CO(g) ΔH=-221 kJ·mol-1
2
则反应2NO(g)+2CO(g)===N (g)+2CO(g) ΔH=________ kJ·mol-1
2 2
【答案】-746.5 kJ·mol-1
【解析】根据平衡常数表达式可写出目标反应,然后根据盖斯定律可知 ΔH=[-180.5-(-221)+2×(-
393.5)]kJ·mol-1=-746.5 kJ·mol-1。
12.应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源。甲醇是一种可再生的清洁能
源,具有广阔的开发和应用前景。
已知:①CHOH(g)+HO(l)===CO (g)+3H(g) ΔH=+93.0 kJ·mol-1
3 2 2 2
②CHOH(g)+O(g)===CO (g)+2H(g) ΔH=-192.9 kJ·mol-1
3 2 2 2
③CHOH(g)===CH OH(l) ΔH=-38.19 kJ·mol-1
3 3
则表示CHOH(l)燃烧热的热化学方程式为____________________________________________________
3
【答案】CHOH(l)+O(g)===CO (g)+2HO(l) ΔH=-726.51 kJ·mol-1
3 2 2 2
【解析】根据盖斯定律,②×3-①×2-③得CHOH(l)+O(g)===CO (g)+2HO(l) ΔH=-726.51 kJ·mol-
3 2 2 2
1。
13.环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
已知: ΔH=100.3 kJ·mol-1 ①
1
H(g)+I(g)===2HI(g) ΔH=-11.0 kJ·mol-1 ②
2 2 2
对于反应: ③ ΔH=________kJ·mol-1
3
【答案】(1)89.3
【解析】根据盖斯定律,反应①+②可得反应③,则ΔH =ΔH +ΔH =100.3 kJ•mol-1 +(-11.0 kJ·mol-1)
3 1 2
=89.3 kJ·mol-1。
14.氨基甲酸铵(H NCOONH )为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行
2 4
探究
已知:Ⅰ.N (g)+3H(g) 2NH (g) ΔH=-92.4 kJ·mol-1
2 2 3 1
Ⅱ.C(s)+O(g) CO(g) ΔH=-393.8 kJ·mol-1
2 2 2
Ⅲ.N (g)+3H(g)+C(s)+O(g) HNCOONH (s) ΔH=-645.7 kJ·mol-1
2 2 2 2 4 3
(1)写出HNCOONH 分解生成NH 与CO 气体的热化学方程式:___________________________。
2 4 3 2
(2)已知:R ln K =-+C(C为常数)。根据上表实验数据得到下图,则该反应的反应热ΔH=______kJ·mol
p-1
【答案】(1)H NCOONH (s) 2NH (g)+CO(g) ΔH=+159.5 kJ·mol-1
2 4 3 2
(2)+144.2
【解析】(1)已知:Ⅰ.N (g)+3H(g) 2NH (g) ΔH =-92.4 kJ·mol-1,Ⅱ.C(s)+O(g) CO(g) ΔH
2 2 3 1 2 2 2
=-393.8 kJ·mol-1,Ⅲ.N (g)+3H(g)+C(s)+O(g) HNCOONH (s) ΔH =-645.7 kJ·mol-1,由盖斯
2 2 2 2 4 3
定律Ⅰ+Ⅱ-Ⅲ得:HNCOONH (s) 2NH (g)+CO(g) ΔH=ΔH+ΔH-ΔH=+159.5 kJ·mol-1。
2 4 3 2 1 2 3
(2)把图像上点的数值代入R ln K =-+C得:69.50=-ΔH×3.19×10-3+C和53.64=-ΔH×3.30×10-3+
p
C,联立求解得,ΔH=+144.2 kJ·mol-1。
15.从空气中捕获CO 直接转化为甲醇是二十多年来“甲醇经济”领域的研究热点,诺贝尔化学奖获得者
2
乔治·安德鲁教授首次以金属钌作催化剂实现了这种转化,其转化如图所示
(1)如图所示转化中,第4步常采取________法将甲醇和水进行分离
(2)如图所示转化中,由第1步至第4步的反应热(ΔH)依次是a kJ·mol-1、b kJ·mol-1、c kJ·mol-1、d kJ·mol
-1,则该转化总反应的热化学方程式是_____________________________________________。
【答案】(1)蒸馏(或分馏)
(2)CO (g)+3H(g) CHOH(l)+HO(l) ΔH=(a+b+c+d)kJ·mol-1
2 2 3 2
【解析】(1)甲醇易挥发,沸点较低,与水的沸点相差较大,可以采用蒸馏或分馏的方法分离甲醇和水。
(2)根据图示是一个闭合的环,说明总反应的反应热是四步反应的反应热之和,结合碳元素守恒,可以写出
总反应的热化学方程式:CO(g)+3H(g) CHOH(l)+HO(l) ΔH=(a+b+c+d)kJ·mol-1。
2 2 3 2
16.推动煤炭清洁高效利用是未来煤炭利用的发展方向,其中煤制天然气(主要成分甲烷)能对燃气资源有
重要补充作用。在催化剂作用下,其涉及的主要反应如下:
CO(g)+3H(g) CH(g)+HO(g) ΔH=-206.2 kJ·mol-1 Ⅰ
2 4 2 1
CO(g)+HO(g) CO(g)+H(g) ΔH=-41.2 kJ·mol-1 Ⅱ
2 2 2 2
CO(g)+4H(g) CH(g)+2HO(g) ΔH Ⅲ
2 2 4 2 3
荷兰埃因霍温大学学者结合实验与计算机模拟结果,研究了在催化剂钴表面上反应Ⅰ的反应历程,如图所
示,其中吸附在钴催化剂表面上的物种用*标注。(1) 该 历 程 中 最 大 能 垒 E = ________kJ·mol - 1 , 写 出 该 步 骤 的 化 学 方 程 式 :
正
______________________________
(2)ΔH=________kJ·mol-1
3
【答案】(1)136.1 CO*+2H*+2H(g)===C*+O*+2H*+2H(g)
2 2
(2)-165.0
【解析】(1)根据图中信息得出,该历程中最大能垒是相对能量7.8 kJ·mol-1到143.9 kJ·mol-1,即E =136.1
正
kJ·mol-1;该步骤的化学方程式为CO*+2H*+2H(g)===C*+O*+2H*+2H(g)。
2 2
(2)根据盖斯定律,反应Ⅰ-反应Ⅱ=反应Ⅲ,ΔH=ΔH-ΔH=-206.2 kJ·mol-1-(-41.2 kJ·
3 1 2
mol-1)=-165.0 kJ·mol-1。