文档内容
2022-2023 学年 江苏常州高级中学
高三年级 1 月月考 化学试卷
总分100分 考试时间100分钟
一、单项选择题(14小题每题3分共42分)
1.下列各组物质按氧化物、单质、混合物的顺序排列的是
A.烧碱、液态氧、碘酒 B.生石灰、白磷、胆矾
C.干冰、铁、氯化氢 D.水、硫黄、漂白粉
2.某元素X 的最高价含氧酸的化学式为 HXO ,则在其气态氢化物中 X 的化合
n 2n﹣2
价为
A.﹣(12﹣5n) B.﹣(12﹣3n) C.﹣(6﹣3n) D.﹣(10﹣n)
3.下列实验操作正确的是
A.蒸馏实验中温度计的水银球应插入液态混合物中
B.用酒精萃取碘水中的碘
C.分液时,使下层液体从下口流出之后,上层液体从上口倒出
D.将浓 溶液逐滴加到煮沸的 溶液制备 胶体
4.常温常压下,0.5mol铝、0.5mol铁分别与足量稀硫酸完全反应,生成氢气的体积分
别为 和 ( 为阿伏加德罗常数的值)。下列说法正确的是
A. L
B.
C.铝、铁消耗硫酸的物质的量相等
D.反应生成的硫酸铝水解形成 胶体,胶体粒子数目为0.55.短周期主族元素W、X、Y、Z的原子序数依次增大,其中Y为金属元素,W、X、
Y三种原子的最外层电子数之比为 ,Z的最高价氧化物对应水化物的化学式为
。下列说法正确的是
A.W、X两种元素原子最多形成两种微粒
B.X和Y形成的物质能作耐火材料
C.W、X的简单氢化物常温下均为气体
D.Z的最高价氧化物对应的水化物是强酸
6.下列有关 、 、 、 的说法正确的是
A. 和 中的键角 前者大
B. 和 的空间构型相同
C. 和 中N原子的杂化方式相同
D. 与 形成的 中,提供孤电子对形成配位键的是
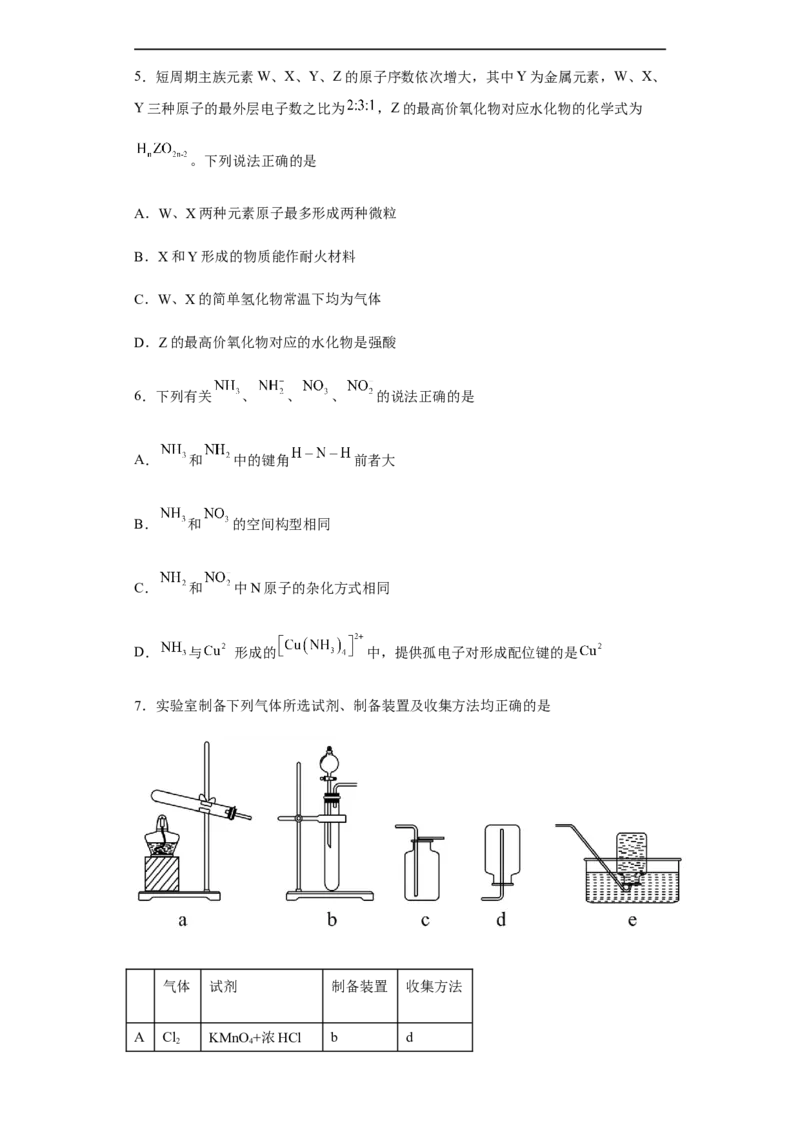
7.实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气体 试剂 制备装置 收集方法
A Cl KMnO +浓HCl b d
2 4B O KMnO a c
2 4
C NO Cu+稀HNO b c
3
D CO CaCO +稀HSO b c
2 3 2 4
A.A B.B C.C D.D
8.在恒温恒容密闭容器中,充入一定量NO(g),发生反应NO(g)
2 4 2 4
2NO (g)ΔH>0,下列说法正确的是
2
A.反应过程中v(N O) =2v(NO)
2 4 消耗 2 生成
B.其他条件不变,升高温度,NO 平衡转化率减小
2 4
C.容器中气体的平均相对分子质量保持不变时即反应达平衡
D.加压,平衡逆向移动,正反应速率或小,逆反应速率加快
9.下列离子方程式书写正确的是
A.氯化铁溶液蚀刻铜板:
B.铁粉与稀硫酸反应:
C.氯化亚铁溶液中通入氯气:
D.氯化镁溶液与氨水反应:
10.有六种有机化合物,分子式如下:(甲) 、(乙) 、(丙) 、
(丁) 、(戊) 、(己) 。经由实验分析,得知其中有一种化合物具
有双键。下列相关叙述中,何者不正确?A.有甲、戊为卤烷
B.有乙可能为醚类
C.有可能有3种化合物为环状结构
D.有具有双键的化合物可能是醛或酮
E.有丁若可使过锰酸钾溶液褪色,则为烯类
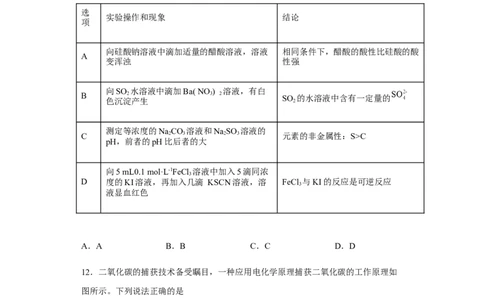
11.根据下列实验操作和现象所得出的结论正确的是
选
实验操作和现象 结论
项
向硅酸钠溶液中滴加适量的醋酸溶液,溶液 相同条件下,醋酸的酸性比硅酸的酸
A
变浑浊 性强
向SO 水溶液中滴加Ba( NO ) 溶液,有白
B 2 3 2 SO 的水溶液中含有一定量的
色沉淀产生 2
测定等浓度的NaCO 溶液和NaSO 溶液的
C 2 3 2 3 元素的非金属性:S>C
pH,前者的pH比后者的大
向5 mL0.1 mol·L-1FeCl 溶液中加入5滴同浓
3
D 度的KI溶液,再加入几滴 KSCN溶液,溶 FeCl 与KI的反应是可逆反应
3
液显血红色
A.A B.B C.C D.D
12.二氧化碳的捕获技术备受瞩目,一种应用电化学原理捕获二氧化碳的工作原理如
图所示。下列说法正确的是
A.该装置中化学能转化为电能B.二氧化碳的捕获在阳极区完成
C.阳极的电极反应式为
D.捕获过程中两极区碳元素的化合价均发生变化
13.下列离子方程式中正确的是( )
A.HSO 与Ba(OH) 溶液反应:Ba2++OH-+H++SO ===BaSO ↓+HO
2 4 2 4 2
B.NaCO 溶液中通入CO:CO +CO+HO===2HCO
2 3 2 2 2
C.向NaOH溶液中滴入少量Ca(HCO ) 溶液:Ca2++HCO +OH-===CaCO ↓+HO
3 2 3 2
D.CHCOOH溶液与NaOH溶液反应:H++OH-===HO
3 2
14.氯碱工业生产中用氨气检查氯气管道是否泄漏,反应的方程式为:8NH +3Cl=
3 2
6NH Cl+N ,若有 56g N 生成,则发生氧化反应的NH 的物质的量是
4 2 2 3
A.16mol B.8mol C.4mol D.3mol
二、工业流程题(共14分)
15.草酸合铁(III)酸钾晶体[K [Fe(C O)]·3H O]是制备负载型活性铁催化剂的主要原料。
3 2 4 3 2
某科研团队以硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]为原料制备草酸合铁(III)酸钾晶体
4 2 4 2 2
的具体流程如图:
回答下列问题:
(1)配制100mL1.00mol·L-1的硫酸亚铁铵溶液。溶液配制过程中需用到的玻璃仪器除
烧杯、玻璃棒、量筒外,还有___。在配制时需加入适量稀硫酸的目的是___。
(2)取12.5mL硫酸亚铁铵溶液于烧杯中,水浴加热至100℃,缓缓滴入饱和HC O
2 2 4
溶液,有黄色沉淀(FeC O·2H O)生成,反应的离子方程式为___。
2 4 2(3)在“酸溶”操作中,需保持溶液的pH为3.5,溶液中 =___。(H C O
2 2 4
的K =10-1.25,K =10-4.27)。
a1 a2
(4)在“反应”中,先维持40℃水浴加热,滴加10mL6%H O 溶液,一段时间后,
2 2
再微沸2min;然后冷却,继续交替滴加HC O 和KC O 溶液直至溶液呈亮绿色。维
2 2 4 2 2 4
持40℃水浴加热使最终所得产品产率最高的原因是__,溶液微沸的目的是__。
(5)经“步骤I”结晶、抽滤、洗涤、避光干燥,最终得到产品5.45g,产品的产率为
____(保留1位小数)。
(6)草酸合铁(I)酸钾晶体为光敏配合物,应避光保存,光照时会发生光化学分解反应
生成草酸钾和草酸亚铁,同时有气体生成,反应的化学方程式为___。
三、有机推断题(共14分)
16.苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效,主要
酸性物质为苹果酸。该苹果酸在分离提纯后的化学分析如下:
①相对分子质量不超过250,完全燃烧后只生成CO 和HO,分子中C、H质量分数分
2 2
别为:w(C)=35.82%,w(H)=4.48%;
②1 mol该酸与足量的NaHCO 反应放出44.8 L CO,与足量的Na反应放出33.6 L
3 2
H(气体体积均已折算为标准状况);
2
③该分子中存在四种不同化学环境的碳原子,分子中不含甲基。
已知:该苹果酸分子有下列转化关系,其中B能使溴的四氯化碳溶液褪色。
回答下列问题:(1)苹果酸分子中所含官能团的名称是_______、_______。
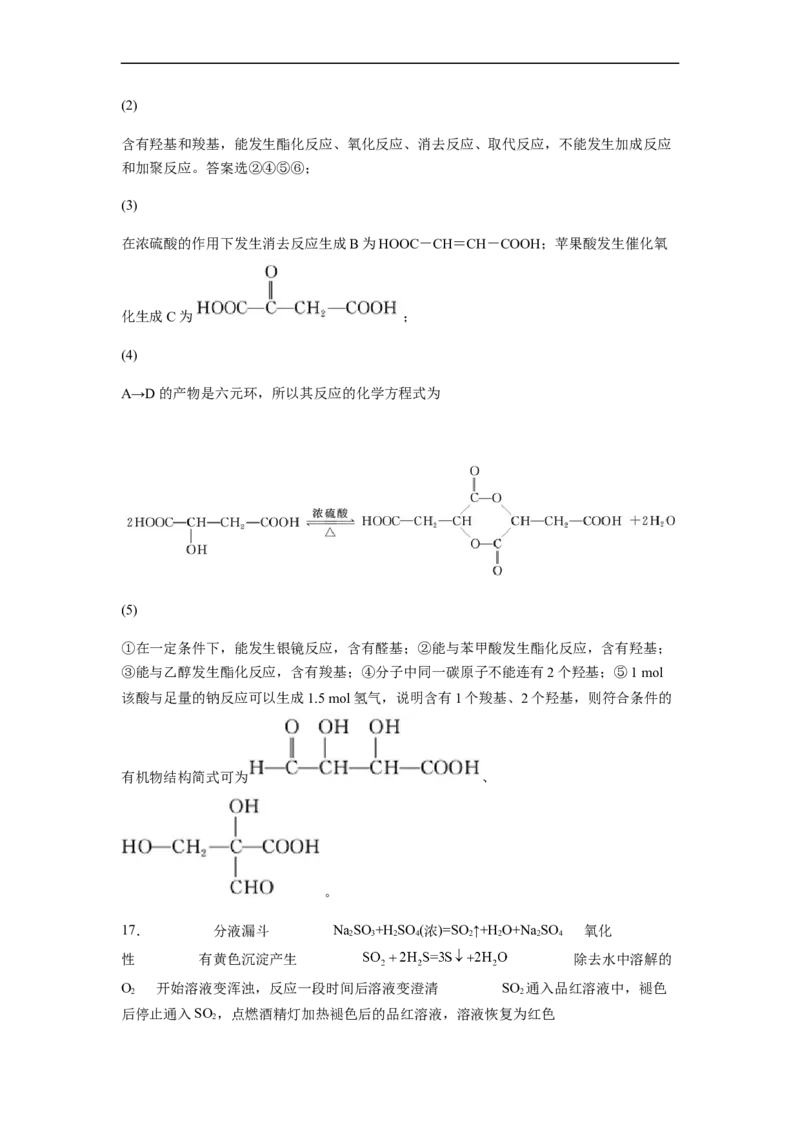
(2)苹果酸能发生的反应有_______(选填序号)。
①加成反应 ②酯化反应 ③加聚反应 ④氧化反应 ⑤消去反应 ⑥取代反应
(3)写出B、C的结构简式:B:_______;C:_______。
(4)写出A→D的化学方程式:_______ 。
(5)该苹果酸有多种同分异构体,写出符合下列条件的两种同分异构体的结构简式:
_______。
①在一定条件下,能发生银镜反应;
②能与苯甲酸发生酯化反应;
③能与乙醇发生酯化反应;
④分子中同一碳原子不能连有2个羟基;
⑤1 mol该酸与足量的钠反应可以生成1.5 mol氢气。
四、实验题(共16分)
17.硫代硫酸钠晶体(Na SO·5H O)是重要的化工原料,广泛的用于印染工业等。某课
2 2 3 2
外兴趣小组在实验室制备NaSO·5H O。回答下列问题:
2 2 3 2
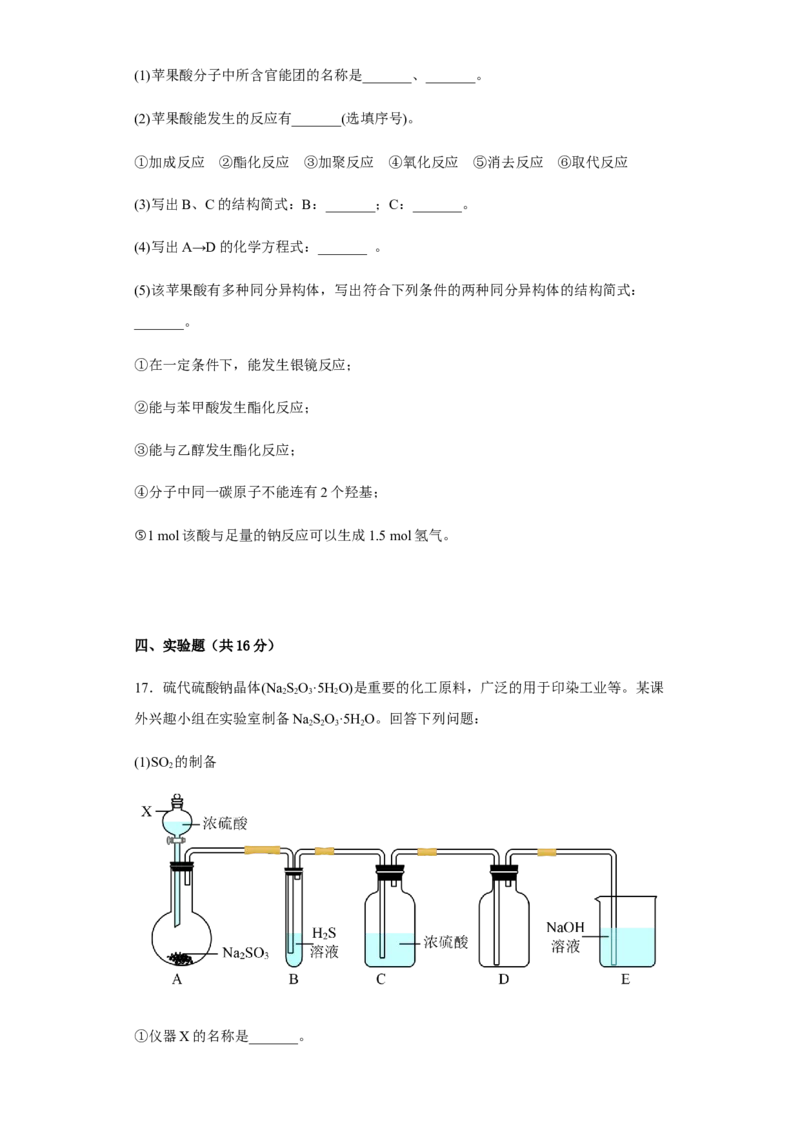
(1)SO 的制备
2
①仪器X的名称是_______。②装置A中反应的化学方程为_______。
③装置B的目的是验证SO 具有_______,产生的现象是_______,反应的化学方程式
2
为_______。
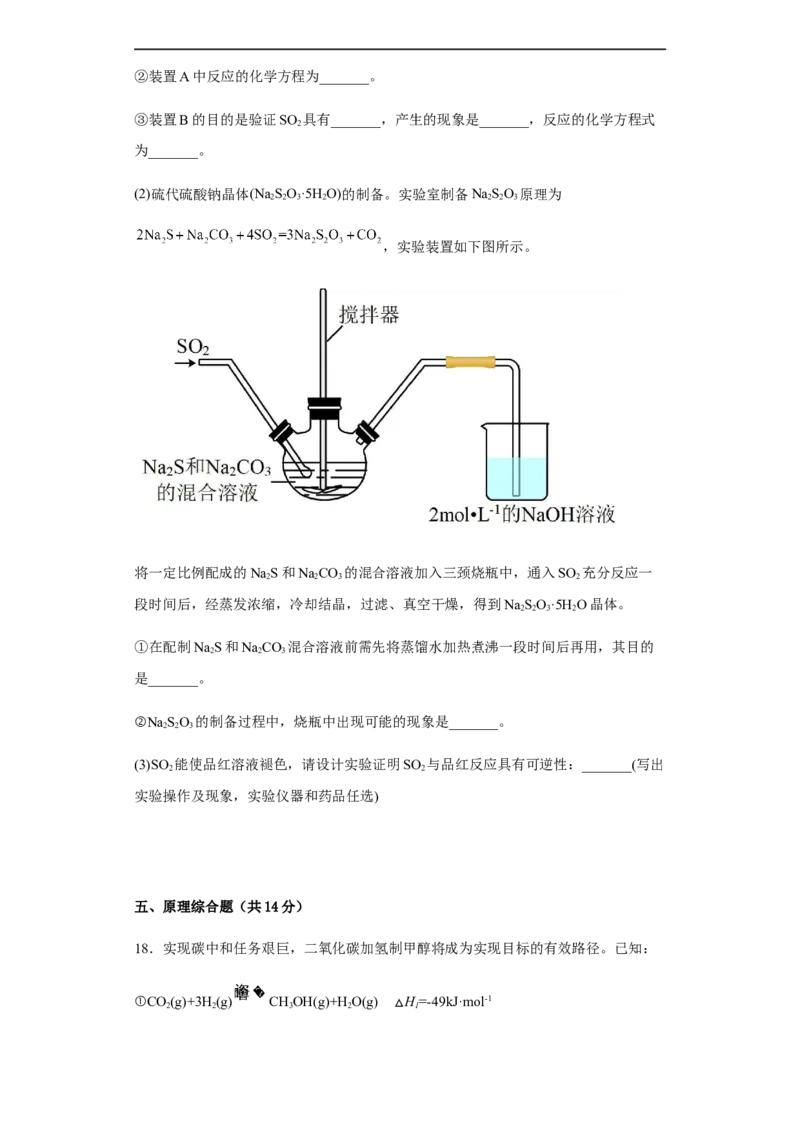
(2)硫代硫酸钠晶体(Na SO·5H O)的制备。实验室制备NaSO 原理为
2 2 3 2 2 2 3
,实验装置如下图所示。
将一定比例配成的NaS和NaCO 的混合溶液加入三颈烧瓶中,通入SO 充分反应一
2 2 3 2
段时间后,经蒸发浓缩,冷却结晶,过滤、真空干燥,得到NaSO·5H O晶体。
2 2 3 2
①在配制NaS和NaCO 混合溶液前需先将蒸馏水加热煮沸一段时间后再用,其目的
2 2 3
是_______。
②Na SO 的制备过程中,烧瓶中出现可能的现象是_______。
2 2 3
(3)SO 能使品红溶液褪色,请设计实验证明SO 与品红反应具有可逆性:_______(写出
2 2
实验操作及现象,实验仪器和药品任选)
五、原理综合题(共14分)
18.实现碳中和任务艰巨,二氧化碳加氢制甲醇将成为实现目标的有效路径。已知:
①CO(g)+3H(g) CHOH(g)+H O(g) H=-49kJ·mol-1
2 2 3 2 1
△②CO (g)+H(g) CO(g)+HO(g) H
2 2 2 2
△
③CO(g)+2H (g) CHOH(g) H=-90kJ·mol-1
2 3 3
△
回答下列问题:
(1) H=_______kJ·mol-1。
2
△
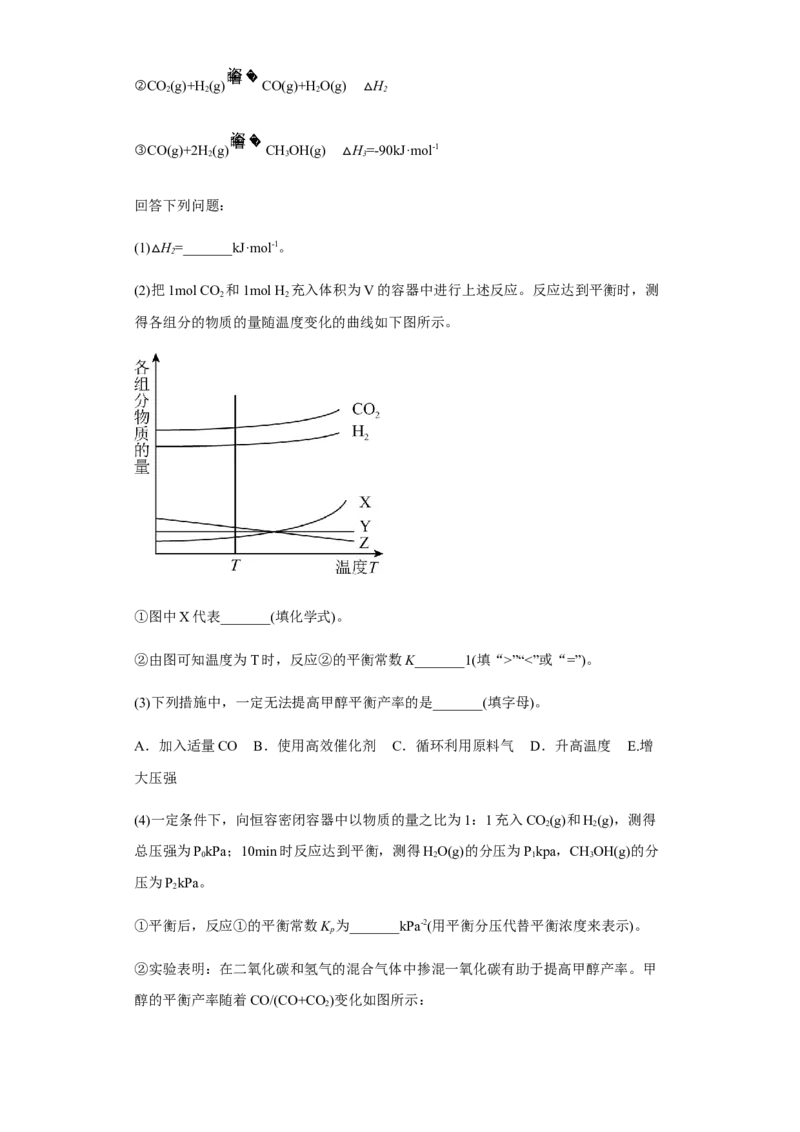
(2)把1mol CO 和1mol H 充入体积为V的容器中进行上述反应。反应达到平衡时,测
2 2
得各组分的物质的量随温度变化的曲线如下图所示。
①图中X代表_______(填化学式)。
②由图可知温度为T时,反应②的平衡常数K_______1(填“>”“<”或“=”)。
(3)下列措施中,一定无法提高甲醇平衡产率的是_______(填字母)。
A.加入适量CO B.使用高效催化剂 C.循环利用原料气 D.升高温度 E.增
大压强
(4)一定条件下,向恒容密闭容器中以物质的量之比为1:1充入CO(g)和H(g),测得
2 2
总压强为PkPa;10min时反应达到平衡,测得HO(g)的分压为Pkpa,CHOH(g)的分
0 2 1 3
压为PkPa。
2
①平衡后,反应①的平衡常数K 为_______kPa-2(用平衡分压代替平衡浓度来表示)。
p
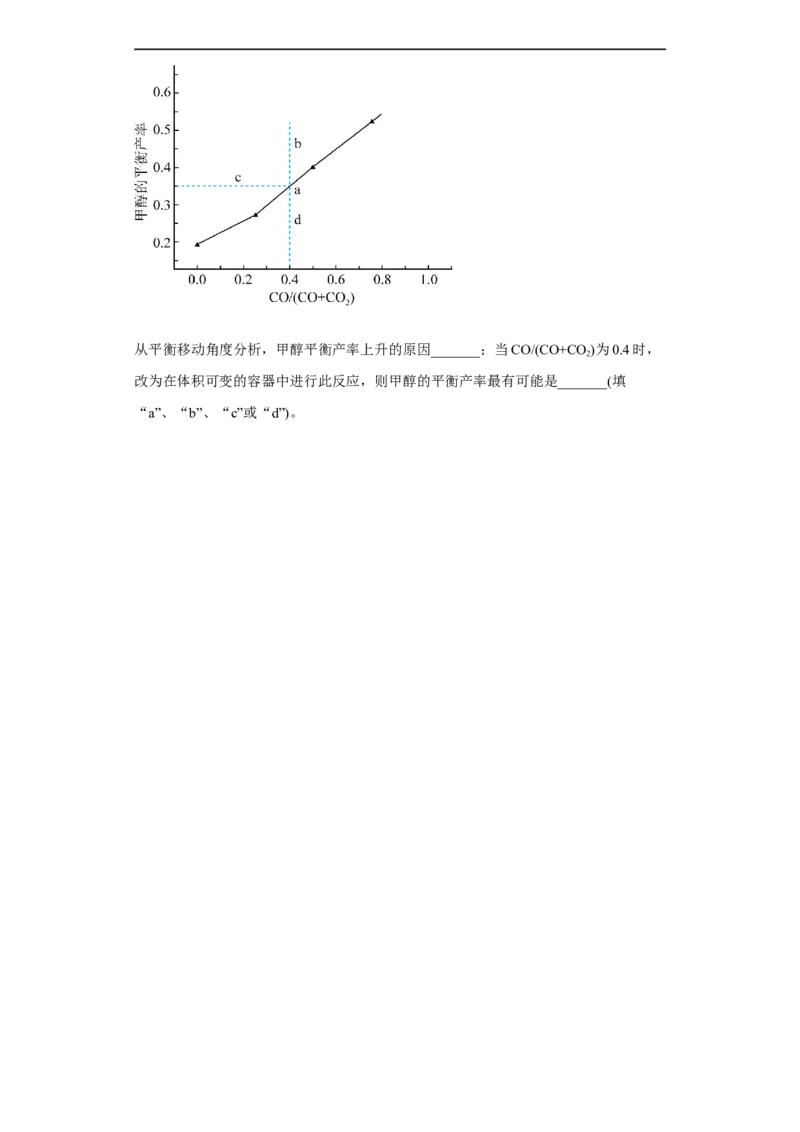
②实验表明:在二氧化碳和氢气的混合气体中掺混一氧化碳有助于提高甲醇产率。甲
醇的平衡产率随着CO/(CO+CO )变化如图所示:
2从平衡移动角度分析,甲醇平衡产率上升的原因_______;当CO/(CO+CO )为0.4时,
2
改为在体积可变的容器中进行此反应,则甲醇的平衡产率最有可能是_______(填
“a”、“b”、“c”或“d”)。答案及解析:
1.D
【详解】A.烧碱为碱,不属于氧化物,A不符合题意;
B.生石灰为氧化钙,属于氧化物,白磷为单质,胆矾为五水硫酸铜,属于化合物,不属
于混合物,B不符合题意;
C.干冰为固体二氧化碳,属于氧化物,铁为单质,氯化氢为化合物,不属于混合物,C不
符合题意;
D.水为氧化物,硫黄为硫单质,漂白粉的有效成分为次氯酸钙,属于混合物,D符合题
意;
故选D。
2.B
【解析】非金属元素的最高正价与最低负价的绝对值之和等于8。
【详解】某元素X 的最高价含氧酸的化学式为 HXO ,设X的化合价为a,则n+a+(-2)
n 2n﹣2
(2n-2)=0,解得a=3n-4,在气态氢化物中 X 显最低价,由元素的最高正价与最低负价的
绝对值之和等于8可知,在其气态氢化物中 X 的化合价为-[8-(3n-4)]=-(12-3n),答案选
B。
【注意】非金属在其气态氢化物中显最低负价,最低负价等于其主族序数-8,最高正价与
最低负价的绝对值之和等于8。
3.C
【详解】A.蒸馏实验中温度计的水银球应与蒸馏烧瓶的支管口相平,A错误;
B.酒精与水互溶,不能用于萃取碘水中的碘,B错误;
C.分液时为了避免污染,下层液体从下口流出,上层液体从上口倒出,C正确;
D.将浓 溶液逐滴加到煮沸的 溶液会得到 沉淀,D错误;
故选C。
4.B
【分析】由 可知,0.5mol铝完全反应消耗0.75mol硫酸,生成0.75mol ;由 可知,0.5mol铁完全反应消耗0.5mol硫酸,
生成0.5mol 。
【详解】A.常温常压下,气体摩尔体积不是22.4 ,则0.5mol 的体积 不是
11.2L,错误;
B.由阿伏加德罗定律可知,同温同压下,气体体积之比等于其物质的量之比,即
,正确;
C.由分析可知,铝、铁消耗的硫酸的物质的量不相等,错误;
D. 胶体粒子是由若干分子聚集在一起的集合体,故粒子数目无法计算,错误。
故选B。
5.B
【分析】由短周期主族元素 W、X、Y、Z 的原子序数依次增大,Z 的最高价氧化物对应
水化物的化学式为 HZO 可知, Z为P 元素;由 W、X、Y、Z 中只有一种金属元素,
n 2n-2
W、X、Y三种原子的最外层电子数之比为2:3:1 可知,W 为C 元素、X为O元素、Y为
Mg元素。
【详解】A.碳元素和氧元素可以形成 CO、CO 、碳酸根离子、草酸根离子等,A项错
2
误;
B.MgO 熔点很高,可作耐火材料,B项正确;
C. O的简单氢化物为HO, 在常温下为液态,C项错误;
2
D. Z元素的最高价氧化物对应的水化物是磷酸,磷酸是三元中强酸,D项错误;
故选B。
6.A
【详解】A. 中N原子的价层电子对数 ,且含有1个孤电子对, 中
N原子价层电子对数 ,且含有2个孤电子对;孤电子对之间的排斥力大于
孤电子对和成键电子对之间的排斥力,前者为三角锥形、后者为V形,则键角:前者大于
后者,故A正确;B. 中N原子价层电子对数 ,且含有1个孤电子对, 中N原子价层
电子对数 ,且不含孤电子对,空间结构:前者为三角锥形、后者为平面三
角形,故B错误;
C. 中N原子价层电子对数 , 中N原子价层电子对数
,氮原子杂化类型:前者为sp3、后者为sp2,故C错误;
D.铜离子含有空轨道、N原子含有孤电子对,所以铜离子提供空轨道、N原子提供孤电
子对形成配位键,故D错误;
故选A。
7.B
【详解】A.氯气密度比空气大,应用向上排空气法收集,d所示为向下排空气法,A错误;
B.KMnO 是固体物质,加热分解产生O,由于O 难溶于水,因此可以用排水方法或向上
4 2 2
排空气的方法收集,故可以使用a、c装置制取和收集O,B正确;
2
C.Cu与稀HNO 反应产生NO气体,NO能够与O 发生反应产生NO 气体,因此不能使
3 2 2
用排空气的方法收集,C错误;
D.CaCO 与稀硫酸反应产生的CaSO、CO 气体,CaSO 微溶于水,使反应不能持续发生,
3 4 2 4
因此不能使用该方法制取CO 气体,D错误;
2
综上所述答案为B。
8.C
【详解】A. 和 均代表正反应速率,在反应过程中反应速率之比等
于化学计量数之比,所以 ,故A错误;
B.NO(g) 2NO (g) ΔH>0,正反应为吸热反应,其他条件不变,升高温度,平衡正
2 4 2
向移动,所以NO 平衡转化率增大,故B错误;
2 4
C.容器中气体的平均相对分子质量为: ,反应物生成物均为气体所以一直不变,反应前后气体总物质的量在改变,所以容器中气体的平均相对分子质量
保持不变时即反应达平衡,故C正确;
D.加压,平衡向气体体积减小的方向移动,也就是逆向移动,但正反应速率和逆反应速
率都加快,故D错误;
答案为C。
9.A
【详解】A.氯化铁溶液蚀刻铜板: ,故正确;
B.铁粉与稀硫酸反应的离子方程式应为: ,故B错误;
C.氯化亚铁溶液中通入氯气的离子方程式应为: ,故C错误;
D.氯化镁溶液与氨水反应的离子方程式应为: ,故
D错误。
综上所述,答案为A。
10.C
【详解】A.(甲) 、(戊) 均为C H 的卤代产物,故A正确;
6 14
B.(乙) 可看做C H 的取代产物,可能存在-O-键,故B正确;
6 14
C.(甲) 、(乙) 、(丙) 、 (戊) 均为饱和烷烃C H 的取
6 14
代产物,不可能形成环状结构,(丁) 、(己) ,可能形成环状结构,故C错误;
D.(己) 可能形成具有双键的醛或酮,故D正确;
E.含有不饱和键的物质可使过锰酸钾溶液褪色,(丁) 为烯类,故E正确;
答案选C。
11.A
【详解】A.向硅酸钠溶液中滴加乙酸溶液,发生强酸制取弱酸的反应,则相同条件下,
乙酸的酸性一定比硅酸强,选项A正确;
B.在酸性条件下,硝酸根离子可氧化二氧化硫,使其转化为硫酸根离子,不能说明SO 的
2水溶液中含有一定量的 ,选项B错误;
C.测定等浓度的NaCO 和NaSO 溶液的pH,可知亚硫酸的酸性大于碳酸的酸性,亚硫
2 3 2 3
酸不是最高价含氧酸,不能比较非金属性,选项C错误;
D.氯化铁过量,不能判断是否为可逆反应,如判断是否为可逆反应,加入的KI溶液需过
量,选项D错误;
答案选A。
12.C
【分析】由图可知,该装置为电解池, 在阳极失去电子发生氧化反应生成二氧化碳
和氧气,放电生成的二氧化碳与氧离子结合生成 , 电极反应式为
, 在阴极得到电子发生还原反应生成氧离子和碳,放电生成
的氧离子捕获二氧化碳生成 ,电极反应式为 。
【详解】A.该装置是将电能转化为化学能的电解池,故A错误;
B.由分析可知,二氧化碳的捕获在阴极区完成,二氧化碳在阳极区只是参与循环,未被
捕获,故B错误;
C.由分析可知, 在阳极失去电子发生氧化反应生成二氧化碳和氧气,电极反应式为
,故C正确;
D.由阳极电极反应式可知, 在阳极失去电子发生氧化反应生成二氧化碳和氧气时,
碳元素的化合价未发生变化,故D错误;
故选C。
13.B
【详解】A.HSO 与Ba(OH) 溶液反应:Ba2++2OH-+2H++SO 2-=BaSO ↓+2HO,A
2 4 2 4 4 2
错误;
B.NaCO 溶液中通入CO 生成碳酸氢钠:CO2-+CO+HO===2HCO -,B正确;
2 3 2 3 2 2 3
C.向NaOH溶液中滴入少量Ca(HCO ) 溶液生成碳酸钙、碳酸钠和水:Ca2++2HCO -+
3 2 3
2OH-===CaCO ↓+CO2-+2HO,C错误;
3 3 2
D.CHCOOH难电离,醋酸溶液与NaOH溶液反应:CHCOOH+OH-= CHCOO-+
3 3 3HO,D错误,
2
答案选B。
14.C
【解析】该反应中,8mol氨气参加反应,2mol氨气的化合价由-3变为0价,为还原剂被氧
化发生氧化反应;
【详解】有56g N 生成,氮气的物质的量为2mol,则有4mol氨气被氧化,答案为C
2
15. 胶头滴管、100mL容量瓶 防止Fe2+和NH 水解 Fe2+
+H C O=FeC O↓+2H+ 101.48 低于40℃氧化反应速率太慢,高于40℃HO 易分
2 2 4 2 4 2 2
解 除去过量的HO 88.8% K[Fe(C O)]•3H O
2 2 3 2 4 3 2
2KC O+2FeC O+2CO ↑+6H O
2 2 4 2 4 2 2
【分析】硫酸亚铁铵溶液在草酸的作用下,可溶解,再在过氧化氢的作用下,亚铁离子被
氧化为铁离子,最终经过洗涤、干燥得到晶体。
【详解】(1)配制100mL的硫酸亚铁铵溶液,需要的玻璃仪器有:烧杯、玻璃棒、量筒、
100mL容量瓶,胶头滴管;加入硫酸,提供酸性环境,可防止Fe2+和NH 水解;
(2)硫酸亚铁铵溶液,水浴加热至100℃,滴入饱和HC O 溶液,有黄色沉淀(FeC O·2H O)
2 2 4 2 4 2
生成,反应的离子方程式为:Fe2++H C O=FeC O↓+2H+;
2 2 4 2 4
(3)已知HC O 的 , ,又该溶
2 2 4
液的pH为3.5,则溶液中 ;
(4)在“反应”中,先维持40℃水浴加热,滴加10mL6%H O 溶液,一段时间后,再微沸
2 2
2min;维持40℃水浴加热的原因是低于40℃氧化反应速率太慢,高于40℃时HO 易分解;
2 2
溶液微沸的目的是除去过量的HO;
2 2
(5)草酸合铁(III)酸钾晶体[K [Fe(C O)]·3H O]由12.5mL1.00mol·L-1的硫酸亚铁铵溶液制得,
3 2 4 3 2
二者是1:1的关系,则草酸合铁(III)酸钾晶体的理论产量为
,产品的产率为 ;
(6)草酸合铁(I)酸钾晶体光照时会发生光化学分解反应生成草酸钾和草酸亚铁,同时有气
体生成,反应的化学方程式为:K[Fe(C O)]•3H O
3 2 4 3 22KC O+2FeC O+2CO ↑+6H O。
2 2 4 2 4 2 2
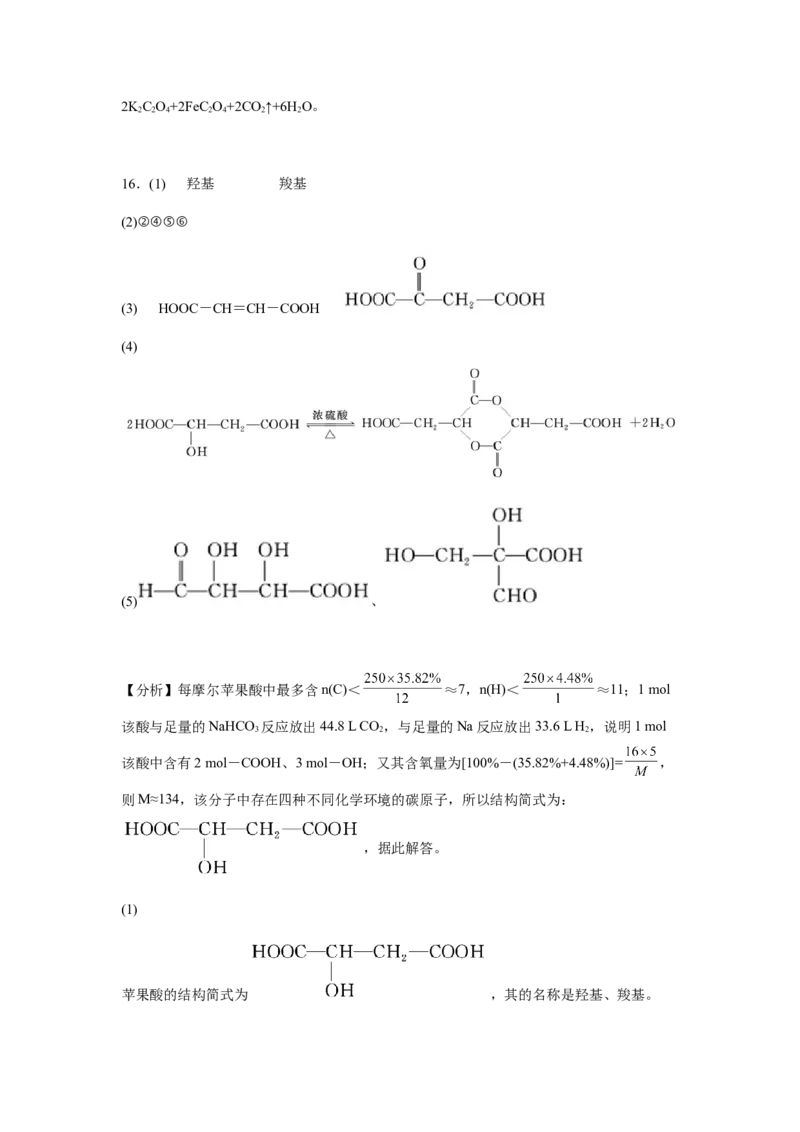
16.(1) 羟基 羧基
(2)②④⑤⑥
(3) HOOC-CH=CH-COOH
(4)
(5) 、
【分析】每摩尔苹果酸中最多含n(C)< ≈7,n(H)< ≈11;1 mol
该酸与足量的NaHCO 反应放出44.8 L CO,与足量的Na反应放出33.6 L H ,说明1 mol
3 2 2
该酸中含有2 mol-COOH、3 mol-OH;又其含氧量为[100%-(35.82%+4.48%)]= ,
则M≈134,该分子中存在四种不同化学环境的碳原子,所以结构简式为:
,据此解答。
(1)
苹果酸的结构简式为 ,其的名称是羟基、羧基。(2)
含有羟基和羧基,能发生酯化反应、氧化反应、消去反应、取代反应,不能发生加成反应
和加聚反应。答案选②④⑤⑥;
(3)
在浓硫酸的作用下发生消去反应生成B为HOOC-CH=CH-COOH;苹果酸发生催化氧
化生成C为 ;
(4)
A→D的产物是六元环,所以其反应的化学方程式为
(5)
①在一定条件下,能发生银镜反应,含有醛基;②能与苯甲酸发生酯化反应,含有羟基;
③能与乙醇发生酯化反应,含有羧基;④分子中同一碳原子不能连有2个羟基;⑤1 mol
该酸与足量的钠反应可以生成1.5 mol氢气,说明含有1个羧基、2个羟基,则符合条件的
有机物结构简式可为 、
。
17. 分液漏斗 NaSO +H SO (浓)=SO↑+H O+Na SO 氧化
2 3 2 4 2 2 2 4
性 有黄色沉淀产生 除去水中溶解的
O 开始溶液变浑浊,反应一段时间后溶液变澄清 SO 通入品红溶液中,褪色
2 2
后停止通入SO ,点燃酒精灯加热褪色后的品红溶液,溶液恢复为红色
2【分析】根据图示,装置A中浓硫酸和NaSO 反应制取SO ,生成的SO 通入到B中HS
2 3 2 2 2
溶液中,二者发生氧化还原反应生成S单质和水,出现黄色沉淀,再通入装置C中浓硫酸
进行吸水干燥,装置D收集SO ,由于二氧化硫有毒,会污染大气,则用E装置氢氧化钠
2
溶液吸收SO ,进行尾气处理,将收集的SO 通入到NaS和NaCO 的混合溶液中发生反应
2 2 2 2 3
,制得NaSO 溶液,经蒸发浓缩,冷却结晶,过
2 2 3
滤、真空干燥,得到NaSO·5H O晶体。
2 2 3 2
【详解】(1)①根据仪器的构造,仪器X的名称是分液漏斗;
②装置A中浓硫酸和NaSO 反应制取SO ,反应的化学方程为
2 3 2
NaSO +H SO (浓)=SO↑+H O+Na SO ;
2 3 2 4 2 2 2 4
③生成的SO 通入到B中HS溶液中,二者发生氧化还原反应生成S单质和水,SO 中S元
2 2 2
素由+4价变为0价,化合价降低,得电子,被还原,作氧化剂,目的是验证SO 具有氧化
2
性,产生的现象是有黄色沉淀产生,反应的化学方程式为 ;
(2)①水中溶解由氧气,能氧化产物,则在配制NaS和NaCO 混合溶液前需先将蒸馏水加
2 2 3
热煮沸一段时间后再用,其目的是除去水中溶解的O;
2
②Na SO 的制备过程中,通入的二氧化硫可与混合溶液中的S2-反应生成S单质,则烧瓶中
2 2 3
出现可能的现象是开始溶液变浑浊,反应一段时间后溶液变澄清;
(3)SO 具有漂白性,能与品红发生络合反应生成不稳定的络合物,使品红溶液褪色,因此
2
将SO 通入品红溶液中,褪色后停止通入SO ,点燃酒精灯加热褪色后的品红溶液,溶液
2 2
恢复为红色,说明SO 与品红反应具有可逆性。
2
18.(1)+41
(2) CO <
(3)BD
(4) 增加CO,反应③正移;反应②平衡逆移。HO(g)消耗、
2
CO(g)和H(g)增加,反应①正移,从而使得甲醇的平衡产率随着一氧化碳掺混比例的增加
2 2
而上升 b
【解析】(1)
依据盖斯定律,反应②=反应①-反应③,则△H=△H-△H,代入数据求得
2 1 3
△H=+41kJ·mol-1。
2(2)
①反应①是放热反应,反应②是吸热反应,升高温度反应①逆向移动、反应②正向移动,
一氧化碳的物质的量增大,因此X代表CO。
②由图示可知,温度为T时,反应物二氧化碳和氢气的物质的量均大于生成物一氧化碳和
水的物质的量,则反应②的平衡常数K<1。
(3)
A.加入适量一氧化碳,反应③平衡正向移动,若以反应③为主,则能提高甲醇平衡产率,
A错误;
B.使用高效催化剂,能缩短达到平衡的时间,但平衡不移动,一定不能提高甲醇平衡产
率,B正确;
C.循环利用原料气,相当于增大二氧化碳和氢气的量,反应①、③均正向移动,能提高
甲醇平衡产率,C错误;
D.升高温度,反应①、③均逆向移动,一定不能提高甲醇平衡产率,D正确;
E.增大压强,反应①、③均正向移动,能提高甲醇平衡产率,E错误;
答案选BD。
(4)
①恒温恒容条件下,物质的量与压强呈正比,初始二氧化碳与氢气物质的量之比为1:1、总
压为PkPa,则初始二氧化碳和氢气分压都为 PkPa,总反应为:CO(g)+3H(g)
0 0 2 2
CHOH(g)+H O(g),依据碳元素守恒,平衡时二氧化碳的分压为( P-P )kPa,依据氢元素
3 2 0 1
守恒,平衡时氢气分压为( P-2P -P )kPa,则反应①压强平衡常数 =
0 2 1
kPa-2。
②由反应可知,增加CO,反应平衡③正移;反应②平衡逆移,HO(g)消耗、CO(g)和
2 2
H(g)增加,反应①正移,从而使得甲醇的平衡产率随着一氧化碳掺混比例的增加而上升;
2
当CO/(CO+CO )为0.4时,由于总反应是气体体积减小的反应,若改为在体积可变的容器
2
中进行此反应,容器体积会减小,相当于给反应加压,平衡正向移动,甲醇的平衡转化率
升高,最有可能是b。