文档内容
河北省“五个一”名校联盟
2023 届高三年级联考(2022.12)
化学试卷
命题单位:唐山市第一中学
(满分:100分,测试时间:75分钟)
可能用到的原子量:H-1、 C-12、 N-14、 O-16、 Al-27、Ti-48、 Fe-56
一、选择题:本题共9小题,每小题3分,共27分,在每小题给出的四个选项中,只有一项是符合题目要
求的。
1. 北京冬奥会彰显了我国的科技实力,下列说法不正确的是
A. 冬奥会采用氢能源保障车有利于“碳达峰”、“碳中和”战略的实施
B. “飞扬”火炬喷口外壳采用聚硅氮烷树脂,该树脂属于无机聚合物
C. 冬奥礼仪服装用到的石墨烯材料既能导热又能导电,石墨烯和碳纳米管互为同分异构体
D. 国家速滑馆采用的硫化镉发电玻璃,可将太阳能转化为电能
2.下列有关物质性质与应用的对应关系正确的是
选项 性质 实际应用
A 小苏打不稳定,受热分解生成CO 用于泡沫灭火器
2
B 聚乙炔是无限延伸的线状结构 用于导电材料
C Al(OH) 受热分解,生成高熔点物质和水 用作塑料的阻燃剂
3
D 石墨是混合型晶体,含大π键 用作润滑剂
3.关于下列仪器使用的说法不正确的是
A.②、④均标有使用温度
B.①、③、④可用作反应容器
C.③、⑤可用于物质分离
D.①、③可加热
4. 设N 为阿伏加德罗常数的值。下列说法不正确的是
A
化学 第1页 共8页A.14 g 聚丙烯中含C—H键的总数目为2N
A
B.常温常压下,22 g 由N O和CO 组成的混合气体中含有的原子数目为1.5N
2 2 A
C.加热条件下,56 g Fe与足量浓硝酸充分反应,转移的电子数为3N
A
D.0.04 g 2H与0.06 g 3H合成4He时,释放1n的数目为0.01N
1 1 2 0 A
5.短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外电子只有一种自旋取向,Y、Z两种原
子均满足s能级上的电子总数与p能级上电子总数相等,W原子的价电子中,在不同形状的原子轨道中
运动的电子数之比为2:1。下列说法正确的是
A.W的第一电离能比同周期相邻元素的小
B.原子半径:r(X)<r(Y)<r(Z)<r(W)
C.工业上电解熔融化合物ZY制备单质Z
D.Y的氢化物为只含极性共价键的极性分子
6.下列离子方程式正确的是
A.电解MgCl 水溶液:2H O+2Cl - 2OH -+H ↑+Cl ↑
2 2 2 2
B.磁性氧化铁溶于HI 溶液:Fe O +8H+=2Fe3++Fe2++4H O
3 4 2
C. 少量SO 通入Ca(ClO) 溶液中:Ca2++2ClO - +2SO +2H O=CaSO +SO 2-+2Cl - +4H+
2 2 2 2 4 4
D.用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO -=3Ag++NO↑+2H O
3 2
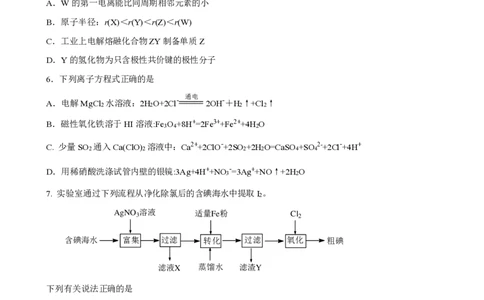
7. 实验室通过下列流程从净化除氯后的含碘海水中提取I 。
2
化学 第2页 共8页
含 碘 海 水
A g N
富
O
集
3 溶 液
滤
过
液
滤
X
适
蒸
量
转
馏
F
化
e
水
粉
滤
过
渣
滤
Y
氧
C l2
化 粗 碘
通电
下列有关说法正确的是
A. 转化过程的离子方程式为Fe+2Ag+=Fe2++2Ag
B. 氧化时,理论上通入氯气的量至少控制为溶液中溶质物质的量的1.5倍
C. 用稀HNO 溶解滤渣Y得到的溶液可循环利用
3
D. 制得的粗碘可先溶于水,再用酒精萃取进一步提纯
8. 下列实验的“操作和现象”与“推测或结论”对应关系正确的是选项 操作和现象 推测或结论
发生的离子反应为:
A 向H O 溶液中加入几滴FeCl 溶液,溶液中产生气泡
2 2 3
2Fe3++H O =O ↑+2Fe2++2H+
2 2 2
B 用铁丝蘸取少量某溶液进行焰色反应,火焰呈黄色 该溶液含有钠盐
向Al与Fe O 反应后的固体产物中先加稀硫酸溶解,再 无法证明反应后固体产物中是否
2 3
C
加入几滴KSCN溶液,溶液不变红 含有Fe O
2 3
向无水乙醇中加入浓硫酸,加热至170℃,将产生的气体
D 使溶液褪色的气体是乙烯
通入酸性高锰酸钾溶液,红色褪去
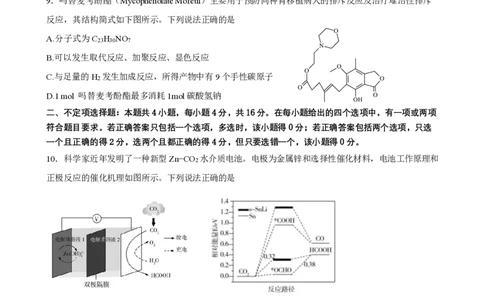
9.吗替麦考酚酯(Mycophenolate Mofetil)主要用于预防同种肾移植病人的排斥反应及治疗难治性排斥
反应,其结构简式如下图所示。下列说法正确的是
A.分子式为C H NO
23 30 7
B.可以发生取代反应、加聚反应、显色反应
C.与足量的H 发生加成反应,所得产物中有9个手性碳原子
2
D.1 mol 吗替麦考酚酯最多消耗1mol碳酸氢钠
二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两项
符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选
一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
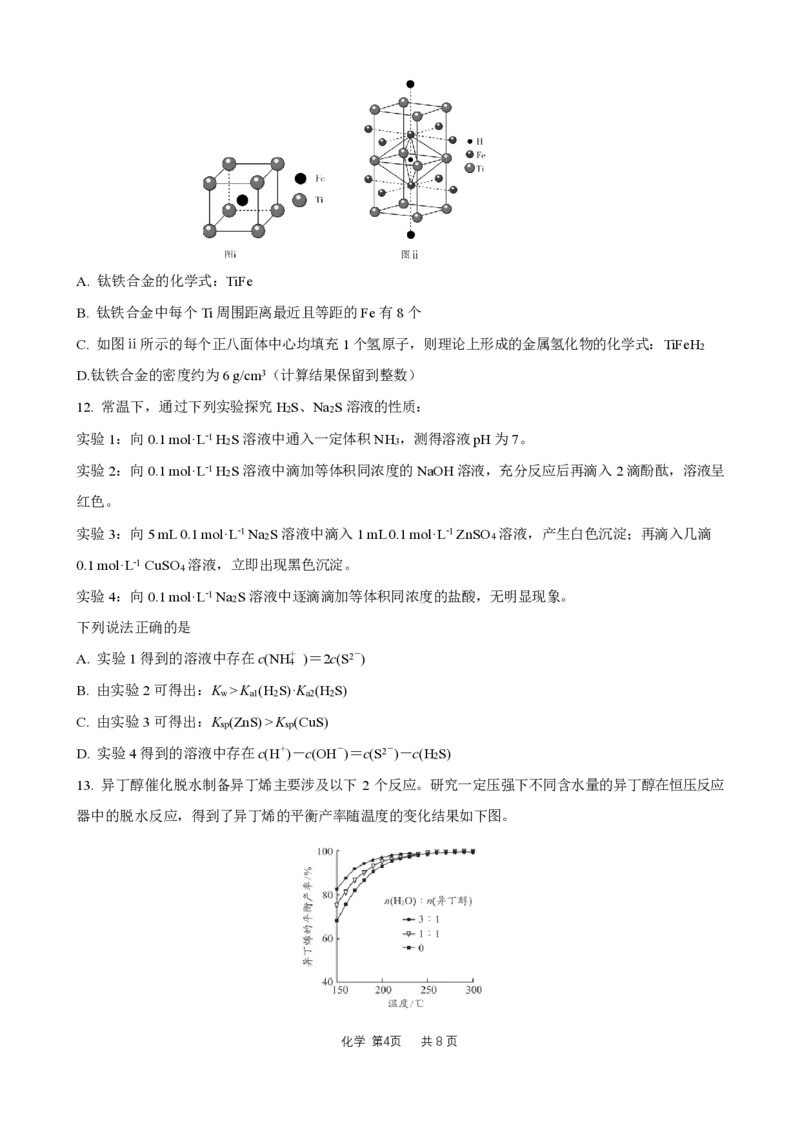
10.科学家近年发明了一种新型Zn−CO 水介质电池。电极为金属锌和选择性催化材料,电池工作原理和
2
正极反应的催化机理如图所示。下列说法正确的是
A.充电时,正极的电极反应式为HCOOH-2e-=CO ↑+2H+
2
B.放电时,负极周围溶液的pH降低
C.使用催化剂Sn或者s-SnLi均能有效减少副产物CO的生成
D.使用s-SnLi催化剂,中间产物更稳定
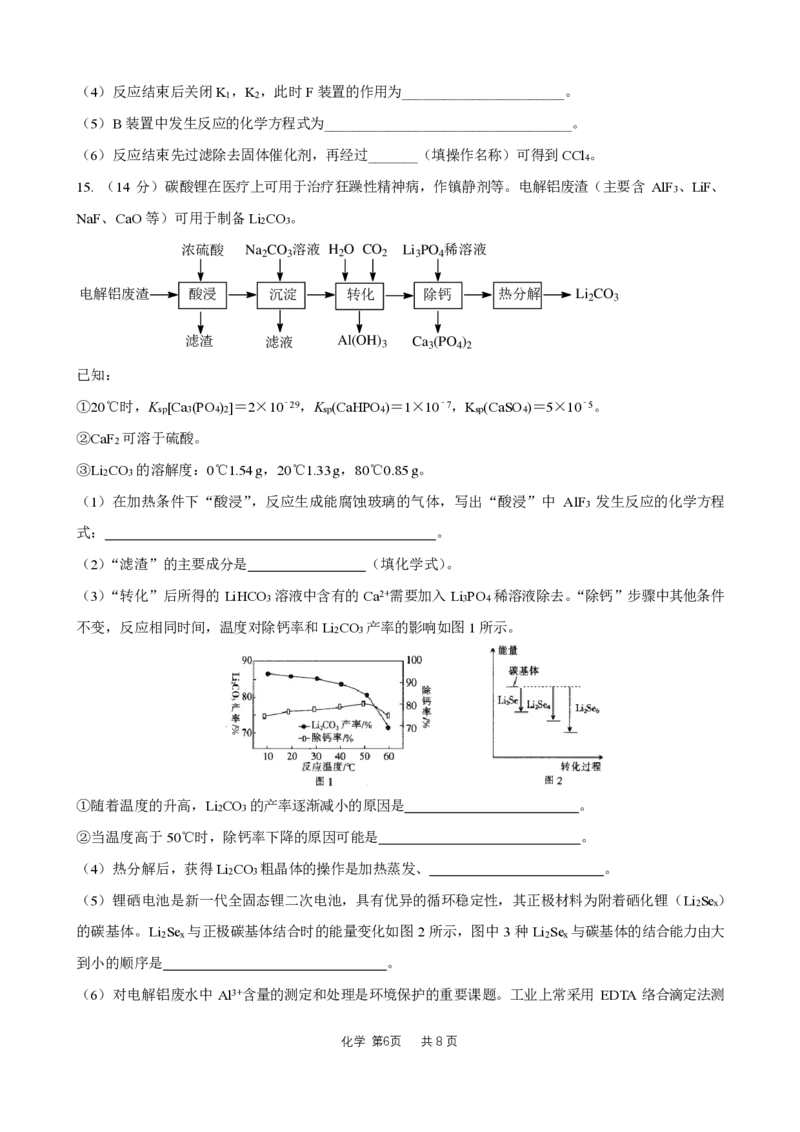
11. 钛铁基储氢合金是由钛、铁两种元素组成的金属化合物。一种钛铁合金的晶胞如图ⅰ所示,晶胞边长
约为3×10-10 m,该合金吸收的氢原子位于如图所示的正八面体的中心,氢被4个钛原子和2个铁原子包
围,如图ⅱ所示。下列说法不正确的是
...
化学 第3页 共8页
O
O
N
O
O
O H
O
OA. 钛铁合金的化学式:TiFe
B. 钛铁合金中每个Ti周围距离最近且等距的Fe有8个
C. 如图ⅱ所示的每个正八面体中心均填充1个氢原子,则理论上形成的金属氢化物的化学式:TiFeH
2
D.钛铁合金的密度约为6 g/cm3(计算结果保留到整数)
12. 常温下,通过下列实验探究H S、Na S溶液的性质:
2 2
实验1:向0.1 mol·L-1 H S溶液中通入一定体积NH ,测得溶液pH为7。
2 3
实验2:向0.1 mol·L-1 H S溶液中滴加等体积同浓度的NaOH溶液,充分反应后再滴入2滴酚酞,溶液呈
2
红色。
实验3:向5 mL 0.1 mol·L-1 Na S溶液中滴入1 mL 0.1 mol·L-1 ZnSO 溶液,产生白色沉淀;再滴入几滴
2 4
0.1 mol·L-1 CuSO 溶液,立即出现黑色沉淀。
4
实验4:向0.1 mol·L-1 Na S溶液中逐滴滴加等体积同浓度的盐酸,无明显现象。
2
下列说法正确的是
A. 实验1得到的溶液中存在c(NH+ )=2c(S2-)
4
B. 由实验2可得出:K > K (H S)·K (H S)
w a1 2 a2 2
C. 由实验3可得出:K (ZnS) > K (CuS)
sp sp
D. 实验4得到的溶液中存在c(H+)-c(OH-)=c(S2-)-c(H S)
2
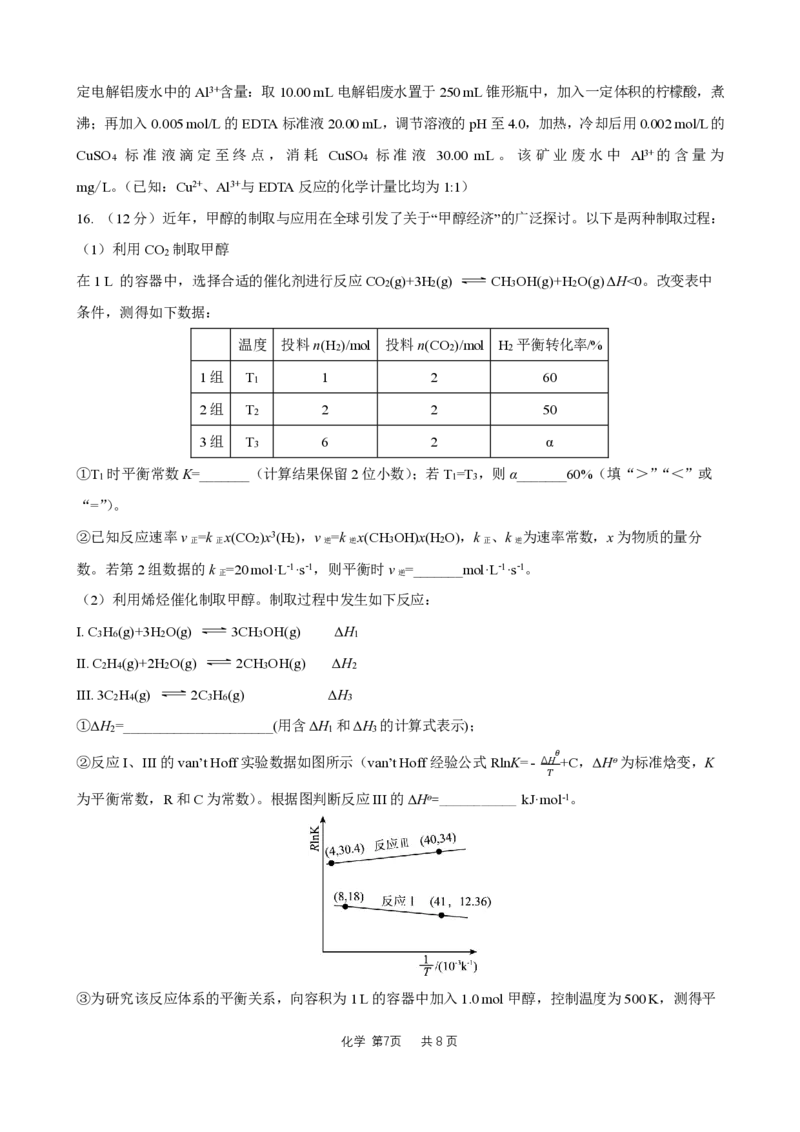
13. 异丁醇催化脱水制备异丁烯主要涉及以下 2 个反应。研究一定压强下不同含水量的异丁醇在恒压反应
器中的脱水反应,得到了异丁烯的平衡产率随温度的变化结果如下图。
化学 第4页 共8页①
化学 第5页 共8页
C H
3
C
C
H
H
3
C H
2
O H ( g ) C H
3
C
C
H
3
C H
2
( g ) + H
2
O ( g )
ΔH = + 28 kJ/mol K (190℃)= 104
1 1
CH 3 CH 3 CH 3
② 2 CH 3 C CH 2 (g) CH 3 C CHC CH 3 (g) ΔH = -72 kJ/mol K (190 ℃)=0.1
2 2
CH
3
二聚异丁烯
下列说法不正确的是
A.其他条件不变时,在催化剂的活性温度内,升高温度有利于异丁烯的制备
B.高于190 ℃时,温度对异丁烯的平衡产率影响不大的原因是K>104、K <0.1
1 2
C. 190℃时,增大n(H O):n(异丁醇),不利于反应②的进行
2
D.若只有异丁烯、水和二聚异丁烯生成,则初始物质浓度c 与流出物质浓度c之间存在: c (异丁醇) =c(异
0 0
丁烯)+2c(二聚异丁烯)
三、非选择题:本题共4小题,共57分。
14.(16分)四氯化碳主要用作优良的溶剂、干洗剂、灭火剂、制冷剂、香料的浸出剂以及农药等,也可
用于有机合成,工业上可用二硫化碳与氯气反应制取四氯化碳。某化学小组用下图实验装置模拟工业制
备四氯化碳。
已知:
①CS 可与溴水反应生成硫酸和氢溴酸;
2
②CS 与Cl 在铁作催化剂的条件下,在85℃~95℃反应可生成四氯化碳;
2 2
③硫单质的沸点445℃,CS 的沸点46.5℃,CCl 的沸点76.8℃、密度1.6 g/cm3。
2 4
(1)CS 分子的空间结构为___________;其中C的杂化轨道类型为__________;写出两个与CS 具有相
2 2
同空间结构和键合形式的分子或离子__________、___________。
(2)上述仪器的连接顺序为a→____→_______→_______→_______→_______→_______→_______→
_______→_______。
A装置中导管k的作用为________________________。
(3)A装置中发生反应的离子方程式为____________________(K Cr O 写成K+、Cr O 2-,其还原产物
2 2 7 2 7
为Cr3+)。(4)反应结束后关闭K ,K ,此时F装置的作用为_______________________。
1 2
(5)B装置中发生反应的化学方程式为___________________________________。
(6)反应结束先过滤除去固体催化剂,再经过_______(填操作名称)可得到CCl 。
4
15. (14 分)碳酸锂在医疗上可用于治疗狂躁性精神病,作镇静剂等。电解铝废渣(主要含 AlF 、LiF、
3
NaF、CaO等)可用于制备Li CO 。
2 3
化学 第6页 共8页
电 解 铝 废 渣
浓
酸
滤
硫
浸
渣
酸 N a C
2
沉
滤
O
3
淀
液
溶 液 H
2
A
O
转
l( O
C
化
H
O
)
2
3
L i3
C
P
除
a
O
3
4
钙
( P
稀
O
溶
)
4 2
液
热 分 解 L i2 C O
3
已知:
①20℃时,K [Ca (PO )]=2×10﹣29,K (CaHPO )=1×10﹣7,K (CaSO )=5×10﹣5。
sp 3 4 2 sp 4 sp 4
②CaF 可溶于硫酸。
2
③Li CO 的溶解度:0℃1.54 g,20℃1.33 g,80℃0.85 g。
2 3
(1)在加热条件下“酸浸”,反应生成能腐蚀玻璃的气体,写出“酸浸”中 AlF 发生反应的化学方程
3
式: 。
(2)“滤渣”的主要成分是 (填化学式)。
(3)“转化”后所得的 LiHCO 溶液中含有的 Ca2+需要加入 Li PO 稀溶液除去。“除钙”步骤中其他条件
3 3 4
不变,反应相同时间,温度对除钙率和Li CO 产率的影响如图1所示。
2 3
①随着温度的升高,Li CO 的产率逐渐减小的原因是 。
2 3
②当温度高于50℃时,除钙率下降的原因可能是 。
(4)热分解后,获得Li CO 粗晶体的操作是加热蒸发、 。
2 3
(5)锂硒电池是新一代全固态锂二次电池,具有优异的循环稳定性,其正极材料为附着硒化锂(Li Se)
2 x
的碳基体。Li Se 与正极碳基体结合时的能量变化如图2 所示,图中3种Li Se 与碳基体的结合能力由大
2 x 2 x
到小的顺序是 。
(6)对电解铝废水中 Al3+含量的测定和处理是环境保护的重要课题。工业上常采用 EDTA 络合滴定法测定电解铝废水中的Al3+含量:取10.00 mL电解铝废水置于250 mL锥形瓶中,加入一定体积的柠檬酸,煮
沸;再加入0.005 mol/L的EDTA标准液20.00 mL,调节溶液的pH至4.0,加热,冷却后用0.002 mol/L的
CuSO 标 准 液滴定至终点,消耗 CuSO 标准 液 30.00 mL 。 该 矿业废水中 Al3+的含量为
4 4
mg/L。(已知:Cu2+、Al3+与EDTA反应的化学计量比均为1:1)
16. (12分)近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨。以下是两种制取过程:
(1)利用CO 制取甲醇
2
在1 L 的容器中,选择合适的催化剂进行反应CO (g)+3H (g) CH OH(g)+H O(g) ΔH<0。改变表中
2 2 3 2
条件,测得如下数据:
温度 投料n(H )/mol 投料n(CO )/mol H 平衡转化率/%
2 2 2
1组 T 1 2 60
1
2组 T 2 2 50
2
3组 T 6 2 α
3
①T 时平衡常数K=_______(计算结果保留2位小数);若T =T ,则α_______60%(填“>”“<”或
1 1 3
“=”)。
②已知反应速率v =k x(CO )x3(H ),v =k x(CH OH)x(H O),k 、k 为速率常数,x为物质的量分
正 正 2 2 逆 逆 3 2 正 逆
数。若第2组数据的k =20 mol·L-1·s-1,则平衡时v =_______mol·L-1·s-1。
正 逆
(2)利用烯烃催化制取甲醇。制取过程中发生如下反应:
I. C H (g)+3H O(g) 3CH OH(g) ΔH
3 6 2 3 1
II. C H (g)+2H O(g) 2CH OH(g) ΔH
2 4 2 3 2
III. 3C H (g) 2C H (g) ΔH
2 4 3 6 3
①ΔH =_____________________(用含ΔH 和ΔH 的计算式表示);
2 1 3
𝜃
②反应I、III的van’t Hoff实验数据如图所示(van’t Hoff经验公式RlnK= - ΔH+C,ΔHɵ为标准焓变,K
𝑇
为平衡常数,R和C为常数)。根据图判断反应III的ΔHɵ=___________ kJ·mol-1。
③为研究该反应体系的平衡关系,向容积为1 L的容器中加入1.0 mol甲醇,控制温度为500 K,测得平
化学 第7页 共8页衡时,甲醇的转化率为0.8,乙烯的物质的量为0.1 mol,则R的数值为_______。(计算结果保留1位小
数,已知:lge=0.43,lg5=0.7)
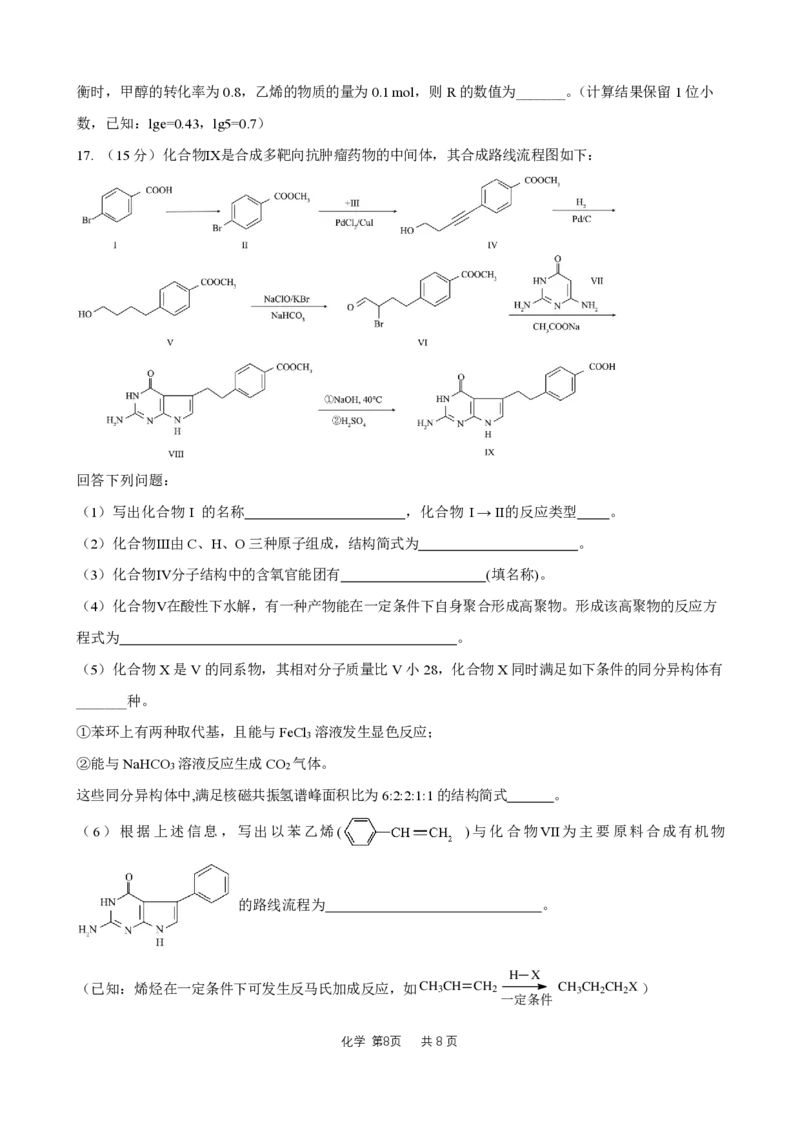
17. (15分)化合物Ⅸ是合成多靶向抗肿瘤药物的中间体,其合成路线流程图如下:
回答下列问题:
(1)写出化合物 Ⅰ 的名称 ,化合物 Ⅰ → Ⅱ的反应类型 。
(2)化合物Ⅲ由C、H、O三种原子组成,结构简式为 。
(3)化合物Ⅳ分子结构中的含氧官能团有 (填名称)。
(4)化合物Ⅴ在酸性下水解,有一种产物能在一定条件下自身聚合形成高聚物。形成该高聚物的反应方
程式为 。
(5)化合物X是V的同系物,其相对分子质量比V小28,化合物X同时满足如下条件的同分异构体有
_______种。
①苯环上有两种取代基,且能与FeCl 溶液发生显色反应;
3
②能与NaHCO 溶液反应生成CO 气体。
3 2
这些同分异构体中,满足核磁共振氢谱峰面积比为6:2:2:1:1的结构简式 。
(6)根据上述信息,写出以苯乙烯( )与化合物Ⅶ为主要原料合成有机物
的路线流程为 。
H X
(已知:烯烃在一定条件下可发生反马氏加成反应,如CH
3
CH CH
2
CH
3
CH
2
CH
2
X)
一定条件
化学 第8页 共8页