文档内容
2023 年常德市高三年级模拟考试
化 学
可能用到的相对原子质量:H-1 C-14 O-16 Na-23 S-32 V-51
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只
有一项是符合题目要求。
1.我国自主研发的“海水无淡化原位直接电解制氢”开辟了全球海水制氢的全新路径,
该技术集“海上风电等能源利用-海水资源利用-氢能生产”为一体,下列有关说法不正
确的是
A.实验室可用蒸馏法将海水淡化
B.绿色零碳氢能是未来能源发展的重要方向
C.该技术所用到的“多孔聚四氟乙烯膜”属于无机非金属材料
D.该技术解决了有害腐蚀性这一长期困扰海水制氢领域的问题
2.我们所感受的各种情绪从本质上讲都是一种化学体验,多巴胺和去甲肾上腺素均属
于神经递质。下列有关两者说法正确的是
A.两者属于同系物
B.等物质的量的两者均能和3mol氢气发
生加成反应
C.去甲肾上腺素的相对分子质量比多巴胺大17
D.1mol去甲肾上腺素最多消耗NaOH的质量与1mol多巴胺所消耗的相等
3.化学实验是人们对知识的获取、验证和创新的重要手段。以下试剂的选择不合理的是
A.实验室可用浓盐酸、二氧化锰、浓硫酸、饱和食盐水制备纯净的氯气
B.用二氧化碳和饱和碳酸氢钠溶液可做喷泉实验
C.可用过氧化钠或次氯酸漂白某些有色物质
D.可利用FeCl 溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀
3
4.乙炔水化法、乙烯氧化法是工业上制备乙醛的两个重要方法,反应原理分别为:
以下叙述不正确的是
A.乙烯氧化法中,生成0.1mol乙醛时,转移的电子数约为1.204×1024
B.C H 的电子式为
2 4
C.根据价层电子互斥模型,18g水的中心原子含有2mol孤电子对
D.标准状况下,11.2L C H 中含有π键的数目约为6.02×1023
2 2
5.作为储氢材料的镧镍合金被广泛应用于电动车辆,某种镧镍合金储氢后所得晶体的
化学式为LaNi H ,晶胞结构如图,晶胞参数为a,下列有关表述不正确的是
5 6
A.Z表示的微粒为H
2
B.每个X原子周围最近且等距离的X原子有6个
C.若A的分数坐标为(0,0.5,0.5),B的分数坐标为
(0.75,0.75,0),则C的分数坐标为(1,0.5,1)
D.若四条竖直棱的棱心位置均插入Z,则晶体的化学式
为LaNi H
5 7
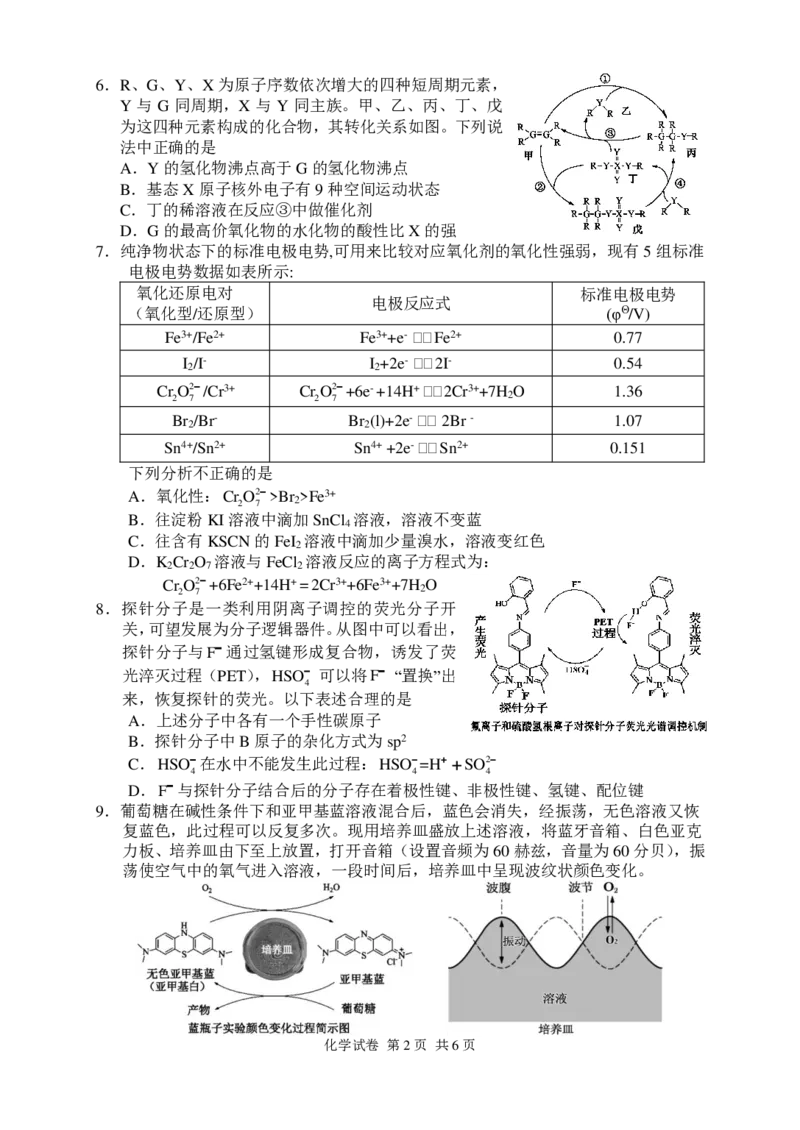
化学试卷 第1页 共6页6.R、G、Y、X为原子序数依次增大的四种短周期元素,
Y 与 G 同周期,X 与 Y 同主族。甲、乙、丙、丁、戊
为这四种元素构成的化合物,其转化关系如图。下列说
法中正确的是
A.Y的氢化物沸点高于G的氢化物沸点
B.基态X原子核外电子有9种空间运动状态
C.丁的稀溶液在反应③中做催化剂
D.G的最高价氧化物的水化物的酸性比X的强
7.纯净物状态下的标准电极电势,可用来比较对应氧化剂的氧化性强弱,现有5组标准
电极电势数据如表所示:
氧化还原电对 标准电极电势
电极反应式
(氧化型/还原型) (φΘ/V)
Fe3+/Fe2+ Fe3++e- ⥫⥫ Fe2+ 0.77
I /I- I +2e- ⥫⥫ 2I- 0.54
2 2
CrO2/Cr3+ CrO2+6e- +14H+ ⥫⥫ 2Cr3++7H O 1.36
2 7 2 7 2
Br /Br- Br (l)+2e- ⥫⥫ 2Br - 1.07
2 2
Sn4+/Sn2+ Sn4+ +2e- ⥫⥫ Sn2+ 0.151
下列分析不正确的是
A.氧化性:CrO2>Br >Fe3+
2 7 2
B.往淀粉KI溶液中滴加SnCl 溶液,溶液不变蓝
4
C.往含有KSCN的FeI 溶液中滴加少量溴水,溶液变红色
2
D.K Cr O 溶液与FeCl 溶液反应的离子方程式为:
2 2 7 2
CrO2+6Fe2++14H+ = 2Cr3++6Fe3++7H O
2 7 2
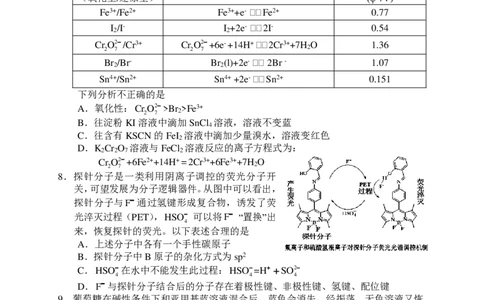
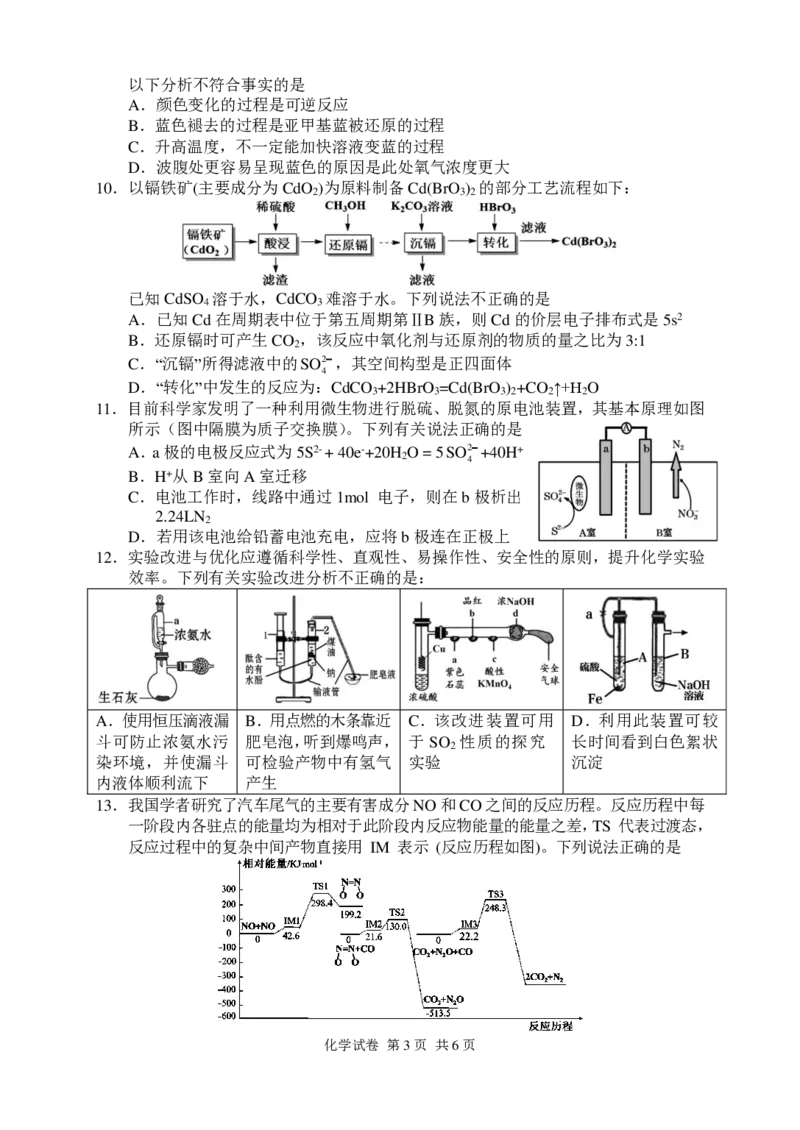
8.探针分子是一类利用阴离子调控的荧光分子开
关,可望发展为分子逻辑器件。从图中可以看出,
探针分子与F 通过氢键形成复合物,诱发了荧
光淬灭过程(PET),HSO 可以将F “置换”出
4
来,恢复探针的荧光。以下表述合理的是
A.上述分子中各有一个手性碳原子
B.探针分子中B原子的杂化方式为sp2
C.HSO在水中不能发生此过程:HSO=H SO2
4 4 4
D.F与探针分子结合后的分子存在着极性键、非极性键、氢键、配位键
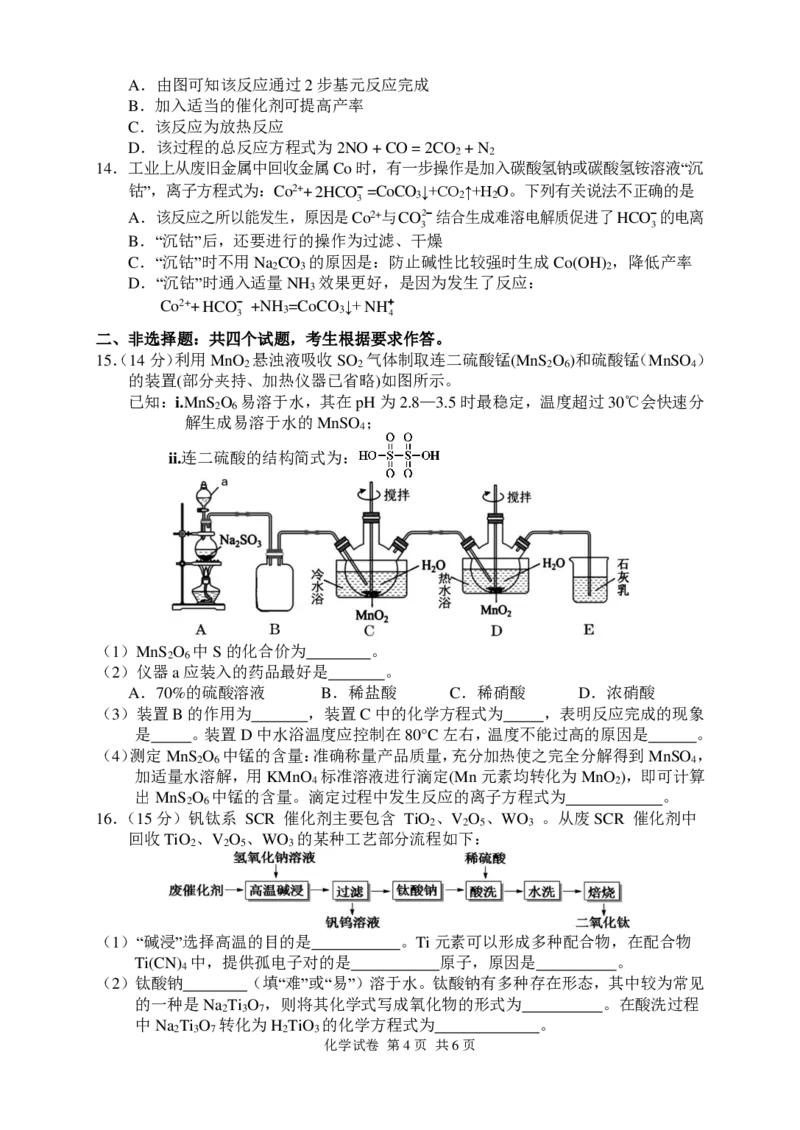
9.葡萄糖在碱性条件下和亚甲基蓝溶液混合后,蓝色会消失,经振荡,无色溶液又恢
复蓝色,此过程可以反复多次。现用培养皿盛放上述溶液,将蓝牙音箱、白色亚克
力板、培养皿由下至上放置,打开音箱(设置音频为60赫兹,音量为60分贝),振
荡使空气中的氧气进入溶液,一段时间后,培养皿中呈现波纹状颜色变化。
化学试卷 第2页 共6页以下分析不符合事实的是
A.颜色变化的过程是可逆反应
B.蓝色褪去的过程是亚甲基蓝被还原的过程
C.升高温度,不一定能加快溶液变蓝的过程
D.波腹处更容易呈现蓝色的原因是此处氧气浓度更大
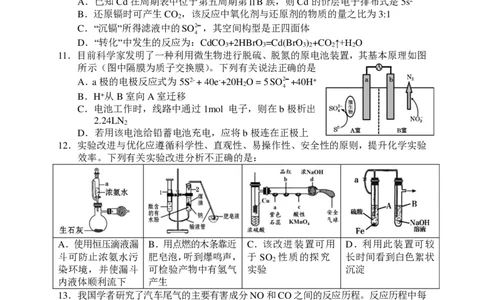
10.以镉铁矿(主要成分为CdO )为原料制备Cd(BrO ) 的部分工艺流程如下:
2 3 2
已知CdSO 溶于水,CdCO 难溶于水。下列说法不正确的是
4 3
A.已知Cd在周期表中位于第五周期第ⅡB族,则Cd的价层电子排布式是5s2
B.还原镉时可产生CO ,该反应中氧化剂与还原剂的物质的量之比为3:1
2
C.“沉镉”所得滤液中的SO2,其空间构型是正四面体
4
D.“转化”中发生的反应为:CdCO +2HBrO =Cd(BrO ) +CO ↑+H O
3 3 3 2 2 2
11.目前科学家发明了一种利用微生物进行脱硫、脱氮的原电池装置,其基本原理如图
所示(图中隔膜为质子交换膜)。下列有关说法正确的是
A.a极的电极反应式为5S2- + 40e-+20H O = 5SO2+40H+
2 4
B.H+从B室向A室迁移
C.电池工作时,线路中通过1mol 电子,则在b极析出
2.24LN
2
D.若用该电池给铅蓄电池充电,应将b极连在正极上
12.实验改进与优化应遵循科学性、直观性、易操作性、安全性的原则,提升化学实验
效率。下列有关实验改进分析不正确的是:
A.使用恒压滴液漏 B.用点燃的木条靠近 C.该改进装置可用 D.利用此装置可较
斗可防止浓氨水污 肥皂泡,听到爆鸣声, 于 SO 性质的探究 长时间看到白色絮状
2
染环境,并使漏斗 可检验产物中有氢气 实验 沉淀
内液体顺利流下 产生
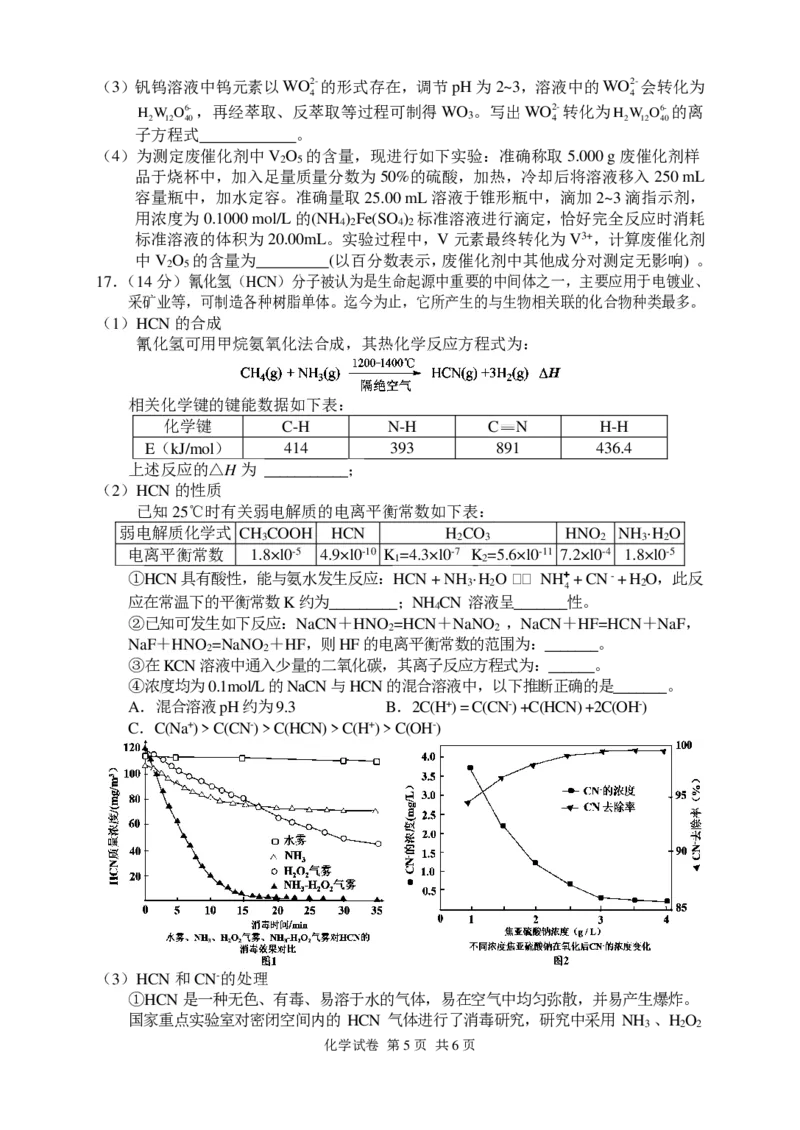
13.我国学者研究了汽车尾气的主要有害成分NO和CO之间的反应历程。反应历程中每
一阶段内各驻点的能量均为相对于此阶段内反应物能量的能量之差,TS 代表过渡态,
反应过程中的复杂中间产物直接用 IM 表示 (反应历程如图)。下列说法正确的是
化学试卷 第3页 共6页A.由图可知该反应通过2步基元反应完成
B.加入适当的催化剂可提高产率
C.该反应为放热反应
D.该过程的总反应方程式为2NO + CO = 2CO + N
2 2
14.工业上从废旧金属中回收金属Co时,有一步操作是加入碳酸氢钠或碳酸氢铵溶液“沉
钴”,离子方程式为:Co2++2HCO=CoCO ↓+CO ↑+H O。下列有关说法不正确的是
3 3 2 2
A.该反应之所以能发生,原因是Co2+与CO2结合生成难溶电解质促进了HCO的电离
3 3
B.“沉钴”后,还要进行的操作为过滤、干燥
C.“沉钴”时不用Na CO 的原因是:防止碱性比较强时生成Co(OH) ,降低产率
2 3 2
D.“沉钴”时通入适量NH 效果更好,是因为发生了反应:
3
Co2++HCO +NH =CoCO ↓+NH
3 3 3 4
二、非选择题:共四个试题,考生根据要求作答。
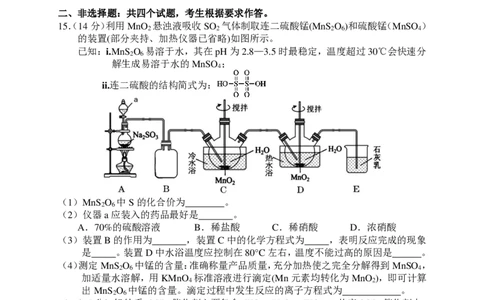
15.(14分)利用MnO 悬浊液吸收SO 气体制取连二硫酸锰(MnS O )和硫酸锰(MnSO )
2 2 2 6 4
的装置(部分夹持、加热仪器已省略)如图所示。
已知:i.MnS O 易溶于水,其在pH为2.8—3.5时最稳定,温度超过30℃会快速分
2 6
解生成易溶于水的MnSO ;
4
ii.连二硫酸的结构简式为:
(1)MnS O 中S的化合价为 。
2 6
(2)仪器a应装入的药品最好是 。
A.70%的硫酸溶液 B.稀盐酸 C.稀硝酸 D.浓硝酸
(3)装置B的作用为 ,装置C中的化学方程式为 ,表明反应完成的现象
是 。装置D中水浴温度应控制在80°C左右,温度不能过高的原因是 。
(4)测定MnS O 中锰的含量:准确称量产品质量,充分加热使之完全分解得到MnSO ,
2 6 4
加适量水溶解,用KMnO 标准溶液进行滴定(Mn元素均转化为MnO ),即可计算
4 2
出MnS O 中锰的含量。滴定过程中发生反应的离子方程式为 。
2 6
16.(15分)钒钛系 SCR 催化剂主要包含 TiO 、V O 、WO 。从废SCR 催化剂中
2 2 5 3
回收TiO 、V O 、WO 的某种工艺部分流程如下:
2 2 5 3
(1)“碱浸”选择高温的目的是 。Ti元素可以形成多种配合物,在配合物
Ti(CN) 中,提供孤电子对的是 原子,原因是 。
4
(2)钛酸钠 (填“难”或“易”)溶于水。钛酸钠有多种存在形态,其中较为常见
的一种是Na Ti O ,则将其化学式写成氧化物的形式为 。在酸洗过程
2 3 7
中Na Ti O 转化为H TiO 的化学方程式为 。
2 3 7 2 3
化学试卷 第4页 共6页(3)钒钨溶液中钨元素以WO2-的形式存在,调节pH为2~3,溶液中的WO2-会转化为
4 4
H W O6-,再经萃取、反萃取等过程可制得WO 。写出WO2-转化为H W O6-的离
2 12 40 3 4 2 12 40
子方程式 。
(4)为测定废催化剂中V O 的含量,现进行如下实验:准确称取5.000 g废催化剂样
2 5
品于烧杯中,加入足量质量分数为50%的硫酸,加热,冷却后将溶液移入250 mL
容量瓶中,加水定容。准确量取25.00 mL溶液于锥形瓶中,滴加2~3滴指示剂,
用浓度为0.1000 mol/L的(NH ) Fe(SO ) 标准溶液进行滴定,恰好完全反应时消耗
4 2 4 2
标准溶液的体积为20.00mL。实验过程中,V元素最终转化为V3+,计算废催化剂
中V O 的含量为 (以百分数表示,废催化剂中其他成分对测定无影响) 。
2 5
17.(14分)氰化氢(HCN)分子被认为是生命起源中重要的中间体之一,主要应用于电镀业、
采矿业等,可制造各种树脂单体。迄今为止,它所产生的与生物相关联的化合物种类最多。
(1)HCN的合成
氰化氢可用甲烷氨氧化法合成,其热化学反应方程式为:
相关化学键的键能数据如下表:
化学键 C-H N-H C N H-H
E(kJ/mol) 414 393 891 436.4
上述反应的△H为 ___________;
(2)HCN的性质
已知25℃时有关弱电解质的电离平衡常数如下表:
弱电解质化学式 CH COOH HCN H CO HNO NH ·H O
3 2 3 2 3 2
电离平衡常数 1.8×l0-5 4.9×l0-10 K =4.3×l0-7 K =5.6×l0-11 7.2×l0-4 1.8×l0-5
1 2
①HCN具有酸性,能与氨水发生反应:HCN + NH ·H O ⥫⥫ NH+ CN - + HO,此反
3 2 4 2
应在常温下的平衡常数K约为_________;NHCN 溶液呈_______性。
4
②已知可发生如下反应:NaCN+HNO =HCN+NaNO ,NaCN+HF=HCN+NaF,
2 2
NaF+HNO =NaNO +HF,则HF的电离平衡常数的范围为:_______。
2 2
③在KCN溶液中通入少量的二氧化碳,其离子反应方程式为:______。
④浓度均为0.1mol/L的NaCN与HCN的混合溶液中,以下推断正确的是_______。
A.混合溶液pH约为9.3 B.2C(H+) = C(CN-) +C(HCN) +2C(OH-)
C.C(Na+) > C(CN-) > C(HCN) > C(H+) > C(OH-)
(3)HCN和CN-的处理
①HCN是一种无色、有毒、易溶于水的气体,易在空气中均匀弥散,并易产生爆炸。
国家重点实验室对密闭空间内的 HCN 气体进行了消毒研究,研究中采用 NH 、HO
3 2 2
化学试卷 第5页 共6页气雾 、NH-HO 气雾和水雾分别单独对 HCN 进行消毒。由图1可知________为最
3 2 2
佳消毒试剂。
②工业生产中含氰(CN -)废水主要来源于选矿、有色金属冶炼等工业,对于含氰废水
都应高度重视并妥善处理,国家关于废水中总氰浓度排放标准为 ≤ 0.5mg/L。某工厂实
验室针对不同浓度焦亚硫酸钠(Na S O )处理含氰废水情况展开研究。反应如下:
2 2 5
S O2 +2CN- +2O + HO = 2CNO- + 2H+ +2SO2
2 5 2 2 4
图2为氧化后CN- 的浓度变化,如果你是工厂研究人员,你认为应选择多大浓度的
Na S O 溶液最合理,请回答并说明理由__________________________。
2 2 5
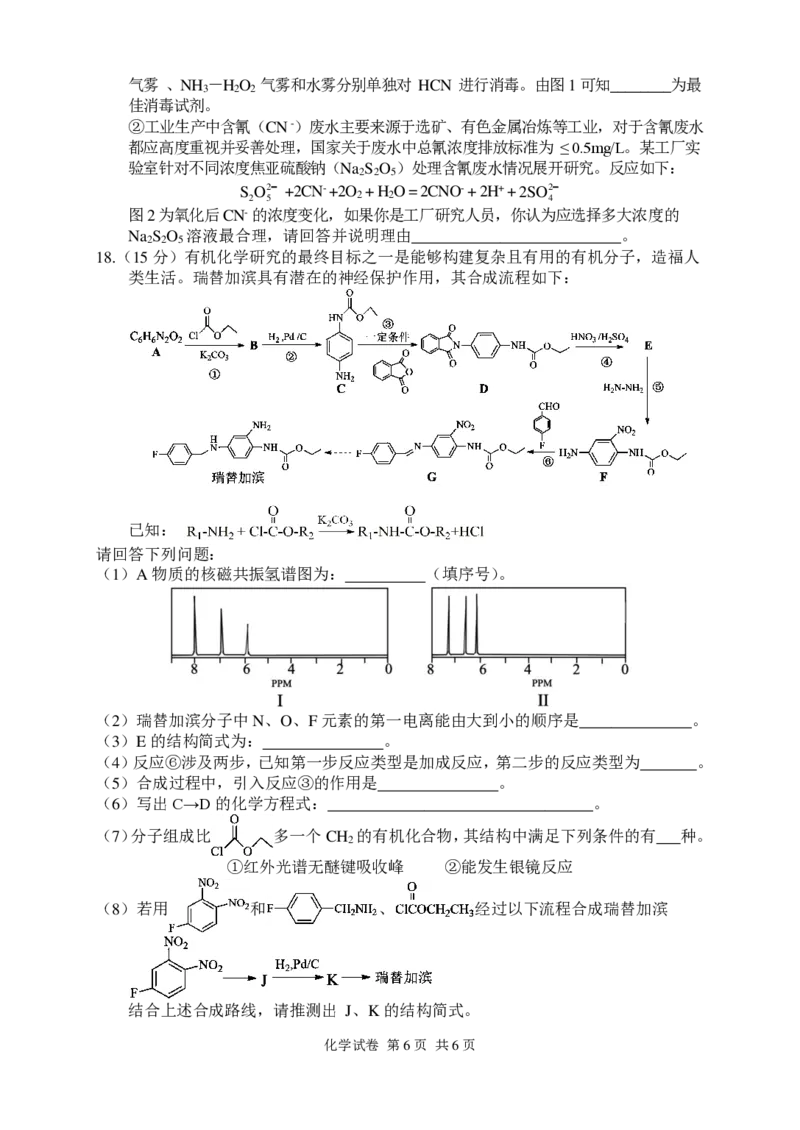
18.(15分)有机化学研究的最终目标之一是能够构建复杂且有用的有机分子,造福人
类生活。瑞替加滨具有潜在的神经保护作用,其合成流程如下:
已知:
请回答下列问题:
(1)A物质的核磁共振氢谱图为: (填序号)。
(2)瑞替加滨分子中N、O、F元素的第一电离能由大到小的顺序是______________。
(3)E的结构简式为: 。
(4)反应⑥涉及两步,已知第一步反应类型是加成反应,第二步的反应类型为 。
(5)合成过程中,引入反应③的作用是 。
(6)写出C→D的化学方程式:_________________________________。
(7)分子组成比 多一个CH 的有机化合物,其结构中满足下列条件的有 种。
2
①红外光谱无醚键吸收峰 ②能发生银镜反应
(8)若用 和 、 经过以下流程合成瑞替加滨
结合上述合成路线,请推测出 J、K的结构简式。
化学试卷 第6页 共6页