文档内容
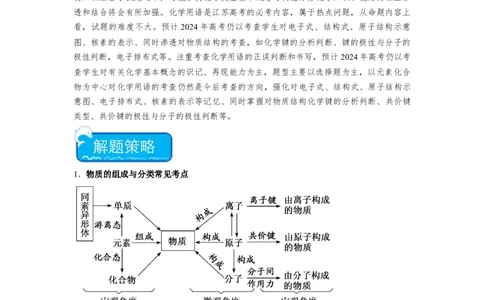
热点 01 物质的组成与分类 化学用语 化学键
物质的组成、分类及变化是江苏高考的常考内容,属于热点问题,从命题内容上看,
试题的难度不大。预计2024年高考仍以考查学生对有关化学基本概念的识记、再现能力为
主,题型主要以选择题为主,主要以物质组成、性质和分类的概念为出发点,以反映重大
科技成果和人们普遍关注的社会问题为切入点,将有关物质组成、分类的概念、有机化合
物知识融合于试题之中,可能涉及化学反应基本概念与其他部分化学知识和能力的相互渗
透和结合将会有所加强。化学用语是江苏高考的必考内容,属于热点问题,从命题内容上
看,试题的难度不大。预计2024年高考仍以考查学生对电子式、结构式、原子结构示意
图、核素的表示、同时渗透对物质结构的考查,如化学键的分析判断、键的极性与分子的
极性判断,电子排布式等。注重考查化学用语的正误判断和书写,预计2024年高考仍以考
查学生对有关化学基本概念的识记、再现能力为主,题型主要以选择题为主,以元素化合
物为中心对化学用语的考查仍然是今后考查的方向,强化对电子式、结构式、原子结构示
意图、电子排布式、核素的表示等记忆、同时掌握对物质结构化学键的分析判断、共价键
类型、共价键的极性与分子的极性判断等。
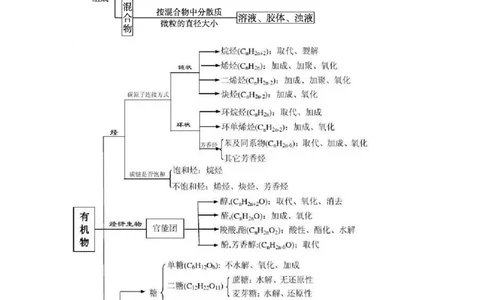
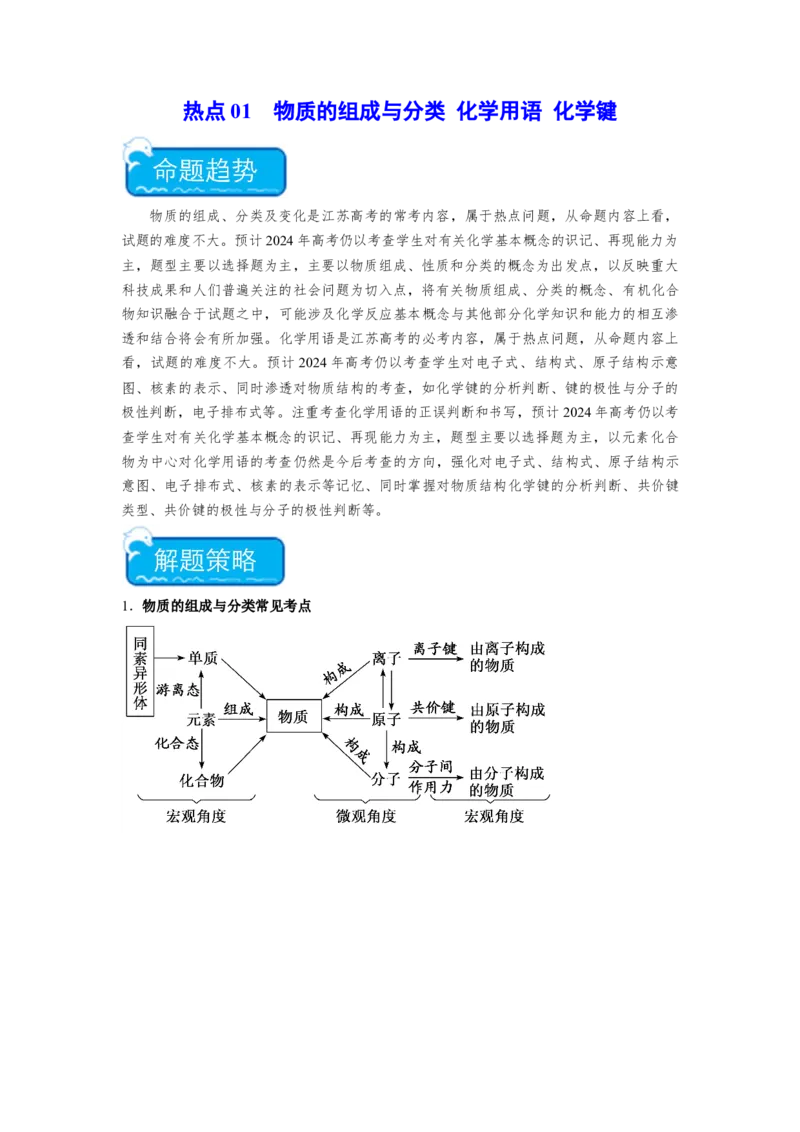
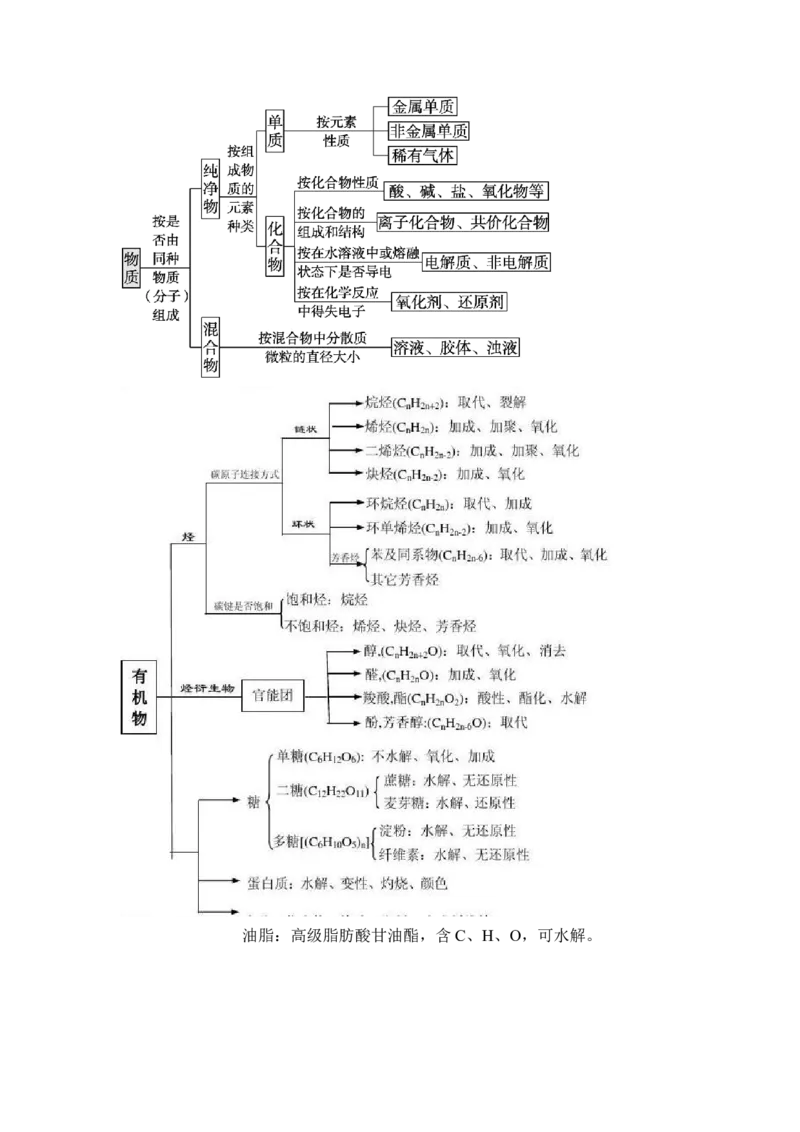
1.物质的组成与分类常见考点油脂:高级脂肪酸甘油酯,含C、H、O,可水解。2.共价键
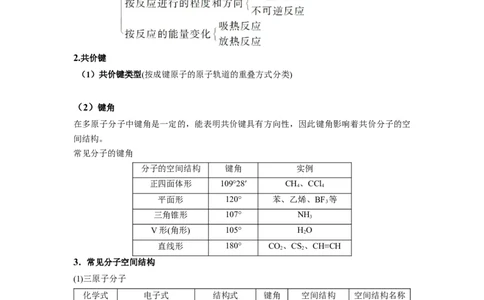
(1)共价键类型(按成键原子的原子轨道的重叠方式分类)
(2)键角
在多原子分子中键角是一定的,能表明共价键具有方向性,因此键角影响着共价分子的空
间结构。
常见分子的键角
分子的空间结构 键角 实例
正四面体形 109°28′ CH、CCl
4 4
平面形 120° 苯、乙烯、BF 等
3
三角锥形 107° NH
3
V形(角形) 105° HO
2
直线形 180° CO、CS、CH≡CH
2 2
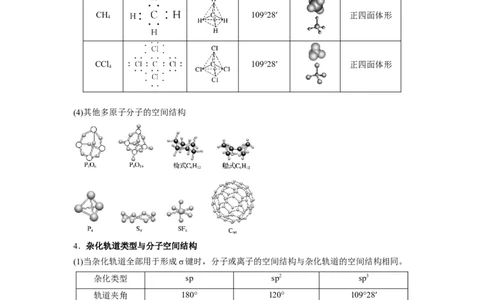
3.常见分子空间结构
(1)三原子分子
化学式 电子式 结构式 键角 空间结构 空间结构名称
CO O==C==O 180° 直线形
2
HO 105° V形
2
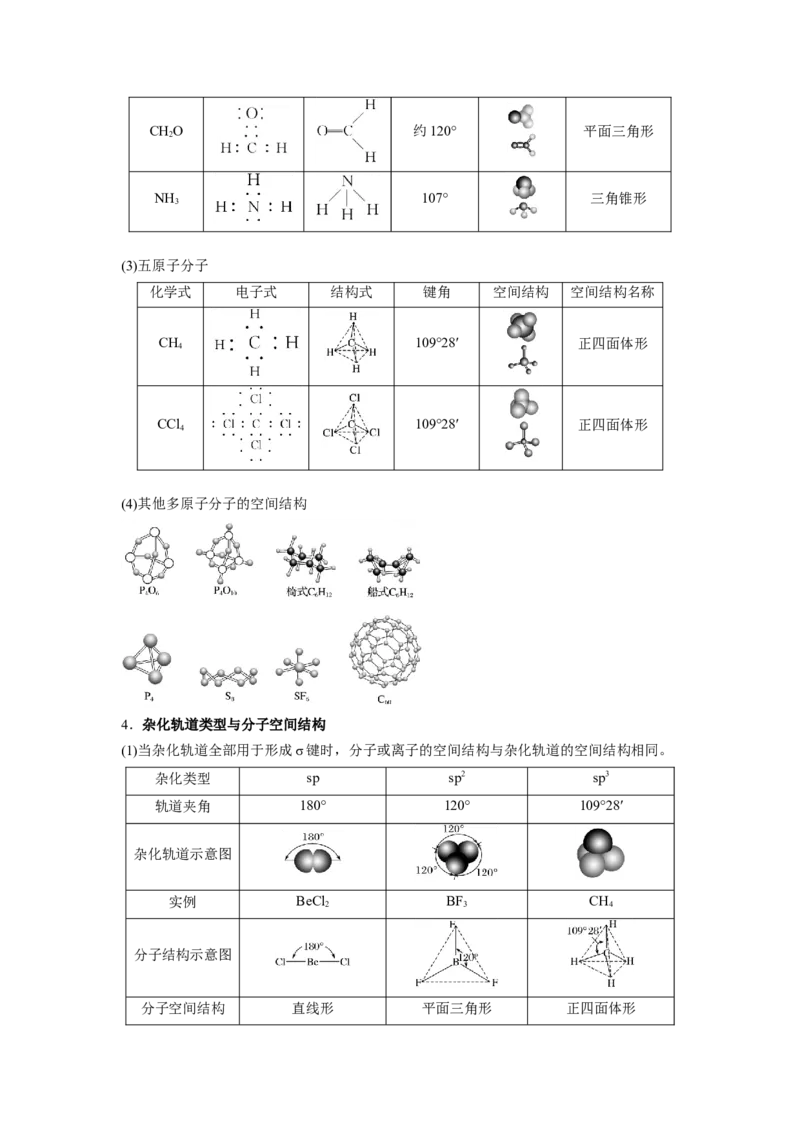
(2)四原子分子
化学式 电子式 结构式 键角 空间结构 空间结构名称CHO 约120° 平面三角形
2
NH 107° 三角锥形
3
(3)五原子分子
化学式 电子式 结构式 键角 空间结构 空间结构名称
CH 109°28′ 正四面体形
4
CCl 109°28′ 正四面体形
4
(4)其他多原子分子的空间结构
4.杂化轨道类型与分子空间结构
(1)当杂化轨道全部用于形成σ键时,分子或离子的空间结构与杂化轨道的空间结构相同。
杂化类型 sp sp2 sp3
轨道夹角 180° 120° 109°28′
杂化轨道示意图
实例 BeCl BF CH
2 3 4
分子结构示意图
分子空间结构 直线形 平面三角形 正四面体形(2)当杂化轨道中有未参与成键的孤电子对时,孤电子对对成键电子对的排斥作用,会使分
子或离子的空间结构与杂化轨道的形状有所不同。
中心原子杂 中心原子孤电子
AB 型分子 空间结构 实例
n
化类型 对数
AB sp2 1 V形 SO
2 2
AB 1 三角锥形 NH 、PCl 、NF 、HO+
3 3 3 3 3
sp3
AB 或(B A) 2 V形 HS、NH
2 2 2
(3)根据杂化轨道数目判断
杂化轨道只能用于形成σ键或者用来容纳未参与成键的孤电子对,而两个原子之间只能形
成一个σ键,故有下列关系:杂化轨道数目=价层电子对数目=σ键电子对数目+中心原
子的孤电子对数目,再由杂化轨道数目确定杂化类型。
杂化轨道数目 2 3 4
杂化类型 sp sp2 sp3
(4)根据杂化轨道的空间分布判断
①若杂化轨道在空间的分布为正四面体或三角锥形,则中心原子发生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则中心原子发生sp杂化。
(3)根据杂化轨道之间的夹角判断
①若杂化轨道之间的夹角为109°28′,则中心原子发生sp3杂化。
②若杂化轨道之间的夹角为120°,则中心原子发生sp2杂化。
③若杂化轨道之间的夹角为180°,则中心原子发生sp杂化。
考向一 物质的组成与分类
1.(2023下·河北石家庄·高二正定中学校考期末)化学与生活密切相关,下列说法正确的
是
A.苯甲酸钠可作为食品防腐剂是由于其具有酸性
B.豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C.SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
【答案】B
【解析】A.苯甲酸钠属于强碱弱酸盐,其水溶液呈碱性,因此,其可作为食品防腐剂不
是由于其具有酸性,A说法不正确;B.胶体具有丁达尔效应,是因为胶体粒子对光线发生了散射;豆浆属于胶体,因此,其
能产生丁达尔效应是由于胶体粒子对光线的散射,B说法正确;
C. 可用于丝织品漂白是由于其能与丝织品中有色成分化合为不稳定的无色物质,C说
法不正确;
D.维生素C具有很强的还原性,因此,其可用作水果罐头的抗氧化剂是由于其容易被氧
气氧化,从而防止水果被氧化,D说法不正确;
综上所述,本题选B。
2.(2022·天津·统考高考真题)近年我国在科技领域不断取得新成就。对相关成就所涉及
的化学知识理解错误的是
A.我国科学家实现了从二氧化碳到淀粉的人工合成,淀粉是一种单糖
B.中国“深海一号”平台成功实现从深海中开采石油和天然气,石油和天然气都是混
合物
C.我国实现了高性能纤维锂离子电池的规模化制备,锂离子电池放电时将化学能转化
为电能
D.以硅树脂为基体的自供电软机器人成功挑战马里亚纳海沟,硅树脂是一种高分子材
料
【答案】A
【解析】A.淀粉是一种多糖,故A错误;
B.石油主要是各种烷烃、环烷烃、芳香烃的混合物,天然气主要含甲烷,还有少量的其
他烷烃气体,因此天然气是混合物,故B正确;
C.锂离子电池放电属于原电池,是将化学能转化为电能,故C正确;
D.硅树脂是高聚物,属于高分子材料,故D正确。
综上所述,答案为A。
3.(2023·湖南·统考高考真题)中华文化源远流长,化学与文化传承密不可分。下列说法
错误的是
A.青铜器“四羊方尊”的主要材质为合金
B.长沙走马楼出土的竹木简牍主要成分是纤维素
C.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
D.铜官窑彩瓷是以黏土为主要原料,经高温烧结而成
【答案】C
【解析】A.四羊方尊由青铜制成,在当时铜的冶炼方法还不成熟,铜中常含有一些杂质,
因此青铜属合金范畴,A正确;
B.竹木简牍由竹子、木头等原料制成,竹子、木头的主要成分为纤维素,B正确;
C.蔡伦用碱液制浆法造纸,将原料放在碱液中蒸煮,原料在碱性环境下发生反应使原有
的粗浆纤维变成细浆,该过程涉及化学变化,C错误;
D.陶瓷是利用黏土在高温下烧结定型生成硅酸铝,D正确;故答案选C。
考向二 化学用语与化学键
4.(2023·辽宁·统考高考真题)下列化学用语或表述正确的是
A.BeCl 的空间结构:V形 B.P 中的共价键类型:非极性键
2 4
C.基态Ni原子价电子排布式:3d10 D.顺—2—丁烯的结构简式:
【答案】B
【解析】A.BeCl 的中心原子为Be,根据VSEPR模型可以计算,BeCl 中不含有孤电子对,
2 2
因此BeCl 为直线型分子,A错误;
2
B.P 分子中相邻两P原子之间形成共价键,同种原子之间形成的共价键为非极性共价键,
4
P 分子中的共价键类型为非极性共价键,B正确;
4
C.Ni原子的原子序数为28,其基态原子的价电子排布为3d84s2,C错误;
D.顺-2-丁烯的结构中两个甲基在双键的同一侧,其结构简式为 ,
D错误;
故答案选B。
5.(2023·湖北·统考高考真题)化学用语可以表达化学过程,下列化学用语的表达错误的
是
A.用电子式表示 的形成:
B.用离子方程式表示 溶于烧碱溶液:
C.用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂:
【答案】D
【解析】A.钾原子失去电子,硫原子得到电子形成硫化钾,硫化钾为离子化合物,用电
子式表示 的形成: ,A正确;B.氢氧化铝为两性氢氧化物,可以和强碱反应生成四羟基合铝酸根离子,离子方程式为:
,B正确;
C.H的s能级为球形,两个氢原子形成氢气的时候,是两个s能级的原子轨道相互靠近,
形成新的轨道,则用电子云轮廓图表示H-H的s-sσ键形成的示意图:
,C正确;
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂为
,D
错误;
故选D。
6.(2023·湖南·统考高考真题)下列化学用语表述错误的是
A.HClO的电子式:
B.中子数为10的氧原子: O
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
【答案】C
【解析】A.HClO中O元素呈负化合价,在结构中得到H和Cl共用的电子,因此HClO
的电子式为 ,A正确;
B.中子数为10,质子数为8的O原子其质量数为10+8=18,其原子表示为 O,B正确;
C.根据VSEPR模型计算,NH 分子中有1对孤电子对,N还连接有3和H原子,因此
3
NH 的VSEPR模型为四面体型,C错误;
3
D.基态N原子的价层电子排布为2s22p3,其电子排布图为 ,D正
确;
故答案选C。
7.(2023·浙江·高考真题)下列化学用语表示正确的是A.中子数为18的氯原子:
B.碳的基态原子轨道表示式:
C. 的空间结构: (平面三角形)
D. 的形成过程:
【答案】C
【解析】A.质量数=质子数+中子数,质量数标注于元素符号左上角,质子数标注于左下
角,中子数为18的氯原子的质量数为17+18=35,核素符号为 ,故A错误;
B.基态碳原子的核外电子排布式为1s22s22p2,根据洪特规则,2p轨道上的2个电子应该
分别在2个轨道上,且自旋方向相同,轨道表示式: ,故B错误;
C.BF 的中心原子B原子孤电子对数= =0,价层电子对数=3,空间构型为平面三角形,
3
空间结构模型为: ,故C正确;
D.HCl是共价化合物,不存在电子得失,其形成过程应为
,故D错误;
故选:C。
(建议用时:25分钟)
1.(2023上·江苏苏州·高三统考阶段练习)“黑金”石墨烯为冬奥会赛场留住温暖,石墨
烯属于
A.有机物 B.单质 C.化合物 D.混合物
【答案】B
【解析】石墨烯是由碳元素组成的一种单质,属于纯净物。
答案选B。2.(2023上·江苏扬州·高三统考阶段练习)反应 可
用于除去 污染。下列说法正确的是
A. 空间构型为三角锥形 B. 电子式:
C. 晶体中既含离子键又含共价键 D.中子数为18的 原子:
【答案】C
【解析】A. 中心原子价层电子对数为3+ =3,且没有孤电子对,
空间构型为平面三角形,故A错误;
B. 是共价化合物,电子式为: ,故B错误;
C. 是离子化合物,含离子键,NH 中含有共价键,故C正确;
D.中子数为18的 原子质量数为18+17=35,表示为 ,故D错误;
故选C。
3.(2023上·江苏·高三专题练习)能源、航天、信息等科技离不开新技术和新材料的发现
和应用。下列有关说法正确的是
A.新一代运载火箭成功应用液氧煤油发动机,煤油是石油分馏所得混合物
B.航天核心舱搭载的柔性太阳能电池板的核心材料是二氧化硅
C.量子通信材料螺旋碳纳米管、石墨烯等纳米材料属于胶体
D.国产航母福建舰舰身材料低碳合金钢耐腐蚀,合金的熔点一定低于成分金属
【答案】A
【解析】A.煤油的主要成分是烃,是石油分馏所得多种碳氢化合物组成的混合物,故A
正确;
B.太阳能电池板的核心材料是单质硅,故B错误;
C.胶体是分散质粒子直径介于1-100nm的分散系,螺旋碳纳米管、石墨烯等纳米材料本
身不是分散系,不属于胶体,故C错误;
D.合金的熔点一般比各成分金属低,但是汞与其它金属形成合金时,合金的熔点大于汞,
故D错误;
故选:A。
4.(2024上·江苏南京·高三南京师大附中校考阶段练习)反应
用于处理汽车尾气中的 。下列说法正确的是
A. 中H元素的化合价为-1 B.NO是酸性氧化物C. 发生氧化反应 D. 的结构式为
【答案】D
【解析】A. 中H元素的化合价为+1,N元素化合价为-3,A错误;
B. NO是非成盐氧化物,B错误;
C. 反应中 中N元素化合价升高,为还原剂,发生氧化反应,NO、 中化合价降
低,为氧化剂,发生还原反应,C错误;
D. 的结构式为 ,D正确;
故答案选D。
5.(2022上·江苏扬州·高三扬州中学校考阶段练习)化学与生产、生活、科技和环境等密
切相关。下列有关说法错误的是
A.84消毒液与洁厕灵不能混用,若混用会产生有毒气体
B.聚合硫酸铁[Fe (OH) (SO )] 是一种新型絮凝剂,可用于水的净化
2 x 4 y n
C.卫星探测器上的太阳能电池帆板主要成分是晶体硅
D.“汽车尾气处理”有助于改善城市空气质量,有利于实现“碳中和”
【答案】D
【解析】A.84消毒液的有效成分是次氯酸钠,洁厕灵的主要成分是盐酸,若将两者混合
使用,可能会发生如下反应:NaClO + 2HCl= NaCl + Cl↑+H O,A正确;
2 2
B.聚合硫酸铁[Fe (OH) (SO )] 溶于水会形成胶体,胶体具有吸附性,可用于水的净化,
2 x 4 y n
B正确;
C.晶体硅是-种性能良好的半导体材料,常用于制作芯片和太阳能电池板,卫星探测器上
的太阳能电池帆板主要成分是晶体硅,C正确;
D.汽车尾气中含有有毒的一氧化碳和一氧化氮,在催化加的作用下将其转化为二氧化碳
和氮气,但汽车尾气处理不能减少二氧化碳的排放,D错误;
故选:D。
6.(2023上·江苏镇江·高三统考期中)下列物品为江苏各地特产,其主要化学成分不能与
其他三种归为一类的是
A.东海水晶 B.宜兴紫砂壶 C.苏州丝绸 D.扬中玉雕
【答案】C
【分析】东海水晶、宜兴紫砂壶、扬中玉雕均属于硅酸盐制品,主要成分均为无机非金属
材料,而苏州丝绸属于天然有机高分子材料,主要成分为蛋白质。
【解析】A.由分析可知,东海水晶属于无机非金属材料,A不符合题意;
B.由分析可知,宜兴紫砂壶属于无机非金属材料,B不符合题意;
C.由分析可知,苏州丝绸属于有机高分子材料,C符合题意;
D.由分析可知,扬中玉雕属于无机非金属材料,D不符合题意;故答案为C。
7.(2023上·江苏连云港·高三统考期中)反应
可用于实验室制取氯气。下列说法正确
的是
A. 中含有离子键和共价键 B.HCl的电子式为
C. 的核外电子排布式为 D. 的空间构型为正四面体
【答案】A
【解析】A.KMnO 中K+与 之间为离子键, 中Mn与O之间为共价键,A项正
4
确;
B.HCl为共价化合物,电子式为 ,B项错误;
C.基态Mn原子的核外电子排布式为[Ar]3d54s2,Mn2+的核外电子排布式为[Ar]3d5,C项错
误;
D.HO的空间构型为V形,D项错误;
2
答案选A。
8.(2023上·江苏南通·高三统考期中)反应
应用于工业上制备CuCl。下
列说法正确的是
A.NaCl的电子式为 B. 中S元素的化合价为+5
C. 空间构型为正四面体形 D. 为非极性分子
【答案】C
【解析】A.NaCl为离子化合物 ,A错误;
B.根据化合价计算, 中S的化合价为+4,B错误;
C.硫酸根中,价层电子对数= ,孤电子对数为0,则硫酸根的空间构
型为正四面体,C正确;
D.HO为V型,属于极性分子,D错误;
2
故答案为:C。
9.(2023上·江苏镇江·高三统考期中)反应 可用于制备
火箭推进剂 。下列说法正确的是
A. 的球棍模型为 B. 分子间可形成氢键C. 的电子式: D. 分子中含有 键
【答案】B
【解析】A.水分子呈V形,氢原子半径小于氧原子,球棍模型为 ,故A错误;
B.由于N元素的非金属性较强,因此 分子间可形成氢键,故B正确;
C. 为离子化合物,电子式为 ,故B错误;
D. 分子的结构式为 ,故D错误;
综上所述,正确的是B项。
10.(2023上·江苏盐城·高三校联考阶段练习)反应CHCHCHOH
3 2 2
CHCH=CH↑+H O可用于制备丙烯。下列表示反应中相关微粒的化学用语正确的是
2 2 2
A.硫原子的结构示意图:
B.HO的电子式:
2
C.聚丙烯的结构简式:
D.中子数为10的氧原子:
【答案】B
【解析】A. 是硫离子的结构示意图,故A错误;
B.HO是共价化合物,其电子式: ,故B正确;
2
C.聚丙烯的结构简式: ,故C错误;
D.中子数为10的氧原子: ,故D错误。
故答案为B。
11.(2023上·江苏徐州·高三徐州市第一中学校联考阶段练习)Cu与KCN溶液反应的化
学方程式为: [Cu(CN) ] ↑。下列说法正确的是
2 3 4 2
A.中子数为35的铜原子:B.K⁺的结构示意图:
C.CN⁻的电子式为:
D. 中存在极性键和非极性键
【答案】C
【解析】A.铜元素符号左上角数值代表质量数=质子数+中子数=29+35=64,正确表示为
,A错误;
B. 该结构为K原子结构示意图,不是离子结构示意图,B错误;
C. 符合碳原子、氮原子成键规律,C正确;
D. 中存在离子键、极性键、配位键,不存在非极性键,D错误;
答案选C。
12.(2023上·江苏苏州·高三校联考阶段练习)反应 可用于
的制备,下列说法正确的是
A. 为非极性分子 B.F 的电子式为
2
C. 中 元素的化合价为-3 D. 属于离子化合物
【答案】D
【解析】A. 分子构型为三角锥,为极性分子,故A错误;
B.F 的电子式为 ,故B错误;
2
C. 中F元素化合价为-1, 元素的化合价为+3,故C错误;
D. 是 和 组成的离子化合物,故D正确;
故答案选D。
13.(2023上·江苏泰州·高三姜堰中学校考期中)银锌电池以 、Zn为两极,KOH溶
液作电解质,原电池反应为: ,下列说法不正确的是
A.基态 的价电子排布式: B. 为共价晶体
C. 的电子式: D.放电时,电子由Zn经外电路流向
【答案】B【解析】A.Zn是30号元素,基态 有28个电子, 的价电子排布式: ,A正
确;
B. 是分子晶体,不是共价晶体,B错误;
C. 的电子式: ,C正确;
D.银锌电池以 、Zn为两极,KOH溶液作电解质,活泼金属锌为负极失去电子,电
子有负极Zn流出经过外电路流向正极Ag O,D正确;
2
答案选B。
14.(2023上·江苏盐城·高三盐城中学校联考期中)水是生命之源,寻找火星水冰是“祝
融”号火星车的任务之一、下列关于水的说法正确的是
A.属于两性氧化物
B.既有氧化性又有还原性
C.与 互为同素异形体
D.不属于电解质
【答案】B
【解析】A.两性氧化物指的是既能与酸反应又能与碱反应的氧化物,A错误;
B.水电解生成氢气和氧气的反应中,水既能做氧化剂也能做还原剂,B正确;
C.同素异形体为由同种元素组成的不同单质,水及双氧水为化合物,C错误;
D.水为弱电解质,D错误;
故答案为:B。
15.(2023上·江苏泰州·高三靖江高级中学校联考阶段练习)氮及其化合物在生活和生产
中占有重要的地位。肼(N H)是高能燃料,具有强还原性,溶于水生成的水合肼是二元弱
2 4
碱,常用作火箭发射的推进剂。常温下,
,可用于生产NH。NO 有
2 4 2
较强的氧化性,但对环境有影响,可以用碱性物质吸收。NH 是工业制备硝酸的重要原料。
3
下列说法正确的是
A.NaClO既含离子键又含共价键 B.NH 的电子式为
3
C.NH 的结构式为: D.Na+与Cl-具有相同的电子层结构
2 4
【答案】A
【解析】A.NaClO为离子化合物,既含离子键又含共价键,A正确;
B.NH 是共价化合物,其电子式为 ,B错误;
3C.根据N原子的成键特点,NH 的结构式为: ,C错误;
2 4
D.Na+是Na原子失去最外层1个电子形成的,Na+核外电子排布为2、8;Cl-是Cl原子获
得1个电子形成的,Cl-核外电子排布为2、8、8,所以Na+和Cl-具有不同的电子层结构,D
错误;
故答案为:A。
16.(2023上·江苏盐城·高三盐城中学校联考期中)反应 可
应用于呼吸面具的供氧。下列说法正确的是
A.中子数为10的氧原子:
B.NaOH的电子式:
C.水形成的冰为共价晶体
D. 晶体中存在非极性共价键
【答案】D
【解析】A.中子数为10的氧原子正确的表示为: ,故A错误;
B.NaOH的电子式正确表示为: ,故B错误;
C.水形成的冰仍然是分子晶体,故C错误;
D.过氧化钠晶体中过氧根离子存在非极性共价键,故D正确;
故选D。
17.(2023上·江苏常州·高三统考期中) 可做燃料,具有较大的燃烧热(
),尿素可用于消除 污染。下列化学用语的表达正确的是
A.用轨道表示式表示石墨烯中C原子的杂化:
B.用电子式表示 的形成:
C. 燃烧的热化学方程式:
D.尿素消除NO污染的化学方程式:
【答案】D
【解析】A.石墨烯中C原子采用sp2杂化,不是sp3杂化,A项错误;
B.二氧化碳是由C原子与两个氧原子通过共用电子对形成的,用电子式表示 的形成:,B项错误;
C.产物中水应为液态水,故该热化学方程式不能表示甲烷燃烧热,C项错误;
D.尿素与NO反应生成N 和HO,化学方程式为 ,
2 2
D项正确;
答案选D。
18.(2023上·江苏徐州·高三统考期中)汽车安全气囊使用时发生反应
,下列说法正确的是
A. 只含离子键 B. 的质子数为10
C. 结构示意图为 D. 的电子式为
【答案】D
【解析】A. 是由Na+和 形成的离子化合物,含离子键和共价键,A错误;
B.O是8号元素, 的质子数为8,B错误;
C. 核外有18个电子,结构示意图为K+ ,C错误;
D. 为离子化合物,电子式为 ,D正确;
故选D。
19.(2023上·江苏苏州·高三统考阶段练习)制备 的一种方法为:
,下列说法正确的是
A.质量数为35、中子数为18的氯原子可表示为
B.基态O原子核外电子轨道表示式为
C. 的电子式为
D. 中含有离子键和共价键
【答案】D
【解析】A.质量数为35、中子数为18的氯原子质子数为17,该原子可表示为 ,A错
误;B.基态氧原子的核外电子轨道表示式为 ,B错误;
C.HCl的电子式为 ,C错误;
D.NaClO中Na+与ClO-之间存在离子键,Cl与O之间存在共价键,D正确;
故选D。
20.(2023上·江苏淮安·高三马坝高中校考阶段练习)根据化学反应的实质是旧键断裂和
新键形成这一观点,下列不属于化学变化的是
A.浓硫酸使蔗糖脱水
B.胆矾晶体受热由蓝色变白色
C.在新制氯水中滴入紫色石蕊试液,溶液先变红后褪色
D.用 萃取碘水中的碘
【答案】D
【解析】A.浓硫酸使蔗糖脱水,有新物质生成,是化学变化,A错误;
B.胆矾晶体受热由蓝色变白色,是结晶水合物失去结晶水发生的化学反应,有新物质生
成,是化学变化,B错误;
C.在新制氯水中滴入紫色石蕊试液,溶液先变红后褪色是由于次氯酸的强氧化性,有新
物质生成,是化学变化,C错误;
D.用 萃取碘水中的碘,是利用了碘在水中和四氯化碳中的溶解度差异,没有新物质
生成,不属于化学变化,D正确;
故选D。