文档内容
高考热点专项 3 陌生元素及其化合物性质探究分析
目录
01考情透视·目标导航............................................................................................................................
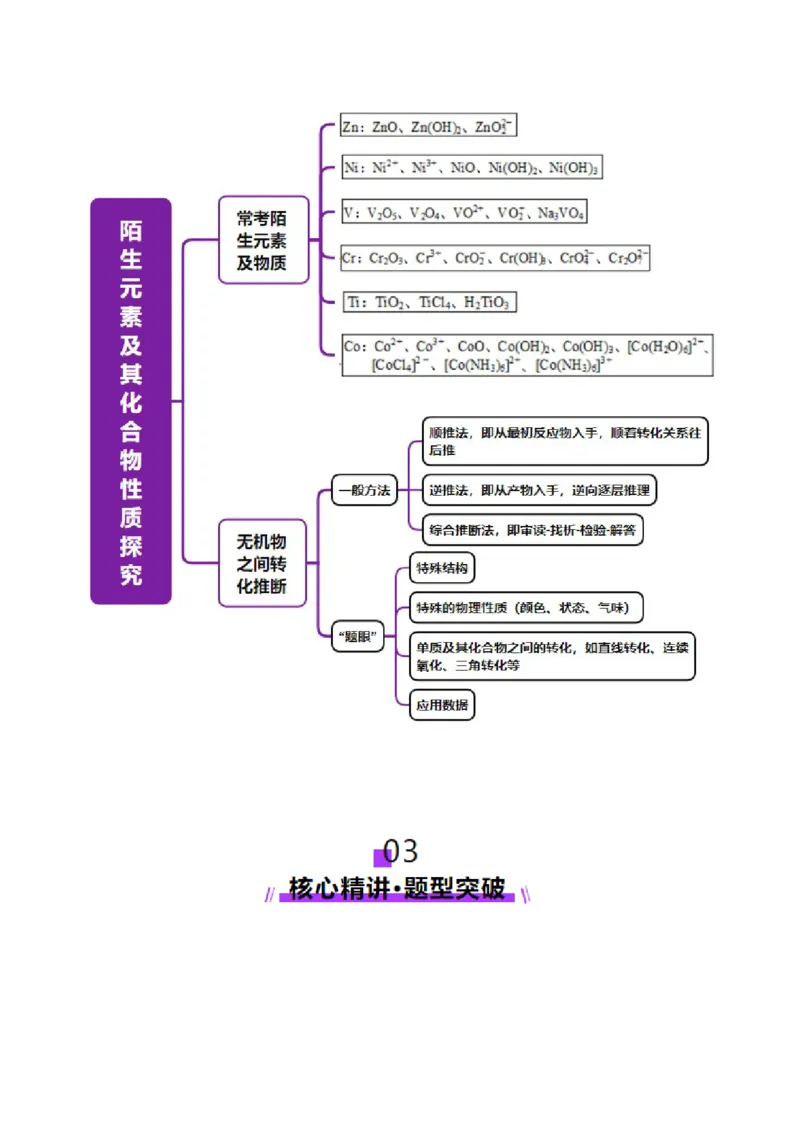
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 过渡元素植入工艺流程或物质制备中...............................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.锌及其重要化合物.........................................................................................................................................
2.钴、镍及其化合物.........................................................................................................................................
3.钒及其化合物.................................................................................................................................................
4.铬及其化合物.................................................................................................................................................
5.钛及其化合物.................................................................................................................................................
6.过渡金属易形成的配合物............................................................................................................................
【命题预测】...........................................................................................................................................................
题型二 以陌生物质为切入考查无机推断.........................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.常见特征反应现象.........................................................................................................................................
2.一些特殊条件.................................................................................................................................................
3.一些特殊数据.................................................................................................................................................
【命题预测】...........................................................................................................................................................
考向1 已知物质为载体..................................................................
考向2 未知物质为载体..................................................................考点要求 考题统计 考情分析
2024·江西卷,15,14分;2024·山
过渡元素 过渡元素是考查元素化合物知识的重要媒
东卷,18,12分;2024·辽吉黑卷,
植入工艺 介,特别是在化工流程或物质制备题中重
16,14分;2024·河北卷,16,14
流程或物 要载体,近年来在高考题中频频出现;无
分;2024·全国新课标卷,8,14
质制备中 机推断题是考查元素及其化合物的一种重
分;2024·江苏卷,14,15分;
要形式,浙江省选考卷已不囿于传统的无
机推断,改头换面以小流程结合定量计算
2024·浙江1月卷,18,10分;
以陌生物 进行推断的形式出现,有着积极导向作
2022·浙江省1月卷,28,10分;
质为切入 用。对高考考生来说,基础知识越牢固,
2022·浙江省6月卷,28,10分;
考查无机 思维迁移越多,从信息中提取知识越快,
2021·浙江省1月卷,28,10分;
推断 解读陌生物质的能力越强。
2021·浙江省6月卷,28,10分;题型一 过渡元素植入工艺流程或物质制备中
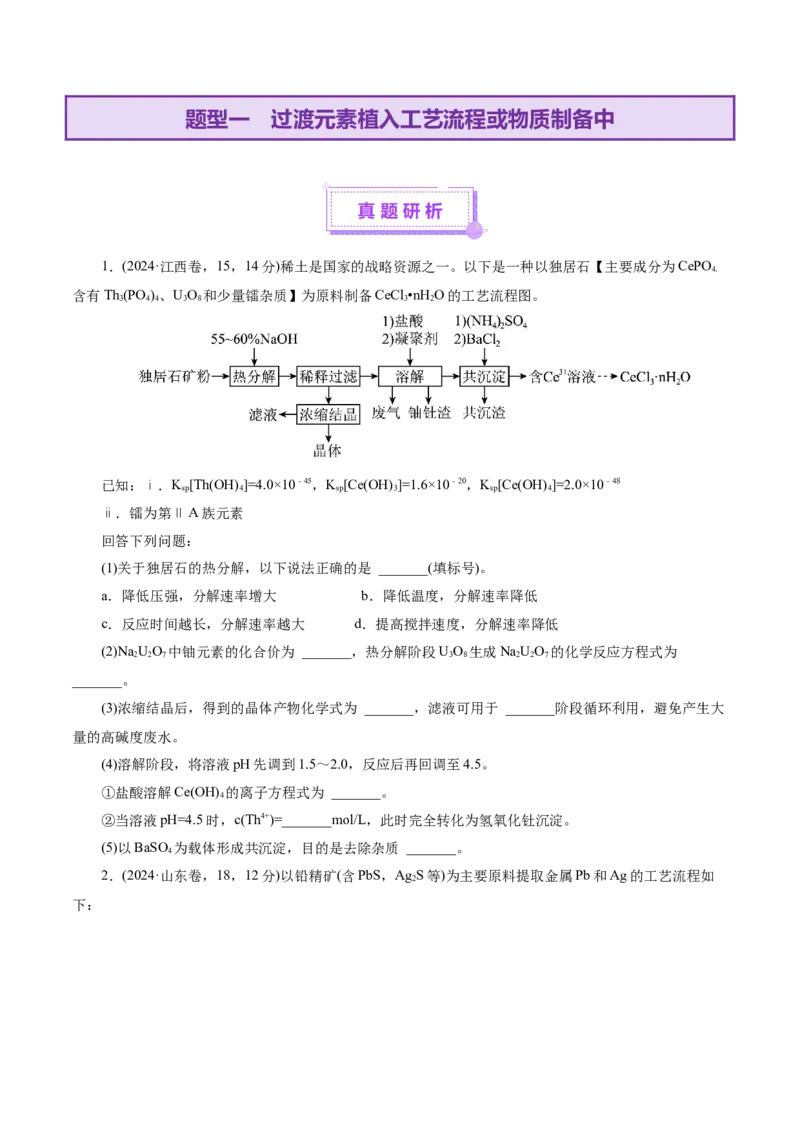
1.(2024·江西卷,15,14分)稀土是国家的战略资源之一。以下是一种以独居石【主要成分为CePO
4.
含有Th(PO )、UO 和少量镭杂质】为原料制备CeCl •nH O的工艺流程图。
3 4 4 3 8 3 2
已知:ⅰ.K [Th(OH) ]=4.0×10﹣45,K [Ce(OH) ]=1.6×10﹣20,K [Ce(OH) ]=2.0×10﹣48
sp 4 sp 3 sp 4
ⅱ.镭为第ⅡA族元素
回答下列问题:
(1)关于独居石的热分解,以下说法正确的是 _______(填标号)。
a.降低压强,分解速率增大 b.降低温度,分解速率降低
c.反应时间越长,分解速率越大 d.提高搅拌速度,分解速率降低
(2)NaUO 中铀元素的化合价为 _______,热分解阶段UO 生成NaUO 的化学反应方程式为
2 2 7 3 8 2 2 7
_______。
(3)浓缩结晶后,得到的晶体产物化学式为 _______,滤液可用于 _______阶段循环利用,避免产生大
量的高碱度废水。
(4)溶解阶段,将溶液pH先调到1.5~2.0,反应后再回调至4.5。
①盐酸溶解Ce(OH) 的离子方程式为 _______。
4
②当溶液pH=4.5时,c(Th4+)=_______mol/L,此时完全转化为氢氧化钍沉淀。
(5)以BaSO 为载体形成共沉淀,目的是去除杂质 _______。
4
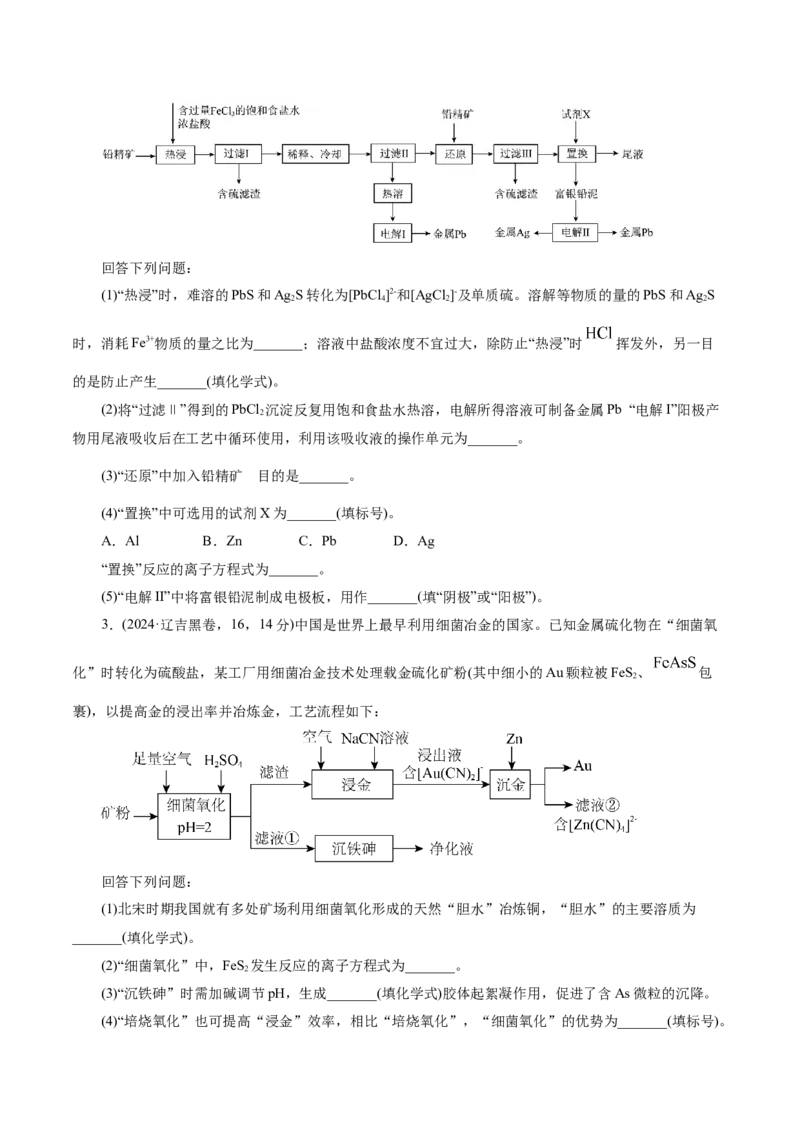
2.(2024·山东卷,18,12分)以铅精矿(含PbS,AgS等)为主要原料提取金属Pb和Ag的工艺流程如
2
下:回答下列问题:
(1)“热浸”时,难溶的PbS和AgS转化为[PbCl]2-和[AgCl]-及单质硫。溶解等物质的量的PbS和AgS
2 4 2 2
时,消耗Fe3+物质的量之比为_______;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,另一目
的是防止产生_______(填化学式)。
(2)将“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属Pb “电解I”阳极产
2
物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为_______。
的
(3)“还原”中加入铅精矿 目的是_______。
(4)“置换”中可选用的试剂X为_______(填标号)。
A.Al B.Zn C.Pb D.Ag
“置换”反应的离子方程式为_______。
(5)“电解II”中将富银铅泥制成电极板,用作_______(填“阴极”或“阳极”)。
3.(2024·辽吉黑卷,16,14分)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧
化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的Au颗粒被FeS、 包
2
裹),以提高金的浸出率并冶炼金,工艺流程如下:
回答下列问题:
(1)北宋时期我国就有多处矿场利用细菌氧化形成的天然“胆水”冶炼铜,“胆水”的主要溶质为
_______(填化学式)。
(2)“细菌氧化”中,FeS 发生反应的离子方程式为_______。
2
(3)“沉铁砷”时需加碱调节pH,生成_______(填化学式)胶体起絮凝作用,促进了含As微粒的沉降。
(4)“培烧氧化”也可提高“浸金”效率,相比“培烧氧化”,“细菌氧化”的优势为_______(填标号)。A.无需控温 B.可减少有害气体产生
C.设备无需耐高温 D.不产生废液废渣
(5)“真金不拍火炼”,表明Au难被O 氧化,“浸金”中NaCN的作用为_______。
2
(6)“沉金”中Zn的作用为_______。
(7)滤液②经HSO 酸化,[Zn(CN) ]2-转化为ZnSO 和HCN的化学方程式为_______。用碱中和HCN可
2 4 4 4
生成_______(填溶质化学式)溶液,从而实现循环利用。
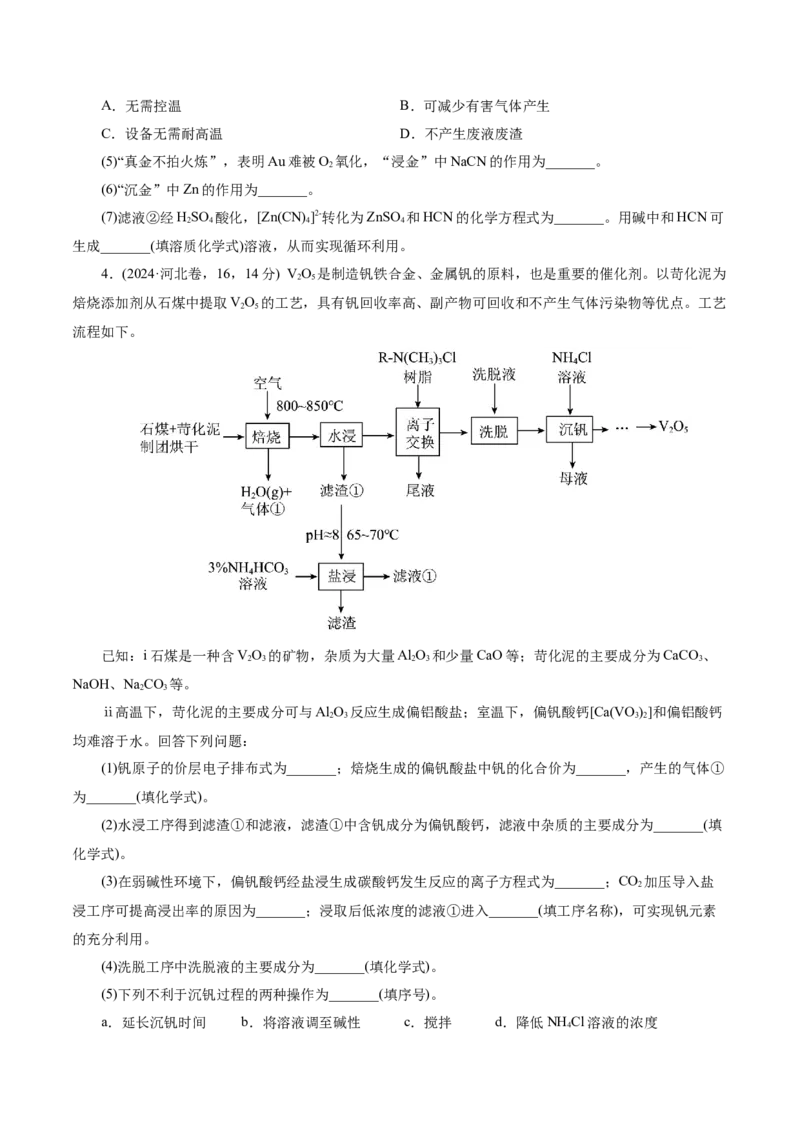
4.(2024·河北卷,16,14分) VO 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为
2 5
焙烧添加剂从石煤中提取VO 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺
2 5
流程如下。
已知:i石煤是一种含VO 的矿物,杂质为大量Al O 和少量CaO等;苛化泥的主要成分为CaCO、
2 3 2 3 3
NaOH、NaCO 等。
2 3
ⅱ高温下,苛化泥的主要成分可与Al O 反应生成偏铝酸盐;室温下,偏钒酸钙[Ca(VO )]和偏铝酸钙
2 3 3 2
均难溶于水。回答下列问题:
(1)钒原子的价层电子排布式为_______;焙烧生成的偏钒酸盐中钒的化合价为_______,产生的气体①
为_______(填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为_______(填
化学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为_______;CO 加压导入盐
2
浸工序可提高浸出率的原因为_______;浸取后低浓度的滤液①进入_______(填工序名称),可实现钒元素
的充分利用。
(4)洗脱工序中洗脱液的主要成分为_______(填化学式)。
(5)下列不利于沉钒过程的两种操作为_______(填序号)。
a.延长沉钒时间 b.将溶液调至碱性 c.搅拌 d.降低NH Cl溶液的浓度
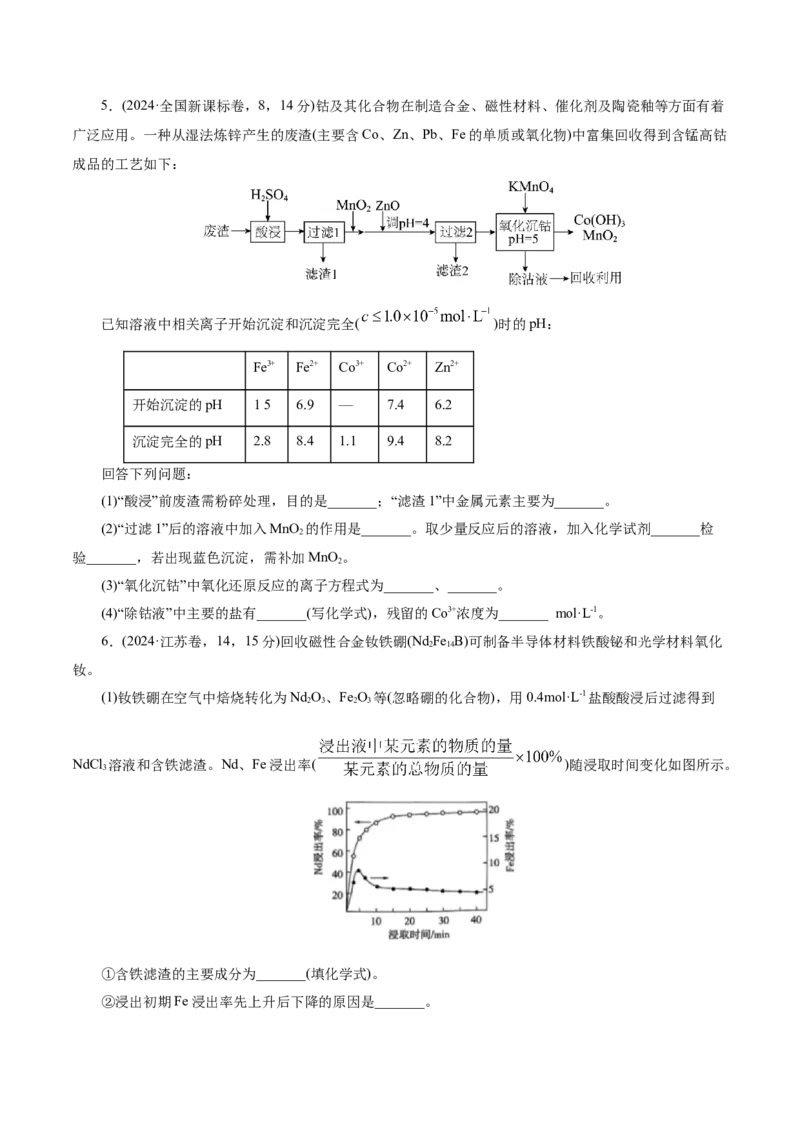
45.(2024·全国新课标卷,8,14分)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着
广泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴
成品的工艺如下:
已知溶液中相关离子开始沉淀和沉淀完全( )时的pH:
Fe3+ Fe2+ Co3+ Co2+ Zn2+
.
开始沉淀的pH 15 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是_______;“滤渣1”中金属元素主要为_______。
(2)“过滤1”后的溶液中加入MnO 的作用是_______。取少量反应后的溶液,加入化学试剂_______检
2
验_______,若出现蓝色沉淀,需补加MnO 。
2
(3)“氧化沉钴”中氧化还原反应的离子方程式为_______、_______。
(4)“除钴液”中主要的盐有_______(写化学式),残留的Co3+浓度为_______ mol·L-1。
6.(2024·江苏卷,14,15分)回收磁性合金钕铁硼(Nd Fe B)可制备半导体材料铁酸铋和光学材料氧化
2 14
钕。
(1)钕铁硼在空气中焙烧转化为Nd O、Fe O 等(忽略硼的化合物),用0.4mol·L-1盐酸酸浸后过滤得到
2 3 2 3
NdCl 溶液和含铁滤渣。Nd、Fe浸出率( )随浸取时间变化如图所示。
3
①含铁滤渣的主要成分为_______(填化学式)。
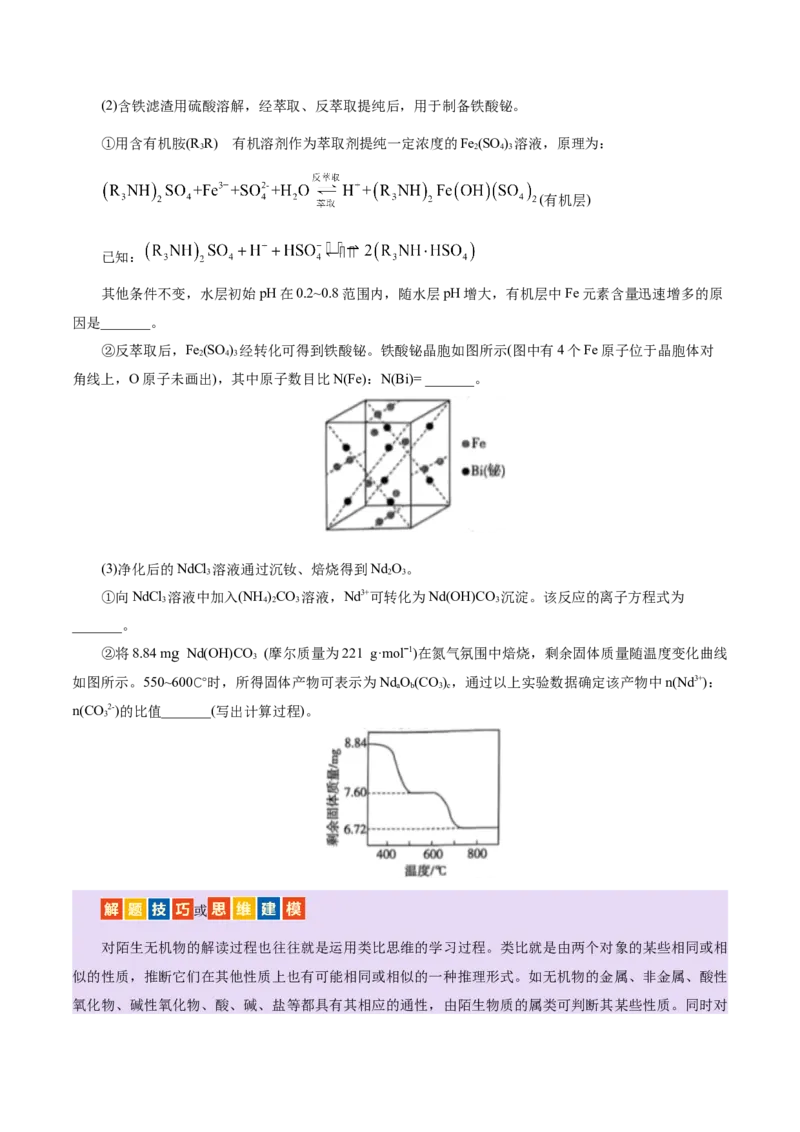
②浸出初期Fe浸出率先上升后下降的原因是_______。(2)含铁滤渣用硫酸溶解,经萃取、反萃取提纯后,用于制备铁酸铋。
的
①用含有机胺(R R) 有机溶剂作为萃取剂提纯一定浓度的Fe (SO ) 溶液,原理为:
3 2 4 3
(有机层)
已知:
其他条件不变,水层初始pH在0.2~0.8范围内,随水层pH增大,有机层中Fe元素含量迅速增多的原
因是_______。
②反萃取后,Fe (SO ) 经转化可得到铁酸铋。铁酸铋晶胞如图所示(图中有4个Fe原子位于晶胞体对
2 4 3
角线上,O原子未画出),其中原子数目比N(Fe):N(Bi)= _______。
(3)净化后的NdCl 溶液通过沉钕、焙烧得到Nd O。
3 2 3
①向NdCl 溶液中加入(NH )CO 溶液,Nd3+可转化为Nd(OH)CO 沉淀。该反应的离子方程式为
3 4 2 3 3
_______。
②将8.84 mg Nd(OH)CO (摩尔质量为221 g·molˉ1)在氮气氛围中焙烧,剩余固体质量随温度变化曲线
3
如图所示。550~600℃时,所得固体产物可表示为NdO(CO),通过以上实验数据确定该产物中n(Nd3+):
a b 3 c
n(CO2-)的比值_______(写出计算过程)。
3
或
对陌生无机物的解读过程也往往就是运用类比思维的学习过程。类比就是由两个对象的某些相同或相
似的性质,推断它们在其他性质上也有可能相同或相似的一种推理形式。如无机物的金属、非金属、酸性
氧化物、碱性氧化物、酸、碱、盐等都具有其相应的通性,由陌生物质的属类可判断其某些性质。同时对陌生物质中的关键元素的价态进行分析:较高价态的有氧化性,较低价态的有还原性,中间价态的既有氧
化性又有还原性。
1.锌及其重要化合物
(1)Zn的性质与Al相似,与强酸、强碱均反应生成H。
2
(2)ZnO、Zn(OH) 与Al O、Al(OH) 均为两性化合物。与酸反应生成Zn2+,与强碱反应生成ZnO。
2 2 3 3
2.钴、镍及其化合物
(1)常温下,钴、镍在空气中能稳定存在,加热条件下可生成CoO、NiO。
(2)CoO溶于酸和强碱溶液,不溶于水、乙醇、氨水,在空气中焙烧至390~890 ℃时生成四氧化三钴。
NiO溶于酸和氨水,不溶于水。
(3)Co(OH) 在空气中缓慢地被氧化为棕褐色的Co(OH) ,Ni(OH) 在空气中较稳定,可采用氧化性较强
2 3 2
的Br 将其氧化。
2
④Co3+、Ni3+在酸性溶液中有强氧化性,易被还原,如Co(OH) 、Ni(OH) 在盐酸中被还原,2Co(OH)
3 3 3
+6HCl===2CoCl +Cl↑+6HO,2Ni(OH) +6HCl===2NiCl +Cl↑+6HO;在 HSO 溶液中被还原,
2 2 2 3 2 2 2 2 3
2Co(OH) +SO+4H+===2Co2++SO+5HO,2Ni(OH) +SO+4H+===2Ni2++SO+5HO。
3 2 3 2
3.钒及其化合物的性质
(1)V:常温下不活泼,不能与非氧化性酸及碱作用,但能溶于氢氟酸、硝酸和王水。
(2)V O :两性氧化物,但以酸性为主,VO +6NaOH===2Na VO +3HO;1 750 ℃发生分解反应:
2 5 2 5 3 4 2
2VO=====2VO +O↑;微溶于水,易形成稳定的胶体;有较强的氧化性:VO +6HCl(浓)===2VOCl +
2 5 2 4 2 2 5 2
Cl↑+3HO。
2 2
(3)VO2+、VO:在酸性介质中,VO具有强氧化性,VO+Fe2++2H+===VO2++Fe3++HO,2VO+
2
HC O+2H+ 2VO2++2CO↑+2HO。
2 2 4 2 2
4.铬及其化合物的性质
(1)Cr:加热时,与O 反应生成Cr O。
2 2 3
(2)Cr O:两性氧化物,Cr O+6H+==2Cr3++3HO;Cr O+2OH-===2CrO+HO。
2 3 2 3 2 2 3 2
(3)Cr(OH) :两性氢氧化物,Cr(OH) +3H+==Cr3++3HO;Cr(OH) +OH-===CrO+2HO。
3 3 2 3 2
(4)CrO与Cr O:(1)可相互转化,2CrO(黄色)+2H 'Cr O(橙色)+HO。(2)强氧化性,如5H++
2 2 2
Cr O+3HSO===2Cr3++3SO+4HO,2NaCrO+16HCl===2CrCl +4NaCl+3Cl↑+8HO。
2 2 2 4 3 2 2
5.钛及其化合物的性质
(1)Ti:常温时与酸不反应,但可与HF反应(Ti+6HF===H TiF +2H↑),也可与热的浓盐酸反应[2Ti+
2 6 2
6HCl(浓) 2TiCl +3H↑]。
3 2
(2)TiO :不溶于水和稀酸,可溶解在HF溶液及热的浓硫酸中;可与Cl 反应:TiO +2Cl===TiCl +
2 2 2 2 4
O ;与碱溶液缓慢反应:TiO +2NaOH===Na TiO +HO;在高温下与 Cl 、C发生反应:TiO +2C+
2 2 2 3 2 2 2
2Cl=====TiCl +2CO。
2 4(3)TiCl :暴露在空气中会冒出白烟,TiCl +3HO===H TiO↓+4HCl;Mg作还原剂时可制备金属钛,
4 4 2 2 3
2Mg+TiCl 2MgCl +Ti。
4 2
6.过渡金属易形成的配合物
(1)金属离子常易水解,其水合离子通常显色,如Cu2+(aq,蓝)、Fe2+(aq,浅绿)、Fe3+(aq,黄)、Cr3+
(aq,绿)。
(2)容易形成配合物的中心离子,如[Cu(NH )]2+、[Ag(NH)]+、[Fe(SCN) ]3-、[Cr(NH )(H O) Cl]2+。
3 4 3 2 6 3 3 2 2
(3)向一些盐溶液中滴加氨水,先生成难溶性碱,继续滴加,生成含氨配合物,如
CuSO (aq)[或AgNO(aq)]――→Cu(OH) (s)[或AgOH(s)]――→[Cu(NH )]2+{或[Ag(NH)]+}。
4 3 2 3 4 3 2
(4)钴的配合物
①Co(Ⅱ)与HO、Cl-配合的平衡转化:[Co(H O) ]2+ [CoCl ]2-。
2 2 6 4
粉红色 蓝色
②Co(Ⅱ)的配合物具有较强的还原性:Co2++6NH →[Co(NH )]2+ [Co(NH )]3+。
3 3 6 3 6
1.(2025·河北省衡水市高三第二次调研)V O 是制造钒铁合金、金属钒的原料,也是重要的催化剂。
2 5
钒矿石中含VO,杂质为大量Al O 和少量CaO等,可通过碱熔法从钒矿石中提取纯度较高的VO,流程
2 5 2 3 2 5
如下:
已知:VO 是以酸性为主的两性化合物,偏钒酸铵(NH VO )与偏钒酸钙[Ca(VO )]均难溶于水,在弱
2 5 4 3 3 2
碱性环境下,偏钒酸钙经盐浸生成碳酸钙。下列说法错误的是
A.气体②的成分为CO
2
B.盐浸工序得到滤渣的成分为CaCO
3
C.洗脱工序中洗脱液的主要成分为NaCl
D.延长沉钒时间、增大NH Cl溶液的浓度有利于沉钒
4
16.[原创题]碳化亚铜(Cu C )这是一种对热和冲击敏感的高爆炸药,把乙炔通入[Cu(NH )] Cl溶液,
2 2 3 2
可以生成碳化亚铜红棕色沉淀,下列关于Cu C 说法正确的是
2 2
A.Cu C 为无机化合物,阴离子可作氧化剂
2 2
B.隔绝空气条件下引爆后不释放气体
C.可以在酸性条件下乙炔气体通过氯化亚铜制得D.易溶于水和大多数有机溶剂
【答案】B
【解析】B项,碳化亚铜为无机化合物,化合物中的阴离子为C 2-,处于低价态,碳元素化合价升高,
2
作还原剂,A不正确;B项,隔绝空气条件下引爆后发生爆炸反应Cu C (s) → 2 Cu(s) + 2 C(s),B正确;
2 2
C项,根据已知条件,乙炔通入[Cu(NH )] Cl生成碳化亚铜沉淀,C不正确;D项,碳化亚铜的红棕色沉
3 2
淀,属于盐难溶于有机溶剂,D不正确;故选B。
3.锌是一种浅灰色的过渡金属。在现代工业中,是电池制造中不可替代且相当重要的金属,以菱锌
矿(主要成分为ZnCO 、ZnO,含有少量SiO 和NaSiO)制备锌单质的流程如图所示:
3 2 2 3
下列说法错误的是( )
A.SO的空间结构为正四面体形
B.滤渣的主要成分为SiO 和HSiO
2 2 3
C.“沉淀”步骤中,消耗CO 的物质的量与消耗Na[Zn(OH) ]的物质的量之比为1∶1
2 2 4
D.“热还原”过程发生了置换反应
4.(2024·长沙模拟)以黄铁矿(主要成分是FeS ,含少量SiO)和软锰矿(主要成分是MnO ,含少量
2 2 2
Fe O、Al O)为原料制备MnSO ·H O的工艺流程如图。下列说法正确的是( )
2 3 2 3 4 2
A.酸浸和沉锰操作均应在较高温度下进行
B.滤渣1的成分中含有S和SiO
2
C.调pH的目的只为除去溶液中的Fe3+
D.沉锰操作中主要反应的离子方程式是 2HCO+Mn2+===MnCO↓ +CO ↑+HO
3 2 2
5.钒元素在酸性溶液中有多种存在形式,其中VO2+为蓝色,VO为淡黄色,VO具有较强的氧化性,
Fe2+、SO等能把VO还原为VO2+。向VOSO 溶液中滴加酸性KMnO 溶液,溶液颜色由蓝色变为淡黄色。
4 4
下列说法不正确的是( )
A.在酸性溶液中氧化性:MnO>VO
B.FeI 溶液与足量酸性(VO )SO 溶液发生反应的离子方程式:Fe2++VO+2H+===Fe3++VO2++HO
2 2 2 4 2C . 向 VOSO 溶 液 中 滴 加 酸 性 KMnO 溶 液 反 应 的 化 学 方 程 式 为 10VOSO + 2HO +
4 4 4 2
2KMnO ===5(VO)SO +2MnSO +2HSO +KSO
4 2 2 4 4 2 4 2 4
D.向含1 mol VO的酸性溶液中滴加1.25 mol FeSO 的溶液完全反应,转移电子为1 mol
4
6.钛合金是一种重要的航空材料,以下是以钛铁矿(主要成分为FeTiO,含FeO和Fe O 等杂质)为原
3 2 3
料制备金属钛及副产品铁红的工艺流程:
已知:①TiO2+易水解为TiO·nH O;高温下钛易与N、H 等反应。
2 2 2 2
②常温下,K [Fe(OH) ]=8.0×10-16,K [FeCO]=3.2×10-11。
sp 2 sp 3
回答下列问题:
(1)钛铁矿溶煮前需要粉碎,其目的是_______ 。
(2)在“滤液”中加入铁屑的作用是_______ 。
(3)FeSO4溶液中加入NH HCO 时还有气体放出,写出反应的化学方程式:_______ ,该反应温度不
4 3
宜过高,原因是_______ 。
(4)制备FeCO 时,若将NH HCO 换成(NH )CO,还会产生Fe(OH) 原因可能是:FeCO+2OH-
3 4 3 4 2 3 2, 3
→Fe(OH) +CO 2-,计算该反应的平衡常数K=_______。
2 3
(5)“富含TiO2+酸性液”加热并过滤后,所得“废液”中溶质的主要成分是_______ 。
(6)已知TiO(s)+2Cl (g)→TiCl (1)+O(g) ΔH=+151kJ·mol-1。该反应极难进行,当向反应体系中加入碳后,
2 2 4 2
则反应在高温条件下能顺利发生,从化学平衡的角度解释原因为_______ 。
(7)镁与TiCl,高温下反应制备粗钛时需加保护气,下列可作为保护气的是_______(填标号)。
A.H B.Ar C.CO D.N
2 2 2
7.一种以钛铁矿(FeTiO,含Fe O、CaO、SiO 等杂质)为主要原料制备钛白粉(TiO)的工艺流程如图
3 2 3 2 2
所示。
已知:①HTiO 不溶于水和稀酸;
2 3
②“酸浸”后钛元素主要以TiO2+形式存在;
③Fe3+在pH=1.8时生成沉淀,pH=4.1时沉淀完全。回答下列问题:
(1)“酸浸”时,常将钛铁矿粉碎,并进行搅拌,其目的是___________。
(2)“酸浸”时,FeTiO 发生反应的化学方程式为___________。
3
(3)滤渣①的主要成分是___________(填化学式)。
(4)流程中加入铁粉的目的是还原体系中的Fe3+。为探究最佳反应条件,某化学兴趣小组在保持反应时
间相同的情况下进行探究得到结果如下图所示。
①保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随pH变化如图甲所示。试分析M点以后体系中
Fe(Ⅲ)含量随着pH增大而增大的原因是___________。
②保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随温度变化如图乙所示。由图可知,还原体系中
Fe(Ⅲ)的最佳反应温度为___________℃。
(5)经处理后,流程中可循环利用的物质除Fe外,还有___________(填化学式)。
(6)如图丙为EFC剑桥法用固体二氧化钛(TiO)生产海绵钛的装置示意图,其原理是在较低的阴极电位
2
下,TiO(阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为___________,产生的气
2
体中X的化学式为___________。
8.用锌精矿(ZnS)和软锰矿(MnO )两种矿料(含少量杂质Fe、Cu、Pb等元素的化合物及SiO)生产硫酸
2 2
锌和硫酸锰的流程如下:已知:ZnSO 的溶解度如图所示:
4
回答下列问题:
(1)基态S原子占据最高能级的原子轨道形状为________________________。
(2)“滤渣1”主要成分为__________________和硫;写出“酸浸”过程中MnO 和ZnS反应的化学方程
2
式:__________________________________________________________________。
(3)“除铁”的萃取剂 1 为磷酸二(2-乙基己基)酯(用 HA 表示),萃取后含铁的物质为
[Fe(HA) (H O) ]ASO ,该物质中Fe3+的配位数为__________。
2 2 2 4
(4)BaS为可溶性钡盐。向“水相1”中加入适量BaS,发生主要反应的离子方程式为____________。
(5)从“反萃取液”中获得ZnSO·H O晶体的操作为控制温度在________________K以上,蒸发至有大
4 2
量固体析出、________________、洗涤、干燥。
(6)ZnSO ·H O产品的纯度可用配位滴定法测定。下列关于滴定分析正确的是____(填字母)。
4 2
A.滴定前,锥形瓶和滴定管均须用标准溶液润洗
B.将标准溶液装入滴定管时,应借助漏斗转移
C.滴定终点时,读取标准溶液体积时俯视滴定管液面,则测得的体积比实际消耗的小
D.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的大
题型二 以陌生物质为切入考查无机推断
1.(2024·浙江1月卷,18,10分)固态化合物Y的组成为MgCaFeMn(CO ),以Y为原料实现如下转
3 4化。
已知:NH 与溶液A中金属离子均不能形成配合物。
3
请回答:
(1)依据步骤Ⅲ,MnCO 、CaCO 和 MgCO 中溶解度最大的是 。写出溶液C中的所有阴离子
3 3 3
。步骤Ⅱ中,加入NH Cl的作用是 。
4
(2)下列说法正确的是_______。
A.气体D是形成酸雨的主要成分 B.固体E可能含有NaCO
2 3
C. 可溶于NH Cl溶液 D.碱性:
4
(3)酸性条件下,固体NaBiO (微溶于水,其还原产物为无色的Bi3+)可氧化Mn2+为MnO -,根据该反应
3 4
原理,设计实验验证Y中含有 元素 ;写出Mn2+转化为MnO -的离子方程式 。
4
2.(2022·浙江省1月卷,28,10分)化合物X由4种元素组成。某兴趣小组按如图流程进行实验:
请回答:
(1)组成X的元素有______,X的化学式为___________。
(2)溶液C中溶质的成分是______(用化学式表示);根据C→D→E的现象,给出相应微粒与阳离子结合
由弱到强的排序_____________________。
(3)X与足量Na反应生成固体F的化学方程式是_____________________。
(4)设计实验确定溶液G中阴离子____________________________________。
3.(2022·浙江省6月卷,28,10分)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:化合物X在空气中加热到 ,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
(4)设计实验,检验尾气中相对活泼的2种气体_______。
4.(2021•浙江1月卷,28,10分)某兴趣小组对化合物X开展探究实验。
其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。请回
答:
(1)组成X的3种元素是______(填元素符号),X的化学式是______。
(2)将固体X加入温热的稀HSO 中,产生气体B,该反应的离子方程式是______。
2 4
(3)步骤I,发生反应的化学方程式是______。
(4)步骤II,某同学未加HO 溶液,发现也会缓慢出现白色浑浊,原因是______。
2 2
(5)关于气体B使品红水溶液褪色的原因,一般认为:B不能使品红褪色,而是B与水反应的生成物使
品红褪色。请设计实验证明______。
5.(2021•浙江6月卷,28,10分)固体化合物X由3种元素组成,某学习小组开展如下探究实验。其中,白色沉淀B能溶于NaOH溶液。请回答:
(1)白色固体C的化学式是_______,蓝色溶液D中含有的溶质是_______(用化学式表示)。
(2)化合物X的化学式是_______;化合物X的一价阴离子与CH 具有相同的空间结构,写出该阴离子
4
的电子式_______。
(3)蓝色溶液A与NH+作用,生成一种气体,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀。
2 5
①写出该反应的离子方程式_______。
②设计实验验证该白色沉淀的组成元素_______。
1.常见特征反应现象
(1)焰色反应:钠元素(黄色)、钾元素(紫色,透过蓝色钴玻璃观察);(2)使品红溶液褪色的气体:
SO (加热后又恢复红色)、Cl(加热后不恢复红色);(3)Fe(OH) 在空气中转变为红褐色Fe(OH) (由白色→灰
2 2 2 3
绿→红褐色);(4)在空气中变为红棕色的气体:NO;(5)气体燃烧火焰呈苍白色:H 在Cl 中燃烧;(6)在空
2 2
气中点燃火焰呈蓝色:CO、H 、CH ;(7)使湿润的红色石蕊试纸变蓝:NH ;(8)使湿润的淀粉碘化钾试纸
2 4 3
变蓝:Cl 、Br 、FeCl 、碘水等;(9)加强碱并加热能放出使湿润的红色石蕊试纸变蓝的气体:原溶液中含
2 2 3
铵盐;(10)氨气遇到挥发性酸生成白烟。
2.一些特殊条件
(1)反应时用到催化剂的反应:实验室制氧气、合成氨、氨的催化氧化等;(2)反应条件是高温的反应:铝热反应,煅烧石灰石的反应,铁和水蒸气的反应,C、H 还原金属氧化
2
物的反应等;
(3)反应条件是电解的反应:电解饱和食盐水、CuSO 溶液等。
4
3.一些特征数据
物质转化时相对分子质量的变化、各元素含量、相对密度等数据都是解题的关键,如CO→CO 、
2
NO→NO 、SO →SO ,转化后分子中都增加1个氧原子,相对分子质量变化均为16。常用物质的相对分子
2 2 3
质量:
NaCO NaHCO Fe O CuO CuSO BaCO BaSO AgCl
2 3 3 2 3 4 3 4
106 84 160 80 160 197 233 143.5
考向 1 已知物质为载体
1.(原创)以铜矿石(主要成分CuO、SiO)为原料实现如下转化:
2
回答下列有关问题:
(1)固体D在工业上用途为_________(写出一例即可),溶液E中含氮微粒有_________。
(2)气体B的主要成分是_______,其常见的一种同素异形体属___________分子(填“极性”或“非极
性”)。
(3)溶液C中含有两种盐,反应IV的离子反应方程式:___________________________。
(4)写出反应V的离子反应方程式:___________________________。
(5)下列说法正确的是_______。
A.SiO 不能与任何酸反应
2
B.反应Ⅱ宜在铁坩埚中进行
C.溶液A经净化处理后可用于黏合剂、防腐剂或制分子筛等
D.反应Ⅲ中发生的离子反应有Ba2++ SO 2-=BaSO ↓
4 4
(6)请设计实验方案验证溶液F中无SO 2-:____________________________________。
4
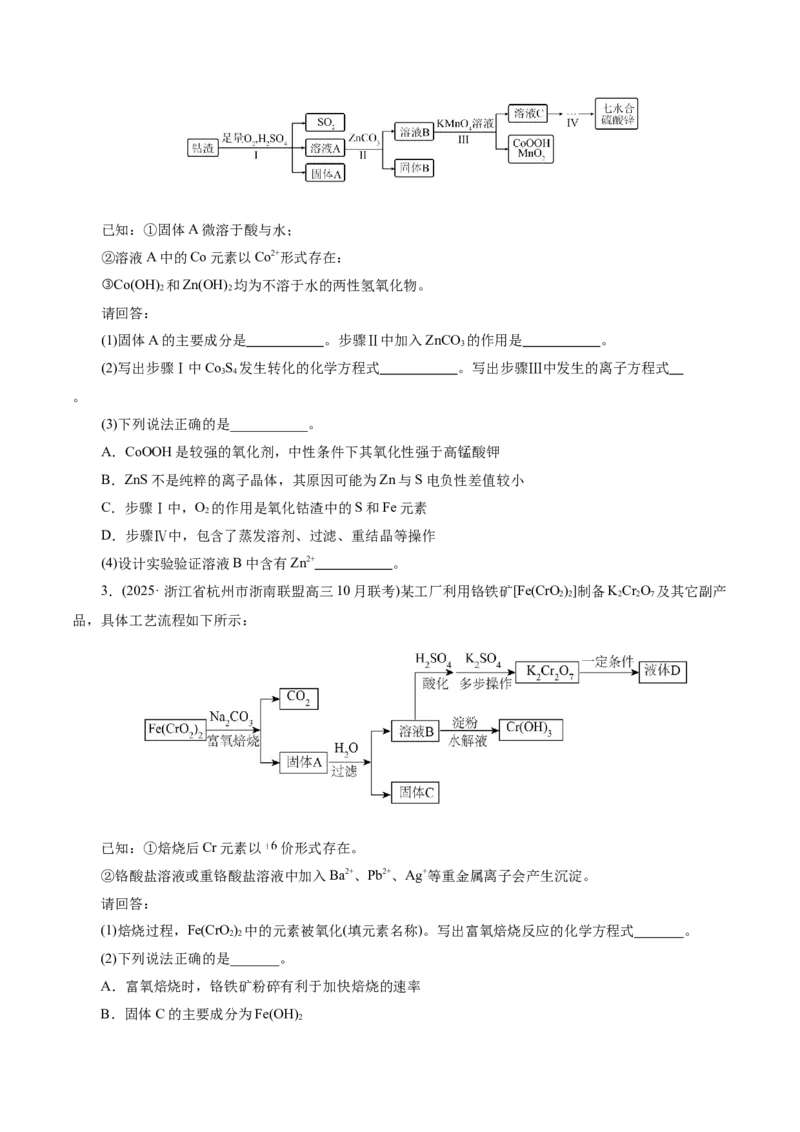
2.(2025·浙江省名校协作体高三联考)湿法炼锌过程中产生的净化钴渣(主要含Co S,ZnS,Ca Fe O)
3 4 2 2 5
实现钴锌分离的流程如下。已知:①固体A微溶于酸与水;
②溶液A中的Co元素以Co2+形式存在:
③Co(OH) 和Zn(OH) 均为不溶于水的两性氢氧化物。
2 2
请回答:
(1)固体A的主要成分是 。步骤Ⅱ中加入ZnCO 的作用是 。
3
(2)写出步骤Ⅰ中Co S 发生转化的化学方程式 。写出步骤Ⅲ中发生的离子方程式
3 4
。
(3)下列说法正确的是___________。
A.CoOOH是较强的氧化剂,中性条件下其氧化性强于高锰酸钾
B.ZnS不是纯粹的离子晶体,其原因可能为Zn与S电负性差值较小
C.步骤Ⅰ中,O 的作用是氧化钴渣中的S和Fe元素
2
D.步骤Ⅳ中,包含了蒸发溶剂、过滤、重结晶等操作
(4)设计实验验证溶液B中含有Zn2+ 。
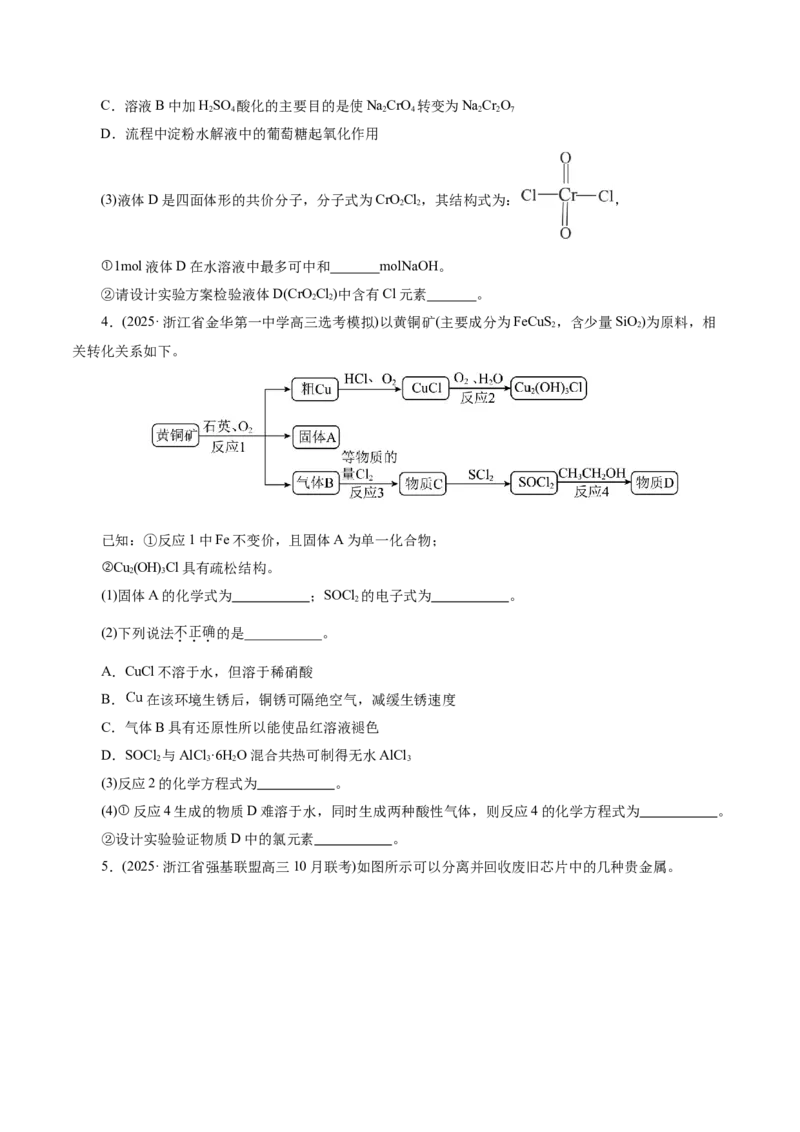
3.(2025· 浙江省杭州市浙南联盟高三10月联考)某工厂利用铬铁矿[Fe(CrO)]制备KCr O 及其它副产
2 2 2 2 7
品,具体工艺流程如下所示:
已知:①焙烧后Cr元素以 价形式存在。
②铬酸盐溶液或重铬酸盐溶液中加入Ba2+、Pb2+、Ag+等重金属离子会产生沉淀。
请回答:
(1)焙烧过程,Fe(CrO) 中的元素被氧化(填元素名称)。写出富氧焙烧反应的化学方程式 。
2 2
(2)下列说法正确的是_______。
A.富氧焙烧时,铬铁矿粉碎有利于加快焙烧的速率
B.固体C的主要成分为Fe(OH)
2C.溶液B中加HSO 酸化的主要目的是使NaCrO 转变为NaCr O
2 4 2 4 2 2 7
D.流程中淀粉水解液中的葡萄糖起氧化作用
(3)液体D是四面体形的共价分子,分子式为CrOCl,其结构式为: ,
2 2
①1mol液体D在水溶液中最多可中和 molNaOH。
②请设计实验方案检验液体D(CrOCl)中含有Cl元素 。
2 2
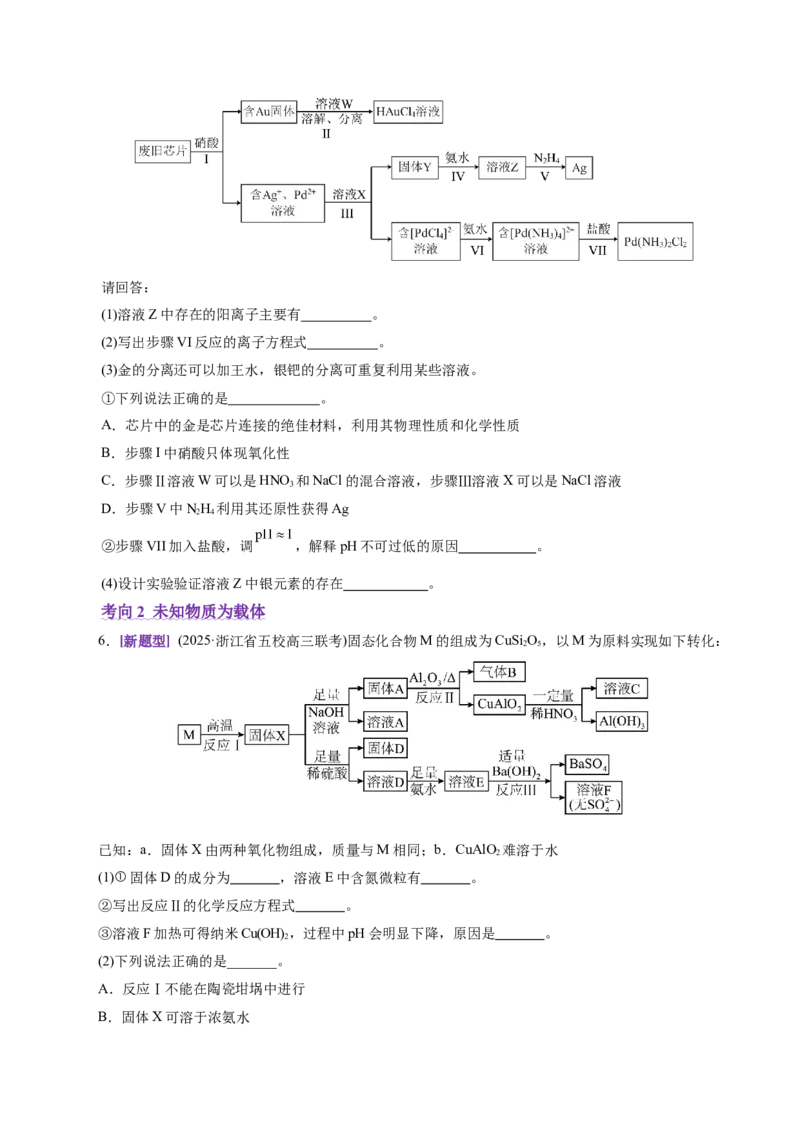
4.(2025·浙江省金华第一中学高三选考模拟)以黄铜矿(主要成分为FeCuS,含少量SiO)为原料,相
2 2
关转化关系如下。
已知:①反应1中Fe不变价,且固体A为单一化合物;
②Cu(OH) Cl具有疏松结构。
2 3
(1)固体A的化学式为 ;SOCl 的电子式为 。
2
(2)下列说法不正确的是___________。
A.CuCl不溶于水,但溶于稀硝酸
B. 在该环境生锈后,铜锈可隔绝空气,减缓生锈速度
C.气体B具有还原性所以能使品红溶液褪色
D.SOCl 与AlCl·6H O混合共热可制得无水AlCl
2 3 2 3
(3)反应2的化学方程式为 。
(4)①反应4生成的物质D难溶于水,同时生成两种酸性气体,则反应4的化学方程式为 。
②设计实验验证物质D中的氯元素 。
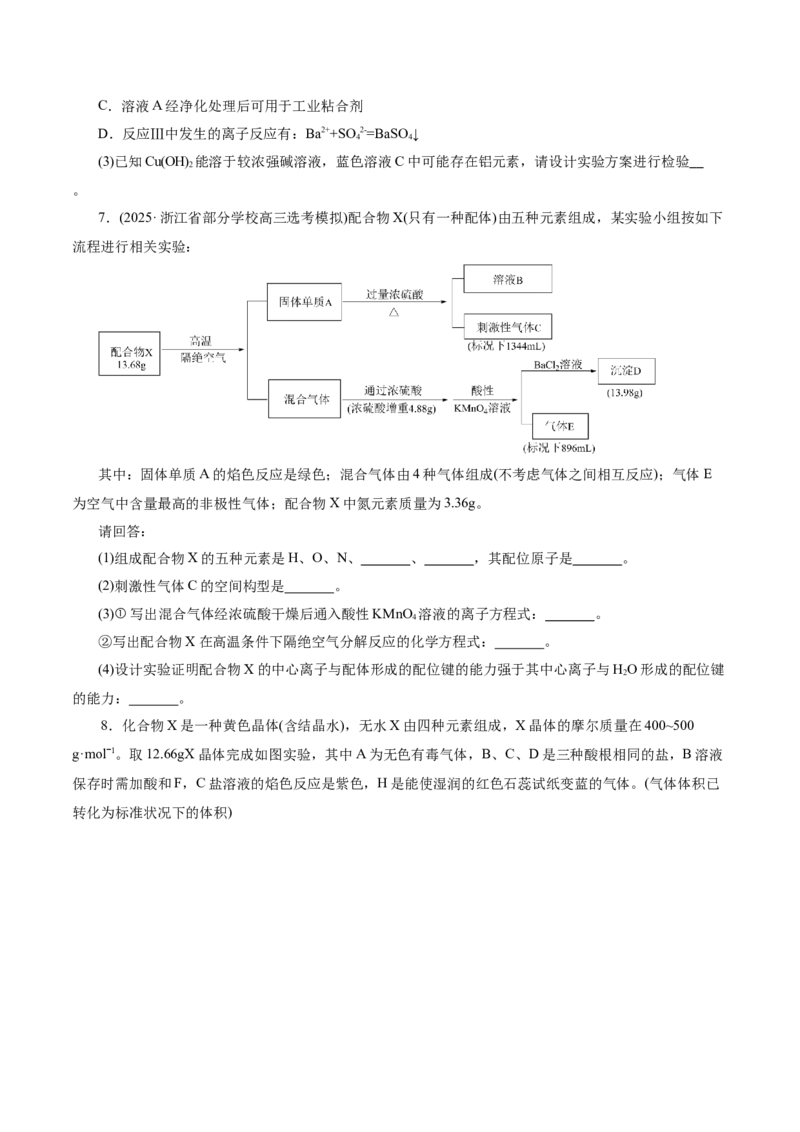
5.(2025·浙江省强基联盟高三10月联考)如图所示可以分离并回收废旧芯片中的几种贵金属。请回答:
(1)溶液Z中存在的阳离子主要有 。
(2)写出步骤VI反应的离子方程式 。
(3)金的分离还可以加王水,银钯的分离可重复利用某些溶液。
①下列说法正确的是 。
A.芯片中的金是芯片连接的绝佳材料,利用其物理性质和化学性质
B.步骤I中硝酸只体现氧化性
C.步骤Ⅱ溶液W可以是HNO 和NaCl的混合溶液,步骤Ⅲ溶液X可以是NaCl溶液
3
D.步骤V中NH 利用其还原性获得Ag
2 4
②步骤VII加入盐酸,调 ,解释pH不可过低的原因 。
(4)设计实验验证溶液Z中银元素的存在 。
考向 2 未知物质为载体
6.[新题型] (2025·浙江省五校高三联考)固态化合物M的组成为CuSi O,以M为原料实现如下转化:
2 5
已知:a.固体X由两种氧化物组成,质量与M相同;b.CuAlO 难溶于水
2
(1)①固体D的成分为 ,溶液E中含氮微粒有 。
②写出反应Ⅱ的化学反应方程式 。
③溶液F加热可得纳米Cu(OH),过程中pH会明显下降,原因是 。
2
(2)下列说法正确的是_______。
A.反应Ⅰ不能在陶瓷坩埚中进行
B.固体X可溶于浓氨水C.溶液A经净化处理后可用于工业粘合剂
D.反应Ⅲ中发生的离子反应有:Ba2++SO2-=BaSO↓
4 4
(3)已知Cu(OH) 能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
2
。
7.(2025·浙江省部分学校高三选考模拟)配合物X(只有一种配体)由五种元素组成,某实验小组按如下
流程进行相关实验:
其中:固体单质A的焰色反应是绿色;混合气体由4种气体组成(不考虑气体之间相互反应);气体E
为空气中含量最高的非极性气体;配合物X中氮元素质量为3.36g。
请回答:
(1)组成配合物X的五种元素是H、O、N、 、 ,其配位原子是 。
(2)刺激性气体C的空间构型是 。
(3)①写出混合气体经浓硫酸干燥后通入酸性KMnO 溶液的离子方程式: 。
4
②写出配合物X在高温条件下隔绝空气分解反应的化学方程式: 。
(4)设计实验证明配合物X的中心离子与配体形成的配位键的能力强于其中心离子与HO形成的配位键
2
的能力: 。
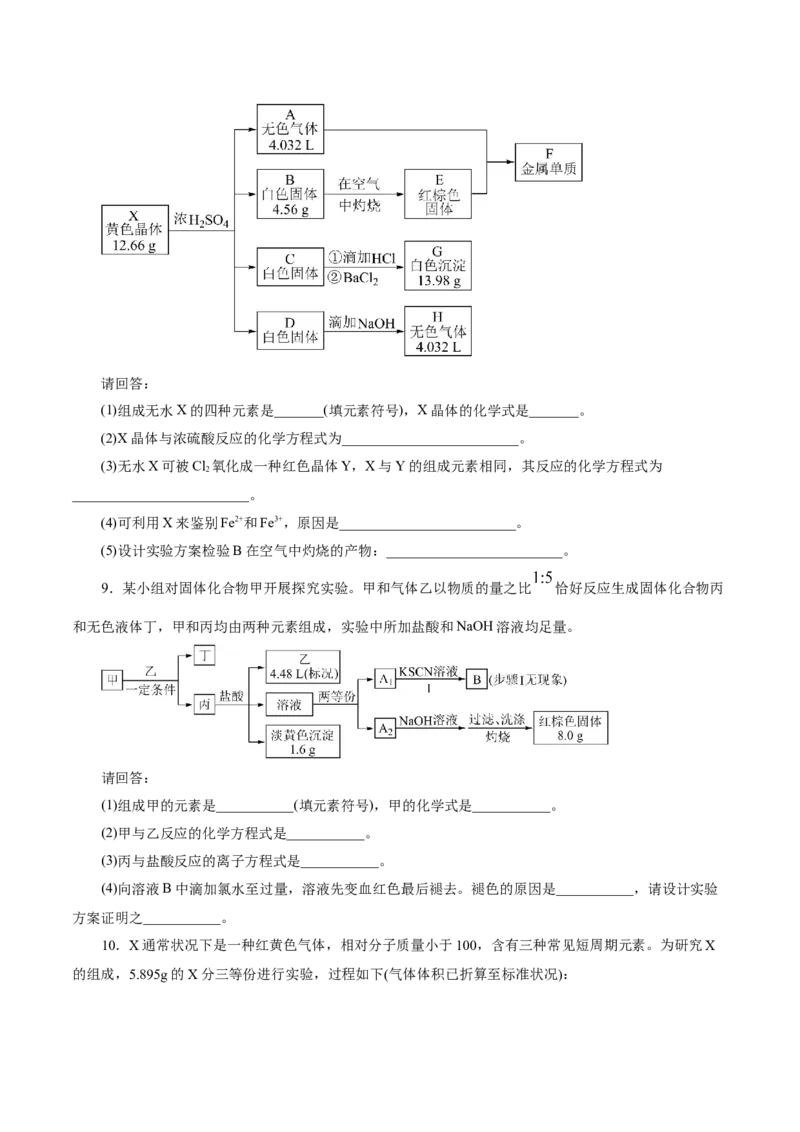
8.化合物X是一种黄色晶体(含结晶水),无水X由四种元素组成,X晶体的摩尔质量在400~500
g·molˉ1。取12.66gX晶体完成如图实验,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B溶液
保存时需加酸和F,C盐溶液的焰色反应是紫色,H是能使湿润的红色石蕊试纸变蓝的气体。(气体体积已
转化为标准状况下的体积)请回答:
(1)组成无水X的四种元素是_______(填元素符号),X晶体的化学式是_______。
(2)X晶体与浓硫酸反应的化学方程式为_________________________。
(3)无水X可被Cl 氧化成一种红色晶体Y,X与Y的组成元素相同,其反应的化学方程式为
2
_________________________。
(4)可利用X来鉴别Fe2+和Fe3+,原因是_________________________。
(5)设计实验方案检验B在空气中灼烧的产物:_________________________。
9.某小组对固体化合物甲开展探究实验。甲和气体乙以物质的量之比 恰好反应生成固体化合物丙
和无色液体丁,甲和丙均由两种元素组成,实验中所加盐酸和NaOH溶液均足量。
请回答:
(1)组成甲的元素是___________(填元素符号),甲的化学式是___________。
(2)甲与乙反应的化学方程式是___________。
(3)丙与盐酸反应的离子方程式是___________。
(4)向溶液B中滴加氯水至过量,溶液先变血红色最后褪去。褪色的原因是___________,请设计实验
方案证明之___________。
10.X通常状况下是一种红黄色气体,相对分子质量小于100,含有三种常见短周期元素。为研究X
的组成,5.895g的X分三等份进行实验,过程如下(气体体积已折算至标准状况):请回答:
(1)X的化学式为_______。溶液A的成分为_______。
(2)X与HO反应的化学方程式为_______。
2
(3)金(Au)可溶于浓B溶液生成C和金的一价配离子(与CH 具有相同的空间结构),写出该反应的化学
4
方程式:_______。
(4)设计一个实验方案,探究溶液F中溶质的阳离子成分:_______。