文档内容
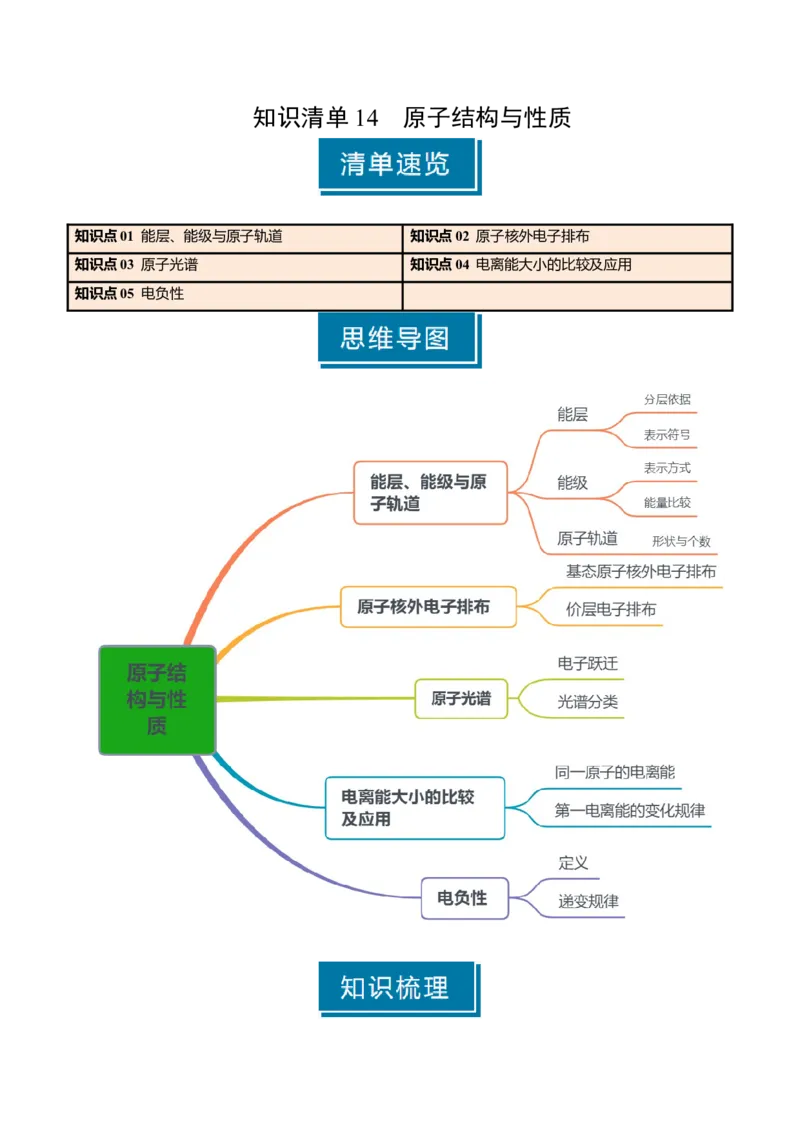
知识清单 14 原子结构与性质
知识点01 能层、能级与原子轨道 知识点02 原子核外电子排布
知识点03 原子光谱 知识点04 电离能大小的比较及应用
知识点05 电负性知识点 01 能层、能级与原子轨道
能层、能级与原子轨道的含义
1.能层(n):(又称:电子层)
(1)分层依据:按照电子的能量差异
(2)表示符号:K、L、M、N、O、P、Q
2.能级:在多电子原子中,同一能层里电子的_能量__也可能不同,又将其分成不同的能级,通常用
_ s 、 p 、 d 、 f __等表示,同一能层里,各能级的能量按_ s 、 p 、 d 、 f __的顺序依次升高,即
_ E (s)< E (p)< E (d)< E (f) __。
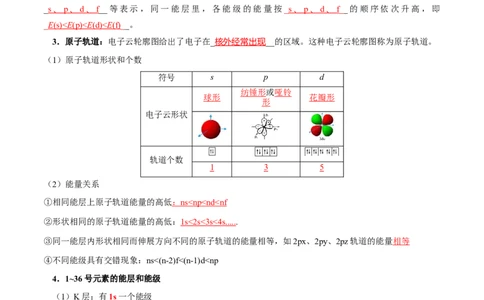
3.原子轨道:电子云轮廓图给出了电子在_核外经常出现__的区域。这种电子云轮廓图称为原子轨道。
(1)原子轨道形状和个数
符号 s p d
纺锤形或哑铃
球形 花瓣形
形
电子云形状
轨道个数
1 3 5
(2)能量关系
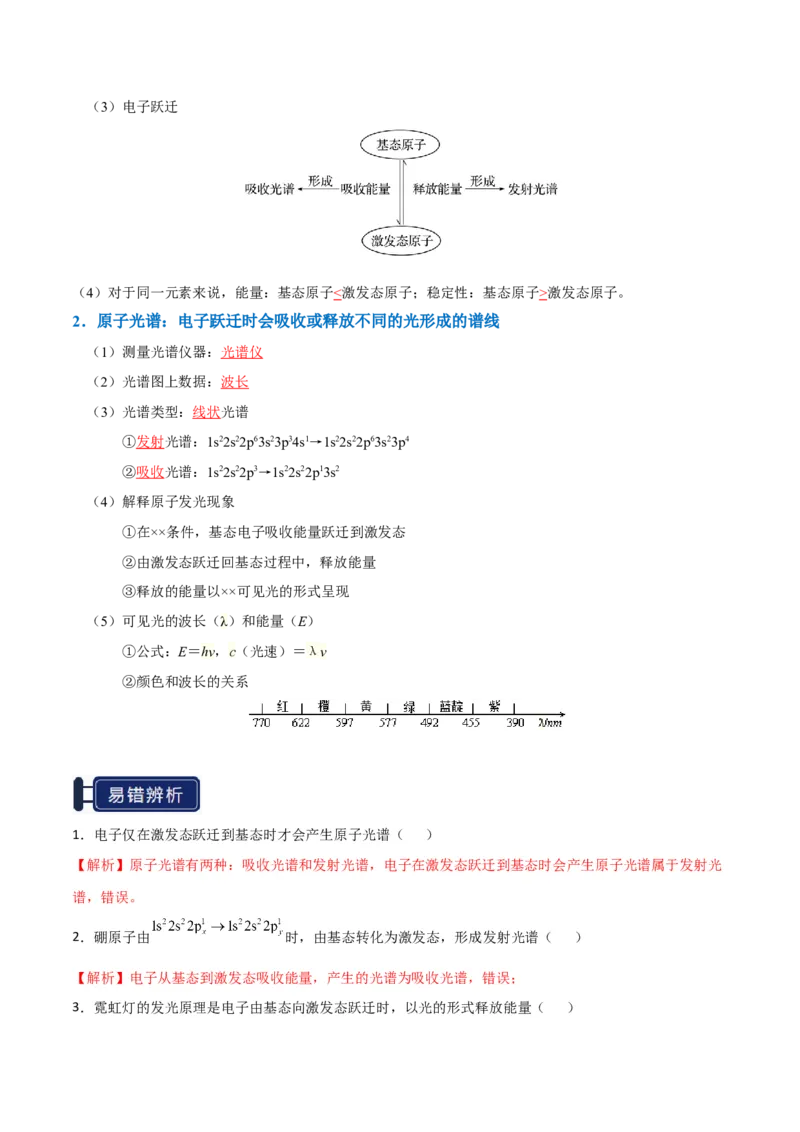
①相同能层上原子轨道能量的高低 : ns激发态原子。
2.原子光谱:电子跃迁时会吸收或释放不同的光形成的谱线
(1)测量光谱仪器:光谱仪
(2)光谱图上数据:波长
(3)光谱类型:线状光谱
①发射光谱:1s22s22p63s23p34s1→1s22s22p63s23p4
②吸收光谱:1s22s22p3→1s22s22p13s2
(4)解释原子发光现象
①在××条件,基态电子吸收能量跃迁到激发态
②由激发态跃迁回基态过程中,释放能量
③释放的能量以××可见光的形式呈现
(5)可见光的波长(λ)和能量(E)
①公式:E=hv,c(光速)=λv
②颜色和波长的关系
1.电子仅在激发态跃迁到基态时才会产生原子光谱( )
【解析】原子光谱有两种:吸收光谱和发射光谱,电子在激发态跃迁到基态时会产生原子光谱属于发射光
谱,错误。
2.硼原子由 时,由基态转化为激发态,形成发射光谱( )
【解析】电子从基态到激发态吸收能量,产生的光谱为吸收光谱,错误;
3.霓虹灯的发光原理是电子由基态向激发态跃迁时,以光的形式释放能量( )【解析】霓虹灯发光是由于霓虹灯管通电后电子获得能量从基态跃迁到激发态,激发态能量高,电子不稳
定,从激发态跃迁到较低的能级,以光的形式释放能量,项错误;
4.“火树银花合,星桥铁锁开”涉及到发光过程是电子由基态到激发态的跃迁过程( )
【解析】“火树银花合,星桥铁锁开”涉及到的发光过程是电子由激发态跃迁至能量较低的激发态或基态
的过程,释放能量,错误;
5.LED灯光与原子核外电子跃迁释放能量有关( )
【解析】LED灯通电后,电子吸收能量由基态跃迁到激发态,然后再从激发态跃迁到基态,将能量以光的
形式释放出来,所以LED灯光与原子核外电子跃迁释放能量有关,正确;
6.萤石夜晚发光与电子跃迁有关( )
【解析】荧光与电子跃迁有关,萤石夜晚发光与电子跃迁有关,正确;
7.基态原子变为激发态原子时要释放能量( )
【解析】基态原子的能量低于激发态原子的能量,所以基态原子变为激发态原子时要吸收能量,错误;
1.下列说法正确的是
A.基态原子吸收能量只能变成一种激发态
B.某原子的电子排布式为 ,其表示的是基态原子的电子排布
C.日常生活中我们看到的许多可见光,如霓虹灯光、节日焰火,是因为原子核外电子发生跃迁吸收能
量导致的
D.电子仅从激发态跃迁到基态时才会产生原子光谱
【答案】B
【解析】A.基态原子吸收不同的能量能变成不同的激发态,A错误;
B.根据构造原理,原子的电子排布式为 ,其表示的是基态K原子的电子排布,B正确;
C.光是电子跃迁释放能量的重要形式,不同元素的原子中电子发生跃迁时吸收或放出的能量是不同的,
霓虹灯光、节日焰火等都与原子核外电子跃迁释放能量有关,而不是吸收能量导致的,C错误;
D.原子光谱有两种,电子从基态跃迁到激发态时产生吸收光谱,电子从较高能级跃迁到较低能级时产生
发射光谱,D错误;
故选B。
2.下列有关说法中正确的是A.电子易从 跃迁到 上
B.电子只有获得能量后才能发生跃迁
C.核外电子排布式为 的碳原子能产生发射光谱
D.灼烧含钠元素物质时,产生黄光过程中相应电子的能量会升高
【答案】C
【解析】A.电子容易在能量相近的不同能级之间产生跃迁, ,电子不易从 跃迁到 上,
A错误;
B.电子由激发态跃迁到基态释放能量,B错误;
C.该碳原子有处于激发态的电子,转化为基态原子的电子 时,能产生发射光谱,C正确;
D.钠元素产生黄光时电子会释放能量,使电子的能量降低,D错误;
答案选C。
3.下列有关光谱的说法中不正确的是
A.吸收光谱和发射光谱都属于原子光谱
B.焰色试验产生的颜色和五彩霓虹灯都是发射光谱
C.原子中的电子在从基态向激发态跃迁时产生的是吸收光谱
D.基态原子获得能量被激发的过程中,会产生暗背景亮线的原子光谱
【答案】D
【解析】A.原子光谱分吸收光谱和发射光谱,A正确;
B.焰色反应产生的颜色和五彩霓虹灯都是发射光谱,B正确;
C.原子中的电子在从基态向激发态跃迁时需要吸收能量,产生的是吸收光谱,C正确;
D.基态原子获得能量被激发,跃迁需要吸收能量,会产生暗背景暗线的原子光谱,即吸收光谱,D错误;
本题选D。
知识点 04 电离能大小的比较及应用
1.概念:气态原子或离子失去1 个电子所需要的最小能量
(1)第一电离能(I):M(g)-e-=M+(g)
1
(2)第二电离能(I):M+(g)-e-=M2+(g)
2(3)第n电离能(I):M(n-1)+(g)-e-=Mn+(g)
n
2.同一原子各级电离能
(1)变化规律:I<I<I<…
1 2 3
(2)变化原因
①电子分层排布 ②各能层能量不同
3.第一电离能变化规律
(1)根据递变规律判断
①基本规律:周期表右上角位置的He 原子的I 最大
1
②特殊规律:同一周期中I,ⅡA>ⅢA;ⅤA>ⅥA
1
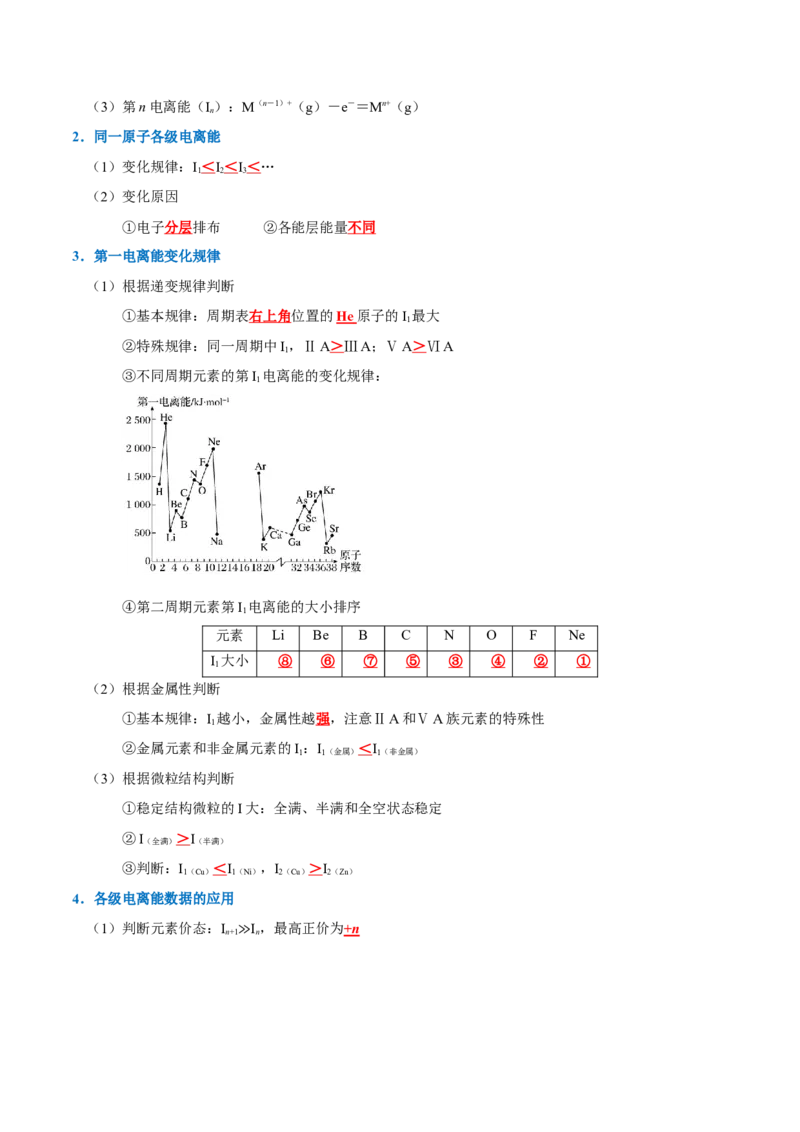
③不同周期元素的第I 电离能的变化规律:
1
④第二周期元素第I 电离能的大小排序
1
元素 Li Be B C N O F Ne
I 大小 ⑧ ⑥ ⑦ ⑤ ③ ④ ② ①
1
(2)根据金属性判断
①基本规律:I 越小,金属性越强,注意ⅡA和ⅤA族元素的特殊性
1
②金属元素和非金属元素的I:I <I
1 1(金属) 1(非金属)
(3)根据微粒结构判断
①稳定结构微粒的I大:全满、半满和全空状态稳定
②I >I
(全满) (半满)
③判断:I <I ,I >I
1(Cu) 1(Ni) 2(Cu) 2(Zn)
4.各级电离能数据的应用
(1)判断元素价态:I I,最高正价为 + n
n+1 n
≫(2)判断某一级电离能最大:第n级电离能最大,说明其最高正价为 + ( n - 1 ) 价
(3)判断电离能的突增点:形成相应电子层最稳定状态后再失去1个电子
突增点的电离能级数
元素
第一
原子 第二次 第三次
次
P I I
6 14
Ca I I I
3 11 19
1.判断正误,正确的打“√”,错误的打“×”。
(1)C、N、O、F四种元素第一电离能从大到小的顺序是N>O>F>C( )
(2)元素的电负性越大,非金属性越强,第一电离能也越大( )
(3)主族元素的电负性越大,元素原子的第一电离能一定越大( )
(4)第一电离能O>N。( )
(5)钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能。( )
(6)根据元素周期律,原子半径Ga小于As,第一电离能Ga大于As。( )
(7)最外层电子排布为ns2np6(当只有K层时为1s2)的原子第一电离能较大。( )
【答案】(1) ( × )(2) ( × )(3) ( × )(4) ( × )(5) ( × )(6) ( × )(7) ( √ )
1.填空。
(1)N、O、S的第一电离能 大小为 ,原因是 。
(2)Li及其周期表中相邻元素的第一电离能 如表所示。 ,原因是 。
,原因是 。
520 900 801Na Mg Al
496 738 578
(3)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. B. C. D.
【答案】(1)N原子2p轨道半充满,比相邻的O原子更稳定,更难失电子;O、S同主族,S原子半径大于O
原子,更易失去电子
(2) Na与Li同族,Na电子层数多,原子半径大,易失去电子;Li、Be、B均为第二周期元素,随原子
序数递增,第一电离能呈增大的趋势,而Be的2s能级处于全充满状态,较难失去电子,故Be的第一电离
能比B的大; Be为 全充满稳定结构,第一电离能最大。与Li相比,B核电荷数大,原子半径小,
较难失去电子,第一电离能较大
(3)A
【解析】(1)N、O同周期,N原子2p轨道半充满,为稳定结构,比相邻的O原子更难失电子,故N的第
一电离能比O大;O、S同主族,S原子半径大于O原子,更易失去电子,故O的第一电离能比S大,所以
N、O、S的第一电离能 大小为 。
(2)Li和Na均为第ⅠA族元素,由于Na电子层数多,原子半径大,故Na比Li容易失去最外层电子,即
;Li、Be、B均为第二周期元素,随原子序数递增,第一电离能呈增大的趋势,而Be的2s
能级处于全充满状态,较难失去电子,故Be的第一电离能比B的大,所以 。
(3)结合各选项可知,B项为基态镁原子,C项为激发态镁原子,A项和D项均为Mg失去一个电子得到
的 ;失去电子后,原子核对最外层电子的吸引力更强,所以 失去一个电子所需能量比Mg失去一
个电子所需能量更大,且由于 ,3s能级上的电子更稳定,故电离3s能级上的电子所需能量更大,故选A。
2.图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图
是 (填标号),判断的根据是 ;第三电离能的变化图是 (填标号)。
a. b. c.
【答案】 a 同一周期第一电离能的总体趋势是增大的,但由于N的 能级为半充满状态,因此
N的第一电离能较C、O两种元素大 b
【解析】C、N、O、F四种元素位于同一周期,同周期元素第一电离能的总体趋势是增大的,但由于N的
能级为半充满状态,(第ⅡA族元素的s能级处于全充满状态;第ⅤA族的p能极处于半充满状态,故同
周期第ⅡA族和第ⅤA族元素的第一电离能均北相邻主族的大。)因此N的第一电离能较C、O两种元素大,
故C、N、O、F的第一电离能从小到大的顺序为 ,满足这一规律的图像为图a;
气态基态 价阳离子失去1个电子生成气态基态 价阳离子所需要的能量为该原子的第三电离能,同周
期原子的第三电离能的总体趋势也是增大的,但由于C原子在失去2个电子之后的 能级为全充满状态,
因此其再失去1个电子需要的能量稍高,N、O、F在失去2个电子后,2p轨道上电子分别为1个、2个、3
个,再失去一个电子所需能量随着核电荷数增加而变大,则满足这一规律的图像为图b;
故答案为:a;同一周期第一电离能的总体趋势是增大的,但由于N的2p能级为半充满状态,因此N的第
一电离能较C、O两种元素大;b。
知识点 05 电负性
1.意义:衡量元素的原子在化合物中得电子能力
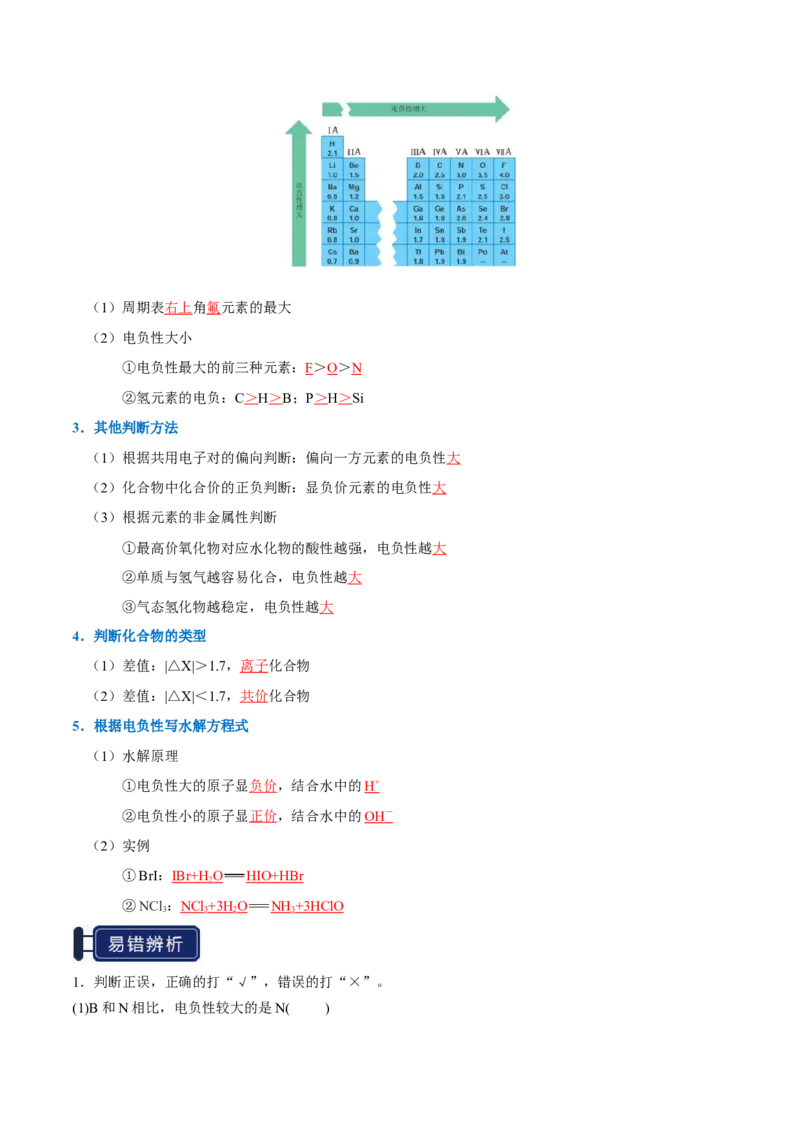
2.递变规律(1)周期表右上角氟元素的最大
(2)电负性大小
①电负性最大的前三种元素:F>O>N
②氢元素的电负:C>H>B;P>H>Si
3.其他判断方法
(1)根据共用电子对的偏向判断:偏向一方元素的电负性大
(2)化合物中化合价的正负判断:显负价元素的电负性大
(3)根据元素的非金属性判断
①最高价氧化物对应水化物的酸性越强,电负性越大
②单质与氢气越容易化合,电负性越大
③气态氢化物越稳定,电负性越大
4.判断化合物的类型
(1)差值:|△X|>1.7,离子化合物
(2)差值:|△X|<1.7,共价化合物
5.根据电负性写水解方程式
(1)水解原理
①电负性大的原子显负价,结合水中的 H +
②电负性小的原子显正价,结合水中的 OH -
(2)实例
①BrI:IBr+H O HIO+HBr
2
②NCl : N Cl +3H O NH +3HCl O
3 3 2 3
1.判断正误,正确的打“√”,错误的打“×”。
(1)B和N相比,电负性较大的是N( )(2)元素的电负性越大,非金属性越强,第一电离能也越大( )
(3)电负性大的元素非金属性强( )
(4)主族元素的电负性越大,元素原子的第一电离能一定越大( )
(5)在元素周期表中,同周期元素电负性从左到右越来越大( )
(6)金属元素电负性一定小于非金属元素电负性( )
(7)在形成化合物时,电负性越小的元素越容易显示正价。( )
【答案】(1)( √ )(2) ( × )(3) ( √ )(4) ( × )(5) ( √ )(6) ( √ )(7) ( √ )
1.侯氏制碱法工艺流程中的主反应为 ,其中W、X、Y、Z、Q、R分
别代表相关化学元素。下列说法正确的是
A.原子半径: B.第一电离能:
C.单质沸点: D.电负性:
【答案】C
【分析】侯氏制碱法主反应的化学方程式为 ,则可推出W、
X、Y、Z、Q、R分别为H元素、C元素、N元素、O元素、 元素、 元素。
【解析】A.一般原子的电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小,则原子半
径: ,故A错误;
B.同周期从左到右元素第一电离能呈增大趋势,ⅡA族、ⅤA族原子的第一电离能大于同周期相邻元素,
则第一电离能: ,故B错误;
C. 、 为分子晶体,相对分子质量越大,沸点越高,二者在常温下均为气体, 在常温下为固体,
则沸点: ,故C正确;
D.同周期元素,从左往右电负性逐渐增大,同族元素,从上到下电负性逐渐减小,电负性: ,
故D错误;
故选C。
2.Ga、As、Se位于元素周期表第四周期。下列说法正确的是
A.原子半径:B.第一电离能:
C.元素电负性:
D.可在周期表中Se附近寻找优良的催化剂材料
【答案】B
【解析】A.同周期元素从左到右,原子半径逐渐减小,则原子半径:r(Ga)>r(As)>r(Se),故A项错误;
B.同周期元素从左到右,第一电离能呈增大趋势,但第ⅡA族、第VA族元素的第一电离能大于相邻元素,
则第一电离能:Ι (Ge)<Ι (Se)<Ι (As),故B项正确;
1 1 1
C.同周期元素从左到右,元素的电负性逐渐增大,则元素电负性:χ(Ge)<χ(As)<χ(Se),故C项错误;
D.在过渡元素区,可寻找优良的催化剂材料,故D项错误;
故本题选B。