文档内容
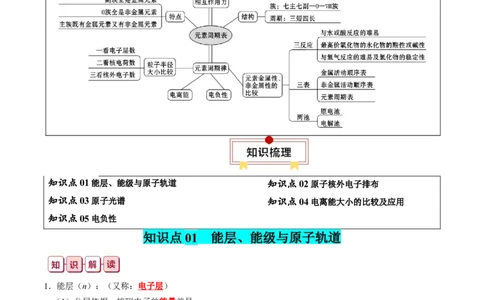
知识清单 15 原子结构与性质
知识点01能层、能级与原子轨道 知识点02原子核外电子排布
知识点03原子光谱 知识点04电离能大小的比较及应用
知识点05电负性
知识点 01 能层、能级与原子轨道
1.能层(n):(又称:电子层)
(1)分层依据:按照电子的能量差异
(2)表示符号:K、L、M、N、O、P、Q
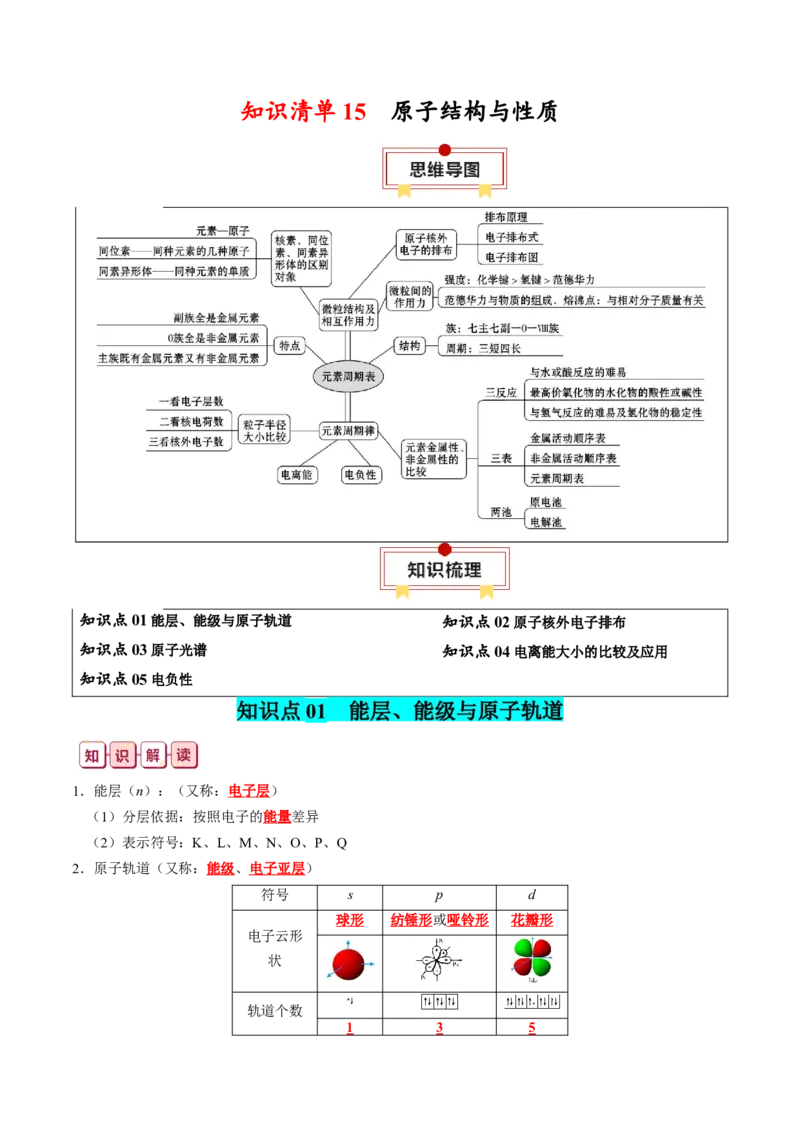
2.原子轨道(又称:能级、电子亚层)
符号 s p d
球形 纺锤形或哑铃形 花瓣形
电子云形
状
轨道个数
1 3 53.1~36号元素的能层和能级
(1)K层:有1s 一个电子亚层
(2)L层:有2s、2p 两个电子亚层
(3)M层:有3s、3p、3d 三个电子亚层
(4)N层:有4s、4p、4d、4f 四个电子亚层
4.原子核外电子排布的原理
(1)能量最低原理:电子尽先排布在能量最低的轨道中。
(2)泡利不相容原理:每个原子轨道上最多只能容纳 2 个自旋方向相反的电子。如:
(3)洪特规则:电子在能量相同原子轨道上排布时,应尽可能分占不同的轨道而且自旋方向相同。
错误 正确
N原子的2p轨道
(4)洪特规则特例:能量相同的原子轨道在下列情况时,体系能量最低
①全满;即s2、p6、d10
②半满;即s1、p3、d5
③全空;即s0、p0、d0
注意:(1)能层数=电子层数。(2) 第一能层(K),只有s能级;第二能层(L),有s、p两种能级,p能级上有
三个原子轨道p、p、p,它们具有相同的能量;第三能层(M),有s、p、d三种能级。
x y z
【典例01】硫的下列4种微粒,若失去一个电子所需要能量最多的是
A.[Ne] B.[Ne] C.[Ne] D.[Ne]
【答案】B
【解析】A、B、C、D四项中的微粒分别对应基态S、 、激发态 、激发态S,激发态上电子能量高,
不稳定,易失去,故需要能量最多的是基态的 ;
答案选B。
【典例02】下列说法正确的是
A.3s2表示3s能级有2个轨道
B.p能级的能量一定比s能级的能量高
C.在离核越近区域内运动的电子,能量越低
D.1个原子轨道里,最少要容纳2个电子
【答案】C【解析】A.s能级只有1个轨道,3s2表示3s能级容纳2个电子,A不正确;
B.p能级的能量不一定比s能级的能量高,如2p能级的能量低于3s能级的能量,B不正确;
C.能量较低的电子,在离核较近的区域运动,在离核越近区域内运动的电子,能量越低,C正确;
D.1个原子轨道里,最多能容纳2个电子,也可以容纳1个电子或不容纳电子,D不正确;
故选C。
知识点 02 原子核外电子排布
1.基态原子核外电子排布
(1)21~30号:[Ar]3dx4s2
①一般最后1位数是几,x就等于几
② Cr:[Ar]3d44s2→ [ A r ] 3d 5 4 s 1
24
③ Cu:[Ar]3d94s2→ [ A r ] 3d 1 0 4 s 1
29
(2)31~36号:[Ar]3d104s24px
①最后1位数是几,x就等于几
② Ge: [ A r ] 3d 1 0 4 s 2 4p 2
32
③ Se: [ A r ] 3d 1 0 4 s 2 4p 4
34
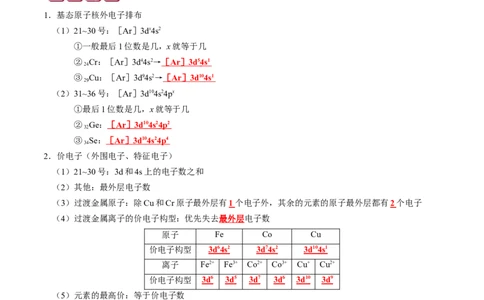
2.价电子(外围电子、特征电子)
(1)21~30号:3d和4s上的电子数之和
(2)其他:最外层电子数
(3)过渡金属原子:除Cu和Cr原子最外层有1 个电子外,其余的元素的原子最外层都有2 个电子
(4)过渡金属离子的价电子构型:优先失去最外层电子数
原子 Fe Co Cu
价电子构型 3d 6 4s 2 3d 7 4s 2 3d 10 4s 1
离子 Fe2+ Fe3+ Co2+ Co3+ Cu+ Cu2+
价电子构型 3d 6 3d 5 3d 7 3d 6 3d 10 3d 9
(5)元素的最高价:等于价电子数
元素 Cr Fe Mn As
价电子构
3d 5 4s 1 3d 4 4s 2 3d 5 4s 2 4s 2 4p 3
型
最高价 +6 +8 +7 +5
(6)过渡金属原子或离子的结构示意图
微粒 V Cr3+ Cu+
结构
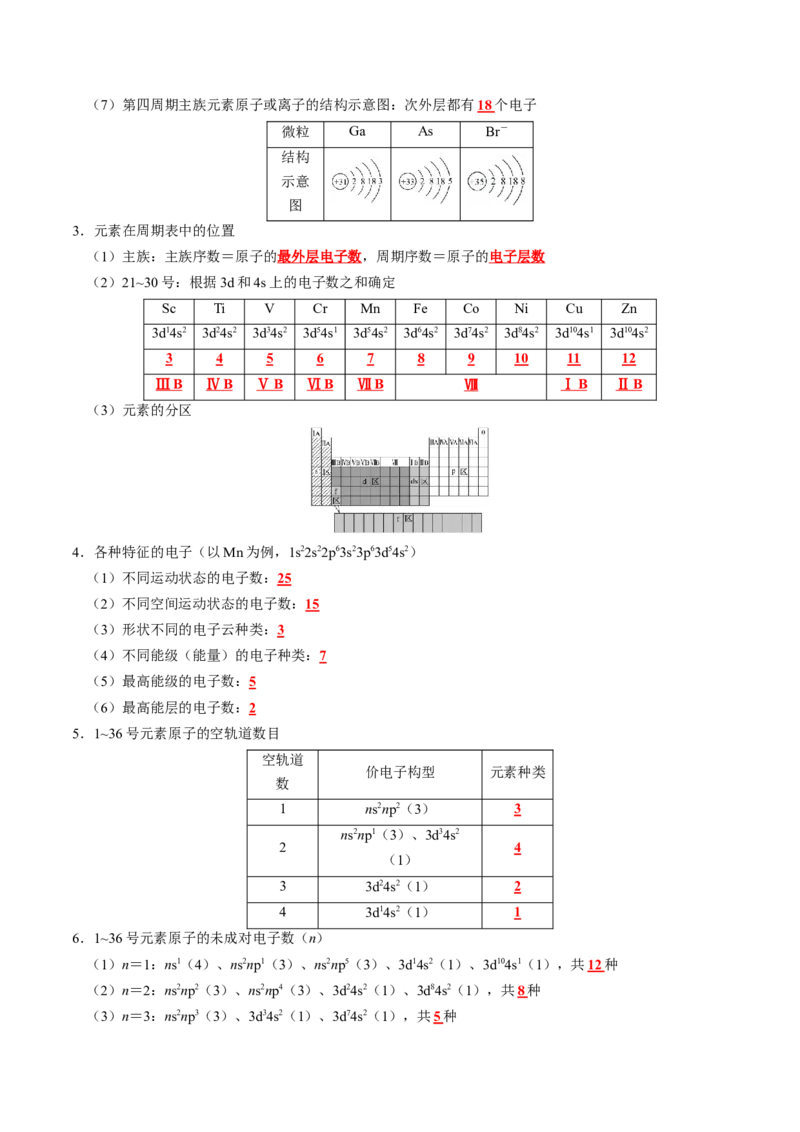
示意图(7)第四周期主族元素原子或离子的结构示意图:次外层都有18 个电子
微粒 Ga As Br-
结构
示意
图
3.元素在周期表中的位置
(1)主族:主族序数=原子的最外层电子数,周期序数=原子的电子层数
(2)21~30号:根据3d和4s上的电子数之和确定
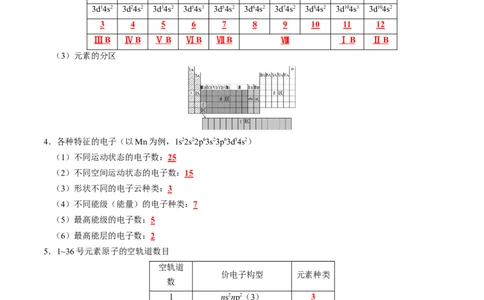
Sc Ti V Cr Mn Fe Co Ni Cu Zn
3d14s2 3d24s2 3d34s2 3d54s1 3d54s2 3d64s2 3d74s2 3d84s2 3d104s1 3d104s2
3 4 5 6 7 8 9 10 11 12
Ⅲ B Ⅳ B Ⅴ B Ⅵ B Ⅶ B Ⅷ Ⅰ B Ⅱ B
(3)元素的分区
4.各种特征的电子(以Mn为例,1s22s22p63s23p63d54s2)
(1)不同运动状态的电子数:25
(2)不同空间运动状态的电子数:15
(3)形状不同的电子云种类:3
(4)不同能级(能量)的电子种类:7
(5)最高能级的电子数:5
(6)最高能层的电子数:2
5.1~36号元素原子的空轨道数目
空轨道
价电子构型 元素种类
数
1 ns2np2(3) 3
ns2np1(3)、3d34s2
2 4
(1)
3 3d24s2(1) 2
4 3d14s2(1) 1
6.1~36号元素原子的未成对电子数(n)
(1)n=1:ns1(4)、ns2np1(3)、ns2np5(3)、3d14s2(1)、3d104s1(1),共12 种
(2)n=2:ns2np2(3)、ns2np4(3)、3d24s2(1)、3d84s2(1),共8 种
(3)n=3:ns2np3(3)、3d34s2(1)、3d74s2(1),共5 种(4)n=4:3d64s2(1),共1 种
(5)n=5:3d54s2(1),共1 种
(6)n=6:3d54s1(1),共1 种
7.基态原子核外电子排布的表示方法(以铁原子为例)
(1)各类要求的电子排布式
①电子排布式:1s22s22p63s23p63d64s2
②简化电子排布式: [ A r ] 3 d 6 4 s 2
③价电子(外围电子、特征电子)排布式: 3 d 6 4s 2
④最外层电子排布式: 4s 2
⑤M层电子排布式: 3s 2 3p 6 3 d 6
⑥最高能级电子排布式: 3 d 6
(2)各类要求的电子排布图
①电子排布图:
②轨道表示式:
③价电子排布图:
④原子结构示意图:
核外电子排布常见错误
(1)在写基态原子的轨道表示式时,常出现以下错误:
① (违反能量最低原理)
② (违反泡利原理)
③ (违反洪特规则)
④ (违反洪特规则)
(2)当出现d轨道时,虽然电子按ns、(n-1)d、np的顺序填充,但在书写电子排布式时,仍把(n-1)d放在
ns前,如Fe:1s22s22p63s23p63d64s2,而失电子时,却先失4s轨道上的电子,如Fe3+:1s22s22p63s23p63d5。
(3)注意比较原子核外电子排布式、简化电子排布式、原子外围电子或价电子排布式的区别与联系。如 Cu
的电子排布式:1s22s22p63s23p63d104s1;简化电子排布式:[Ar]3d104s1;外围电子或价电子排布式:3d104s1。
【典例03】短周期元素R基态原子最外层的p能级上有2个未成对电子。下列关于基态R原子的描述正确
的是A.基态R原子核外电子的电子云轮廓图有两种:球形和哑铃形
B.基态R原子的价层电子排布式为ns2np2(n=2或3)
C.基态R原子的原子轨道总数为9
D.基态R原子的轨道表示式为
【答案】A
【分析】由“短周期元素R基态原子最外层的p能级上有2个未成对电子”可知,可能有两种情况:p能
级上只有2个电子,R为第ⅣA族元素,C或Si;p能级上有4个电子,R为第ⅥA族元素,O或S,由此
可知:
【解析】A.基态R原子核外电子的电子云轮廓图有两种:球形和哑铃形,A正确;
B.基态R原子的价层电子排布式还可能为ns2np4,B错误;
C.R元素一共有4种可能,C错误;
D.R元素还有可能为C,D错误;
故选A。
【典例04】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L能层
中p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物
是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)写出M、R的价层电子排布式:M 、R 。
(2)写出X、Y的价层电子轨道表示式:X 、Y 。
(3)写出Z的核外电子排布式: 。Z的核外未成对电子数为 。
【答案】(1) 2s22p4 3s1
(2)
(3) 1s22s22p63s23p63d54s1(或[Ar]3d54s1) 6
【分析】M基态原子L能层中p轨道电子数是s轨道电子数的2倍,则M的价电子排布式为2s22p4,则M
为氧元素;R是同周期元素中最活泼的金属元素,M、R原子序数依次增大,则R为钠元素;X和M形成
的一种化合物是引起酸雨的主要大气污染物,则X为硫元素,推知Y为氯元素;Z的基态原子4s和3d轨
道半充满,即为3d54s1,则Z为Cr;
【解析】(1)结合上述分析可知,M、R分别为氧、钠,价层电子排布式分别为2s22p4、3s1。
答案为:2s22p4;3s1。
(2)上述分析可知X、Y分别为硫、氯,价层电子轨道表示式分别为: 、 。
答案为: ; 。
(3)Z为铬元素,核外电子排布式:1s22s22p63s23p63d54s1(或[Ar]3d54s1),核外未成对电子数为6。
答案为:1s22s22p63s23p63d54s1(或[Ar]3d54s1);6。知识点 03 原子光谱
1.电子的跃迁
(1)基态电子:处于最低能量的电子
(2)激发态电子:能量比基态电子高的电子
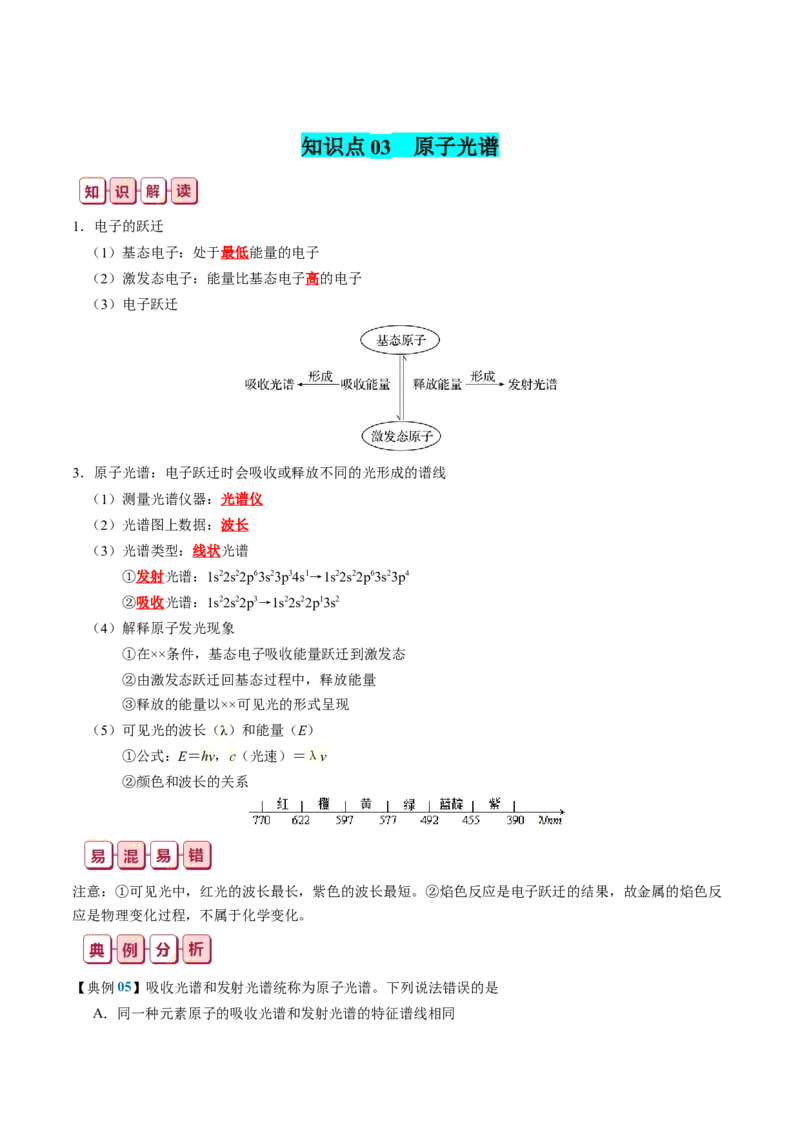
(3)电子跃迁
3.原子光谱:电子跃迁时会吸收或释放不同的光形成的谱线
(1)测量光谱仪器:光谱仪
(2)光谱图上数据:波长
(3)光谱类型:线状光谱
①发射光谱:1s22s22p63s23p34s1→1s22s22p63s23p4
②吸收光谱:1s22s22p3→1s22s22p13s2
(4)解释原子发光现象
①在××条件,基态电子吸收能量跃迁到激发态
②由激发态跃迁回基态过程中,释放能量
③释放的能量以××可见光的形式呈现
(5)可见光的波长(λ)和能量(E)
①公式:E=hv,c(光速)=λv
②颜色和波长的关系
注意:①可见光中,红光的波长最长,紫色的波长最短。②焰色反应是电子跃迁的结果,故金属的焰色反
应是物理变化过程,不属于化学变化。
【典例05】吸收光谱和发射光谱统称为原子光谱。下列说法错误的是
A.同一种元素原子的吸收光谱和发射光谱的特征谱线相同B.霓虹灯光与原子核外电子发生跃迁释放能量有关
C.光谱仪可以摄取元素的吸收光谱和发射光谱
D.目前发现的元素都是通过原子光谱发现的
【答案】D
【解析】A.不同元素的原子发生跃迁时会吸收或释放不同的光,可以用光谱仪摄取各种元素的电子的吸
收光谱或发射光谱,同一种元素原子的吸收光谱和发射光谱的特征谱线相同,故A正确;
B.电子跃迁本质上是组成物质的粒子中电子的一种能量变化,霓虹灯广告与原子核外电子发生跃迁释放
能量有关,故B正确;
C.吸收光谱和发射光谱都是线谱,区别在于前者显示黑色线条,而发射光谱显示光谱中的彩色线条,可
以用光谱仪摄取各种元素电子的吸收光谱或发射光谱,故C正确;
D.每种元素都有自己的特征谱线,在历史上许多元素是通过原子光谱发现的,如铯和铷,但目前发现的
元素并非都是通过原子光谱发现的,故D错误;
故选D。
【典例06】对充有氛气的霓虹灯管通电,灯管发出红光,产生这一现象的主要原因是
A.电子由激发态向基态跃迁时吸收除红光以外的光
B.电子由激发态向基态跃迁时以光的形式释放能量
C.电子由基态向激发态跃迁时吸收除红光以外的光
D.通电后在电场作用下,氖原子与构成灯管的物质发生反应
【答案】B
【解析】霓虹灯发红光是因为电子吸收能量后跃迁到能量较高的轨道,能量较高轨道上的电子会跃迁回能
量较低的轨道而以光的形式释放能量。综上所述故选B。
知识点 04 电离能大小的比较及应用
1.概念:气态原子或离子失去1 个电子所需要的最小能量
(1)第一电离能(I):M(g)-e-=M+(g)
1
(2)第二电离能(I):M+(g)-e-=M2+(g)
2
(3)第n电离能(I):M(n-1)+(g)-e-=Mn+(g)
n
2.同一原子各级电离能
(1)变化规律:I<I<I<…
1 2 3
(2)变化原因①电子分层排布
②各能层能量不同
3.第一电离能变化规律
(1)根据递变规律判断
①基本规律:周期表右上角位置的He 原子的I 最大
1
②特殊规律:同一周期中I,ⅡA>ⅢA;ⅤA>ⅥA
1
元素 Li Be B C N O F Ne
I 大小 ⑧ ⑥ ⑦ ⑤ ③ ④ ② ①
1
(2)根据金属性判断
①基本规律:I 越小,金属性越强,注意ⅡA和ⅤA族元素的特殊性
1
②金属元素和非金属元素的I:I <I
1 1(金属) 1(非金属)
(3)根据微粒结构判断
①稳定结构微粒的I大:全满、半满和全空状态稳定
②I >I
(全满) (半满)
③判断:I <I ,I >I
1(Cu) 1(Ni) 2(Cu) 2(Zn)
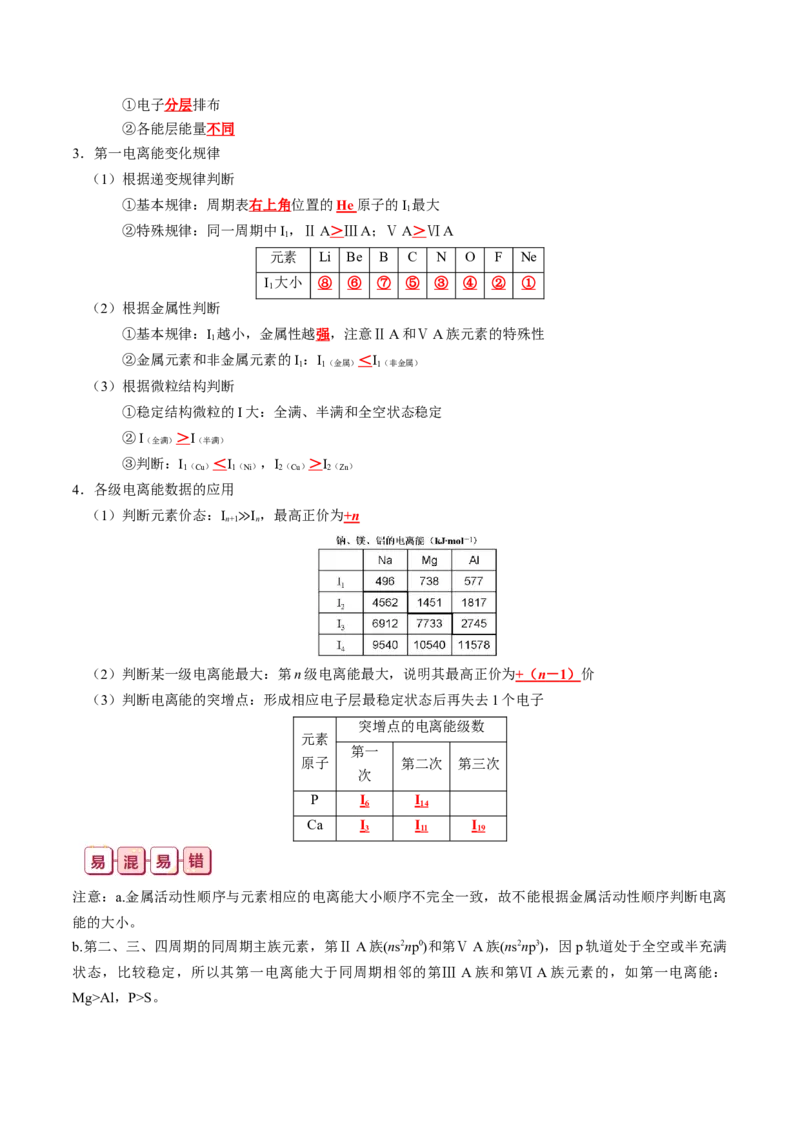
4.各级电离能数据的应用
(1)判断元素价态:I I,最高正价为 + n
n+1 n
≫
(2)判断某一级电离能最大:第n级电离能最大,说明其最高正价为 + ( n - 1 ) 价
(3)判断电离能的突增点:形成相应电子层最稳定状态后再失去1个电子
突增点的电离能级数
元素
第一
原子 第二次 第三次
次
P I I
6 14
Ca I I I
3 11 19
注意:a.金属活动性顺序与元素相应的电离能大小顺序不完全一致,故不能根据金属活动性顺序判断电离
能的大小。
b.第二、三、四周期的同周期主族元素,第ⅡA族(ns2np0)和第ⅤA族(ns2np3),因p轨道处于全空或半充满
状态,比较稳定,所以其第一电离能大于同周期相邻的第Ⅲ A族和第ⅥA族元素的,如第一电离能:
Mg>Al,P>S。【典例07】某短周期金属原子X的逐级电离能如图所示,下列说法正确的是
A.X在化合物中可能为+3价
B.X可能在周期表第二周期
C.X在周期表第VA族
D.X的最高价氧化物是碱性氧化物
【答案】A
【解析】A.从图分析,该元素的电离能第四电离能突然变大,故说明该元素的最外层有3个电子,X在
化合物中可能为+3价,A正确;
B.第二周期最外层有3个电子的为硼,不是金属元素,B错误;
C.最外层有3个电子,为第ⅢA族,C错误;
D.最高价氧化物若为铝,则为两性氢氧化物,D错误;
故选A。
【典例08】下表列出了某短周期金属元素R的各级电离能数据(用 、 ……表示),有关R元素的说法中,
正确的是
电离能/(kJ·mol-1)
元素
……
181
578 2745 11577 ……
7
A.R元素的最高正化合价为+2价
B.R元素的第一电离能高于同周期相邻元素的
C.R的氧化物为两性氧化物
D.R元素形成的单质熔点远高于其氧化物
【答案】C
【解析】A.从数据看,R的第三电离能和第四电离能差距很大,即R易失去三个电子,所以它的化合价
为+3价,A项错误;
B.R的价电子排布为ns2np1,失去一个电子后s全满稳定,而R前面的相邻元素为ns2稳定难失电子,所
以R的第一电离能不是全部高于同周期相邻元素,B项错误;
C.R为Al,Al O 为两性氧化物,C项正确;
2 3D.R的单质为金属晶体,而氧化铝为混合晶体,其熔点高达2000多度,远高于铝的,D项错误;
故选C。
知识点 05 电负性
1.意义:衡量元素的原子在化合物中得电子能力
2.递变规律
(1)周期表右上角氟元素的最大
(2)电负性大小
①电负性最大的前三种元素:F>O>N
②氢元素的电负:C>H>B;P>H>Si
3.其他判断方法
(1)根据共用电子对的偏向判断:偏向一方元素的电负性大
(2)化合物中化合价的正负判断:显负价元素的电负性大
(3)根据元素的非金属性判断
①最高价氧化物对应水化物的酸性越强,电负性越大
②单质与氢气越容易化合,电负性越大
③气态氢化物越稳定,电负性越大
4.判断化合物的类型
(1)差值:|△X|>1.7,离子化合物
(2)差值:|△X|<1.7,共价化合物
5.根据电负性写水解方程式
(1)水解原理
①电负性大的原子显负价,结合水中的 H +
②电负性小的原子显正价,结合水中的 OH -
(2)实例
①BrI:IBr+H O HIO+HBr
2
②NCl : N Cl +3H O NH +3HCl O
3 3 2 3注意:a.共价化合物中,两种元素电负性差值越大,它们形成共价键的极性就越强。
b.两元素电负性差值大于1.7时,一般形成离子键,小于1.7时,一般形成共价键,如AlCl 中两元素的电
3
负性之差为1.5,因此AlCl 含有共价键,属于共价化合物。
3
c.位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右。
【典例09】四种元素基态原子的电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p5 ④1s22s22p3
则下列有关比较中正确的是
A.第一电离能:④>③>②>① B.电负性:③>④>①>②
C.简单离子半径:②>①>③>④ D.最高正化合价:③>④=②>①
【答案】B
【分析】根据四种元素基态原子的电子排布式,①是S,②是P,③是F,④是N元素。
【解析】A.一般情况下同一周期元素,原子序数越大,元素的第一电离能越大。但若元素处于第ⅡA族、
第VA族,由于原子最外层电子处于全充满、半充满的稳定状态,其第一电离能大于同一周期相邻元素。
同一主族元素,原子序数越大,元素的第一电离能越小,则四种元素的第一电离能大小关系为:③>④>
②>①,A错误;
B.元素的非金属性越强,其电负性就越大。同一周期元素,原子序数越大,元素的非金属性越强,同一
主族元素,原子序数越大,元素的非金属性越弱,则元素的电负性大小关系为:③>④>①>②,B正确;
C.核外电子层结构相同,原子序数越大,离子半径越小,则简单离子半径大小关系为:②>①>④>③,
C错误
D.F元素非金属性很强,原子半径很小,与其它元素反应只能得到电子或形成共用电子对时偏向F元素,
因此没有与族序数相等的最高化合价,故F元素化合价不是在所有元素中最高的,D错误;
故选B。
【典例10】下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号,其中J为0族
元素。
X Y Z
R
W
J
下列说法正确的是
A.R基态原子的轨道表示式为B. 与 的半径大小关系为
C.X的第一电离能大于Y的第一电离能
D.表中电负性最大的元素为W
【答案】C
【分析】J为0族元素,J为Xe,X为N,Y为O,Z为F,R为S,W为Br。
【解析】A.R为S,基态原子的轨道表示式为: ,A错误;
B.Y为O,核外电子排布相同,核电荷数越小,半径越大,故O2->Na+,B错误;
C.X为N,Y为O,N的核外电子排布为半满结构,第一电离能大于O,C正确;
D.同周期从左往右电负性逐渐增大,同主族从上往下电负性逐渐减弱,表中电负性最大的元素为F,D错
误;
故选C。