文档内容
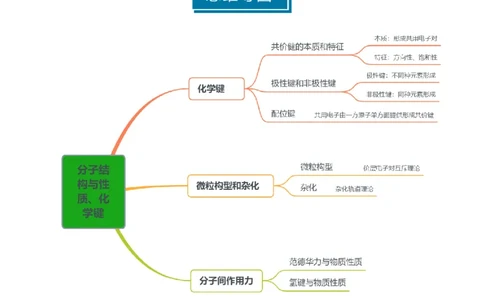
知识清单 15 分子结构与性质、化学键
知识点01 化学键 知识点02 微粒构型和杂化
知识点03 分子间作用力
知识点 01 化学键
一、共价键的特征及成键原则1.共价键的本质和特征
本质 两原子之间形成共用电子对
共价键 一定有饱和性
特征
有方向性( 键除外)
2.常见原子的成键数目
IA IIA IIIA IVA VA VIA VIIA
H Be B、Al C、Si N、P O、S F、Cl
3.形成化学键的目的:使体系的能量最 ,达到稳定结构
二、极性键和非极性键
1.分类依据:
2.极性键和非极性键的比较
分类 极性共价键 非极性共价键
成键原子 元素原子 元素原子
电子对 偏移 偏移
成键原子的电性 一个原子呈 电性(δ+),一个原子呈 电性(δ-) 呈
3.极性强弱:成键元素的电负性 越大,共用电子对偏移程度越大,极性越 。
4.键的极性对化学性质的影响
(1)共价键的极性越强,键的活泼性也越 , 发生断裂, 发生相关的化学反应。
(2)成键元素的原子吸引电子能力越强,电负性越 ,共价键的极性就越 ,在化学反应中该分子
的反应活性越 ,在化学反应中越 断裂。
5.键的极性对羧酸酸性的影响
①酸性强弱 三氟乙酸 三氯乙酸
(1)三氟
乙酸与三氯乙 电负性:F Cl 极性:F-C Cl-C 极性:FC- ClC-
②原因 3 3
酸的酸性强弱 羟基极性:三氟乙酸 三氯乙酸
①酸性强
(2)甲 甲酸 乙酸 丙酸
弱:
酸、乙酸和丙
烷基(-R)是 基团,烷基越长 效应越大,使羧基中的羟基
酸的酸性强弱 ②原因
极性 ,羧酸的酸性 。随着烷基加长,酸性差异越来越
三、σ 键和 键
1.分类依据:
2.形成
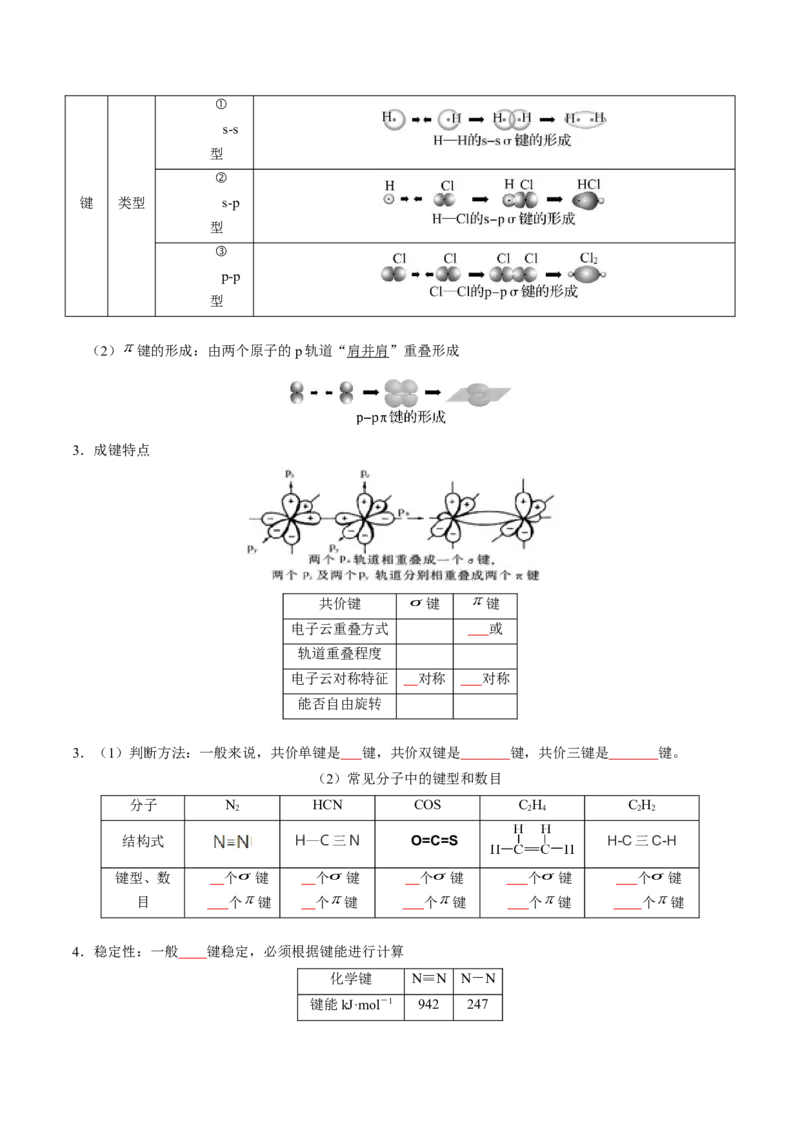
(1)σ 键的形成
σ
形成 由成键原子的s轨道或p轨道重叠形成①
s-s
型
②
键 类型 s-p
型
③
p-p
型
(2) 键的形成:由两个原子的p轨道“肩并肩”重叠形成
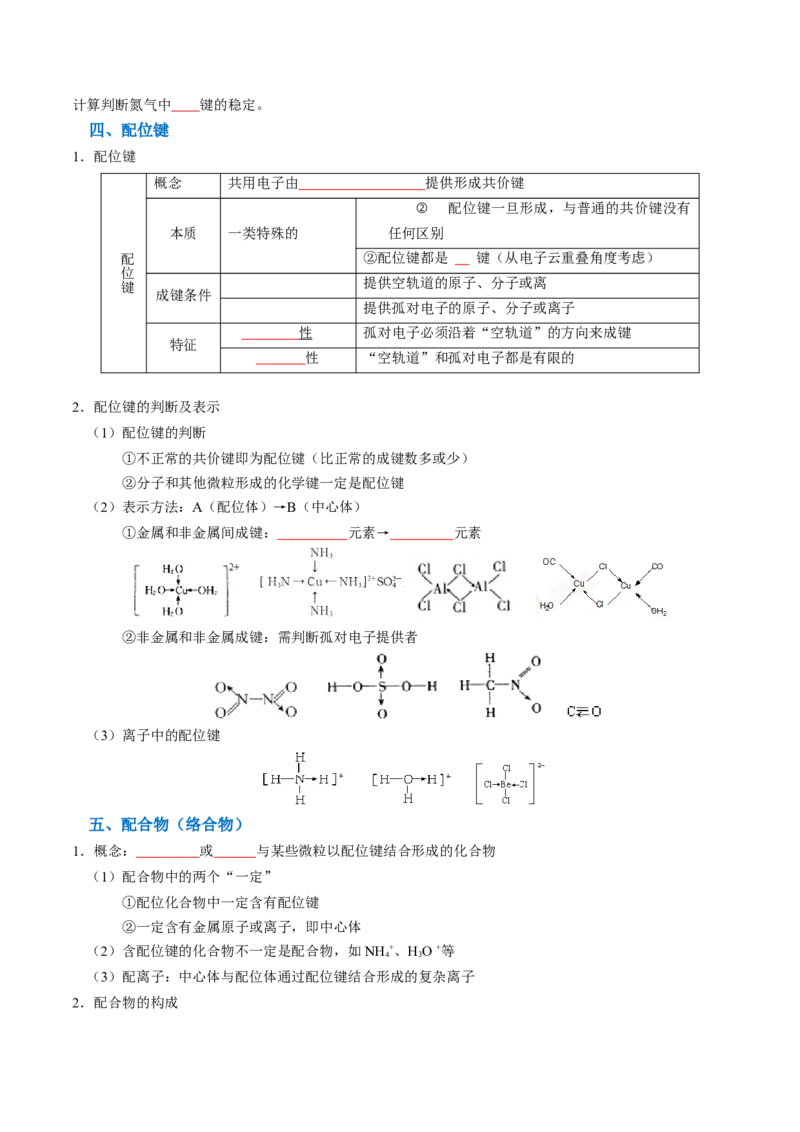
3.成键特点
共价键 σ 键 键
电子云重叠方式 或
轨道重叠程度
电子云对称特征 对称 对称
能否自由旋转
3.(1)判断方法:一般来说,共价单键是 键,共价双键是 键,共价三键是 键。
(2)常见分子中的键型和数目
分子 N HCN COS C H C H
2 2 4 2 2
结构式 H—C三N O=C=S H-C三C-H
键型、数 个σ 键 个σ 键 个σ 键 个σ 键 个σ 键
目 个 键 个 键 个 键 个 键 个 键
4.稳定性:一般 键稳定,必须根据键能进行计算
化学键 N≡N N-N
键能kJ·mol-1 942 247计算判断氮气中 键的稳定。
四、配位键
1.配位键
概念 共用电子由 提供形成共价键
② 配位键一旦形成,与普通的共价键没有
本质 一类特殊的 任何区别
配 ②配位键都是 键(从电子云重叠角度考虑)
位
提供空轨道的原子、分子或离
键
成键条件
提供孤对电子的原子、分子或离子
性 孤对电子必须沿着“空轨道”的方向来成键
特征
性 “空轨道”和孤对电子都是有限的
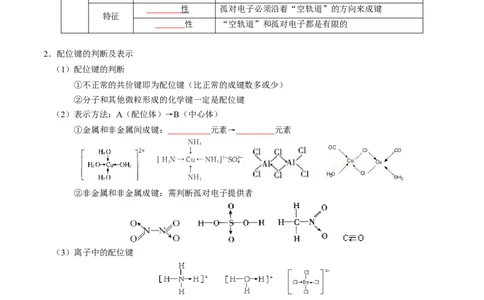
2.配位键的判断及表示
(1)配位键的判断
①不正常的共价键即为配位键(比正常的成键数多或少)
②分子和其他微粒形成的化学键一定是配位键
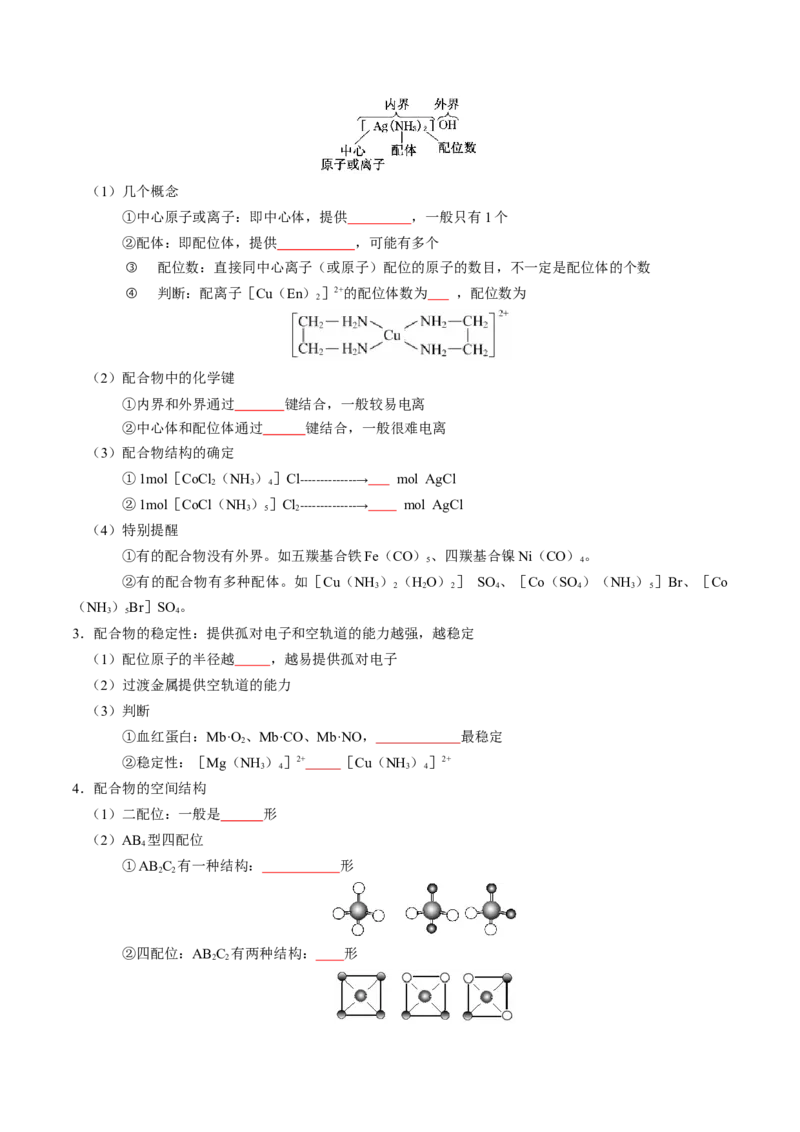
(2)表示方法:A(配位体)→B(中心体)
①金属和非金属间成键: 元素→ 元素
②非金属和非金属成键:需判断孤对电子提供者
(3)离子中的配位键
五、配合物(络合物)
1.概念: 或 与某些微粒以配位键结合形成的化合物
(1)配合物中的两个“一定”
①配位化合物中一定含有配位键
②一定含有金属原子或离子,即中心体
(2)含配位键的化合物不一定是配合物,如NH +、HO +等
4 3
(3)配离子:中心体与配位体通过配位键结合形成的复杂离子
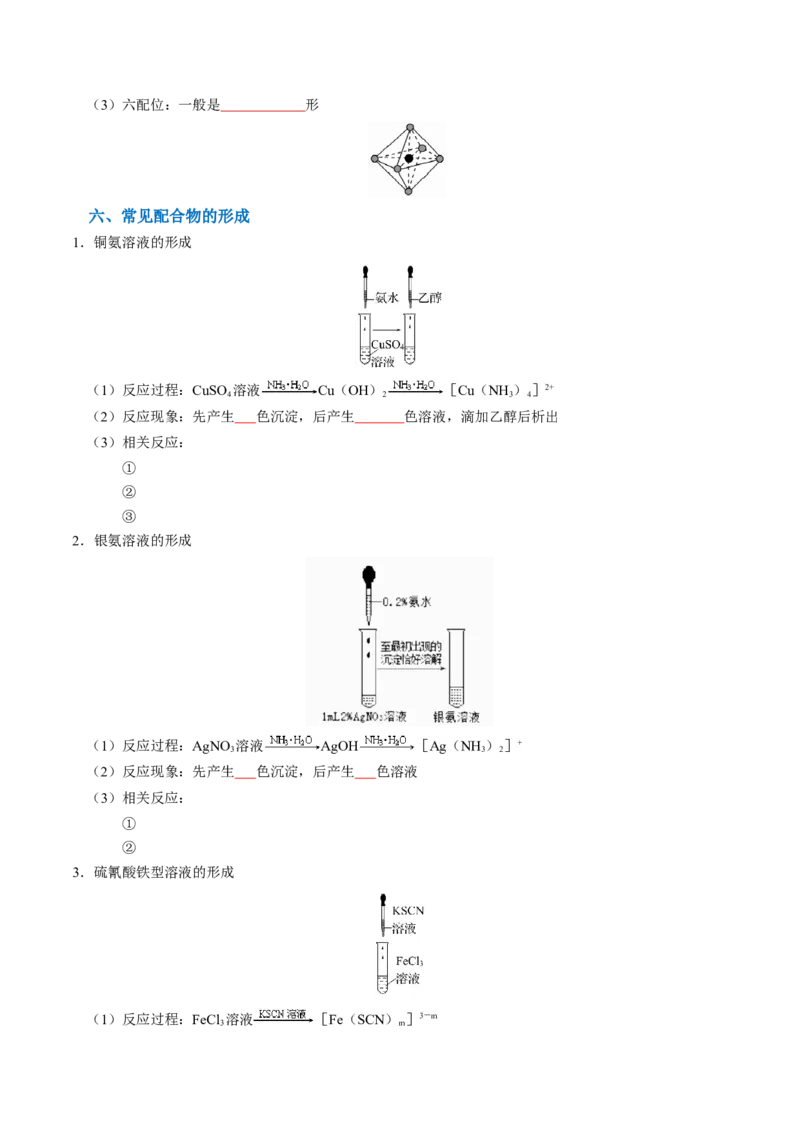
2.配合物的构成(1)几个概念
①中心原子或离子:即中心体,提供 ,一般只有1个
②配体:即配位体,提供 ,可能有多个
③ 配位数:直接同中心离子(或原子)配位的原子的数目,不一定是配位体的个数
④ 判断:配离子[Cu(En)]2+的配位体数为 ,配位数为
2
(2)配合物中的化学键
①内界和外界通过 键结合,一般较易电离
②中心体和配位体通过 键结合,一般很难电离
(3)配合物结构的确定
①1mol[CoCl (NH )]Cl--------------→ mol AgCl
2 3 4
②1mol[CoCl(NH )]Cl--------------→ mol AgCl
3 5 2
(4)特别提醒
①有的配合物没有外界。如五羰基合铁Fe(CO)、四羰基合镍Ni(CO)。
5 4
②有的配合物有多种配体。如[Cu(NH ) (HO) ] SO 、[Co(SO )(NH ) ]Br、[Co
3 2 2 2 4 4 3 5
(NH )Br]SO 。
3 5 4
3.配合物的稳定性:提供孤对电子和空轨道的能力越强,越稳定
(1)配位原子的半径越 ,越易提供孤对电子
(2)过渡金属提供空轨道的能力
(3)判断
①血红蛋白:Mb·O、Mb·CO、Mb·NO, 最稳定
2
②稳定性:[Mg(NH )]2+ [Cu(NH )]2+
3 4 3 4
4.配合物的空间结构
(1)二配位:一般是 形
(2)AB 型四配位
4
①AB C 有一种结构: 形
2 2
②四配位:AB C 有两种结构: 形
2 2(3)六配位:一般是 形
六、常见配合物的形成
1.铜氨溶液的形成
(1)反应过程:CuSO 溶液 Cu(OH) [Cu(NH )]2+
4 2 3 4
(2)反应现象:先产生 色沉淀,后产生 色溶液,滴加乙醇后析出
(3)相关反应:
①
②
③
2.银氨溶液的形成
(1)反应过程:AgNO 溶液 AgOH [Ag(NH )]+
3 3 2
(2)反应现象:先产生 色沉淀,后产生 色溶液
(3)相关反应:
①
②
3.硫氰酸铁型溶液的形成
(1)反应过程:FeCl 溶液 [Fe(SCN) ]3-m
3 m(2)反应现象:产生 色溶液
(3)相关反应:
①m=1:
②m=2:
③m=3:
④m=4:
⑤m=5:
⑥m=6:
4.四羟基合铝酸盐的形成
(1)反应过程:AlCl 溶液 Al(OH) [Al(OH)]-
3 3 4
(2)反应现象:先产生 色沉淀,后产生 色溶液
(3)相关反应:
①
②
1.判断正误,正确的打“√”,错误的打“×”。
(1)共价键的成键原子只能是非金属原子。( )
(2)在任何情况下,都是σ键比π键强度大。( )
(3)所有分子中都存在化学键。( )
(4)气体单质中一定存在σ键,可能存在π键。( )
(5)σ键比π键的电子云重叠程度大,形成的共价键弱。( )
(6)H O 分子中既有极性键,又有非极性键。( )
2 2
(7)H 分子中的共价键不具有方向性。( )
2
(8)分子的稳定性与分子间作用力的大小无关。( )
(9)通常σ键比π键的电子云重叠程度大,形成的共价键强。( )
(10)s-s σ键与s-p σ键的电子云形状对称性相同。( )
(11)碳碳双键的键能是碳碳单键键能的2倍。( )
(12)σ键能单独形成,而π键一定不能单独形成。( )
(13)σ键可以绕键轴旋转,π键一定不能绕键轴旋转。( )
(14)常温常压下4.4 g乙醛所含σ键数目为0.7N 。( )
A
(15)CS 分子中σ键与π键的数目之比是2∶1。( )
2
(16)Zn的氯化物与氨水反应可形成配合物[Zn(NH )]Cl ,1 mol该配合物中含有σ键的数目为14N 。(
3 4 2 A
)
(17)乙炔分子中既有非极性键又有极性键,既有σ键又有π键。( )1.下列有关化学键类型的叙述正确的是( )
A.化合物NH 所有原子最外层均满足2个或8个电子的稳定结构,则1 mol NH 中含有5N 个N—H σ键
5 5 A
(N 表示阿伏加德罗常数的值)
A
B.乙烯酮的结构简式为CH===C===O,其分子中含有极性共价键和非极性共价键,且σ键与π键数目之
2
比为1∶1
C.已知乙炔的结构简式为CH≡CH,则乙炔中存在2个σ键(C—H)和3个π键(C≡C)
D.乙烷分子中只存在σ键,不存在π键
2.回答下列问题:
(1)1 mol HOOCCH CHCHO分子中含有_ __mol单键,_ __mol双键;含有_ __mol π键,_ __mol σ键。
2 2
(2)在[Ag(NH)]+中_ __的_ __原子提供孤电子对,_ __提供空轨道。
3 2
3.(1)Co的氯化物与氨水反应可形成配合物[CoCl(NH )]Cl ,1 mol该配合物中含有σ键的数目为_ __,
3 5 2
含1 mol [CoCl(NH )]Cl 的溶液中加入足量AgNO 溶液,生成_ __mol AgCl沉淀。
3 5 2 3
(2)下列物质中,①只含有极性键的分子是_ ,②既含离子键又含共价键的化合物是_ __;③只存在σ
键的分子是_ __,④同时存在σ键和π键的分子是_ __。
A.H B.CO C.CHCl D.C H E.C H F.CaCl G.(NH )SO
2 2 2 2 3 6 2 6 2 4 2 4
知识点 02 微粒构型和杂化
一、价层电子对互斥理论
1.(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力_ __,体系的能量_ __。
②孤电子对的排斥力较大,孤电子对_ __,排斥力越强,键角_ __。
(2)用价层电子对互斥理论推测分子的立体构型的关键是判断分子中的中心原子上的价层电子对数。
其中:a是中心原子的价电子数(阳离子要减去电荷数、阴离子要加上电荷数),b是与中心原子结合的原子
最多能接受的电子数,x是与中心原子结合的原子数。
(3)价层电子对互斥模型与分子立体构型的关系
价层电 成键 孤电子 电子对立
分子立体构型 实例 键角
子对数 对数 对数 体构型
2 2 0 直线形 _ __形 BeCl 180°
2CO
2
3 0 _ __形 BF 120°
3
3 三角形
2 1 _ __形 SnBr 105°
2
4 0 _ __形 CH 109°28′
4
4 3 1 四面体形 _ __形 NH 107°
3
2 2 _ _形 HO 105°
2
二、杂化轨道理论
1.(1)杂化轨道的定义:在外界条件的影响下,原子内部能量_ __的原子轨道重新组合的过程叫原子轨
道的杂化,组合后形成的一组新的原子轨道,叫杂化原子轨道,简称杂化轨道。
(2)杂化轨道的类型与分子立体构型的关系
(3)由杂化轨道数判断中心原子的杂化类型
杂化轨道用来形成σ键和容纳孤电子对,所以有公式:
杂化轨道数=中心原子的孤电子对数+中心原子的σ键个数。
代表物 杂化轨道数 中心原子杂化轨道类型
CO 0+2=2
2
CHO 0+3=3
2
CH 0+4=4
4
SO 1+2=3 _ __
2
NH 1+3=4 _ __
3
HO 2+2=4 _ __
2
(4)中心原子杂化类型和分子构型的相互判断
分子组成 中心原子的 中心原子的
分子空间构型 示例
(A为中心原子) 孤电子对数 杂化方式
0 sp _ __ BeCl
2
AB 1 sp2 _ __ SO
2 2
2 sp3 _ __ HO
2
0 sp2 _ __ BF
3
AB
3
1 sp3 _ __ NH
3
AB 0 sp3 _ __ CH
4 42.判断分子或离子中心原子的杂化类型的五种方法
(1)根据杂化轨道的空间分布构型判断。
①若杂化轨道在空间的分布为正四面体形或三角锥形,则分子或离子的中心原子发生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则分子或离子的中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则分子或离子的中心原子发生sp杂化。
(2)根据杂化轨道之间的夹角判断。
若杂化轨道之间的夹角为109.5°,则分子或离子的中心原子发生sp3杂化;若杂化轨道之间的夹角为120°,
则分子或离子的中心原子发生sp2杂化;若杂化轨道之间的夹角为180°,则分子或离子的中心原子发生sp
杂化。
(3)根据等电子原理进行判断。
如CO 是直线形分子,CNS-、N与CO 是等电子体,所以这些离子构型均为直线形,中心原子均采用 sp
2 2
杂化。
(4)根据中心原子的价电子对数判断。
如中心原子的价电子对数为4,是sp3杂化,价电子对数为3,是sp2杂化,价电子对数为2,是sp杂化。
(5)根据分子或离子中有无π键及π键数目判断。
如没有π键为sp3杂化,含一个π键为sp2杂化,含两个π键为sp杂化。
3.轨道构型和微粒构型的区别
(1)轨道构型(VSEPR模型)
n 2 3 4
杂化方式 sp sp2 sp3
轨道构型
(理想化模型)
形 形 形
轨道夹角 180° 120° 109°28′
(2)轨道构型和微粒构型的关系
微粒 杂化方式 VSEPR模型 微粒构型 分子极性
SO
2
SO
3
NO
2
-
NO
3
-
NO+
2
三、分子的极性1.化学键极性和分子极性的关系
2.分子极性的判断方法
(1)根据键的极性判断
①只含有非极性键的双原子分子或多原子分子是 分子。如O、H、P、C 。
2 2 4 60
②含有极性键的双原子分子都是 分子。如HCl、HF、HBr。
③含有极性键的多原子分子,空间结构对称的是 分子;空间结构不对称的是 分子。
(2)判断AB 型分子极性的经验规律
n
①中心原子A的化合价的绝对值等于该元素所在的主族序数,则为 分子;若不等,则为 分子。
②中心原子有孤电子对,则为 分子;若无孤电子对,则为 分子。
(3)结构判断
①对称性判断:高度对称的是非极性分子
分子
分子类型
②孤电子对判断:中心原子上含孤电子对的一定是 分子
③构型判据:分子构型和轨道构型完全一致的是 分子
分子 HCHO PCl PCl SF
3 5 6
轨道构
型
分子构
型
分子类
型
(4)AB C 型分子
2 2
①立体结构:只有一种结构, 分子②平面结构:两种结构
图示
分子类
型
(5)实验判据:相似相溶原理
①极性分子易溶于 溶剂
②非极性分子易溶于 溶剂
四、键参数的比较
1.共价键的键能的比较
(1)键能和键长的关系:键长越 ,键能越大
(2)同种元素不同类型键能:叁键 双键 单键
(3)共价分子的键能和稳定性的关系
①共价单键:半径越 ,键能越 ,分子越稳定
②叁键或双键:断裂 个键的能量越大,越稳定
③实例:活泼性CO N
2
化学键 C-O C=O C≡O
键能/kJ•mol-
351 803 1071
1
化学键 N-N N=N N≡N
键能/kJ•mol-
159 418 946
1
2.共价键的键长的比较
(1)看有成键原子上是否都有孤对电子
①无孤对电子:只看成键原子的半径之和
②有孤对电子:还要看孤对电子之间的排斥作用
③键长比较
微粒组 键长长短
NH 和PH N-H P-H
3 3
金刚石和晶体硅 C-C Si-Si
稳定性:HO<NH<CHCH O-O N-N C-C
2 2 2 4 3 3
O、O-、O+、O2- 氧氧键: > > >
2 2 2 2
(2)看能否形成 键:形成 键使键长变
①乙烷、苯和乙烯:C-C 特殊键 C=C
②金刚石和石墨中的碳碳键:金刚石 石墨
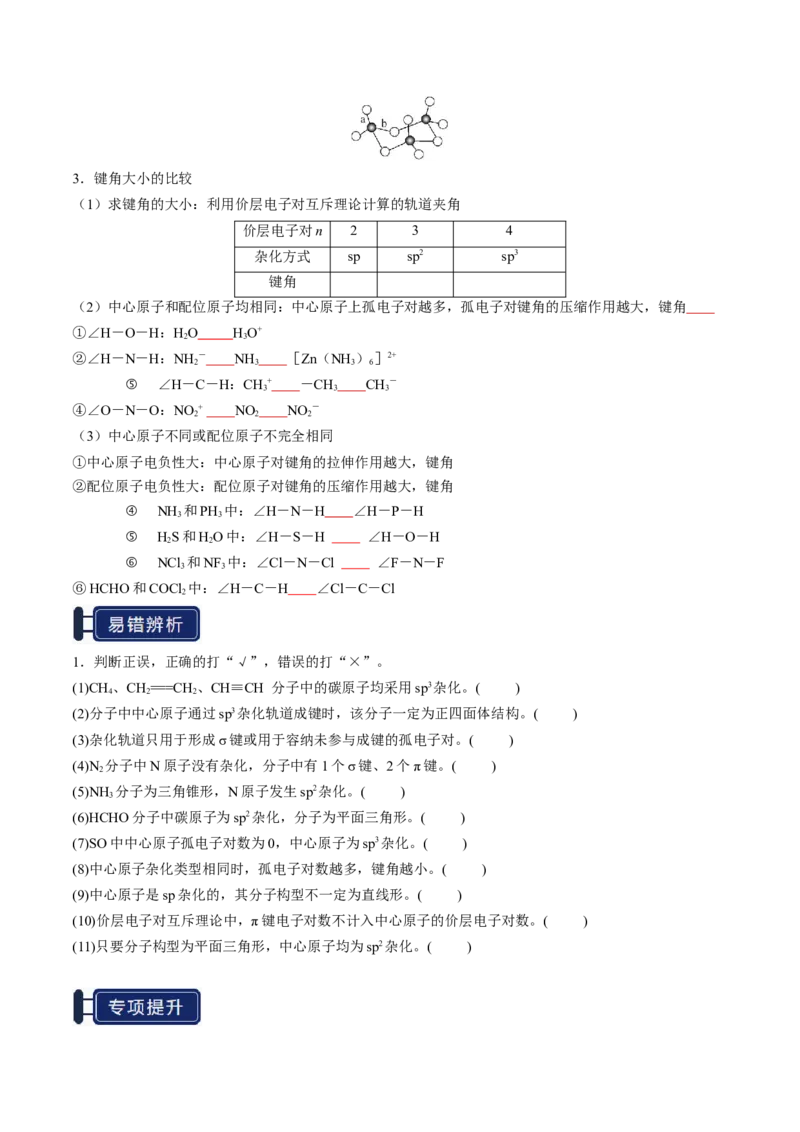
③SO 的三聚体环状结构,键长:a b
33.键角大小的比较
(1)求键角的大小:利用价层电子对互斥理论计算的轨道夹角
价层电子对n 2 3 4
杂化方式 sp sp2 sp3
键角
(2)中心原子和配位原子均相同:中心原子上孤电子对越多,孤电子对键角的压缩作用越大,键角
①∠H-O-H:HO HO+
2 3
②∠H-N-H:NH - NH [Zn(NH )]2+
2 3 3 6
⑤ ∠H-C-H:CH+ -CH CH-
3 3 3
④∠O-N-O:NO + NO NO -
2 2 2
(3)中心原子不同或配位原子不完全相同
①中心原子电负性大:中心原子对键角的拉伸作用越大,键角
②配位原子电负性大:配位原子对键角的压缩作用越大,键角
④ NH 和PH 中:∠H-N-H ∠H-P-H
3 3
⑤ HS和HO中:∠H-S-H ∠H-O-H
2 2
⑥ NCl 和NF 中:∠Cl-N-Cl ∠F-N-F
3 3
⑥HCHO和COCl 中:∠H-C-H ∠Cl-C-Cl
2
1.判断正误,正确的打“√”,错误的打“×”。
(1)CH 、CH===CH 、CH≡CH 分子中的碳原子均采用sp3杂化。( )
4 2 2
(2)分子中中心原子通过sp3杂化轨道成键时,该分子一定为正四面体结构。( )
(3)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对。( )
(4)N 分子中N原子没有杂化,分子中有1个σ键、2个π键。( )
2
(5)NH 分子为三角锥形,N原子发生sp2杂化。( )
3
(6)HCHO分子中碳原子为sp2杂化,分子为平面三角形。( )
(7)SO中中心原子孤电子对数为0,中心原子为sp3杂化。( )
(8)中心原子杂化类型相同时,孤电子对数越多,键角越小。( )
(9)中心原子是sp杂化的,其分子构型不一定为直线形。( )
(10)价层电子对互斥理论中,π键电子对数不计入中心原子的价层电子对数。( )
(11)只要分子构型为平面三角形,中心原子均为sp2杂化。( )1.用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下
列判断正确的是( C )
A.SO 、CS、HI都是直线形的分子
2 2
B.BF 键角为120°,SnBr 键角大于120°
3 2
C.HCHO、BF、SO 都是平面三角形的分子
3 3
D.PCl 、NH 、PCl 都是三角锥形的分子
3 3 5
2.填空:
(1)比较键角大小(填“>”“=”或“<”)。
①HO_ __HO+ ②NH _ __NH ③CO_ __SO ④NH _ __PH ⑤NF _ __NCl
2 3 3 3 3 3 3
(2)①甲醇分子内碳原子的杂化方式为_ __,甲醇分子内的O—C—H键角_ __(填“大于”“等于”或“小
于”)甲醛分子内的O—C—H键角。
②氯丙烯分子( )中碳原子轨道杂化类型是_ __。
③在BF 分子中,F—B—F的键角是_ __,硼原子的杂化轨道类型为_ __,BF 和过量NaF作用可生成
3 3
NaBF ,BF的立体构型为_ __。
4
④SO的立体构型是_ __,其中硫原子的杂化轨道类型是_ __。
(3)写出下列分子或离子的中心原子的价层电子对数、杂化类型、立体构型。
①NCl ②HO+ ③CO ④NO
3 3
(4)已知HO、NH 、CH 三种分子中,键角由大到小的顺序是CH>NH>H O,请分析可能的原因。
2 3 4 4 3 2
知识点 03 分子间作用力
一、分子间作用力
1.概念:分子间存在 (1)实质: 作用
的相互作用力 (2)存在:分子和分子之间或 原子之间
分
子 (1) :普通的分子间作用力
2.分类
间 (2) :特殊的分子间作用力
作 (1)作用范围很小,一般认为 分子中无分子间作用力
3.特点
用 (2)比化学键 得多
力 4.外界条件对分子间 (1)压强:增大压强,分子间作用力
作用力的影响 (2)温度:升高温度,分子间作用力
二、范德华力与物质性质
范 特点 方向性, 饱和性(1)分子的极性越大,范德华力越
影响因素
德 (2)组成和结构相似的物质,相对分子质量越大,范德华力越
华 (1)组成和结构相似的分子,相对分子质量越大,熔沸点越
作用效果
力 (2)由分子构成的晶体熔点 、挥发性 、硬度
范德华力与化学键 (1)范德华力主要影响物质的 性质,如物质的熔、沸点等
作用效果的区别 (2)化学键主要影响物质的 性质,如热稳定性等
三、氢键与物质性质
1.氢
键的
电性作用(介于范德华力和共价键之间)
实
质:
2.氢 (1)“-”表示共价键,“…”表示氢键
键的 ①分子中必须有
表示 ②氢原子两边有电负性 、半径 、具有 的元素(F、O、N)
方 ③-NH +中的N原子能否形成氢键:
3
法:X (2)氢键形成的一般条件
- H …
⑦ -CHO中的H原子能否形成氢键:
Y
3.氢 (1) : 沿着孤对电子的伸展方向成键
键的 氢原子与孤电子对相对应
(2) 性:
特点
(1)三种气态氢化物: 、
、
4.
(2)含 物质含氧酸、含
氢
氧酸的酸式盐、醇、酸、酚
键 及它们的水溶液
的
(3)含 物质:NH 、
存 3
NH、DNA双螺旋体
在 2 4①链状
NH ·HO 胆矾
3 2
(1)分子间氢键;普遍存
5.
在
氢
②环状:分子中含多个N、O、F原子
键
二聚乙酸 二聚甲酸 四聚甲醇 环状碳酸氢盐
的
类
型
硝酸 水杨醛 邻硝基苯酚 邻氨基苯酚
(2)分子内氢键:含多个
N、O、F原子,且为 关
系
6. (1)对物质熔沸点的影响 ①分子间氢键相当于增大了相对分子质量,故熔沸点
氢 ②分子内氢键未增大分子量,却降低了分子极性,故熔沸点
键 ③形成的分子间氢键越多,熔沸点越
的 (2)对物质的电离的影 酸性氢原子形成氢键,电离程度 ,酸性
作 响:
用 (3)对液体的黏度的影响 :分子间有氢键的
甘油 甘醇 HPO 浓硫酸
效 液体,一般黏度较 3 4
果(4)冰的密度: 结冰时水中的氢键 ,水分子间的空隙 ,体积 ,密度
7.冰晶体中氢键键能的计算
(1)冰晶体中氢键的结构式
(2)1个水分子可以形成 个氢键,完全属于该水分子的氢键有 个
(3)冰的升华热= +
四、物质溶解性的比较
1.相似相溶原理:极性相似的分子间范德华力较大,其溶解度也大
(1)极性分子易溶于 溶剂
(2)非极性分子易溶于 溶剂
2.氢键对物质溶解性的影响
(1)若溶质和溶剂分子间形成氢键,溶质在水中的溶解度
(2)若溶质分子中存在氢键,则它在水中的溶解度反常的
3.某些基团对物质溶解性的影响
(1)常见的亲水基和憎水基
①亲水基:羟基、羧基、氨基、醛基等
②憎水基:烃基、酯基等
(2)随着溶质分子中憎水基个数的增多,溶质在水中的溶解度
①甲醇、乙醇、甘油和水以任意比互溶
②戊醇在水中的溶解度明显减小
4.如果溶质和溶剂发生反应,将 物质的溶解性
5.常见的极性分子和非极性分子
(1)HO、NH 、SO 、酒精等为 分子
2 3 2
(2)CCl 、CS、苯等为 分子
4 2
五、无机含氧酸的酸性
1.酸的元数=酸中羟基上的氢原子数,不一定等于酸中的氢原子数
亚磷
磷的含氧酸 磷酸 偏磷酸 次磷酸
酸
结构式
羟基氢原子
数
酸的元数
2.无机含氧酸[(HO) RO]的酸性
m n
(1)非羟基氧原子数不同① 基本规律:非羟基氧原子数n越多,酸性越
②典型实例:
HClO>HSO >HPO >HSiO,HClO>HClO>HClO>HClO
4 2 4 3 4 4 4 4 3 2
② 宏观解释:
④微观解释:
(2)非羟基氧原子数相同
①基本规律:中心元素的非金属性越强,酸性越
③ 典型实例:HClO>HBrO ,HCO>HSiO,HPO >HAsO
4 4 2 3 2 3 3 4 3 4
③微观解释:
六、分子的手性
1.手性异构体
(1)概念:具有完全相同的 和 的一对分子,如同左手与右手一样互为 ,却在三维
空间里 ,互称手性异构体。
(2)又名:手性同分异构体、对映异构体、光学异构体
2.手性分子:有 的分子。
(1)手性分子的确定
①两个分子具有 的组成和原子排列;
②两个分子化学键的种类、数目及分子的极性
③两个分子互为镜像;
④两个分子在三维空间里不能重合。如图:
(2)手性碳原子:有机物中含有的碳原子连有 个互 的原子或基团,即*C。
① 手性碳原子一定是 碳原子,且碳原子是 杂化。
②不饱和碳原子(如碳碳双键、-C≡C-等中的碳原子)一定 手性碳原子。
③有机物分子中如果有一个手性碳原子,则该有机物分子就是手性分子,具有手性异构体。3.手性分子的应用
(1)医药领域
①现今使用的药物中手性药物超过50%
②对于手性药物,一个异构体可能 ,而另一个异构体可能是 甚至是 的
(2)合成领域
①手性催化剂: 或者主要 一种手性分子的合成
②用 生产药物,可以只得到或者主要得到一种 ,这种独特的合成方法称为
手性合成
七、超分子
1.概念:由 或 的分子通过 相互作用形成的分子聚集体。
2.应用
(1)分离C 和C
60 70
将C 和C 的混合物加入一种空腔大小适配C 的“杯酚”中,得到超分子“杯酚”C 和C ;加入
60 70 60 60 70
甲苯溶剂,甲苯将C 溶解,经过滤后分离出C ;再向不溶物中加入氯仿,氯仿溶解“杯酚”而将不溶解
70 70
的C 释放出来并沉淀。从而将C 和C 分离开来。
60 60 70
(2)冠醚识别碱金属离子
冠醚分子中有大小不同的 适配不同大小的碱金属离子,而形成冠醚-碱金属离子超分子。
3.重要特征: 和 。
1.判断正误,正确的打“√”,错误的打“×”。
(1)以极性键结合起来的分子一定是极性分子。( )
(2)非极性分子中,一定含有非极性共价键。( )
(3)极性分子中一定不含有非极性共价键。( )
(4)卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而增大。( )
4
(5)乙醇分子和水分子间只存在范德华力。( )
(6)碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键。( )
(7)H O比HS稳定是因为水分子间存在氢键。( )
2 2
(8)可燃冰(CH·8H O)中甲烷分子与水分子形成了氢键。( )
4 2
(9)氢键的存在一定使物质的熔、沸点升高。( )
(10)氢键具有方向性和饱和性。( )
(11)高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性。( )
(12)邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点。( )
(13)卤素氢化物中,HCl的沸点最低的原因是其分子间的范德华力最小。( )
(14)因为碳氢键键能小于碳氧键,所以CH 熔点低于CO。( )
4 2
(15)BCl 与NCl 均为三角锥形,为极性分子。( )
3 3
(16)H O 分子间存在氢键。( )
2 2(17) 为手性分子。( )
(18)氨水中氨分子与水分子间形成了氢键。( )
1.(1)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因: _ 。
GeCl GeBr GeI
4 4 4
熔点/ ℃ -49.5 26 146
沸点/ ℃ 83.1 186 约400
(2)硫酸镍溶于氨水形成[Ni(NH )]SO 蓝色溶液。
3 6 4
①[Ni(NH )]SO 中阴离子的立体构型是_ __。
3 6 4
② 在[Ni(NH )]2+中Ni2+与NH 之间形成的化学键称为_ __,提供孤电子对的成键原子是_ __。
3 6 3
③氨的沸点_ __(填“高于”或“低于”)膦(PH ),原因是_ __;氨是_ __(填“极性”或
3
“非极性”)分子,中心原子的轨道杂化类型为_ __。
2.完成下列填空。
①元素As与N同族。预测As的氢化物分子的立体结构为_ __,其沸点比NH 的_ __(填“高”或
3
“低”),其判断理由是 __。
②HO与CHCHOH可以任意比例互溶,除因为它们都是极性分子外,还因为_ __。
2 3 2
③如图为S 的结构。其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为_ _。
8
3.①下表列出了含氧酸酸性强弱与非羟基氧原子数的关系。
次氯酸 磷酸 硫酸 高氯酸
含氧酸结构 Cl—OH
非羟基氧原子数 0 1 2 3
酸性 弱酸 中强酸 强酸 比硫酸酸性更强
由此可得出的判断含氧酸酸性强弱的一条经验规律是_ _。
②磷有三种含氧酸HPO 、HPO 、HPO ,其中磷元素均以sp3杂化与相邻原子形成四个σ键,则HPO 的
3 2 3 3 3 4 3 3
结构式是_ __,写出HPO 与足量氢氧化钠溶液反应的化学方程式:_ __。
3 2
③磷的三种含氧酸HPO 、HPO 、HPO 的酸性强弱顺序为HPO