文档内容
知识清单 21 电离平衡
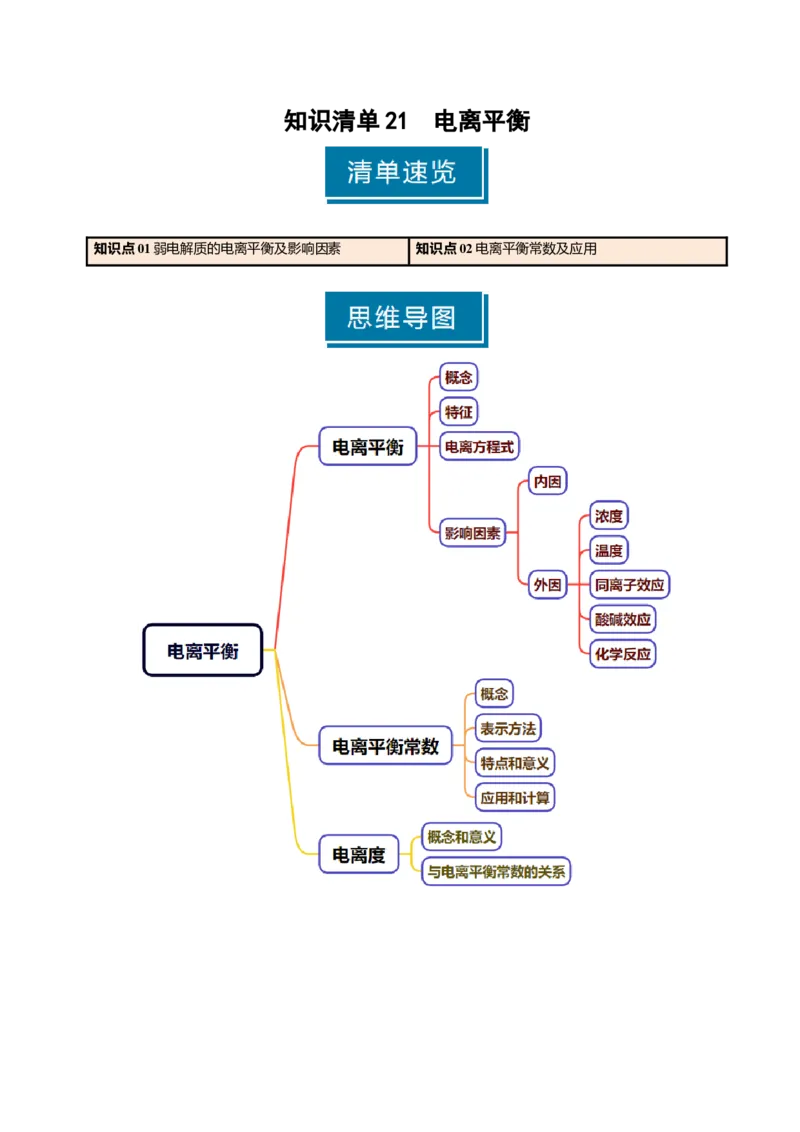
知识点01弱电解质的电离平衡及影响因素 知识点02电离平衡常数及应用知识点 01 弱电解质的电离平衡及影响因素
1.电离平衡
(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离______________的速率和_____________________
的速率相等时,电离过程达到了平衡。
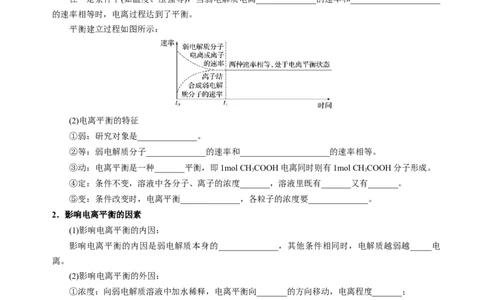
平衡建立过程如图所示:
(2)电离平衡的特征
①弱:研究对象是______________。
②等:弱电解质分子______________的速率和_____________________的速率相等。
③动:电离平衡是一种_______平衡,即1mol CHCOOH电离同时则有1mol CHCOOH分子形成。
3 3
④定:条件不变,溶液中各分子、离子的浓度_______,溶液里既有_______又有_______。
⑤变:条件改变时,电离平衡______________,各粒子的浓度要______________。
2.影响电离平衡的因素
(1)影响电离平衡的内因:
影响电离平衡的内因是弱电解质本身的______________,其他条件相同时,电解质越弱越_____电
离。
(2)影响电离平衡的外因:
①浓度:向弱电解质溶液中加水稀释,电离平衡向_______的方向移动,电离程度_______;
②温度:电解质的电离一般是吸热过程,升高温度,电离平衡向_______的方向移动,电离程度
_______;
③同离子效应:加入与电解质电离出相同离子的强电解质,电离平衡向______________的方向移动,
电离程度_______;
④酸碱效应:加入强酸(或强碱),弱酸(或弱碱)的电离平衡向______________的方向移动,电
离程度_______;弱碱(或弱酸)的电离平衡向_______的方向移动,电离程度_______;
⑤加入能与离子反应的物质,电离平衡向_______的方向移动,电离程度_______。
以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOH(aq)CHCOO-(aq)+H+(aq) ΔH
3 3 3
>0的影响。改变条件 平衡移动方向 n(H+) c(H+) 导电能力
加水稀释
加入少量冰醋酸
通入HCl(g)
加NaOH(s)
加CHCOONa(s)
3
升高温度
【易错提醒】
(1)一般情况下,加水稀释时,弱电解质电离产生离子的浓度减小,并非溶液中所有离子的浓度都减
小。如CHCOOH溶液加水稀释时,c(CHCOO-)、c(H+)减小,但溶液中c(OH-)反而增大。
3 3
(2)电离平衡向右移动,电离程度不一定增大,如向CHCOOH溶液中加入冰醋酸,CHCOOH电离
3 3
程度减小。
3.电解质溶液的导电能力
电解质溶液的导电能力取决于溶液中自由移动离子的浓度和离子所带电荷数,自由移动离子的浓度
越_______、离子所带电荷数越_______,导电能力越强。
【特别提示】
1.判断弱电解质的三个角度
角度1:弱电解质的定义,即弱电解质不能完全电离。如0.1 mol·L-1的CHCOOH溶液的pH>1。
3
角度2:弱电解质溶液中存在电离平衡,条件改变,平衡移动。如pH=1的CHCOOH溶液加水稀
3
释10倍后,17。
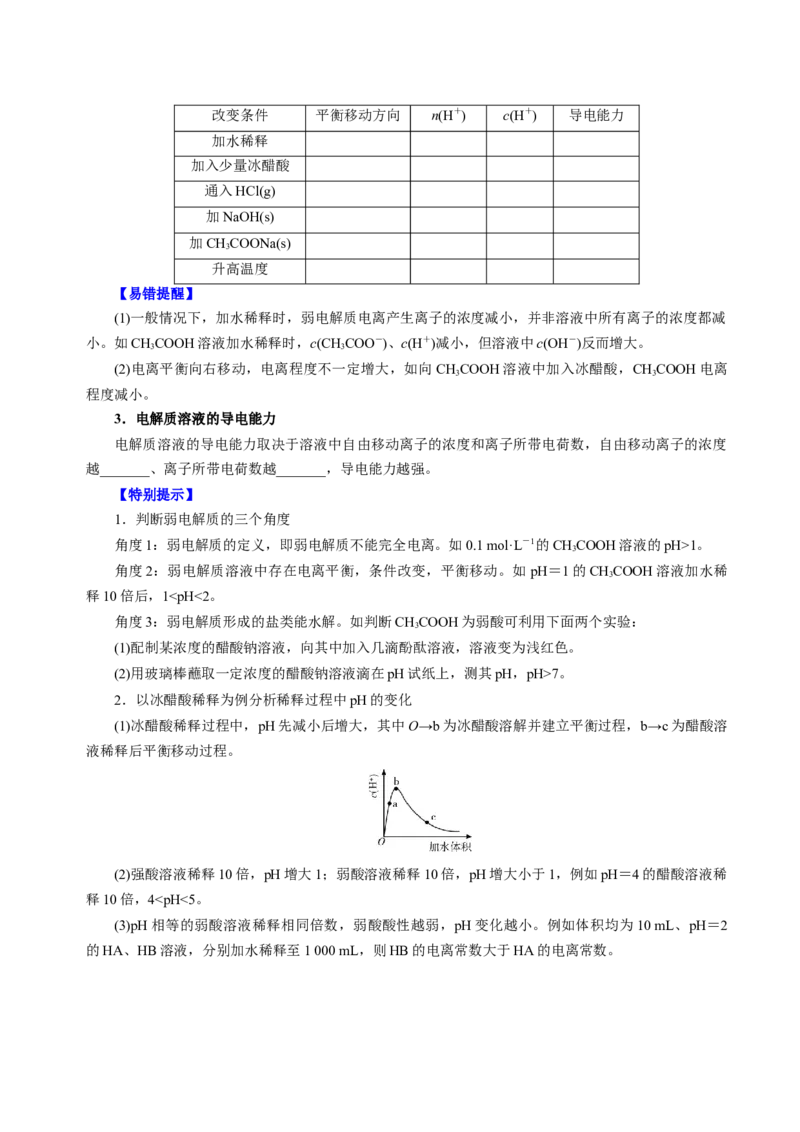
2.以冰醋酸稀释为例分析稀释过程中pH的变化
(1)冰醋酸稀释过程中,pH先减小后增大,其中O→b为冰醋酸溶解并建立平衡过程,b→c为醋酸溶
液稀释后平衡移动过程。
(2)强酸溶液稀释10倍,pH增大1;弱酸溶液稀释10倍,pH增大小于1,例如pH=4的醋酸溶液稀
释10倍,4K(HY),则酸性:HX>HY。( )
a a
(4)相同温度下,电离常数越大,溶液中c(H+)一定越大。( )
(5)25 ℃时,向0.1 mol·L-1的醋酸溶液中加入少量冰醋酸,其电离度变小。( )
(6)弱电解质的电离程度越大,电离常数越大。( )
(7)电离常数越大,表示该电解质电离能力越强。( )
(8)电离常数大的酸溶液中的c(H+)一定大于电离常数小的溶液。( )
(9)对于1 mol·L-1的CHCOOH溶液,升高温度,电离程度增大。( )
3
(10)温度不变,向NH ·H O溶液中加入NH Cl,平衡左移,电离平衡常数减小。( )
3 2 4
(11)要增大某种弱电解质的电离平衡常数,只能采取升高温度的方法。( )
(12)对于CHCOOHCHCOO-+H+,在一定温度下,加入盐酸平衡左移,电离平衡常数减小。( )
3 3
(13)对于0.1 mol·L-1的氨水,加水稀释后,溶液中c(NH)·c(OH-)变小。( )
(14)常温下,向10 mL pH=3的醋酸溶液中加水稀释后,溶液中不变。( )一、电离平衡常数及应用
部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HS HCO HClO
2 2 3
电离平衡 K =1.1×10-7 K =4.5×10-7
a1 a1
K=1.77×10-4 K=4.0×10-8
a a
常数(25℃) K =1.3×10-13 K =4.7×10-11
a2 a2
按要求回答下列问题:
(1)HCOOH、HS、HCO、HClO的酸性由强到弱的顺序为________________________。
2 2 3
(2)相同浓度的HCOO-、HS-、S2-、HCO、CO、ClO-结合H+的能力由强到弱的顺序为
____________________________________________________________________。
(3)运用上述电离常数及物质的特性判断下列化学方程式不正确的是________(填序号)。
①次氯酸与NaHCO 溶液的反应:HClO+HCO===ClO-+HO+CO↑
3 2 2
②少量CO 通入NaClO溶液中:CO+HO+2ClO-===CO+2HClO
2 2 2
③少量CO 通入NaClO溶液中:CO+HO+ClO-===HCO+HClO
2 2 2
④硫化氢通入NaClO溶液中:HS+ClO-===HS-+HClO
2
⑤碳酸钠滴入足量甲酸溶液中:2HCOOH+CO===2HCOO-+CO↑+HO
2 2
二、判断微粒浓度比值的大小
常温下,将0.1 mol·L-1的CHCOOH溶液加水稀释,请填写下列表达式中的数据变化情况(填“变
3
大”“变小”或“不变”)。
(1)________;
(2)________;
(3)________;
(4) ________;
(5)________。
三、电离平衡常数的计算
1.常温下,向a mol·L-1 CHCOONa溶液中加入等体积的b mol·L-1盐酸使溶液呈中性,不考虑盐
3
酸和醋酸的挥发,则CHCOOH的电离常数K=______________(用含a和b的代数式表示)。
3 a
2.常温下,0.1 mol·L-1的HA溶液中HA、HA-、A2-在三者中所占的物质的量分数(分布分数)随
2 2
pH变化的关系如图所示。
(1)H A的电离方程式为____________________________,HA的二级电离常数K =_______。
2 2 a2(2)已知25 ℃时HF的K=10-3.45,将少量HA的溶液加入足量NaF溶液中,发生反应的离子方程式
a 2
为____________________________。