文档内容
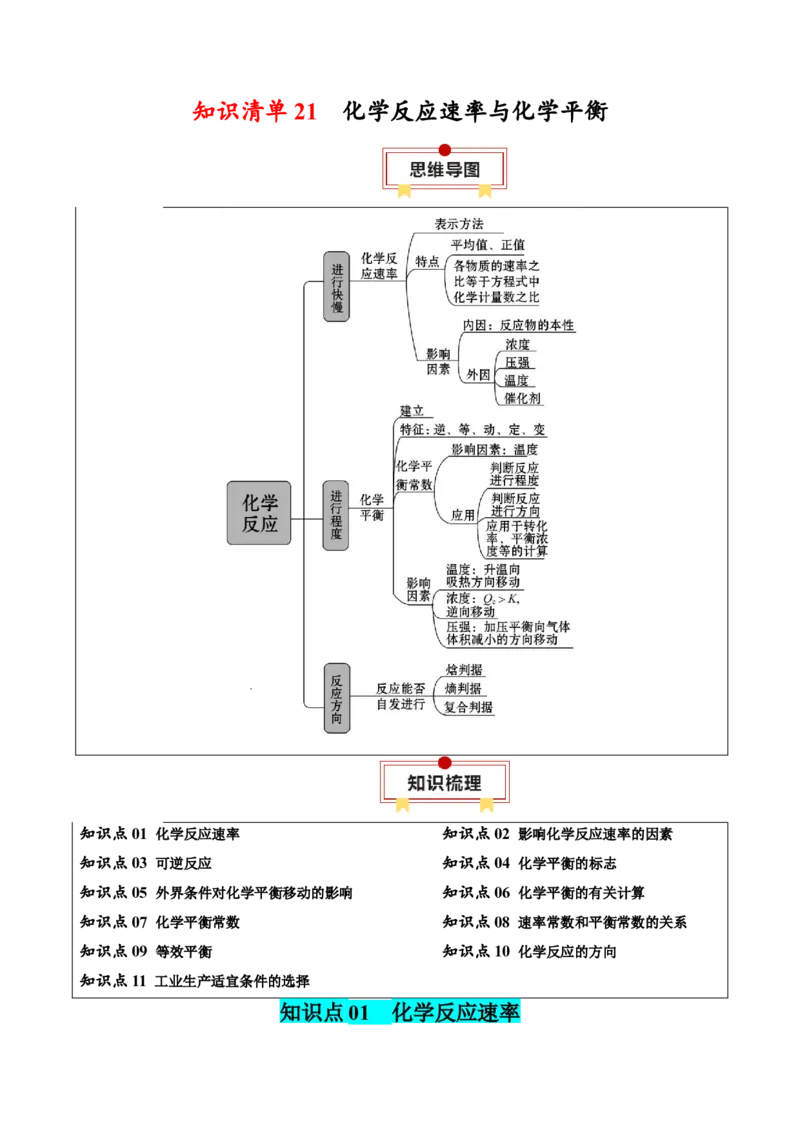
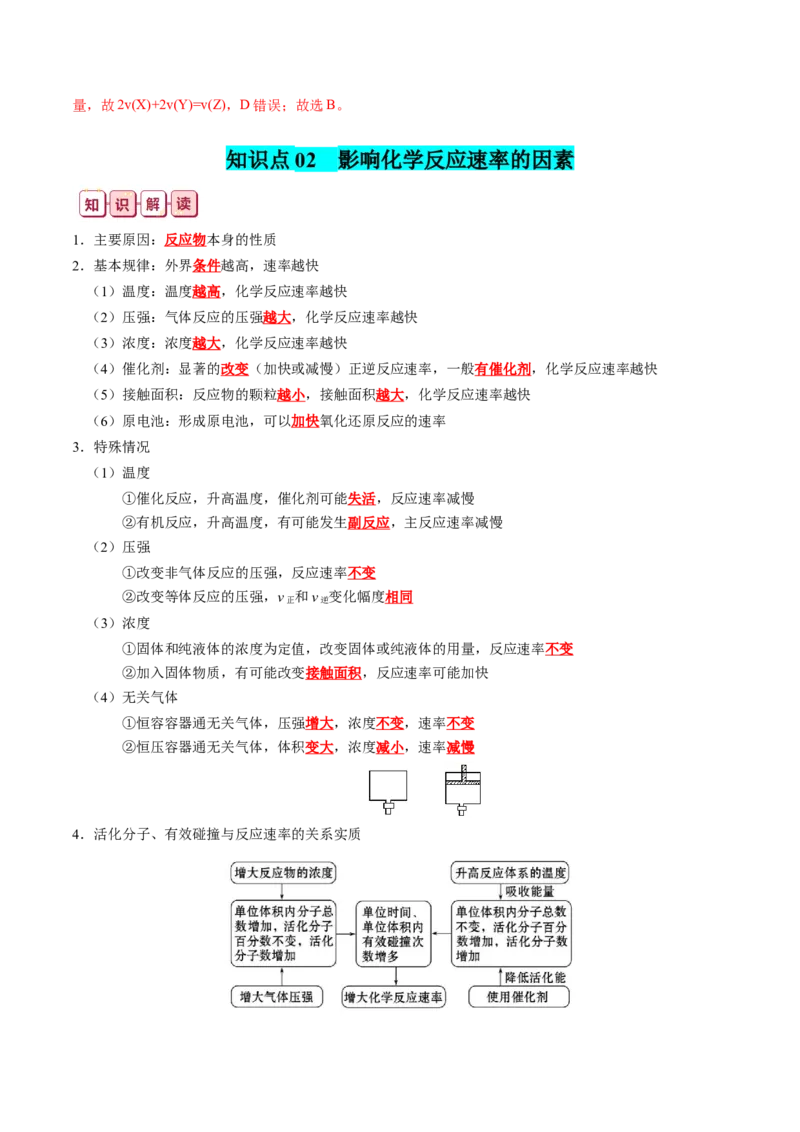
知识清单 21 化学反应速率与化学平衡
知识点01 化学反应速率 知识点02 影响化学反应速率的因素
知识点03 可逆反应 知识点04 化学平衡的标志
知识点05 外界条件对化学平衡移动的影响 知识点06 化学平衡的有关计算
知识点07 化学平衡常数 知识点08 速率常数和平衡常数的关系
知识点09 等效平衡 知识点10 化学反应的方向
知识点11 工业生产适宜条件的选择
知识点 01 化学反应速率1.概念:用来衡量化学反应进行快慢的物理量
2.表示:单位时间内某种量的变化量
3.化学反应速率的计算
△c △n
(1)常规公式:v=△t =V×△t
①常用单位: mol·L - 1 · s - 1 或 mol·L - 1 ·min - 1 或 mol·L - 1 ·h - 1
②适用范围:表示气体物质或溶液中可溶性物质的速率,不表示固体或纯液体物质的速率
△X
(2)非常规公式:v=△t
(X代表n、P、m、V等量)
①常用单位: mol·min - 1 、 Pa·min - 1 、 g·min - 1 、 L·min - 1
②适用范围:任何物质的反应速率
(3)利用关系式计算
①应用前提:同一化学反应
②常用关系:速率比=化学计量数比=物质的量浓度变化比=物质的量变化比
4.大小比较
(1)比较前提:同一反应,同一物质,同一单位
(2)换算方法:各物质的速率除以相应的化学计量数,数大的速率快
5.说明
(1)化学反应速率表示某段时间内的平均反应速率,不表示即时速率
(2)化学反应速率只有正值,没有负值
(3)随着反应的进行,反应物的浓度等量逐渐减小,反应速率越来越慢
1.速率大小比较“三步骤”
(1)“一看”单位是否一致,不一致转化为同一单位。
(2)“二化”将不同物质表示的反应速率转化为同一物质表示的化学反应速率。
(3)“三比较”比较数值大小。
2.比较反应速率快慢的常用方法:
(1)定性描述——通过在相同时间点,不同的实验现象来判断反应的快慢。
①观察产生气泡的快慢;
②观察试管中剩余锌粒的多少;
③用手接触试管,感受试管外壁温度的高低。
(2)定量描述——通过实验测量来判断反应的快慢。
①测定气体的体积或体系的压强;
②测定物质的物质的量的变化;③测定物质或离子的浓度变化;
④测定体系的温度或反应的热量变化。
若有多种测量方案时,一般采取易操作,现象明显的实验方案。
【典例 01】(2023 春·四川内江·高三四川省资中县第二中学校考开学考试)对于可逆反应
,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A. B.
C. D.
【答案】B
【分析】速率比等于化学计量数比,都转化为用A物质表示的反应速率,速率的单位都用mol/(L·min),然
后进行比较。
【解析】A. ;B.v(A)= v(B)= ×1.5 mol L−1min−1=1.0 mol L−1min−1;C.
⋅ ⋅ ⋅ ⋅
v(A)= v(D)=0.8 mol L−1min−1;D.v(A)= v(C)= ×0.1 mol L−1min−1=0.05molL−1min−1;可见反应速率最大
的是1molL−1min−1; ⋅ 故 ⋅ 选B。 ⋅ ⋅ ⋅ ⋅
【典例02】(2023·辽宁丹东·统考一模)恒温恒容条件下,向密闭容器中加入一定量X,反应X=2Z经历
⋅ ⋅
两步:①X→Y;②Y→2Z。图为该体系中X、Y、Z浓度随时间变化的曲线。下列说法正确的是
A.a为 随t的变化曲线
B. 时,Y的消耗速率大于生成速率
C.随着 的减小,反应①、②速率均降低
D.体系中
【答案】B
【解析】A.反应X=2Z经历两步:①X→Y;②Y→2Z,可知c(Y)先增大,后减小,A错误;B.t 时Y
1
的浓度在下降,消耗速率大于生成速率,B正确;C.由图甲中的信息可知,随c(X)的减小,c(Y)先增大后
减小,c(Z)增大,因此,反应①的速率随c(X)的减小而减小,而反应②的速率先增大后减小,C错误;D.
根据体系中发生的反应可知,在Y的浓度达到最大值之前,单位时间内X的减少量等于Y和Z的增加量,
因此,v(X)=v(Y)+ v(Z),但是,在Y的浓度达到最大值之后,单位时间内Z的增加量等于Y和X的减少量,故2v(X)+2v(Y)=v(Z),D错误;故选B。
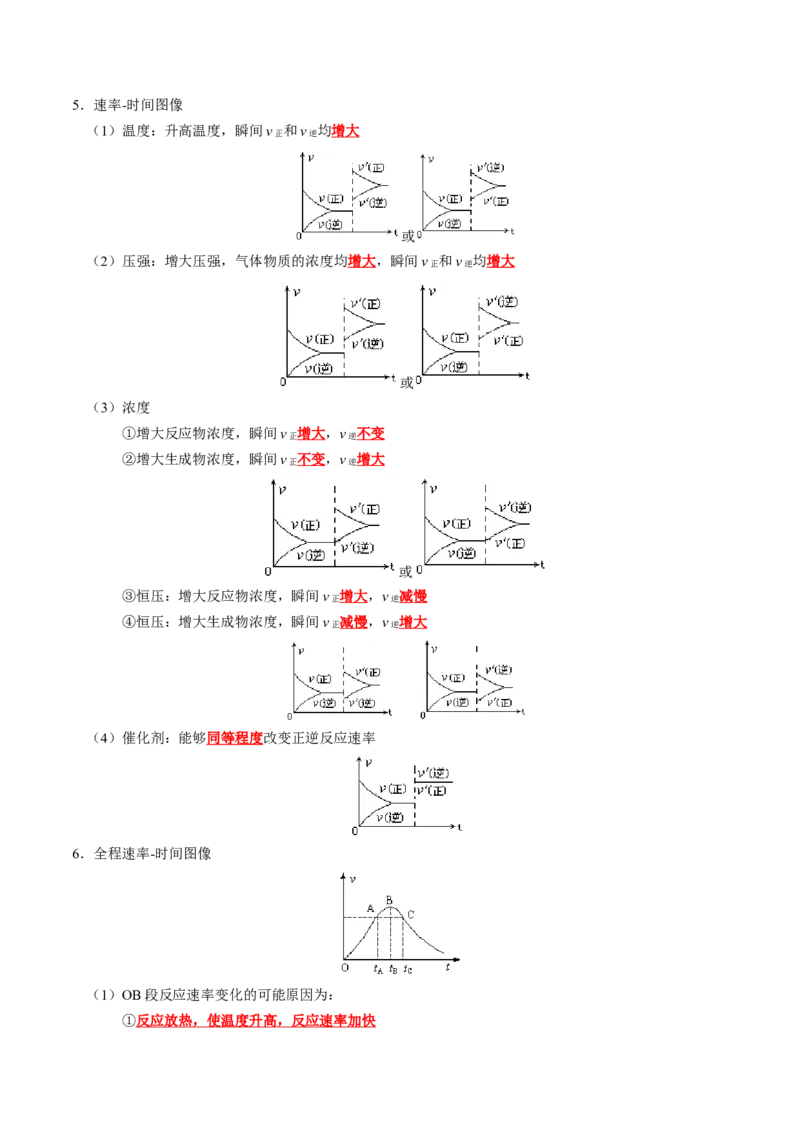
知识点 02 影响化学反应速率的因素
1.主要原因:反应物本身的性质
2.基本规律:外界条件越高,速率越快
(1)温度:温度越高,化学反应速率越快
(2)压强:气体反应的压强越大,化学反应速率越快
(3)浓度:浓度越大,化学反应速率越快
(4)催化剂:显著的改变(加快或减慢)正逆反应速率,一般有催化剂,化学反应速率越快
(5)接触面积:反应物的颗粒越小,接触面积越大,化学反应速率越快
(6)原电池:形成原电池,可以加快氧化还原反应的速率
3.特殊情况
(1)温度
①催化反应,升高温度,催化剂可能失活,反应速率减慢
②有机反应,升高温度,有可能发生副反应,主反应速率减慢
(2)压强
①改变非气体反应的压强,反应速率不变
②改变等体反应的压强,v 和v 变化幅度相同
正 逆
(3)浓度
①固体和纯液体的浓度为定值,改变固体或纯液体的用量,反应速率不变
②加入固体物质,有可能改变接触面积,反应速率可能加快
(4)无关气体
①恒容容器通无关气体,压强增大,浓度不变,速率不变
②恒压容器通无关气体,体积变大,浓度减小,速率减慢
4.活化分子、有效碰撞与反应速率的关系实质5.速率-时间图像
(1)温度:升高温度,瞬间v 和v 均增大
正 逆
或
(2)压强:增大压强,气体物质的浓度均增大,瞬间v 和v 均增大
正 逆
或
(3)浓度
①增大反应物浓度,瞬间v 增大,v 不变
正 逆
②增大生成物浓度,瞬间v 不变,v 增大
正 逆
或
③恒压:增大反应物浓度,瞬间v 增大,v 减慢
正 逆
④恒压:增大生成物浓度,瞬间v 减慢,v 增大
正 逆
(4)催化剂:能够同等程度改变正逆反应速率
6.全程速率-时间图像
(1)OB段反应速率变化的可能原因为:
①反应放热,使温度升高,反应速率加快②反应生成催化剂,反应速率加快
(2)BC段反应速率变化的可能原因为:反应物浓度降低,反应速率减慢
7.探究外界条件对化学反应速率的影响
(1)方法:控制变量法
(2)溶液反应:加水调节溶液的总体积不变,以保证某种成分的浓度不变
(3)实例:探究Y溶液浓度对反应速率的影响
实验(混合溶液) 1 2 3 4 5 6
6 6
4mol/LX溶液/mL 60 60 60 60
0 0
2
饱和Y溶液/mL 0 1.0 5.0 10 40
0
4 2
HO/mL 39 35 30 0
2
0 0
8.速率方程
(1)意义:表示反应物浓度与反应速率的定量关系
(2)举例:A(g)+B (g) 2AB(g),v=kcα(A)·cβ(B )
2 2 2 2
(3)测定方法:α、β必须通过实验测定,无法直接写出。
①H+Cl 2HCl,v=k[c(H )][c(Cl )]1/2
2 2 2 2
②N(g)+3H (g) 2NH (g),v=kc(N)·c1.5(H)·c-1(NH )
2 2 3 2 2 3
(4)反应速率常数
①符号:反应速率方程中的比例系数k
②意义:通常k越大,反应进行得越快,反应的活化能越小
③影响因素:温度、催化剂、固体表面性质
不同的外界条件对化学反应速率影响的注意点:
1.浓度:增大浓度、速率增大;减少浓度、速率减小;改变纯固体或纯液体的量对化学反应速率没
有影响。
2.压强:①必须有气体参加;②压强的改变实质是改变浓度。
3.温度:无论是吸热反应还是放热反应,升高温度,速率增大,降低温度,速率减小。
4.催化剂:催化剂只改变反应速率,不改变反应的方向,也不改变反应热的大小,若是可逆反应,
则同等程度改变正、逆反应速率。
【典例03】(2023·浙江宁波·镇海中学校考模拟预测)一定温度下,利用测压法在刚性反应器中研究固体
催化剂作用下的A的分解反应: 。体系的总压强p随时间t的变化如表所示:t/min 0 100 150 250 420 500 580
p/kPa 12.1 13.3 13.9 15.1 17.14 x 19.06
下列说法不正确的是
A.100~150min,消耗A的平均速率为
B.其他条件不变,420min时向刚性容器中再充入少量A,反应速率比原420min时大
C.推测x为18.1
D.升高体系温度,不一定能加快反应速率
【答案】B
【解析】A.反应 ,反应前后气体压强变化和生成C的量成正比,同时A的变化为
变化量的 ,用压强代表浓度,则100~150min体系压强变化=13.9kPa-13.3kPa=0.06kPa,消耗A的平均速
率= =0.006kPamin-1,故A正确;B.其他条件不变,420min时向刚性容器中再充入少量
⋅
A,相当于增大压强,反应在固体催化剂表面进行,固体表面积一定,反应速率不变,故B错误;C.0~
100min,压强变化为1.2kPa,150min~250min,压强变化1.2kPa,则100kPa~500kPa,体系压强变化
1.2×4kPa=4.8kPa,则500min时,体系压强=13.3kPa+4.8kPa=18.1kPa,故C正确;D.反应在催化剂表面反
应,升高体系温度,催化剂活性减小时,反应速率减小,不一定能加快反应速率,故D正确;故选:B。
【典例04】(2023·北京西城·统考一模)探究影响HO 分解速率的影响因素,实验方案如图。
2 2
下列说法不正确的是
A.对比①②,可探究FeCl 溶液对HO 分解速率的影响
3 2 2
B.对比②③④,可探究温度对HO 分解速率的影响
2 2
C.HO 是直线形的非极性分子
2 2
D.HO 易溶于水,主要是由于HO 与HO分子之间能形成氢键
2 2 2 2 2
【答案】C
【解析】A.实验②是在实验①的溶液中加入催化剂FeCl ,与实验①做对比实验,可探究FeCl 溶液对
3 3
HO 分解速率的影响,A正确;B.实验②是参照,③、④相当于在②的基础上升高和降低温度,可探究
2 2
温度对HO 分解速率的影响,B正确;C.HO 的分子结构为 ,分子结构不对称,为极性分子,
2 2 2 2
C不正确;D.HO 为极性分子,水也为极性分子,HO 易溶于水,满足相似相溶原理,更主要是HO 与
2 2 2 2 2 2
HO分子之间能形成氢键,D正确;故选C。
2知识点 03 可逆反应
1.可逆反应的判断:反应形式相反,反应条件相同
2.可逆反应的特点
(1)同步性:正逆反应同时进行
(2)等同性:反应条件完全相同
(3)共存性
①反应不可能进行到底,即反应体系中反应物与生成物共存
②各组分的浓度都大于零
3.证明某反应为可逆反应
(1)检验出某种生成物
(2)检验量少的反应物是否有剩余
4.化学平衡状态的特征
【典例05】已知: 溶液是检验 的试剂,若溶液中存在 ,将产生蓝色沉淀。将
的KI溶液和 的 溶液等体积混合后,取混合液分别完成下列实验,其中能
说明溶液中存在化学平衡“ ”的是
实验编
实验操作 实验现象
号
① 滴入KSCN溶液 溶液变红色
② 滴入 溶液 有黄色沉淀生成
③ 滴入 溶液 有蓝色沉淀生成
④ 滴入淀粉溶液 溶液变蓝色
A.① B.②和④ C.③和④ D.①和②
【答案】A【详解】 的 溶液c(Fe3+)为0.1 ,与0.2 的KI等体积混合反应,I-过量。
①检验出Fe3+,说明过量的KI仍不能使Fe3+完全转化,该反应为可逆反应;②由于KI过量,不管反应是
否可逆,一定能检验到I-;③检验到Fe2+,只能证明反应已发生,与可逆反应无关;④同③,证明反应已
发生;因此,实验①可证明反应为可逆反应;
答案选A。
【典例06】在一密闭容器中进行反应:2SO (g)+O(g) 2SO (g),已知反应过程中某一时刻SO 、O、SO
2 2 3 2 2 3
的浓度分别为0.1 mol/L、0.05 mol/L、0.3 mol/L。当反应达到平衡时,可能存在的数据是
⇌
A.SO 为0.4 mol/L,O 为0.2 mol/L
2 2
B.SO 、SO 均为0.8 mol/L
2 3
C.SO 为0.4 mol/L
3
D.SO 为0.35 mol/L
2
【答案】D
【分析】 ,该反应为可逆反应,物质浓度范
围:0<c(SO )<0.4 mol/L,0<c(O)<0.2 mol/L,0<c(SO )<0.4 mol/L。
2 2 3
【详解】A.SO 和O 的浓度增大,说明反应向逆反应方向进行建立平衡,若SO 完全反应,则SO 和O
2 2 3 2 2
的浓度浓度分别为0.4mol/L、0.2mol/L,三氧化硫不可能完全转化,故A错误;
B.根据分析和硫原子守恒可知c(SO )+ c(SO )=0.4mol/L,当SO 、SO 均为0.8 mol/L时,0.8 mol/L+0.8
2 3 2 3
mol/L<0.4 mol/L,故B错误;
C.SO 为0.4mol/L,SO 的浓度增大,说明该反应向正反应方向进行建立平衡,若二氧化硫和氧气完全反
3 3
应,SO 的浓度的浓度为0.4mol/L,达到平衡的实际浓度应该小于0.4mol/L,故C错误;
3
D. SO 为0.35mol/L,SO 的浓度增大,说明反应向逆反应方向进行建立平衡,若SO 完全反应,则SO
2 2 3 2
的浓度浓度为0.4mol/L,实际浓度为0.35mol/L小于0.4mol/L,故D正确;
故答案为:D。
知识点 04 化学平衡的标志
1.速率标志(本质标志):v =v
正 逆
(1)同一组分的生成速率和消耗速率相等
(2)不同物质的正逆反应速率比等于化学计量数之比
2.宏观标志:某些量开始变化,后来不变
(1)一定达到平衡的情况
①某组分的质量、物质的量、浓度、颜色不再变化②反应物的转化率不再变化
(2)特殊情形
①绝热容器:容器的温度不变时,一定达到平衡状态
②可逆电池:电流或电压等于零时,一定达到平衡状态
(3)判断化学平衡状态的常用公式
m m -m
气体 总 固或液
V V
①混合气体的密度:ρ= 气体= 气体
m m -m
气体 总 固或液
②混合气体的平均摩尔质量:M= n 气体 = n 气体
③气体状态方程:PV=nRT
3.限度标志
(1)反应物的转化率最大,百分含量最小
(2)生成物的产率最大,百分含量最大
(3)图像获取
①前提:在多个相同的容器中,加入相同量的反应物
②过程:测相同时间内,不同条件下相关量,描点绘出图像
(4)图像解读
①极限点:刚好达到平衡
②极限点前:非平衡点,受速率控制,加催化剂,反应物的转化率变大
③极限点后:新平衡点,受平衡控制,加催化剂,反应物的转化率不变
4.几种特殊反应的平衡依据
(1)量比不变型
①反应物或生成物量的比不变,不一定达到平衡状态
②反应物和生成物量的比不变,一定达到平衡状态
(2)量相等型
①反应物和生成物的量相等,不一定达平衡状态
②反应物和反应物的量相等,不一定达平衡状态
③量不变≠量相等≠量或量的比等于某一具体的数
(3)等体反应型:3A(g) 2B(g)+C(g)
①恒温恒压:混合气体的体积不变,一定达到平衡状态
②恒温恒容:混合气体的压强不变,不一定达到平衡状态
(4)固液参与型:2A(g) 2B(g)+C(s)①混合气体的密度不变,一定达到平衡状态(恒T、V)
②混合气体的平均摩尔质量不变,一定达到平衡状态
(5)固液分解型:2A(s) 2B(g)+C(g)
①混合气体的密度不变,一定达到平衡状态(恒T、V)
②混合气体的平均摩尔质量不变,不一定达到平衡状态
③某种气体组分的物质的量分数不变,不一定达到平衡状态
5.注意平衡标志和平衡特征的区别
(1)平衡标志:能够说明反应达到平衡状态的某些事实
(2)平衡特征:平衡时存在的某些事实,但不一定能用于判断是否达到平衡
利用相关物质的一些物理量来判断化学反应是否达到平衡时,该“量”一定是“变量”,当“变
量”不变时,才说明达到平衡状态。
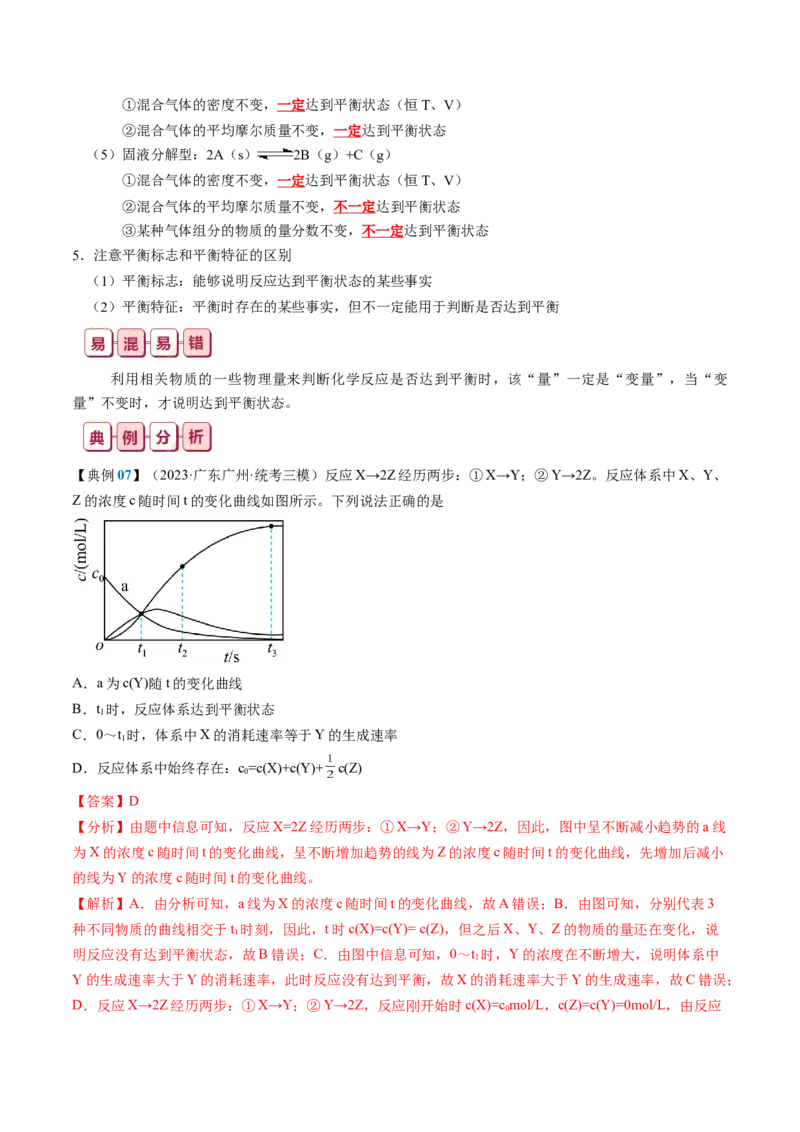
【典例07】(2023·广东广州·统考三模)反应X→2Z经历两步:①X→Y;②Y→2Z。反应体系中X、Y、
Z的浓度c随时间t的变化曲线如图所示。下列说法正确的是
A.a为c(Y)随t的变化曲线
B.t 时,反应体系达到平衡状态
1
C.0~t 时,体系中X的消耗速率等于Y的生成速率
1
D.反应体系中始终存在:c=c(X)+c(Y)+ c(Z)
0
【答案】D
【分析】由题中信息可知,反应X=2Z经历两步:①X→Y;②Y→2Z,因此,图中呈不断减小趋势的a线
为X的浓度c随时间t的变化曲线,呈不断增加趋势的线为Z的浓度c随时间t的变化曲线,先增加后减小
的线为Y的浓度c随时间t的变化曲线。
【解析】A.由分析可知,a线为X的浓度c随时间t的变化曲线,故A错误;B.由图可知,分别代表3
种不同物质的曲线相交于t 时刻,因此,t时c(X)=c(Y)= c(Z),但之后X、Y、Z的物质的量还在变化,说
1
明反应没有达到平衡状态,故B错误;C.由图中信息可知,0~t 时,Y的浓度在不断增大,说明体系中
1
Y的生成速率大于Y的消耗速率,此时反应没有达到平衡,故X的消耗速率大于Y的生成速率,故C错误;
D.反应X→2Z经历两步:①X→Y;②Y→2Z,反应刚开始时c(X)=c mol/L,c(Z)=c(Y)=0mol/L,由反应
0的系数关系可知,X的消耗量等于Y的生产量,Y的消耗量等于Z生成量的一半,则反应体系中始终存在:
c=c(X)+c(Y)+ c(Z),故D正确;故选D。
0
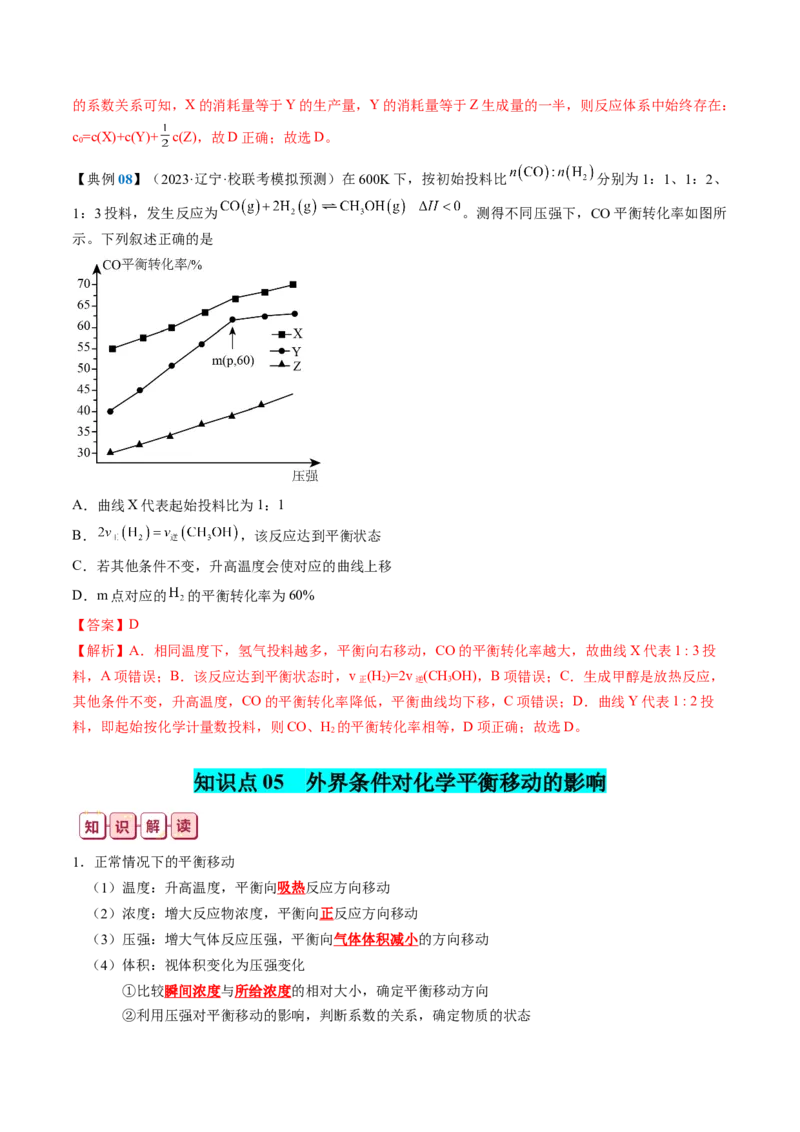
【典例08】(2023·辽宁·校联考模拟预测)在600K下,按初始投料比 分别为1:1、1:2、
1:3投料,发生反应为 。测得不同压强下,CO平衡转化率如图所
示。下列叙述正确的是
A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
【答案】D
【解析】A.相同温度下,氢气投料越多,平衡向右移动,CO的平衡转化率越大,故曲线X代表1 : 3投
料,A项错误;B.该反应达到平衡状态时,v (H )=2v (CHOH),B项错误;C.生成甲醇是放热反应,
正 2 逆 3
其他条件不变,升高温度,CO的平衡转化率降低,平衡曲线均下移,C项错误;D.曲线Y代表1 : 2投
料,即起始按化学计量数投料,则CO、H 的平衡转化率相等,D项正确;故选D。
2
知识点 05 外界条件对化学平衡移动的影响
1.正常情况下的平衡移动
(1)温度:升高温度,平衡向吸热反应方向移动
(2)浓度:增大反应物浓度,平衡向正反应方向移动
(3)压强:增大气体反应压强,平衡向气体体积减小的方向移动
(4)体积:视体积变化为压强变化
①比较瞬间浓度与所给浓度的相对大小,确定平衡移动方向
②利用压强对平衡移动的影响,判断系数的关系,确定物质的状态③反应:xA(g)+yB(g) zC(g)
c(A)=0.5mol·L-
原平衡
1
体积加倍新平 c(A)=0.3mol·L-
衡 1
平衡移动方向 逆反应
x、y、z的关系 x + y > z
2.特殊情况下的平衡移动
(1)向容器中通入无关气体
①恒容容器:压强增大,浓度不变,速率不变,平衡不移动
②恒压容器:体积增大,浓度减小,速率减慢,平衡向气体体积增大的方向移动
(2)同倍数改变反应物和生成物浓度
①恒温恒容:相当于改变压强
②恒温恒压:瞬间各组分的浓度不变,平衡不移动
(3)不同倍数改变反应物和生成物浓度
①Q<K:平衡正向移动,v >v
正 逆
②Q=K:平衡不移动,v =v
正 逆
③Q>K:平衡逆向移动,v <v
正 逆
3.水对平衡移动的影响
(1)溶液反应:加水,相当于稀释,平衡向可溶性微粒系数和增大的方向移动
①A(aq)+B(aq) C(aq)+D(aq):不移动
②A(aq) C(aq)+D(aq)+H O(l):正向移动
2
③A(aq)+B(aq)+H O(l) C(aq):逆向移动
2
(2)水蒸气或非溶液反应:当成普通的反应物或生成物即可
①C(s)+H O(g) CO(g)+H (g):通入HO(g)正向移动
2 2 2
②2A(g)+O (g) 2C(g)+H O(g):通入HO(g)逆向移动
2 2 2
③RCOOH(l)+R′OH(l) RCOOR′(l)+H O(l),加浓硫酸正向移动
2
4.勒夏特列原理及其应用
(1)原理:改变影响平衡移动的一个条件,平衡向减弱该条件方向移动
(2)前提:必须存在可逆过程(存在平衡)
①化学平衡:N(g)+3H (g) 2NH (g)
2 2 3
②电离平衡:CHCOOH CHCOO-+H+
3 3
③水解平衡:Fe3++3H O Fe(OH)+3H+
2 3
④沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq)
⑤气体溶解平衡:O(g) O(aq)
2 2
⑥结晶溶解平衡:KNO(s) K+(aq)+NO -(aq)
3 3
(3)必须有平衡移动,且实际移动方向符合理论移动方向①催化剂不能使平衡移动,无法用勒夏特列原理解释。
②等体反应改变压强,平衡不移动,无法用勒夏特列原理解释。
(3)“加的多,剩的多”原理
①增大X的浓度,新平衡时c(X)一定比原平衡时的大
②增大压强,新平衡时P一定比原平衡时的大
③升高温度,新平衡时T一定比原平衡时的大
(4)“单一气体型”反应的特殊性
①反应形式:A(s) xB(s)+yC(g)
②改变压强、浓度,平衡移动,新平衡时P、c不变
(5)“单侧气体型”反应的特殊性
①反应形式:A(s) xB(g)+yC(g)
②改变压强、同倍数改变浓度,平衡移动,新平衡时P、c不变
③改变一种气体浓度,平衡移动,新平衡时c变大
外界条件对化学平衡移动影响的理解
1.浓度:①浓度指与反应有关的气体或溶液中实际参加反应离子的浓度。②改变纯固体或纯液体的
量对平衡无影响。
2.温度:任何化学反应都伴有能量的变化(放热或吸热),所以,改变温度一定会使化学平衡发生
移动。
3.压强:
(1)无气体参与的化学反应,由于改变压强不能改变化学反应速率,所以改变压强不能使无气体物
质存在的化学平衡发生移动。
(2)对于反应前后气体分子数相等的可逆反应,改变压强后,正、逆反应速率同时、同等程度地改
变,因此增大或减小压强不能使其化学平衡发生移动。
(3)“无关气体”(不与原平衡体系中各物质反应的气体)对化学平衡的影响。
①恒温、恒容条件下
原平衡体系―――――――→体系总压强增大―→体系中各组分的浓度不变―→平衡不移动
②恒温、恒压条件下
原平衡体系充入―――――――→容器容积增大―→体系中各组分的浓度减小――――――――→
4.催化剂:催化剂同等程度改变正逆反应速率,不影响平衡移动。
【典例09】(2023·江苏盐城·盐城市伍佑中学校考模拟预测)卤族元素单质及其化合物应用广泛。具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
反应生成硫酰氟( )。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37.
通入 酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用 制备 的热化
学方程式为 。下列关于反应
的说法不正确的是
A.保持其他条件不变,平衡时升高温度,
B.保持其他条件不变,平衡时通入 ,达到新平衡时 变小
C.反应生成1mol ,转移电子数目为
D.及时分离出CO,有利于 生成
【答案】B
【解析】A.该反应的正反应是放热反应,保持其他条件不变,平衡时升高温度,v正、v逆都增大,由于
温度对吸热反应影响更大,因此升高温度后,v正<v逆,A正确;B.该反应的化学平衡常数K=
,化学平衡常数只与温度有关,保持其他条件不变,平衡时通入Cl,即增大了反应物的
2
浓度,化学平衡正向移动,但由于温度不变,因此化学平衡常数不变,因此平衡时通入Cl,达到新平衡时
2
不变,B错误;C.根据反应方程式可知:反应生成1 mol TiCl ,反应过程中转移4 mol
4
电子,则转移电子数目为 ,C正确;D.及时分离出CO,即减小了生成物的浓度,化学平衡
正向移动,会产生更多的TiCl ,因此有利于TiCl 生成,D正确;故合理选项是B。
4 4
【典例10】(2023·上海静安·统考二模)聚丙烯腈纤维俗名人造羊毛,由丙烯腈聚合而得。用丙烯合成丙
烯腈的反应如下: 2C H(g)+2NH (g)+3O(g) 2C HN(g)+6HO(g)+1030kJ
3 6 3 2 3 3 2
(1)某密闭容器中发生上述反应,生成丙烯腈的反应速率与反应时间的关系如下图所示。
t 时刻表示体系改变的反应条件为 ; t 时刻表示体系改变了另一反应条件,此时平衡 移动
1 2
(填“正向”、“逆向”或“不”)。
丙烯的转化率与反应温度的关系如图示:(2)有利于提高丙烯平衡转化率的反应条件有 ;
(3)最大转化率所对应的温度为460℃。当温度低于460℃时,丙烯的转化率 (填“是”或“不是”)
所对应温度下的平衡转化率,理由是 。
(4)一定条件下,在2L恒容密闭容器中,通入84g C H、34g NH、96g O ,若该反应5 min到达a点,则0
3 6 3 2
~5min内丙烯的平均反应速率为 mol∙L−1∙min−1。
【答案】 (1)使用了催化剂 正向
(2)降低温度、降低压强
(3)不是 该反应的正反应为放热反应,平衡状态下,若升高温度,平衡朝逆反应方向移动,平衡转化
率将降低
(4)0.12
【解析】(1)碳元素是6号元素,则硅原子核外电子排布为2、6,则硅在元素周期表中的位置是第二周
期IVA族;根据同电子层结构核多径小,则C、N、O三种元素的原子半径由小到大的顺序为r(O)<r(N)<
r(C);故答案为:第二周期IVA族;r(O)<r(N)<r(C)。
(2)t 时刻反应速率都增大,且增大程度相等,则表示体系改变的反应条件为使用催化剂;由于生成丙烯
1
腈的反应是体积增大的放热反应,而根据图中信息是反应速率降低,则也可能为降温,也可能减小压强,
t 时刻表示体系改变了另一反应条件,无论是降温还是减小压强,平衡都是正向移动;故答案为:使用了
2
催化剂;正向。
(3)由于反应是体积增大的放热反应,有利于提高丙烯平衡转化率的反应条件有降低温度、降低压强;
故答案为:降低温度、降低压强。
(4)该反应的正反应为放热反应,平衡状态下,若升高温度,平衡朝逆反应方向移动,平衡转化率将降
低,而图中曲线是随温度升高平衡转化率在逐渐升高,因此当温度低于460℃时,丙烯的转化率不是所对
应温度下的平衡转化率;故答案为:不是;该反应的正反应为放热反应,平衡状态下,若升高温度,平衡
朝逆反应方向移动,平衡转化率将降低。
(5)一定条件下,在2L恒容密闭容器中,通入84g C H(物质的量为2mol)、34g NH、96g O ,,若该反
3 6 3 2
应5 min到达a点,则0~5min内丙烯的平均反应速率为 ;
故答案为:0.12。
知识点 06 化学平衡的有关计算1.常用计算公式
某物质反应的量
该物质的总量
(1)反应物的转化率: = ×100%
某组分的量
混合物的总量
(2)某组分的百分含量:含量= ×100%
①常见量:体积分数、物质的量分数
②关系式:体积分数=物质的量分数
(3)气体状态方程:PV=nRT
条件 公式 文字叙述
V n N
1 1 1
同温同压 气体体积比=物质的量比=分子数比
V n N
2= 2= 2
P n N
1 1 1
同温同容 气体压强比=物质的量比=分子数比
P n N
2= 2= 2
ρ V n N 气体密度比=气体体积反比
1 2 2 2
同温同压同质量
ρ V n N
2= 1= 1= 1 =物质的量反比=分子数反比
2.计算模式——“三段式”
(1)确定反应物或生成物的起始加入量。
(2)确定反应过程的变化量。
(3)确定平衡量。
(4)依据题干中的条件,建立等量关系进行计算。
反应 aA(g) + bB(g) cC(g) + dD(g)
起始量/mol m n 0 0
转化量/mol ax bx cx dx
平衡量/mol m-ax n-bx cx dx
ax
①反应速率:v(A)=
V×t
(时间为tmin)
bx
n
②反应物转化率: (B)= ×100%
cx
③C的体积分数:φ(C)=_
m-ax+n-bx+cx+dx
×100%
p n
始 始 m+n
④反应前后气体的压强比:
p
平=
n 平=m-ax+n-bx+cx+dx
(恒温恒容)
V n
始 始 m+n
⑤反应前后气体的体积比:
V
平=
n 平=m-ax+n-bx+cx+dx
(恒温恒压)ρ
始
V
平
n
平
m-ax+n-bx+cx+dx
⑥反应前后气体的密度比: ρ 平= V 始= n 始= m+n (恒温恒压)
(5)也可以直接根据分压和分体积进行计算
①恒温恒容:气体压强比=物质的量比=化学计量数比
aA +bB
反应 cC(g) +dD(g)
(g) (g)
起始量Pa P P 0 0
A B
转化量Pa ax bx cx dx
平衡量Pa P-ax P -bx cx dx
A B
②恒温恒压:气体体积比=物质的量比=化学计量数比
aA +bB
反应 cC(g) +dD(g)
(g) (g)
起始量L V V 0 0
A B
转化量L ax bx cx dx
平衡量L V -ax V -bx cx dx
A B
【典例11】用CH 还原SO 不仅可以消除污染,而且可以得到单质S,反应如下:
4 2
t℃时,在容积为2L的恒容密闭容器中测的反应在不
同时刻各物质的物质的量如下表:
物质的量(mol)时间(min)
0 2 4 6 8 10
物质
SO 4.8 2.64 1.8 1.8 2.1 2.1
2
CO 0 1.08 1.5 1.5 1.75 1.75
2
下列说法不正确的是
A.前2min的平均反应速率v(CH)=0.27mol·L-1·min-1
4
B.6min时SO 的转化率等于10min时SO 的转化率
2 2
C.其它条件不变,在第10min后降低温度,可使容器中的CO 的浓度升高到1.4mol·L-1
2
D.向容器内通入适量的HS,会使平衡逆向移动
2
【答案】C
【详解】A.根据 可知,前2min甲烷物质的量变化
1.08mol,则 ,故A正确;B.根据表中数据可知6min时SO 的转化量为4.8mol-1.8mol=3mol,SO 转化率为 =62.5%;6min
2 2
后向反应体系中加入二氧化硫,导致平衡发生移动,10min时处于新的平衡,根据硫原子守恒,加入的
SO 的物质的量为0.3mol+(1.75mol-1.5mol) 2=0.8mol,则SO 的转化率为 =62.5%;所以转化
2 2
率相等,故B 正确;
C.10min时,二氧化硫浓度1.05mol/L,二氧化碳浓度0.875mol/L,若不改变容器体积,结合方程式,当
二氧化硫全部转化为二氧化碳的浓度1.2mol/L,但该反应为可逆反应,低温平衡正向移动,二氧化碳浓度
不能达到1.4mol/L,故C错误;
D.HS会与二氧化硫发生氧化还原反应,导致平衡逆向移动,故D正确;
2
答案选C。
【典例12】(2023·重庆·校联考模拟预测)一定温度下,在三个容积均为2.0L的恒容密闭容器中仅发生反
应:CHCOOH(g) CHOH(g)+CO(g) ΔH>0。下列说法正确的是
3 3
物质的起始浓度/mol·L-1 物质的平衡浓度/mol·L-1
容器编号 温度/K
c(CHOH) c(CO) c(CHCOOH) c(CHCOOH)
3 3 3
I 230 0.60 0.60 0 0.40
II 230 0.30 0.30 0.40
III 210 0 0 0.60
A.达平衡时,容器I与容器II中的总压强之比为6∶7
B.达平衡时,容器II中 比容器I中的大
C.达平衡时,容器III与容器I中的正反应速率相等
D.达平衡时,容器I中CHOH转化率与容器III中CHCOOH转化率之和大于1
3 3
【答案】B
【分析】容器Ⅰ中,依据表中数据,可建立下列三段式:
平衡常数K= =0.10。
容器Ⅱ中,浓度商Q= =0.225>0.10,所以平衡逆向移动,依据表中数据,设参加反应CO的物
质的量浓度为x,则可建立下列三段式:平衡常数K= ,可求出x=0.08mol/L(另一结果0.62mol/L舍去)。
【解析】A.达平衡时,容器I与容器II中的总压强之比为0.80:(1.0-0.08)=20∶23,A不正确;B.达平衡
时,容器I中 = ,容器II中 = >2,所以容器II中
比容器I中的大,B正确;C.若容器III与容器I的温度相同,容器III与容器I是等效平衡,
但容器III温度低,所以达平衡时,容器III比容器I中的正反应速率慢,C不正确;D.若容器III与容器I
的温度相同,达平衡时,容器I中CHOH转化率与容器III中CHCOOH转化率之和等于1,现在容器III
3 3
温度低,相当于达平衡后降低温度,平衡逆向移动,CHCOOH转化率降低,则容器I中CHOH转化率与
3 3
容器III中CHCOOH转化率之和小于1,D不正确;故选B。
3
知识点 07 化学平衡常数
1.三种平衡常数:a A(g)+b B(g) c C(g)+d D(g)
cc(C)×cd(D)
K=ca(A)×cb(B)
c
(1)浓度平衡常数:
①平衡量必须为平衡时的浓度
②等体反应:可以用平衡时的物质的量代替平衡时的浓度
③恒压条件下:先计算平衡体积,再算平衡常数
pc(C)×pd(D)
K =
pa(A)×pb(B)
p
(2)压强平衡常数:
①平衡量为平衡时的浓度、物质的量、体积等均可
n n
i i
n n
②分压P i =P 总 ×x i =P 总 × 总=(P 1 +P 2 +P 3 +…)× 总
③恒容条件下:先计算平衡总压,再算平衡常数或直接根据分压计算xc(C)×xd(D)
(3)物质的量分数平衡常数:K=xa(A)×xb(B)
x
①平衡量为平衡时的浓度、物质的量、体积等均可
n
i
n
②物质的量分数:x= 总
i
2.影响因素
(1)内因:化学反应的本身(某一具体反应)
{放热反应:K值减小
¿¿¿¿
(2)外因:反应体系的温度,升高温度
3.熵
(1)表达式
cc(C)×cd(D)
①浓度熵:Q=ca(A)×cb(B)
c
pc(C)×pd(D)
②压强熵:Q=
pa(A)×pb(B)
p
xc(C)×xd(D)
③物质的量分数熵:Q=xa(A)×xb(B)
x
(2)意义:Q越大,反应逆向进行的程度越大
(3)应用:判断反应是否达到平衡或反应进行的方向
①Q>K,反应逆向进行,v <v
正 逆
②Q=K,反应达到平衡状态,v =v
正 逆
③Q<K,反应正向进行,v >v
正 逆
4.平衡常数与书写方式的关系
(1)正逆反应平衡常数的关系是:K ·K =1
正 逆
(2)化学计量数变成n倍,平衡常数变为 n 次方 倍
(3)反应③=反应①+反应②,则:△H= △ H + H ,K =K ·K
3 1 2 3 1 2
K
△ 1
K
(4)反应③=反应①-反应②,则:△H= △ H - △ H ,K = 2
3 1 2 3
K
1a
1 1
K
1
(5)反应③=a×反应①-b ×反应②,则:△H
3
=a H
1
-b △ H
2
,K
3
= 2b
5.计算方法:三段式
△
(1)计算依据
①任何情况:气体物质的量变化比=气体浓度变化比=化学计量数比
②恒温恒容:气体压强变化比=物质的量变化比=化学计量数比
③恒温恒压:气体体积变化比=物质的量变化比=化学计量数比
(2)可以直接根据分物质的量、分压和分体积进行计算(3)同一容器内的多平衡体系,相同组分的平衡浓度相同
①a A(g) b B(g)+c C(g),c C(g) d D(g)+e E(g)
②计算K 、K 时,用到的c(C)相同
1 2
化学平衡常数是指某一具体反应的平衡常数,即确定系数的化学反应的平衡常数,方程式的计量数等倍扩
大或缩小,尽管是同一反应,平衡常数也会改变。
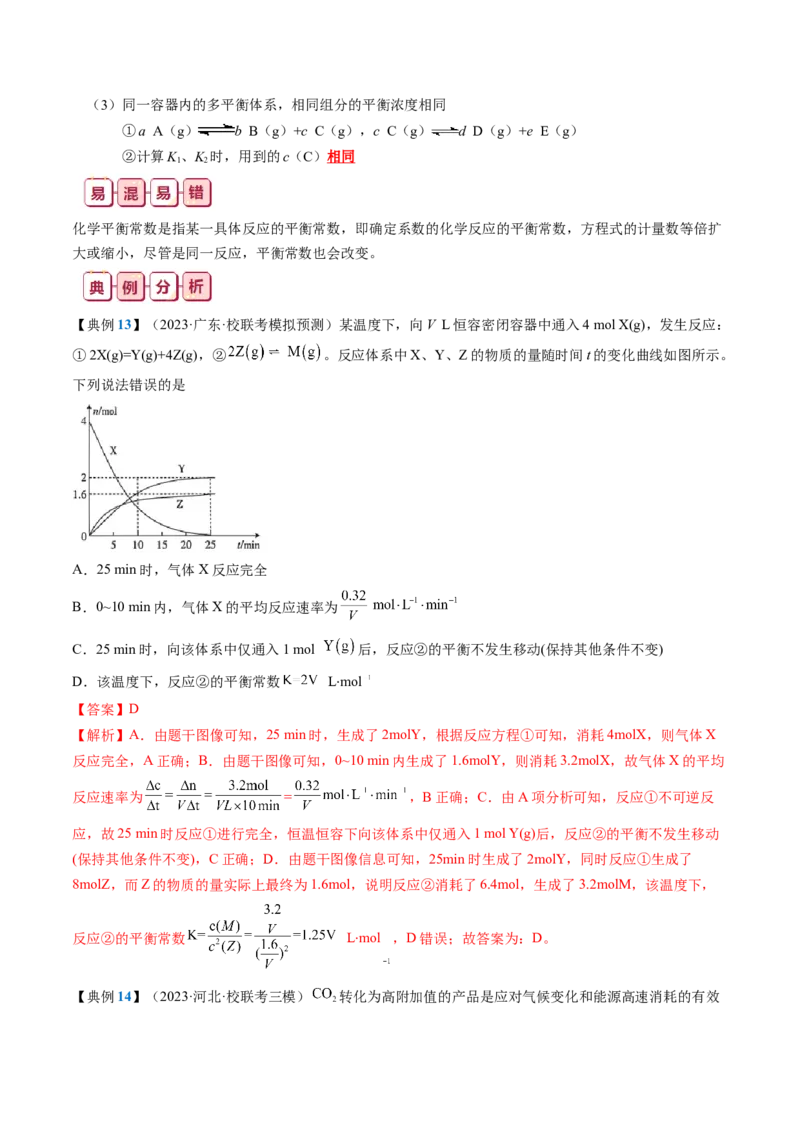
【典例13】(2023·广东·校联考模拟预测)某温度下,向V L恒容密闭容器中通入4 mol X(g),发生反应:
①2X(g)=Y(g)+4Z(g),② 。反应体系中X、Y、Z的物质的量随时间t的变化曲线如图所示。
下列说法错误的是
A.25 min时,气体X反应完全
B.0~10 min内,气体X的平均反应速率为
C.25 min时,向该体系中仅通入1 mol 后,反应②的平衡不发生移动(保持其他条件不变)
D.该温度下,反应②的平衡常数 Lmol
【答案】D
⋅
【解析】A.由题干图像可知,25 min时,生成了2molY,根据反应方程①可知,消耗4molX,则气体X
反应完全,A正确;B.由题干图像可知,0~10 min内生成了1.6molY,则消耗3.2molX,故气体X的平均
反应速率为 = ,B正确;C.由A项分析可知,反应①不可逆反
应,故25 min时反应①进行完全,恒温恒容下向该体系中仅通入1 mol Y(g)后,反应②的平衡不发生移动
(保持其他条件不变),C正确;D.由题干图像信息可知,25min时生成了2molY,同时反应①生成了
8molZ,而Z的物质的量实际上最终为1.6mol,说明反应②消耗了6.4mol,生成了3.2molM,该温度下,
反应②的平衡常数 Lmol ,D错误;故答案为:D。
⋅
【典例14】(2023·河北·校联考三模) 转化为高附加值的产品是应对气候变化和能源高速消耗的有效措施,我国科学家研究 加氢制备甲醇方面取得一定进展。在一定温度和压强下, 加氢制备甲醇的
过程中主要发生如下三个反应,反应I、II、III对应的平衡常数分别为 、 和 。
I.
II.
III.
回答下列问题:
(1) ; 、 和 三者之间的关系为 。
(2)为提高甲醇的平衡产率,可通过 (填“升高”或“降低”)温度, (填“增大”或
“减小”)压强来实现。
(3)在两种不同的条件下, 的平衡转化率和 的选择性如下表所示。条件 (填“1”或
“2”)中甲醇的产率更高。
条件 的平衡转化率/% 的选择性/%
1 27 68
2 21.3 97.7
(4)T℃时,将 的混合气体充入压强为 的恒压密闭容器中,在催化剂的作用下发
生如下两个反应:
①
②
反应达到平衡状态时, 和 的分压相等,甲醇的选择性是CO的2倍,则 的平衡转化率为
,反应②的 (列出计算式即可,分压=总压×物质的量分数)。
【答案】 (1)
(2)降低 增大
(3)2
(4)50%或0.5
【解析】(1)利用盖斯定律,反应Ⅲ=反应Ⅰ+反应Ⅱ,解出 。平衡常
数 ;
(2)反应Ⅰ和反应Ⅲ中,均在低温和增压条件下,有利于提高甲醇的平衡产率,降温,反应Ⅱ平衡逆移,
抑制副反应的发生,增大压强对反应Ⅱ无影响;(3)比较条件1和条件2时甲醇的产率,根据信息可知,受 的平衡转化率和甲醇的选择性共同影响,
将两者相乘,计算数值越大,甲醇产率越高,故答案为2;
(4) ,设 , 。依据题给信息 的选择性是CO的2
倍,设转化生成的 为 ,则生成的CO为 。列三段式:
依据反应达到平衡状态时, 和 的分压相等,则 , ,解得
,代入三段式:
, 的物质的量分数为 , 的
物质的量分数为 , 的物质的量分数为 , 的物质的量分数为 ,在
下进行反应,代入反应②的 表达式即可, ,同时,计算出
的平衡转化率为 ;知识点 08 速率常数和平衡常数的关系
1.基元反应:a A(g)+b B(g) c C(g)+d D(g)
2.速率方程
(1)抽象化速率方程:笼统的正逆反应速率
①v =k ·ca(A)·cb(B)、v =k ·cc(C)·cd(D)
正 正 逆 逆
②v =k ·pa(A)·pb(B)、v =k ·pc(C)·pd(D)
正 正 逆 逆
③v =k ·xa(A)·xb(B)、v =k ·xc(C)·xd(D)
正 正 逆 逆
(2)具体化速率方程:以具体物质表示的正逆反应速率
①v =k ·ca(A)·cb(B)、v =k ·cc(C)·cd(D)
A正 正 C逆 逆
②v =k ·pa(A)·pb(B)、v =k ·pc(C)·pd(D)
A正 正 C逆 逆
③v =k ·xa(A)·xb(B)、v =k ·xc(C)·xd(D)
A正 正 C逆 逆
3.速率常数和平衡常数的关系
k k k
正 正 正
k k k
(1)抽象化:平衡条件v
正
= v
逆
,① 逆=K
c
;② 逆=K
p
;③ 逆=K
x
v k k k
A正 a 正 a 正 a 正 a
(2)具体化:平衡条件 v C逆=c ,① k 逆=c K;② k 逆=c K ;③ k 逆=c K
c p x
(3)升温对k 、k 的影响
正 逆
①放热反应:K值减小;k 值增大,k 值增大,k 变化更大
正 逆 逆
②吸热反应:K值增大;k 值增大,k 值增大,k 变化更大
正 逆 正
v
正
v
4.计算某刻 逆
v k ×ya(A)×yb(B) ya(A)×yb(B)
正 正
(1)抽象化:
v
逆=
k
逆
×yc(C)×yd(D)
=K·
yc(C)×yd(D)
v
A正
k
正
×ya(A)×yb(B)
a
ya(A)×yb(B)
(2)具体化: v C逆= k 逆 ×yc(C)×yd(D) =c ×K× yc(C)×yd(D)
【典例15】(2023·湖南·校联考模拟预测)在一定温度下,以 为催化剂,氯苯和 在 溶液中发生反
应
反应①: (邻二氯苯)
反应②: (对二氯苯)
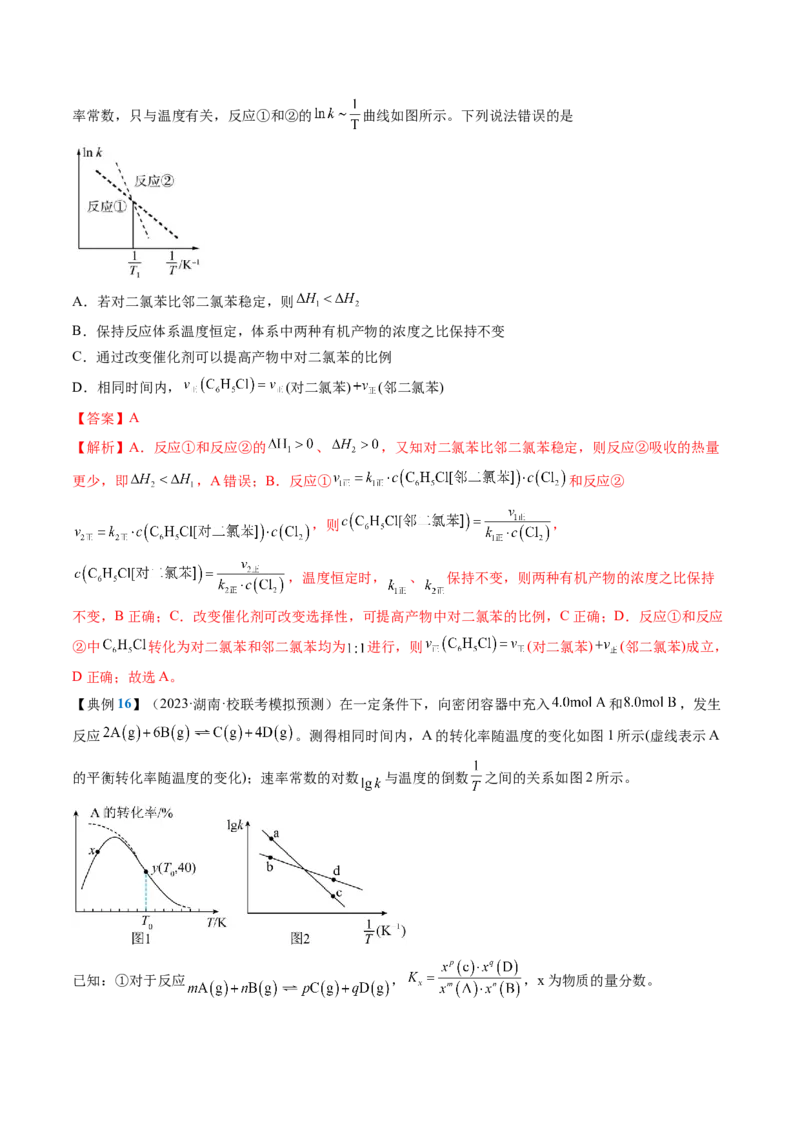
反应①和②存在的速率方程: 和 , 、 为速率常数,只与温度有关,反应①和②的 曲线如图所示。下列说法错误的是
A.若对二氯苯比邻二氯苯稳定,则
B.保持反应体系温度恒定,体系中两种有机产物的浓度之比保持不变
C.通过改变催化剂可以提高产物中对二氯苯的比例
D.相同时间内, (对二氯苯) (邻二氯苯)
【答案】A
【解析】A.反应①和反应②的 、 ,又知对二氯苯比邻二氯苯稳定,则反应②吸收的热量
更少,即 ,A错误;B.反应① 和反应②
,则 ,
,温度恒定时, 、 保持不变,则两种有机产物的浓度之比保持
不变,B正确;C.改变催化剂可改变选择性,可提高产物中对二氯苯的比例,C正确;D.反应①和反应
②中 转化为对二氯苯和邻二氯苯均为 进行,则 (对二氯苯) (邻二氯苯)成立,
D正确;故选A。
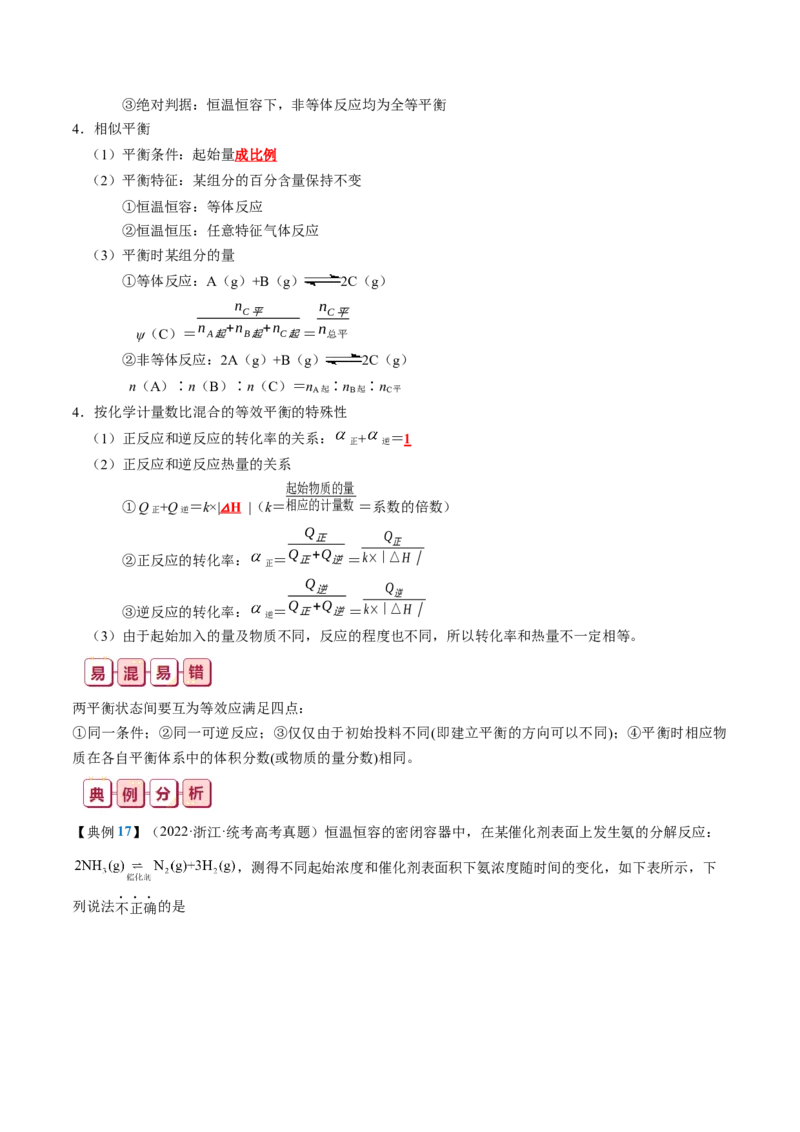
【典例16】(2023·湖南·校联考模拟预测)在一定条件下,向密闭容器中充入 和 ,发生
反应 。测得相同时间内,A的转化率随温度的变化如图1所示(虚线表示A
的平衡转化率随温度的变化);速率常数的对数 与温度的倒数 之间的关系如图2所示。
已知:①对于反应 , ,x为物质的量分数。②已知该反应的速率方程 , , 、 是速率常数。
下列说法错误的是
A.由上图判断,该反应的 B.曲线ac代表 ,bd代表
C. 时,该反应的平衡常数 D.升高温度时, 减小
【答案】A
【解析】A.由图可知,随温度升高,A的平衡转化率降低,该反应为放热反应, ,A错误;B.由
于 ,升高温度平衡逆向移动,说明 随温度变化比 随温度变化慢,图像bd的斜率小于曲线ac,
所以曲线ac代表 ,曲线bd代表 ,B正确;C. 时,A的平衡转化率为40%,A转化的物质的量为
% ,则
该反应的平衡常数 ,C正确;D. ,正反应放热,
升高温度平衡逆向移动,说明温度对逆反应速率影响大于正反应速率,升高温度时, 减小,D正确;
故选:A。
知识点 09 等效平衡
1.含义
2.解题方法:极端假设法
(1)按照系数将新加入的原料的量全部换算成起始时反应物或生成物的量
(2)将换算量与原配比量相比较(相等或成比例)
3.全等平衡
(1)平衡条件:起始量相等
(2)平衡特征
①直接判据:某组分的质量、物质的量不变
②间接判据:恒温恒容下,物质的量浓度不变③绝对判据:恒温恒容下,非等体反应均为全等平衡
4.相似平衡
(1)平衡条件:起始量成比例
(2)平衡特征:某组分的百分含量保持不变
①恒温恒容:等体反应
②恒温恒压:任意特征气体反应
(3)平衡时某组分的量
①等体反应:A(g)+B(g) 2C(g)
n n
C平 C平
n +n +n n
ψ(C)= A起 B起 C起= 总平
②非等体反应:2A(g)+B(g) 2C(g)
n(A)∶n(B)∶n(C)=n ∶n ∶n
A起 B起 C平
4.按化学计量数比混合的等效平衡的特殊性
(1)正反应和逆反应的转化率的关系: + =1
正 逆
(2)正反应和逆反应热量的关系
起始物质的量
①Q +Q =k×| H |(k=相应的计量数=系数的倍数)
正 逆
Q
△ 正 Q 正
②正反应的转化率: 正 = Q 正 +Q 逆=k×|△H|
Q Q
逆 逆
③逆反应的转化率: 逆 = Q 正 +Q 逆=k×|△H|
(3)由于起始加入的量及物质不同,反应的程度也不同,所以转化率和热量不一定相等。
两平衡状态间要互为等效应满足四点:
①同一条件;②同一可逆反应;③仅仅由于初始投料不同(即建立平衡的方向可以不同);④平衡时相应物
质在各自平衡体系中的体积分数(或物质的量分数)相同。
【典例17】(2022·浙江·统考高考真题)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
【答案】C
【解析】A.实验①中,0~20min,氨气浓度变化量为2.40 10-3mol/L-2.00 10-3mol/L=4.00 10-4mol/L,
v(NH )= =2.00 10-5mol/(L·min),反应速率之比等于化学计量数之比,v(N )= v(NH )=1.00
3 2 3
10-5mol/(L·min),A正确;B.催化剂表面积大小只影响反应速率,不影响平衡,实验③中氨气初始浓度
与实验①中一样,实验③达到平衡时氨气浓度为4.00 10-4mol/L,则实验①达平衡时氨气浓度也为4.00
10-4mol/L,而恒温恒容条件下,实验②相对于实验①为减小压强,平衡正向移动,氨气浓度减小,因此实
验②60min时处于平衡状态,根据等效平衡可以判断x<0.2,即x≠0.4,B正确;C.实验①、实验②中
0~20min、20min~40min氨气浓度变化量都是4.00 10-4mol/L,实验②中60min时反应达到平衡状态,实验
①和实验②催化剂表面积相同,实验①中氨气初始浓度是实验②中氨气初始浓度的两倍,实验①60min时
反应未达到平衡状态,相同条件下,增加氨气浓度,反应速率并没有增大,C错误;D.对比实验①和实
验③,氨气浓度相同,实验③中催化剂表面积是实验①中催化剂表面积的2倍,实验③先达到平衡状态,
实验③的反应速率大,说明相同条件下,增加催化剂的表面积,反应速率增大,D正确;答案选C。
【典例18】一定条件下存在反应: 。图1、图2表示起始时容器甲、丙
体积都是V,容器乙、丁体积都是 ;向甲、丙内都充入2amolSO 和amolO 并保持恒温;向乙、丁内都
2 2
充入amolSO 和0.5amolO 并保持绝热(即与外界无热量交换),在一定温度时开始反应。
2 2
下列说法正确的是
A.图1达平衡时, :甲=乙
B.图1达平衡时,平衡常数K:甲<乙
C.图2达平衡时,所需时间:丙<丁D.图2达平衡时, 的体积分数:丙>丁
【分析】恒温恒压条件下,甲和乙为等效平衡,容器乙为绝热恒压容器,由二氧化硫与氧气的反应为放热
反应可知,保持绝热的乙容器相对于甲容器为升高温度,温度升高,平衡向逆反应方向移动,则乙容器中
二氧化硫浓度大于甲容器、反应的化学平衡常数小于甲容器;恒温恒容条件下,丙和丁为等效平衡,容器
丁为绝热恒容容器,保持绝热的丁容器相对于丙容器为升高温度,升高温度,化学反应速率加快,平衡向
逆反应方向移动,则丁容器的反应速率快于丙容器、三氧化硫的体积分数小于丙容器。
【解析】A.由分析可知,乙容器中二氧化硫浓度大于甲容器,故A错误;B.由分析可知,乙容器中反
应的化学平衡常数小于甲容器,故B错误;C.由分析可知,丁容器的反应速率快于丙容器,故C错误;
D.由分析可知,丁容器的三氧化硫的体积分数小于丙容器故D正确;故选D。
【答案】D
知识点 10 化学反应的方向
1.焓判据:放热反应有利于反应自发进行
2.熵判据:熵增反应有利于反应自发进行
(1)物质的混乱度:体系的混乱度越大,熵值越大
(2)物质的聚集状态:同一物质:S(g)>S(l)>S(s)
(3)物质的复杂程度:一般组成物质的原子种类相同时,分子中的原子数目越多,其混乱度越大,熵
值越大
(4)计算式:△S=S(生成物)-S(反应物)
变化过程 熵变 反应类型
增体反应 S>0 熵增反应
减体反应 S<0 熵减反应
△
盐的溶解 S>0 熵增反应
△
电离过程 S>0 熵增反应
△
3.复合判据: Δ H - T Δ S < 0 ,反应正向自发进行
△
(1)适用条件:恒温恒压
(2)局限性:只能判断反应发生的可能性,不能判断反应是否实际发生
4.温度对反应方向的影响
(1)△H<0,△S>0:在任何温度时都能够自发进行
(2)△H>0,△S<0:在任何温度时都不能自发进行
(3)△H<0,△S<0:低温自发
(4)△H>0,△S>0:高温自发5.反应自发进行的最低或最高温度的计算
(1)计算依据:△H-T S≤0
△H
△
①若△S>0,则T≥△S ,为最低温度
△H
②若△S<0,则T≤△S ,为最高温度
(2)注意单位的换算
①△S的单位为: J · mol - 1 · K - 1
②△H的单位为: kJ · mol - 1
③T的单位为:K
在用判据ΔH-TΔS判断时要注意ΔH与ΔS的单位的差别,需要转换。
(1)不能片面地用焓判据、熵判据孤立判断。
(2)不能忽视温度在大多数化学反应方向判断中的作用。
(3)不能错误认为“自发反应”不需要任何条件。
(4)不能忽视ΔH、T、ΔS单位的协调一致。
【典例19】25℃、1.01×105Pa时,反应2NO(g)=4NO (g)+O(g) ΔH=+109.8kJ·mol-1,该反应能自发进行的
2 5 2 2
原因是
A.该反应是吸热反应
B.该反应是放热反应
C.该反应是熵减小的反应
D.该反应的熵增大效应大于能量效应
【答案】D
【详解】该反应是吸热反应,能够自发进行是由于该反应为熵增大的反应,并且熵增效应大于能量效应,
故选D。
【典例20】(2023·江苏南京·统考二模)反应
可实现 的资源化,下列说法正确的是A.上述反应在任何温度下均可自发进行
B.上述反应每消耗1mol 同时形成7mol σ键
C.上述反应平衡常数
D.催化剂可以降低上述反应的焓变,提高化学反应速率
【答案】B
【解析】A.△H-T S<0时反应自发进行,该反应△H<0,△S<0,反应在较低温度下可自发进行,A错误;
B.根据 △ ,反应每消耗1mol ,生成
0.5molCHOCH 、1.5molHO,形成7mol σ键,B正确;C.上述反应平衡常数 ,
3 3 2
C错误;D.催化剂可以加快反应速率,但是不改变反应的焓变,D错误;故选B。
知识点 11 工业生产适宜条件的选择
1.选择原则:反应速率快,产品含量高
(1)温度
①所选温度兼顾反应速率快,产品含量高
②尽可能选择催化剂的最大温度
(2)压强
①所选压强对反应物转化率的影响变化幅度大
②压强不能无限大,防止增大设备成本和动力成本
(3)催化剂
①选用催化效率高的催化剂
②催化剂对反应有选择性,同一反应物选用不同的催化剂,产物可能不同
A+B C A+B D
③某些物质能够使催化剂中毒,失去活性
(4)浓度:原料尽可能循环利用
①适当增大廉价物质的浓度,提高难获得原料的转化率。
②必要时可以采用循环反应,以增大原料利用率。
(5)反应热的综合利用:一般采用热交换器
(6)反应容器的选择:恒压容器有利于提高反应物的转化率
2.工业合成氨生产条件的选择
(1)合成氨生产的要求。①反应要有较快的反应速率。
②要最大限度地提高平衡混合物中NH 的含量。
3
(2)合成氨生产条件的选择依据。
①化学反应速率和化学平衡原理的有关知识。
②合成氨生产中的动力、材料、设备、生产成本等因素。
(3)选择合成氨生产条件的理论分析。
外界因素 理论分析
压强越大越有利于合成氨,但在实际生产中,应根据反应设备可使用的
压强 钢材质量及综合指标来选择压强,大致分为低压、中压和高压三种类
型,一般采用高压
温度越高,反应速率越大,但不利于氨的合成,在实际生产中一般控制
温度
反应温度在700 K 左右(且在此温度时催化剂的活性最大)
催化剂 使用催化剂可以大幅度提高反应速率,合成氨生产一般选择铁作催化剂
合成氨生产通常采用N 和H 物质的量之比为 1 ∶ 2.8 的投料比,并且及
2 2
浓度
时将氨气从反应混合物中分离出去
其他 为提高平衡转化率,工业合成采用的原料循环利用
【典例21】焦炉煤气(主要成分:CH、CO、H、CO)在炭催化下,使CH 与CO 重整生成H 和CO。其
4 2 2 4 2 2
主要反应为
反应I:
反应II:
反应III:
反应IV:
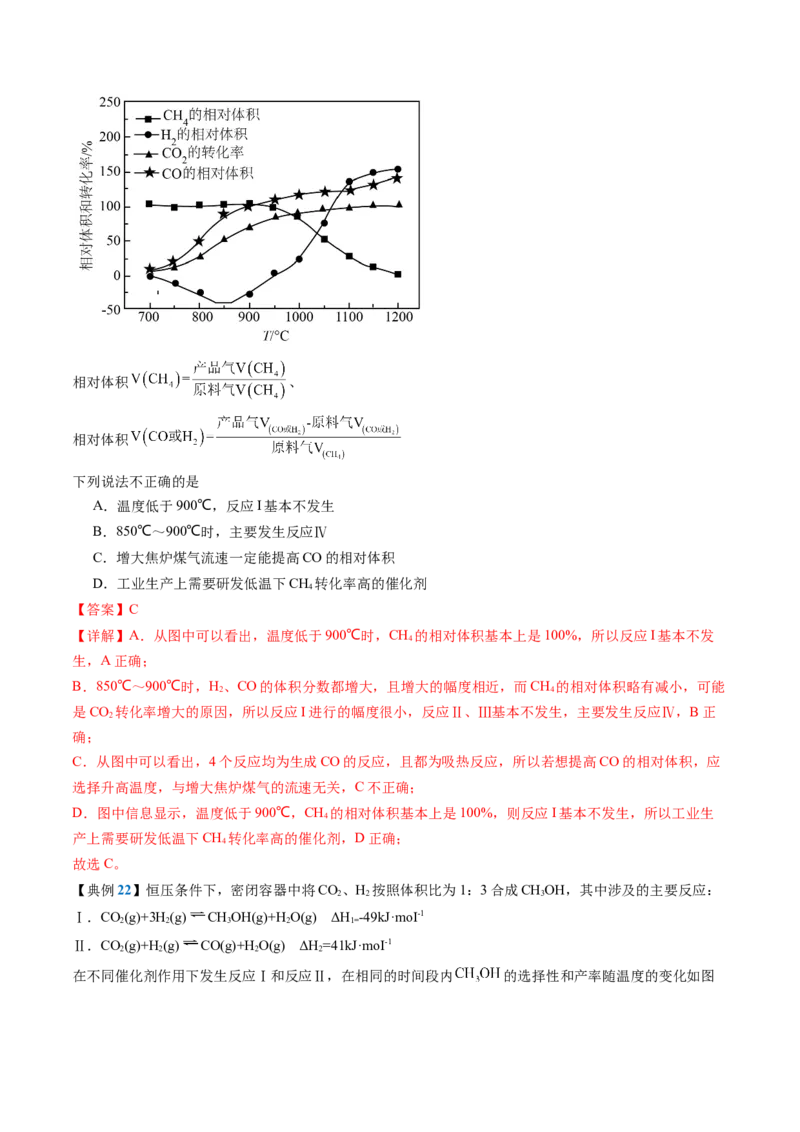
在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH、CO、H 的相对体积和CO 的转化
4 2 2
率随温度变化的曲线如图所示。相对体积 、
相对体积
下列说法不正确的是
A.温度低于900℃,反应I基本不发生
B.850℃~900℃时,主要发生反应Ⅳ
C.增大焦炉煤气流速一定能提高CO的相对体积
D.工业生产上需要研发低温下CH 转化率高的催化剂
4
【答案】C
【详解】A.从图中可以看出,温度低于900℃时,CH 的相对体积基本上是100%,所以反应I基本不发
4
生,A正确;
B.850℃~900℃时,H、CO的体积分数都增大,且增大的幅度相近,而CH 的相对体积略有减小,可能
2 4
是CO 转化率增大的原因,所以反应I进行的幅度很小,反应Ⅱ、Ⅲ基本不发生,主要发生反应Ⅳ,B正
2
确;
C.从图中可以看出,4个反应均为生成CO的反应,且都为吸热反应,所以若想提高CO的相对体积,应
选择升高温度,与增大焦炉煤气的流速无关,C不正确;
D.图中信息显示,温度低于900℃,CH 的相对体积基本上是100%,则反应I基本不发生,所以工业生
4
产上需要研发低温下CH 转化率高的催化剂,D正确;
4
故选C。
【典例22】恒压条件下,密闭容器中将CO、H 按照体积比为1:3合成CHOH,其中涉及的主要反应:
2 2 3
Ⅰ.CO(g)+3H(g) CHOH(g)+H O(g) ΔH -49kJ·moI-1
2 2 3 2 1=
Ⅱ.CO(g)+H(g) CO(g)+HO(g) ΔH=41kJ·moI-1
2 2 2 2
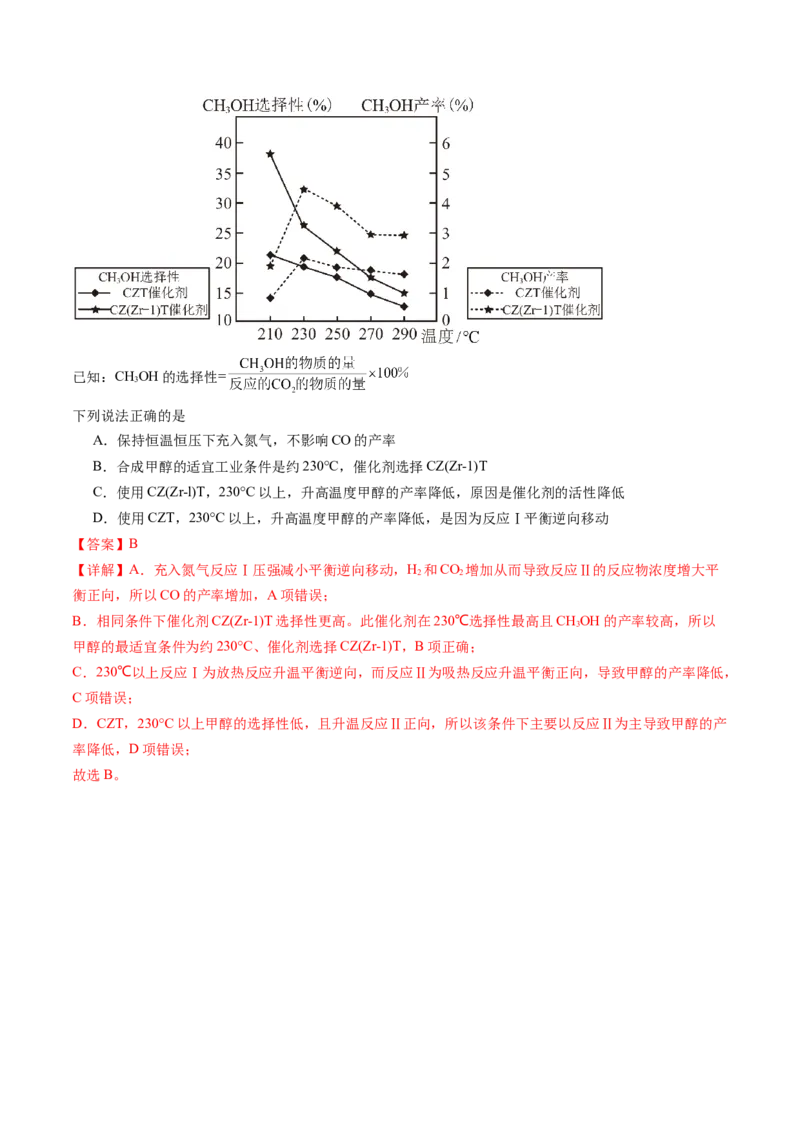
在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内 的选择性和产率随温度的变化如图已知:CHOH的选择性=
3
下列说法正确的是
A.保持恒温恒压下充入氮气,不影响CO的产率
B.合成甲醇的适宜工业条件是约230°C,催化剂选择CZ(Zr-1)T
C.使用CZ(Zr-l)T,230°C以上,升高温度甲醇的产率降低,原因是催化剂的活性降低
D.使用CZT,230°C以上,升高温度甲醇的产率降低,是因为反应Ⅰ平衡逆向移动
【答案】B
【详解】A.充入氮气反应Ⅰ压强减小平衡逆向移动,H 和CO 增加从而导致反应Ⅱ的反应物浓度增大平
2 2
衡正向,所以CO的产率增加,A项错误;
B.相同条件下催化剂CZ(Zr-1)T选择性更高。此催化剂在230℃选择性最高且CHOH的产率较高,所以
3
甲醇的最适宜条件为约230°C、催化剂选择CZ(Zr-1)T,B项正确;
C.230℃以上反应Ⅰ为放热反应升温平衡逆向,而反应Ⅱ为吸热反应升温平衡正向,导致甲醇的产率降低,
C项错误;
D.CZT,230°C以上甲醇的选择性低,且升温反应Ⅱ正向,所以该条件下主要以反应Ⅱ为主导致甲醇的产
率降低,D项错误;
故选B。