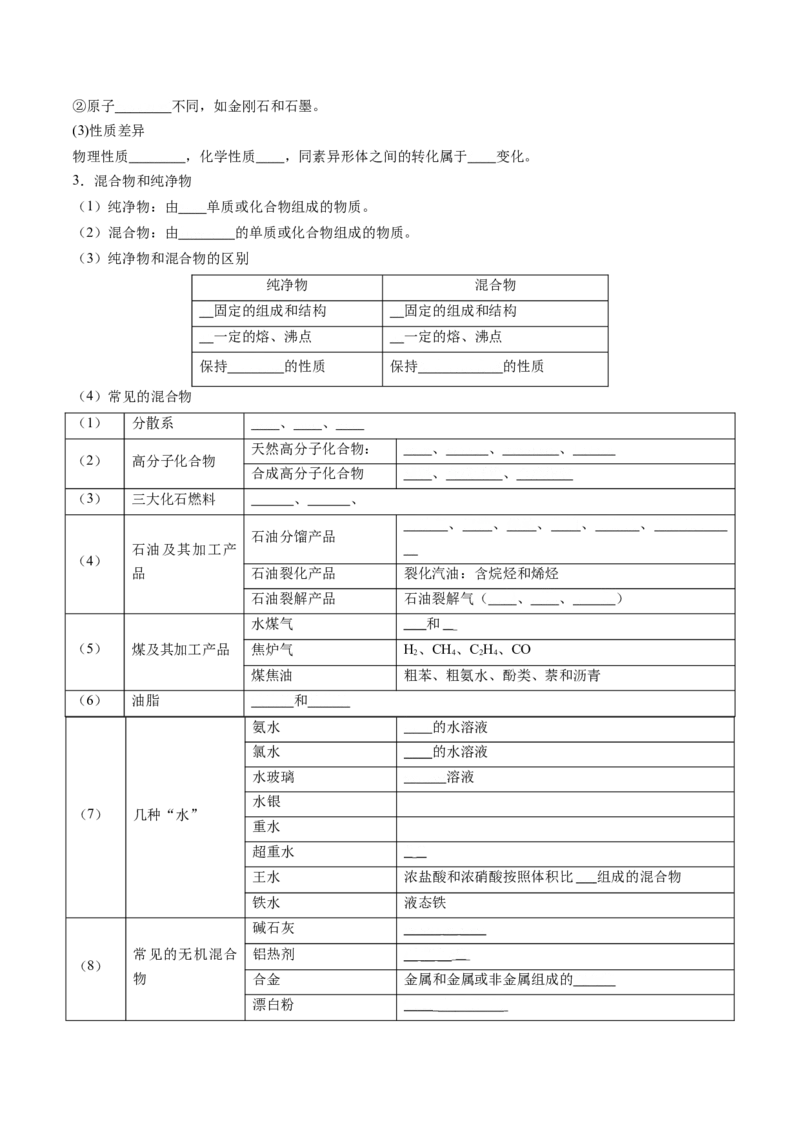文档内容
第 01 讲 物质的分类及转化
目录
01
2
02 知识导图·思维引航.........................................................................................................................3
03 考点突破·考法探究.........................................................................................................................5
考点一 物质的组成与分类.............................................................................................................5
知识点1 物质的组成....................................................................................................................5
知识点2 物质的分类....................................................................................................................7
考向1 考查物质的组成的判断..................................................................................................10
考向2 根据标准对物质进行分类..............................................................................................10
考点二 物质的性质与变化...........................................................................................................11
知识点1 物理性质和化学性质..................................................................................................11
知识点2 物理变化和化学变化..................................................................................................11
考向1 传统文化中物质的性质和变化......................................................................................16
考向2 物质变化的性质及其应用..............................................................................................17
考向3 化学反应类型的判断......................................................................................................18
考点三 分散系与胶体...................................................................................................................19
知识点1 分散系..........................................................................................................................19
知识点2 胶体..............................................................................................................................20
考向1 分散系及其分类..............................................................................................................22
考向2 胶体的组成、性质、制备..............................................................................................23
考向3 胶体性质的应用..............................................................................................................24
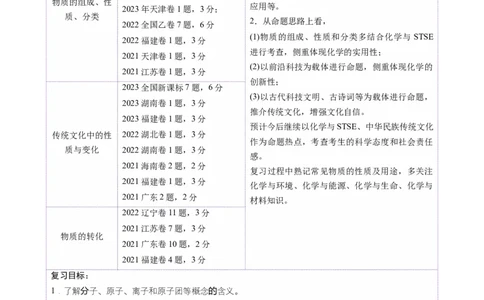
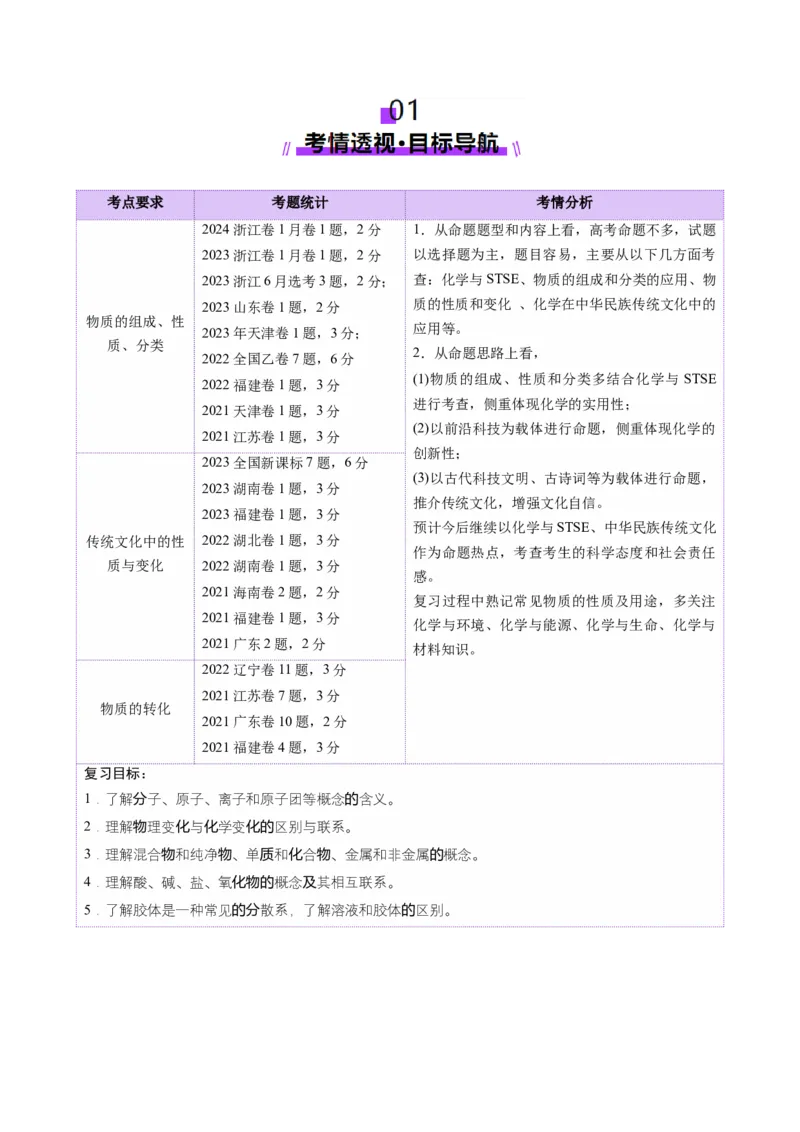
0425考点要求 考题统计 考情分析
2024浙江卷1月卷1题,2分 1.从命题题型和内容上看,高考命题不多,试题
2023浙江卷1月卷1题,2分 以选择题为主,题目容易,主要从以下几方面考
2023浙江6月选考3题,2分; 查:化学与STSE、物质的组成和分类的应用、物
2023山东卷1题,2分 质的性质和变化 、化学在中华民族传统文化中的
物质的组成、性
应用等。
2023年天津卷1题,3分;
质、分类
2.从命题思路上看,
2022全国乙卷7题,6分
(1)物质的组成、性质和分类多结合化学与 STSE
2022福建卷1题,3分
进行考查,侧重体现化学的实用性;
2021天津卷1题,3分
(2)以前沿科技为载体进行命题,侧重体现化学的
2021江苏卷1题,3分
创新性;
2023全国新课标7题,6分
(3)以古代科技文明、古诗词等为载体进行命题,
2023湖南卷1题,3分
推介传统文化,增强文化自信。
2023福建卷1题,3分
预计今后继续以化学与STSE、中华民族传统文化
传统文化中的性 2022湖北卷1题,3分
作为命题热点,考查考生的科学态度和社会责任
质与变化 2022湖南卷1题,3分
感。
2021海南卷2题,2分
复习过程中熟记常见物质的性质及用途,多关注
2021福建卷1题,3分
化学与环境、化学与能源、化学与生命、化学与
2021广东2题,2分
材料知识。
2022辽宁卷11题,3分
2021江苏卷7题,3分
物质的转化
2021广东卷10题,2分
2021福建卷4题,3分
复习目标:
1.了解分子、原子、离子和原子团等概念的含义。
2.理解物理变化与化学变化的区别与联系。
3.理解混合物和纯净物、单质和化合物、金属和非金属的概念。
4.理解酸、碱、盐、氧化物的概念及其相互联系。
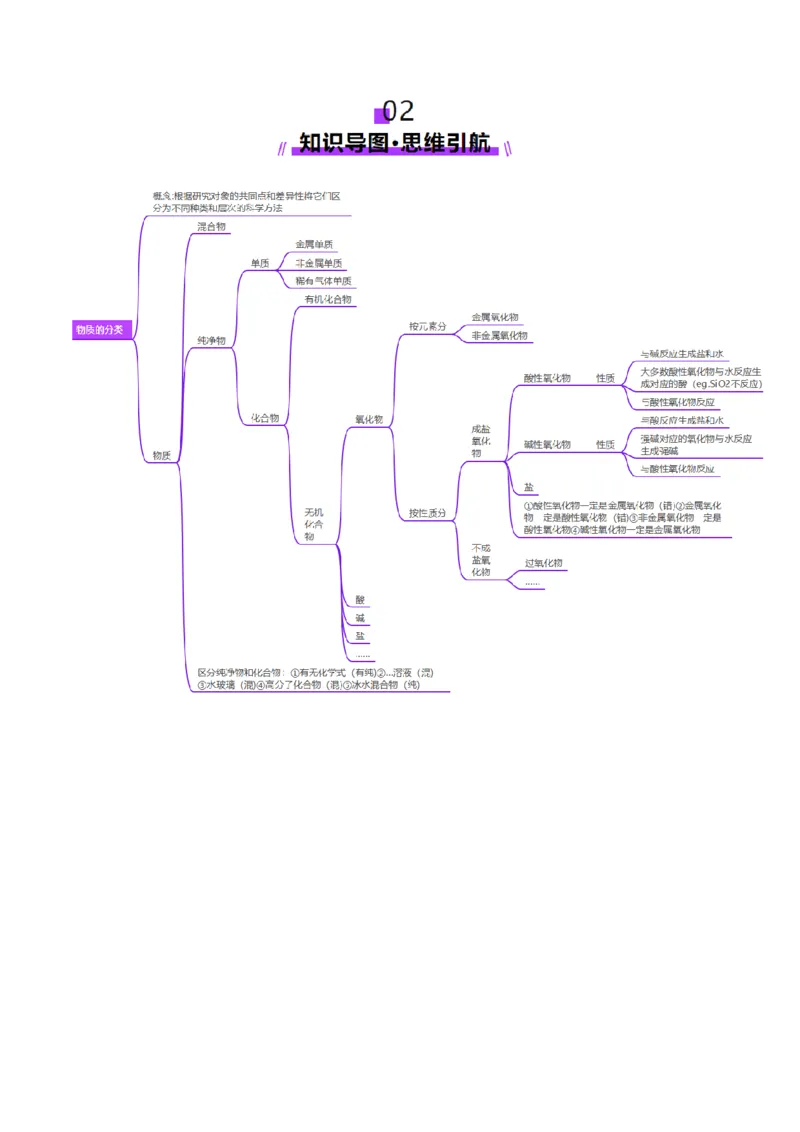
5.了解胶体是一种常见的分散系,了解溶液和胶体的区别。考点一 物质的组成与分类
知识点1 物质的组成
1.元素、物质及微粒间的关系
(1)宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
①分子:保持物质化学性质的最小微粒。
②原子:化学变化中的最小微粒。
③离子:带电荷的原子或原子团。
④原子团:在许多化学反应里,作为一个整体参加反应,如同一个原子一样的原子集团。
【特别提醒】“基”与“官能团”、“原子团”的区别
①基是指带有单电子的原子团。如-CH、-CH-(亚甲基)、-CHCH、-OH。
3 2 2 3
②官能团是指决定有机物化学性质的原子或原子团。如-OH、-CHO、-COOH、-X(卤素原子)等。
③“基”和“官能团”呈电中性,而CO、NO、SO、NH等原子团可带负电荷或正电荷。
(2)元素:具有相同核电荷数的一类原子的总称。
元素在自然界的存在形式有游离态和化合态。
①游离态:元素以单质形式存在的状态。
②化合态:元素以化合物形式存在的状态。
(3)元素与物质的关系
元素――→
(4)原子与物质的关系
2.同素异形体
(1)概念:同种元素形成的不同单质叫同素异形体。
(2)形成方式
①原子个数不同,如O 和O;
2 3②原子排列方式不同,如金刚石和石墨。
(3)性质差异
物理性质差别较大,化学性质相似,同素异形体之间的转化属于化学变化。
3.混合物和纯净物
(1)纯净物:由同种单质或化合物组成的物质。
(2)混合物:由几种不同的单质或化合物组成的物质。
(3)纯净物和混合物的区别
纯净物 混合物
有固定的组成和结构 无固定的组成和结构
有一定的熔、沸点 无一定的熔、沸点
保持一种物质的性质 保持原有物质各自的性质
(4)常见的混合物
(1) 分散系 溶液、浊液、胶体
天然高分子化合物: 淀粉、纤维素、天然橡胶、蛋白质
(2) 高分子化合物
合成高分子化合物 塑料、合成纤维、合成橡胶
(3) 三大化石燃料 、 、
石油气、汽油、煤油、柴油、石蜡油、润滑油、沥
石油分馏产品
石油及其加工产 青
(4)
品 石油裂化产品 裂化汽油:含烷烃和烯烃
石油裂解产品 石油裂解气(乙烯、丙烯、丁二烯)
水煤气 CO 和H
2
(5) 煤及其加工产品 焦炉气 H、CH、C H、CO
2 4 2 4
煤焦油 粗苯、粗氨水、酚类、萘和沥青
(6) 油脂 动物油和植物油
氨水 氨气的水溶液
氯水 氯气的水溶液
水玻璃 硅酸钠溶液
水银
(7) 几种“水”
重水
超重水 TO
2
王水 浓盐酸和浓硝酸按照体积比1:3 组成的混合物
铁水 液态铁
碱石灰 NaOH 和 CaO
常见的无机混合 铝热剂 Al 和 Fe O
2 3
(8)
物 合金 金属和金属或非金属组成的混合物
漂白粉 CaCl 和 Ca(ClO )
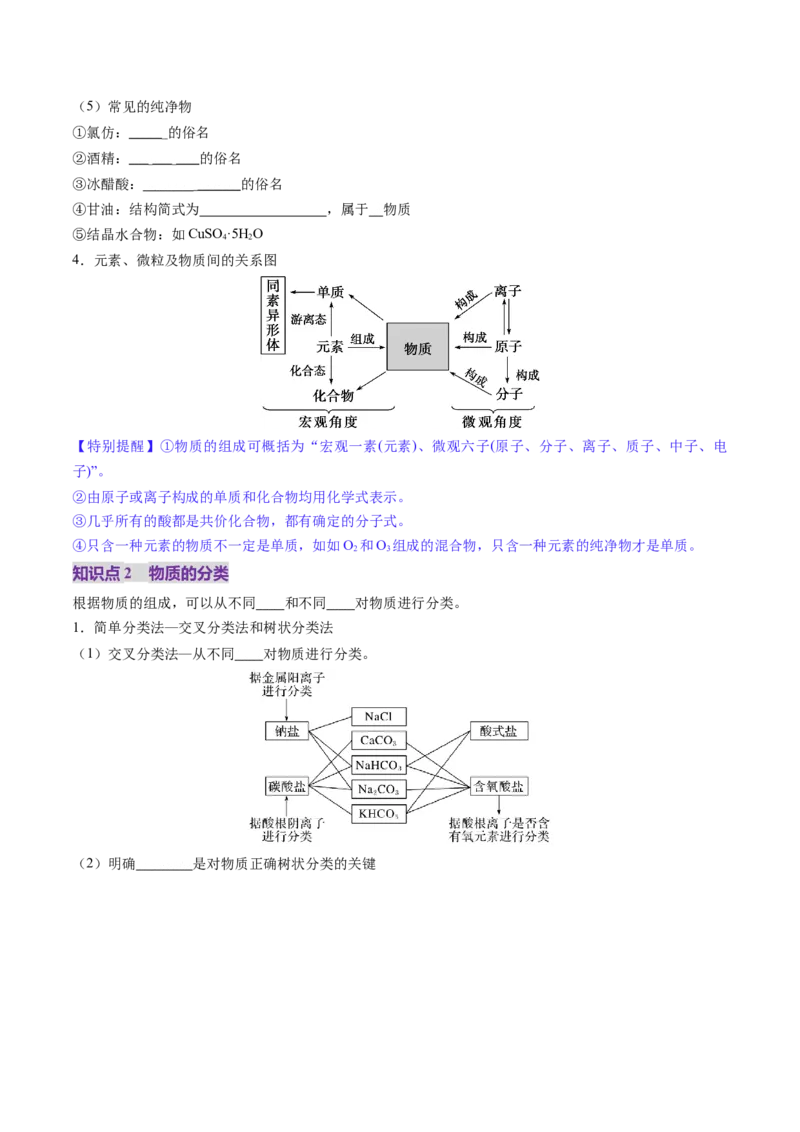
2 2(5)常见的纯净物
①氯仿:CHCl 的俗名
3
②酒精:CHCHOH 的俗名
3 2
③冰醋酸: 固体 CH COOH 的俗名
3
④甘油:结构简式为 ,属于醇物质
⑤结晶水合物:如CuSO ·5H O
4 2
4.元素、微粒及物质间的关系图
【特别提醒】①物质的组成可概括为“宏观一素(元素)、微观六子(原子、分子、离子、质子、中子、电
子)”。
②由原子或离子构成的单质和化合物均用化学式表示。
③几乎所有的酸都是共价化合物,都有确定的分子式。
④只含一种元素的物质不一定是单质,如如O 和O 组成的混合物,只含一种元素的纯净物才是单质。
2 3
知识点2 物质的分类
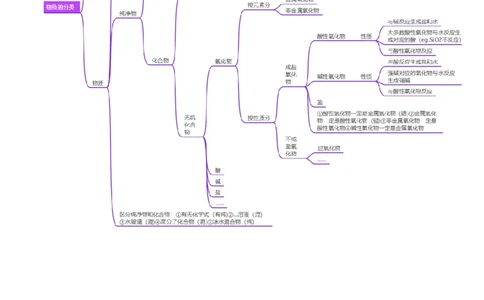
根据物质的组成,可以从不同层次和不同角度对物质进行分类。
1.简单分类法—交叉分类法和树状分类法
(1)交叉分类法—从不同角度对物质进行分类。
(2)明确分类标准是对物质正确树状分类的关键(3)树状分类法在无机化合物分类中的应用
按不同层次对物质进行逐级分类,各层之间属于包含关系。
【特别提醒】1)熟悉常见的混合物
(1)气体混合物:空气、水煤气(CO和H)、爆鸣气(H 和O)、天然气(主要成分是CH)、焦炉气(主要成分
2 2 2 4
是H 和CH)、高炉煤气、石油气、裂解气。
2 4
(2)液体混合物:氨水、氯水、王水、天然水、硬水、软水、水玻璃、福尔马林、浓硫酸、盐酸、汽油、植
物油、胶体。
(3)固体混合物:大理石、碱石灰、漂白粉、高分子化合物、玻璃、水泥、合金、铝热剂。
2)正确理解几个“一定”“不一定”
(1)酸性氧化物和碱性氧化物
a.碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物(如MnO 为酸性氧化物、Al O 为两
2 7 2 3
性氧化物、NaO 为过氧化物)。
2 2b.酸性氧化物不一定是非金属氧化物(如MnO);非金属氧化物也不一定是酸性氧化物(如CO、NO)。
2 7
c.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱(如SiO、Fe O)。
2 2 3
d.酸性氧化物都是对应酸的酸酐,但酸酐不一定都是酸性氧化物,如乙酸酐[(CH CO) O]。
3 2
e.溶于水生成酸的氧化物不一定是酸性氧化物,如 NO ;溶于水生成碱的氧化物不一定是碱性氧化物,如
2
NaO。
2 2
(2)共价化合物和离子化合物
a.由非金属元素组成的化合物不一定是共价化合物,如铵盐。
b.由金属元素和非金属元素组成的化合物不一定是离子化合物,如AlCl 。
3
(3)纯净物和混合物
a.只含一种元素的物质不一定是纯净物,也可能是混合物,如O 和O,金刚石和石墨,正交硫和单斜
2 3
硫。
b.结晶水合物属于纯净物,如CuSO ·5H O、KAl(SO )·12H O等物质。
4 2 4 2 2
c.同位素形成的单质或化合物是纯净物,如H 与D、HO与DO。
2 2 2 2
d.分子式为C H 的物质存在多种同分异构体,可能是纯净物也可能是混合物。
5 10
3)确定某酸是几元酸,不能依据分子中氢原子的个数,如CHCOOH不是四元酸,而是一元酸。
3
4)对氧化物的深刻认识
(1)金属氧化物不一定是碱性氧化物,如MnO 是酸性氧化物,Al O 是两性氧化物。
2 7 2 3
(2)非金属氧化物不一定是酸性氧化物,如NO、CO是不成盐氧化物。
(3)酸性氧化物、碱性氧化物不一定能与水反应生成相应的酸或碱,如SiO 、Fe O 都不溶于水,也不与水
2 2 3
反应。
(4)与碱反应生成盐和水的氧化物不一定是酸性氧化物,如 2NO +2NaOH===NaNO +NaNO +HO,NO
2 3 2 2 2
不是酸性氧化物。
考向1 考查物质的组成的判断
例1 (2024·重庆荣昌·模拟预测)齐鲁文化底蕴深厚,下列物质的主要化学成分不能与其他三种归为一
类的是
A.崂山绿茶 B.鲁锦 C.曲阜楷木雕 D.莱芜锡雕
【反思归纳】(1)由相同元素组成的物质不一定是纯净物。如由O、O 组成的气体就是混合物。
2 3
(2)一种分子式不只表示一种物质。如C H 的结构有正丁烷和异丁烷。
4 10
(3) NO 不属于酸性氧化物。
2
(4)能与酸反应生成盐和水的氧化物就是碱性氧化物,如NaO 不属于碱性氧化物。
2 2
(5)酸性氧化物不一定是非金属氧化物,如MnO 属于酸性氧化物。
2 7
【变式训练1】(2024·河南·模拟预测)2023年是共建“一带一路”倡议提出10周年。下列古代“丝绸之路”有关商品的主要成分属于无机物的是
A.玉器 B.丝绸 C.香料 D.皮草
【变式训练2】(2024·湖南·二模)下列属于酸性氧化物的是
A. B. C. D.
【变式训练3】(2024·贵州·模拟预测)“挖掘文物价值,讲好中国故事”。下列有关文物的叙述正确的是
A.“良渚古城遗址”出土的良渚陶器制作原料是石灰石、纯碱和二氧化硅
B.“贾湖骨笛”制作材料是鹤类尺骨,它的成分 属于有机高分子材料
C.台北故宫的“东坡肉形石”是一块天然玛瑙石,其矿物主要化学成分为
D.“马家窑”出土的铜刀表面的绿色物质,其主要成分是
考向2 根据标准对物质进行分类
例2 (2024·安徽滁州·一模)分类法是认识物质世界、学习化学的重要方法之一。下列分类中正确的是
A.金属材料:生铁、不锈钢、玻璃钢 B.可加热的容器:试管、烧杯、集气瓶
C.混合物:空气、石油、冰水共存物 D.可回收物:旧报纸、旧纸箱、易拉罐
【思维建模】从组成、熔沸点、性质角度区分纯净物和混合物
①纯净物:有固定的组成和结构;有固定的熔沸点;保持一种物质的性质
②混合物:无固定的组成和结构;无固定的熔沸点;保持原有物质各自的性质。
【变式训练1】(2024·贵州·三模)下列关于物质分类的说法正确的是
A.云、雾、紫水晶都属于胶体 B.硫酸钡、乙酸都属于强电解质
C. 、 、 均为酸性氧化物 D.液氨、液氯、干冰均为化合物
【变式训练2】(2024·浙江台州·二模)一定条件下 和 发生反应,生成的化合物属于
A.非电解质 B.氧化物 C.有机物 D.盐
考点二 物质的性质与变化
知识点1 物理性质和化学性质
物理性质 化学性质
概念 物质不需要发生化学变化就表现出来的性 物质在化学变化中表现出来的性质
质
实质 物质的分子组成和结构没有发生改变时呈 物质的分子组成和结构发生改变时呈现的
现的性质 性质
性质表现 颜色、状态、气味、密度溶解性、熔点、 氧化性、还原性、酸碱性、稳定性、可燃
沸点、硬度、导电性、导热性、光泽、延 性等
展性、挥发性等知识点2 物理变化和化学变化
1.物理变化与化学变化的比较
比较 物理变化 化学变化
变化
特征 没有新物质生成 有新物质生成
实质 构成物质的粒子间隔发生变化 物质的组成、结构发生变化,分子中原子重新组合
关系 化学变化中一定伴随着物理变化发生,但物理变化过程中不一定有化学变化
【特别提醒】①化学变化中常伴有发光、放热现象,但有发光、放热现象的变化不一定属于化学变化,如
金属受热发光。
②化学变化中一定存在化学键的断裂和形成,但存在化学键断裂的变化不一定是化学变化,如HCl溶于
水、熔融NaCl电离等。
③原子的裂变、聚变虽有新物质生成,但它不属于中学化学意义上的化学变化。
④物理变化与化学变化的判断方法
宏观 有新物质生成的是化学变化,反之应是物理变化
微观 有旧化学键断裂,同时有新化学键生成的是化学变化
二者关系 化学变化中一般伴随着物理变化,但物理变化过程中一定没有化学变化
2.常见的物理变化和化学变化
(1)化学变化:同素异形体之间的相互转化、CuSO ·5H O的脱水、蛋白质变性、电解质溶液导电、浓硫酸
4 2
脱水、煤的气化和液化。
(2)物理变化:金属导电、盐析、活性炭吸附、渗析。
(3)爆炸有的是化学变化引起的,有的是物理变化引起的。
3.化学反应的分类
化学反应
4.单质、氧化物、酸、碱和盐的转化关系
5.从电离角度认识酸、碱、盐电离出的阳离子全部是H+的化合物是酸,分为强酸与弱酸、含氧酸与无氧酸等;但
酸
能电离出H+的物质不一定是酸,如NaHSO 是一种盐
4
电离出的阴离子全部是OH-的化合物是碱,分为强碱与弱碱、可溶性碱与难溶性碱
碱
等
由金属阳离子(或铵根离子)与酸根离子构成的化合物是盐,分为可溶性盐与难溶性
盐
盐,酸式盐、碱式盐与正盐等
【特别提醒】1)从物质的分类上,纵向、横向构建知识分类意识。横向以化合价为基础,结合氧化还原
反应规律,学会分析物质的化学转化关系;纵向则对比同类物质的性质差异,把握物质性质差异性。
2)物质之间是否反应,不仅与物质结构、性质有关,而且与物质所在环境有关,在研究物质性质时,要
注意通性与个性之间的关系,在每条通性之外都存在个性。备考时,注意掌握化学中Na、Mg、Al、Fe、
Cu、C、Si、N、S、Cl等常见元素的单质、氧化物、酸或碱、盐之间的相互关系及每一步关系中各种可能
的变化方式和方法,归纳总结物质之间不能转化的情形。
3)常见物质间转化的几个误区
①S燃烧不能直接生成SO 而是生成SO 。
3 2
②AlO、SiO、Fe O 与HO不反应,不能直接转化为Al(OH) 、HSiO、Fe(OH) 。
2 3 2 2 3 2 3 2 3 3
③NH 催化氧化不能直接生成NO 。
3 2
④Fe与Cl 反应不能生成FeCl 。
2 2
⑤Fe与H+、Cu2+、S、I 反应不能生成Fe3+。
2
6.不同类别的无机物之间转化的一般规律
1)金属单质及其化合物的转化
金属单质――→碱性氧化物――→碱――→盐
如:Na――→NaO――→NaOH――→NaSO
2 2 4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转化关系。
2)非金属单质及其化合物的转化
非金属单质――→酸性氧化物――→酸――→盐
如:S――→SO ――→HSO ――→NaSO
2 2 3 2 3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
3)物质转化中的特殊性
(1)金属一般不和碱反应,铝能和氢氧化钠溶液反应 2Al+2NaOH+2H O 2NaAlO +3H ↑
2 2 2
(2)非金属单质一般不和酸反应,硅能和氢氟酸反应 Si+4HF SiF ↑+2H ↑
4 2
(3)酸性氧化物不一定不能和酸反应 SiO +4HF SiF ↑+2H O
2 4 2
(4)碱性氧化物和酸不一定发生复分解反应
①3FeO+10HNO(稀) 3 Fe ( NO )+NO↑+5HO
3 3 3 2
②Fe O+6HI 2FeI+I ↓+3H O
2 3 2 2 2
(5)碱和酸不一定发生中和反应
①3Fe(OH)+10HNO(稀) 3 Fe ( NO )+NO↑+8HO
2 3 3 3 2②Fe O+6HI 2FeI+I ↓+3H O
2 3 2 2 2
4)不能一步实现的反应
(1)不能一步生成的氧化物
①HS(或S)不能一步转化为SO
2 3
②N (或NH )不能一步转化为NO
2 3 2
③Fe(OH) 不能一步生成Fe O
2 2 3
④Fe不能一步生成Fe O
2 3
(2)不能一步生成的酸或碱:难溶性酸或碱
①Fe O、Al O、CuO与水不能反应生成相应的碱
2 3 2 3
②SiO 不能与水一步反应生成HSiO
2 2 3
(3)不能一步生成的硫化物或氯化物
①Cu和S反应不能生成CuS
②Fe和Cl 反应不能生成FeCl
2 2
③Fe和I 反应不能生成FeI
2 3
(4)电解法制备物质
①不能用电解熔融的AlCl 制备金属铝
3
②不能用电解熔融的MgO 或MgCl 溶液制备金属镁
2
③不能用电解NaCl 溶液制备金属钠
7.物质变化中的“三馏”、“四色”、“五解”和“十八化”归类
物理变化 化学变化
三馏 蒸馏、分馏 干馏
显色反应、颜色反应、指示剂变色反
四色 焰色反应
应
五解 潮解 分解、电解、水解、裂解
氢化、氧化、水化、
风化、炭化、钝化、
十八化 熔化、汽化、液化、酸化 催化、皂化、歧化、
卤化、硝化、酯化、
裂化、油脂的硬化
【易错提醒】常见的易混淆物质变化
(1)化学变化:结晶水合物的脱水、同素异形体间的转化、蛋白质的变性、电解、水解、煤的干馏、气化和
液化,石油的裂化与裂解等。
(2)物理变化:焰色试验、活性炭的吸附、盐析、蒸馏、升华、潮解等。
(3)核反应:即不是物理变化,也不是化学变化。
定义 原子核发生变化,即质子数或中子数发生变化
核
变 核裂变 概念 一个原子核分裂成几个原子核的变化。化 235 1 141 92 1
核反应方程式 U+ n→ Ba+ Kr+3 n
92 0 56 36 0
概念 由较轻的原子核变化为较重的原子核的变化
核聚变
1 2 4 1
核反应方程式 H+ H→ He+ n
1 1 2 0
同位素之间的转化 14 12 _______
如 C→ C
6 6
判断下列变化
不同元素之间的转化 238 206 _______
U→ Pb
是否是核变化 92 82
同种元素的原子和离子之间的转化 Na→Na+ _______
(4)同一名称两种变化
自由电子导电 发生物理变化
(1) 导电
自由离子导电 发生化学变化
物理爆炸 如轮胎爆炸
(2) 爆炸
化学爆炸 如炸药爆炸
物理升华 如 碘 、干冰升华
(3) 升华
化学升华(假升华) 氯化铵升华
物理气化 如液氨气化
(4) 气化
化学气化 如煤的气化
物理液化 如氯气液化
(5) 液化
化学液化 如煤的液化
8.物质性质与变化的关系
物质的性质是物质固有的属性,是物质的基本特征,是变化的内因(即变化的依据)。物质变化就是物质的
形态发生了变化(物理变化)或者物质的分子构成发生了变化(化学变化)。变化是一个过程或现象,是性质的
具体体现,即性质决定变化,变化体现性质。物质具有某种性质,才会发生对应的变化;物质发生了某种
变化,说明了该物质具备某种性质。
9.常见物质的转化规律
①“强制弱”规律分类 实例 离子方程式
酸 CHCOONa+HCl CHCOO-+H+=== CHCOOH
3 3 3
碱 FeCl +NaOH Fe3++3OH-=== Fe(OH) ↓
3 3
氧化剂 Cl+KI Cl+2I-===I +2Cl-
2 2 2
还原剂 Fe+CuSO Cu2++Fe===Cu+Fe2+
4
②“易溶制难溶”规律
如NaSO 溶液与BaCl 溶液反应,其离子方程式为Ba2++SO===BaSO ↓
2 4 2 4
③“难挥发制易挥发”规律
如:HSO +2NaCl=====NaSO +2HCl↑,HPO +NaBr=====NaH PO +HBr↑
2 4 2 4 3 4 2 4
考向1 传统文化中物质的性质和变化
例1 银雀山汉墓是全国规模较大的古代墓群之一,出土了大量文物,出土的下列文物中与其他成分分类不
同的是
A.帛画 B.竹简 C.陶器 D.漆器
【思维建模】解题传统文化试题的关键和基本思路
解答此类试题的关键是根据所给文本信息提取有效信息并正确解读,转化为化学学科中物质的物理性质、
化学性质、分离与提纯方法、反应类型及反应原理等熟悉的教材知识。解题的基本思路如下:
物理性质
化学性质 对照
信息提取
材料信息 化学反应类型 选项
分离与提纯方法 检验
化学反应原理
【变式训练1】(2024·安徽安庆·三模)中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.蔡伦造纸采用碱液制浆,该过程不涉及化学变化
B.羟基磷灰石是龟甲的成分之一,属于无机物
C.制作徽墨的松烟颗粒直径约30~50nm,溶于水可产生丁达尔现象
D.安徽繁昌窑所产青白瓷是以黏土为原料高温烧结而成
【变式训练2】(2024·安徽合肥·一模)三星堆遗址考古发掘出多件重要文物,如青铜神树、黄金手杖、丝
绸黑炭、象牙等。下列叙述错误的是
A.青铜的硬度比纯铜低
B.自然界中的金元素主要以游离态存在
C.丝绸到黑炭的转化涉及到氧化还原反应
D.象牙中含有的胶原蛋白属于有机高分子
考向2 物质变化的性质及其应用例1(2024·江西·模拟预测)下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 某杯酚可用于分离 和 分子直径小于 分子直径
B 镁粉加入小苏打溶液中快速产生气体 小苏打溶于水吸热
C 溶液显酸性 能与水分子形成氢键
D 能用NaOH溶液吸收 属于酸性氧化物
【思维建模】判断物质变化的基本思路为
【变式训练1】(2023·上海徐汇·统考二模)下列变化中,属于物理变化的是
A.氯气液化 B.石油裂化 C.金属钝化 D.蔗糖炭化
【变式训练2】(2024·陕西西安·二模)化学与生产、生活、科技、环境等关系密切。下列说法正确的是
A.汽车尾气催化转化器可有效减少 的排放,实现“碳中和”
B.维生素C用于抗衰老保健品的辅料,因其有较强的氧化性能清除体内自由基
C.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
D.甲壳质又称几丁质,是虾、蟹、昆虫等外壳的重要成分,它属于有机物
【变式训练3】(2024·安徽滁州·一模)下列说法正确的是
A.在同一化合物中,金属元素显正价,则非金属元素一定显负价
B.化学变化常伴随着发光,则有发光现象的变化一定是化学变化
C.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物
D.催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂
考向3 化学反应类型的判断
例1(23-24高三上·山西大同·期末)锶与钙位于同一主族,其化合物应用广泛,SrSO 常用于陶瓷工业。
4
以青石精矿(主要含SrSO )为原料制备高纯硫酸锶的部分工艺流程如图所示:
4下列说法错误的是
A.气体 可以循环利用
B.“转化”的总离子方程式为
C.“转化”中反应温度不宜过高且控制氨水过量
D.流程中涉及分解反应和化合反应
【思维建模】各反应类型间的关系:
【变式训练1】(2024·山西晋中·三模) 还原 是实现“双碳”经济的有效途径之一。在密闭容器
中( 和 按物质的量之比1:3投料,反应经如图所示的流程(主要产物已标出)可实现 的高效转
化。
下列说法正确的是
A.该反应的催化剂为 和 B.过程iii在恒压条件下通入He,有利于增加CO的产量
C.过程i、ii、iii均涉及置换反应 D.每生成4mol的CO,转移的电子数约为
【变式训练2】(2024·辽宁沈阳·模拟预测)下列化合物中不能由化合反应直接得到的是
A. B. C. D.
【变式训练3】(2024·安徽滁州·一模)课外实验可以帮助我们更好地学习化学知识。金属活动性强弱的探
究过程如下,其中不正确的是(已知:白醋的水溶液显酸性,与稀盐酸的化学性质相似)
A.实验一证明铁的金属活动性比铜强
B.实验二的现象是铜丝不断减少,表面有银白色固体析出,无色溶液变为黄色C.实验一烧杯②中发生的是置换反应
D.实验过程中存在不规范操作
考点三 分散系与胶体
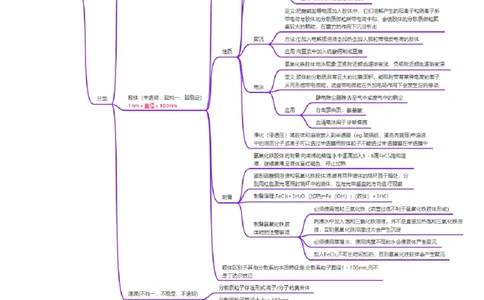
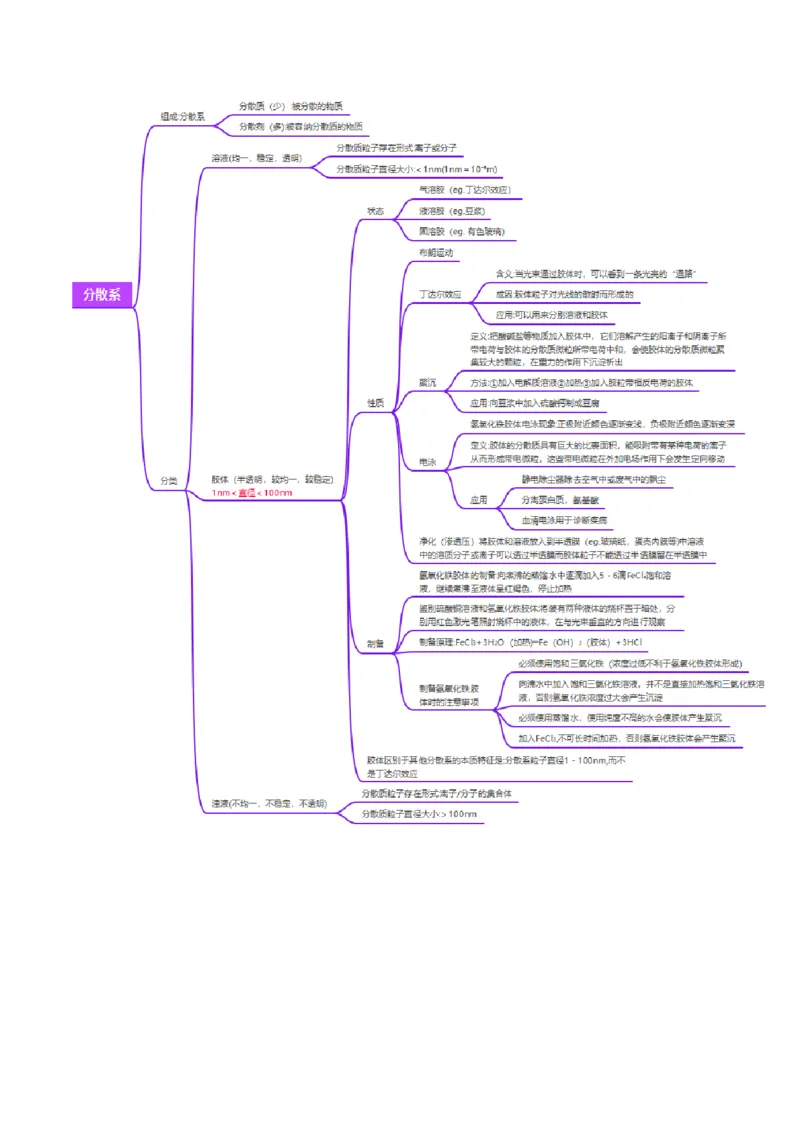
知识点1 分散系
1.概念:一种(或多种)物质分散到另一种(或多种)物质中所得到的体系。被分散的物质称为分散质,起容纳
分散质作用的物质称为分散剂,分散系都是混合物。
2.分类:
①按照分散质粒子的大小,分为三种分散系
②按照分散质和分散剂的状态,分为9种分散系
如烟属于气固分散系;雾属于气液分散系;悬浊液属于液固分散系;合金属于固固分散系。
③三种分散系比较
分散系 溶液 胶体 浊液
分散质粒子直径大小 < 1 nm 1 ~ 100 nm >100 nm
巨大分子或离
分散质微粒成分 离子或小分子 大分子或离子集合体
子集合体
不均匀、不透
外观特征 均匀、透明 均匀、透明或半透明
明
稳定,静置无沉 不稳定,静置
稳定性 较稳定
淀 有沉淀或分层
分散质能否透过滤纸 能 能 不能
饱和溶液、不饱 固溶胶、液溶胶、气溶 悬浊液、乳浊
分类
和溶液 胶 液
食盐水、蔗糖溶
实例 Fe(OH) 胶体 泥水
3
液
知识点2 胶体
1.常见的胶体
(1) 气溶胶 云、烟、雾(2) 液溶胶 豆浆、氢氧化铝胶体、Fe(OH) 胶体、硅酸胶体
3
(3) 固溶胶 果冻、宝石、烟水晶、有色玻璃
(4) 三种有机胶体 淀粉溶液、 肥皂 水 、蛋白质溶液
2.胶体的性质
①丁达尔效应:可见光束通过胶体时,在入射光侧面可看到一条光亮的通路,这是胶体粒子对光线散射而形
成的,可用此性质来鉴别溶液和胶体。
②布朗运动:胶粒永不停息地做无规则运动的现象叫做布朗运动,是胶体稳定的次要原因。
③电泳:由于胶体粒子带有电荷,在电场作用下,胶体粒子在分散剂中作定向移动的现象。此性质可用于工
业上的静电除尘。
a.概念:在外电场的作用下胶体微粒发生定向移动。
b.原因:胶体微粒比表面积大,吸附能力强,吸附了带电离子而带电荷。带正电荷的胶粒:氢氧化物胶
粒、金属氧化物胶粒;带负电荷的胶粒:硅酸胶粒、非金属氧化物胶粒、非金属硫化物胶粒、金属硫化物
胶粒。
c.规律:带正电荷的胶粒向阴极移动,带负电荷的胶粒向阳极移动。
d.变化:发生化学变化(电解反应)
④聚沉
a.概念:使胶体凝聚形成沉淀析出的现象。
b.方法:加热或搅拌、加入 电 解质 溶液、加入带相反电荷的胶体粒子的胶体。
c.应用,如制作豆腐、明矾净水等。
⑤介稳性:胶体的稳定性介于溶液和浊液之间,属于介稳体系。
⑥渗析:利用半透膜(如羊皮纸、膀胱膜等)使胶体和其中所含的可溶性杂质分离的过程称为渗析,又称
透析。半透膜的细孔能让可溶性杂质的分子或离子通过,但不能让较大的胶粒通过,因而可以达到分离的
目的。渗析是一种物理分离方法。
【易错提醒】(1)胶体不带电,胶体中的微粒能吸附体系中的带电粒子而使胶粒带电荷,但整个体系仍呈电中性。
(2)并不是所有的胶体都有电泳现象,如淀粉胶体粒子不带电荷而无电泳现象。
(3)胶体聚沉属于物理变化。
(4)明矾[KAl(SO)·12H O]、FeCl ·6H O等净化水的原因是Al3+、Fe3+水解生成Al(OH) 、Fe(OH) 胶体,胶
4 2 2 3 2 3 3
体粒子具有较大的表面积,能在水中吸附悬浮固体形成沉淀,从而达到净化水的目的。
(5)同种胶体粒子的电性相同,互相排斥,是胶体较稳定的主要原因,次要原因是布朗运动。
3.胶体的形成
(1)形成过程:将纳米颗粒分散到适当的分散剂中形成的一种分散系
(2)结构特点:胶粒是高分子或多分子聚合体
①胶体中所含胶粒的个数不确定
②胶粒所带的电荷数不确定
(3)胶体的介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,属于介稳体系。
胶体具有介稳性的两个原因:
原因一 胶体粒子可以通过吸附而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥(要使胶体聚
沉,就要克服排斥力,消除胶粒所带电荷 )。
原因二 胶体粒子在不停地做布朗运动,与重力作用相同时便形成沉降平衡的状态。
(4)淀粉胶体的特殊性
①结构特征:淀粉胶体为分子胶体,胶粒不带电荷
②性质特性:加入电解质溶液不能发生聚沉,通电后不能发生电泳
4.Fe(OH) 胶体的制备
3
①制备原理:FeCl +3HO Fe(OH) (胶体)+3HCl
3 2 3
②具体操作:用烧杯取少量蒸馏水,加热至沸腾;向沸水中逐滴加入适量的饱和 FeCl 溶液;继续煮沸至
3
溶液呈红褐色,停止加热,即得Fe(OH) 胶体。
3
③除去胶体中所含杂质
a.胶体中的悬浊液:过滤
b.胶体中的分子或离子:渗析
④实验方法证明Fe(OH) 胶体和Cl-两者已经分离完全: 取最后一次渗析液与 洁净 的试管中,加入硝酸银溶
3
液,若无白色沉淀产生,则说明两者已经完全分离。
5.胶体的应用
(1)胶体的聚沉
①卤水点豆腐 ②河海交界处容易形成三角洲 ③FeCl 溶液常用作凝血剂
3(2)胶体的吸附性
①明矾、Fe (SO ) 溶液净水 ②Al(OH) 胶体作漂白剂
2 4 3 3
(3)胶体的丁达尔现象
①清晨阳光穿过茂密树木枝叶产生的美丽光线 ②电影院光柱 ③海市蜃楼
(4)胶体的电泳:工业上的静电除尘。
考向1 分散系及其分类
例1 (2024·海南省·模拟预测)“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一
种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质
①是溶液②是胶体③能产生丁达尔效应④能透过滤纸⑤不能透过滤纸⑥静置后会析出黑色沉淀
A.①④⑤ B.②③④ C.②③⑤ D.①③④⑥
【易错提醒】①纳米材料本身不是胶体,只有分散到水中才能形成胶体。②不同分散系的本质区别是分散
质的大小,而不是丁达尔效应。
【变式训练1】(2024·湖南·二模)能产生“丁达尔效应”的是
A.蔗糖溶液 B.硫酸铜溶液 C.氧化铁固体 D.氢氧化铁胶体
【变式训练2】(23-24高三上·宁夏银川·阶段考试)下列关于溶液和胶体的叙述,正确的是
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
考向2 胶体的组成、性质、制备
例1 (2024·湖南常德·模拟预测)下列说法正确的是
A.NaCl溶于水形成的分散系是一种胶体
B.向NaOH溶液中滴加饱和FeCl 溶液可制取Fe(OH) 胶体
3 3
C.直径在80nm左右的新冠病毒颗粒是由蛋白质构成的,在空气中不能形成气溶胶
D.用一束强光可区别FeCl 溶液和Fe(OH) 胶体
3 3
【易错警示】
1.利用丁达尔效应可以快速鉴别溶液与胶体,但胶体区别于其他分散系的本质特征是胶体粒子的直径介
于1~100 nm之间,而不是丁达尔效应。
2.胶体不带电荷,胶体粒子(分散质)带电荷,但淀粉胶体的胶体粒子也不带电荷,但整个分散系仍呈电中
性。
3.Fe(OH) 胶体中,Fe(OH) 胶粒数目远小于铁原子的数目。
3 3
4.胶粒有很大的比表面积,吸附能力很强。
5.胶体中的分散质微粒能透过滤纸,但不能透过半透膜,因此可用过滤的方法分离胶体和浊液,用渗析的
方法分离胶体和溶液。6.书写Fe(OH) 胶体制备化学方程式的四个易错点。
3
①用“===”而不用“ ”;
②Fe(OH) 分子式后注明胶体而不使用“↓”符号;
3
③反应条件是“△”;
④HCl后不能标“↑”符号。
【变式训练1】(2024·陕西西安·一模)新型冠状病毒由蛋白质外壳和单链核酸组成,如图所示,直径为
下列说法错误的是
A.新型冠状病毒扩散到空气中可能形成胶体
B.新型冠状病毒的蛋白质外壳中存在氢键
C.止咳祛痰药盐酸氨溴索的化学式为 属于混合物
D. 泡腾片和酒精均可杀灭新冠病毒,二者消毒原理不同
【变式训练2】(2024·贵州·一模)纳米级 具有优良的催化性能。一种制备原理如下:
。下列叙述正确的是
A.过滤操作能提纯 形成的胶体
B. 形成的胶体中分散剂直径在1nm~100mm之间
C.持续加热上述混合物仍能观察到砖红色液体
D. 液体能观察到一条光亮的“通路”的原因是分散质颗粒对可见光散射
考向3 胶体性质的应用
例1(2024·福建宁德·三模)松花蛋(皮蛋)是一种用禽蛋加工制成的食品。制作松花蛋的原料泥需要
、食品级金属盐(较常用的是 )等。下列说法错误的是
A.蛋黄成分中的油脂是天然高分子
B.蛋清遇 会聚沉,这个过程发生了蛋白质的变性
C.蛋壳膜可用于提纯、精制胶体
D.制作过程中生成的 可以堵住蛋壳的气孔来调节 渗透量
【变式训练1】(23-24高三上·广西·期中)量子点是一类非常小的纳米尺度颗粒,也被称为半导体纳米
晶,量子点技术获得2023年化学诺贝尔奖,下列说法正确的是
A.碳量子点是一种新型具有荧光性质的纳米碳材,属于胶体
B.有些胶体具有电泳现象,是因为胶体带电C.胶体的丁达尔效应是胶体中分散质微粒对可见光散射而形成的
D.胶体能吸附水中的色素,悬浮固体、重金属Cu2+等达到净水的目的
【变式训练2】(2024·福建厦门·三模)我国明代李时珍《本草纲目》中记载豆腐制作过程:“凡黑豆…皆
可为之。水浸,硙碎。滤去渣,煎成。以卤汁或山鞋叶或酸浆醋淀,就釜收之”。制作过程不涉及的操作
及现象是
A.溶解 B.过滤 C.聚沉 D.蒸馏
1.(2023·天津卷)利用18O示踪技术研究HO 与Cl 的反应历程,结果如下:
2 2 2
①
②
下列叙述正确的是
A.反应①是置换反应
B.18O的核电荷数是18
C.18O与16O互为同素异性体
D.反应历程中 中的O-O键未发生断裂
2.(2023·福建卷)唐代陆羽《茶经·三之造》中记载茶叶制作过程:“晴采之,蒸之,捣之,拍之,焙
之,穿之,封之,茶之干矣”。以下操作中最不可能引起化学变化的是
A.蒸 B.捣 C.焙 D.封
3.(2023·湖南卷)中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.青铜器“四羊方尊”的主要材质为合金
B.长沙走马楼出土的竹木简牍主要成分是纤维素
C.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
D.铜官窑彩瓷是以黏土为主要原料,经高温烧结而成
4.(2023·辽宁卷)科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是
A.利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
B.发现了月壤中的“嫦娥石[(Ca Y)Fe(PO)]”:其成分属于无机盐
8 4 7
C.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
5.(2023·浙江卷)下列物质中属于耐高温酸性氧化物的是
A. B. C. D.
6.(2022·福建卷)福建多个科研机构经过长期联合研究发现,使用 和改性的 基催化剂,可打通从
合成气经草酸二甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是A.草酸属于无机物 B. 与石墨互为同分异构体
C. 属于过渡元素 D.催化剂通过降低焓变加快反应速率
7.(2022·广东卷)北京冬奥会成功举办、神舟十三号顺利往返、“天宫课堂”如期开讲及“华龙一号”
核电海外投产等,均展示了我国科技发展的巨大成就。下列相关叙述正确的是
A.冬奥会“飞扬”火炬所用的燃料 为氧化性气体
B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C.乙酸钠过饱和溶液析出晶体并放热的过程仅涉及化学变化
D.核电站反应堆所用铀棒中含有的 与 互为同位素
8.(2021·江苏卷)下列有关物质的性质与用途不具有对应关系的是
A.铁粉能与O 反应,可用作食品保存的吸氧剂
2
B.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C.FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D.聚合硫酸铁能水解并形成胶体,可用于净水
9.(2021·江苏卷)黑火药是中国古代四大发明之一,其爆炸反应为2KNO+S+3C=KS+N↑+3CO ↑。下列
3 2 2 2
说法正确的是
A.黑火药中含有两种单质 B.爆炸时吸收热量
C.反应中S作还原剂 D.反应为置换反应
10.(2021·福建卷)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误的是
A.FeSO 的分解产物X为FeO B.本流程涉及复分解反应
4
C.HNO 的沸点比HSO 的低 D.制备使用的铁锅易损坏
3 2 4