文档内容
第 09 讲 钠及其重要化合物
01 模拟基础练
【题型一】钠及其氧化物
【题型二】碳酸钠和碳酸氢钠
【题型三】碱金属 焰色试验
02 重难创新练
03 真题实战练
题型一 钠及其氧化物
1.(2024·江苏扬州·模拟预测)钠钾合金常温下呈液态,可用作快中子反应堆的热交换剂,这主要是因为
钠钾合金
A.易与 反应 B.易与 反应
C.熔点低、导热性好 D.密度小、硬度小
【答案】C
【解析】钠、钾为金属,具有良好的导电、导热能力,钠钾合金熔点低,常温下呈液态,具有良好的导热
性,可用作快中子反应堆的热交换剂,故C符合题意;答案为C。
2.(2024·海南省直辖县级单位·模拟预测)钠与水的反应是一个经典实验,下列有关该实验的操作或现象
说法错误的是
A.用镊子从煤油中取出钠块
B.切取绿豆粒大小的钠块,用滤纸吸干煤油,放入盛有水的烧杯中
C.钠在水面上快速游动,并有轻微的嘶嘶声
D.将剩余的钠放入废液缸中
【答案】D
【解析】A.钠存放在煤油中,则用镊子从煤油中取出钠块,故A正确;B.钠质地软,可以用小刀切取
绿豆粒大小的钠块,用滤纸吸干煤油,放入盛有水的烧杯中,故B正确;C.钠与水反应剧烈,产生氢
气,密度比水小,钠在水面上快速游动,并有轻微的嘶嘶声,故C正确;D.取钠切割后,将剩余的钠块
应放回原试剂瓶,钠易被氧化、且与水反应生成强碱,则不能放入废液缸,故D错误。答案选D。
3.(2024·重庆·三模)下列叙述正确的是
A.向饱和食盐水中先通 后,再通 ,可获得大量纯碱
B. 与水反应,红热的 与水蒸气反应均有气体单质生成C. 的金属活性比 强,工业上用 与 的水溶液反应制
D.煤中含有苯、甲苯等芳香烃,通过煤的干馏可获得苯、甲苯等芳香烃
【答案】B
【解析】A.向饱和食盐水中先通 后,再通 ,生成的是碳酸氢钠,碳酸氢钠受热分解才生成碳酸
钠,即纯碱,A错误;B. 与水反应生成氢氧化钠和氧气,红热的 与水蒸气反应生成四氧化三铁
和氢气,均有气体单质生成,B正确;C. 是活泼金属,要先与溶液中的水反应生成氢氧化钠和氢气,
用 与 的水溶液反应无法制得 ,C错误;D.煤的干馏产品中含苯、甲苯等,煤中不含,干馏
后分馏可得苯、甲苯等芳香烃,D错误;
故选B。
4.(2024·浙江台州·二模)在潜水艇和消防员的呼吸面具中, 作为氧气的来源。下列说法不正确的
是
A. 和 反应可生成
B. 可使酚酞溶液先变红色后褪色
C.工业上用未经过处理的空气和钠直接反应来制备
D.可用焰色试验来检验 中的阳离子
【答案】C
【解析】A. 和 反应可生成 和NaOH,A正确;B. 具有强氧化性且与水反应生成
氢氧化钠,故可使酚酞溶液先变红色后褪色,B正确;C.若工业上用未经过处理的空气和钠直接反应来
制备 ,空气中的二氧化碳和水等与钠反应产生杂质,C不正确;D.可用焰色试验来检验 中
的阳离子,焰色为黄色,D正确;答案选C。
5.(2024·浙江·模拟预测)对下列事实进行归纳推测,推测合理的是
选项 事实 推测
A NaO 与CO 反应生成NaCO 和O NaO 与SO 反应生成NaSO 和O
2 2 2 2 3 2 2 2 2 2 3 2
AlCl 溶液与过量NaOH溶液反应生成 AlCl 溶液与过量氨水反应生成
3 3
B
[Al(OH) ]- [Al(OH) ]-
4 4
C NaH与HO反应生成氢气 AlH 与NH 反应生成H
2 3 3 2
D Ca(ClO) +H O+CO=CaCO ↓+2HClO 酸性强弱:HCO>HCO->HClO
2 2 2 3 2 3 3
【答案】C
【解析】A.NaO 与CO 反应生成NaCO 和O,由于NaO 具有强氧化性,SO 具有还原性,则NaO 与
2 2 2 2 3 2 2 2 2 2 2
SO 反应生成NaSO ,不能生成NaSO 和O,A错误;B.由于Al(OH) 只溶于强碱溶液中不溶于弱碱溶
2 2 4 2 3 2 3
液中,故AlCl 溶液与过量NaOH溶液反应生成[Al(OH) ]-,而AlCl 溶液与过量氨水反应生成Al(OH) ,B
3 4 3 3错误;C.NaH与HO反应生成氢气的本质是NaH中的H-与HO中的H+发生歧化反应生成为H,因此
2 2 2
AlH 与NH 反应时也能这样生成H,C正确;D.该反应之所以能够发生,是由于生成了难溶物质碳酸
3 3 2
钙,不能根据强酸制备弱酸的规律得到结论,D错误;答案选C。
题型二 碳酸钠、碳酸氢钠
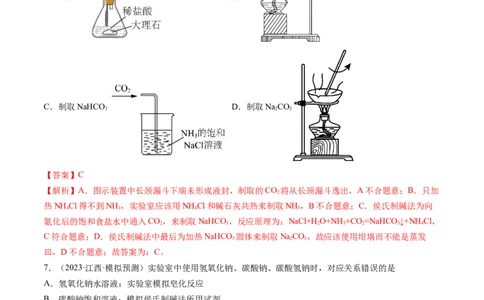
6.(2024·江苏泰州·模拟预测)实验室模拟侯氏制碱法制备NaCO,下列装置与原理均正确的是
2 3
A.制取CO B.制取NH
2 3
C.制取NaHCO D.制取NaCO
3 2 3
【答案】C
【解析】A.图示装置中长颈漏斗下端未形成液封,制取的CO 将从长颈漏斗逸出,A不合题意;B.只加
2
热NH Cl得不到NH ,实验室应该用NH Cl和碱石灰共热来制取NH ,B不合题意;C.侯氏制碱法为向
4 3 4 3
氨化后的饱和食盐水中通入CO,来制取NaHCO ,反应原理为:NaCl+H O+NH +CO =NaHCO↓+NHCl,
2 3 2 3 2 3 4
C符合题意;D.侯氏制碱法中最后为加热NaHCO 固体来制取NaCO,故应该使用坩埚而不能是蒸发
3 2 3
皿,D不合题意;故答案为:C。
7.(2023·江西·模拟预测)实验室中使用氢氧化钠、碳酸钠、碳酸氢钠时,对应关系错误的是
A.氢氧化钠水溶液:实验室模拟皂化反应
B.碳酸钠饱和溶液:模拟侯氏制碱法所用试剂
C.碳酸钠饱和溶液:制备乙酸乙酯实验中收集产品
D.碳酸氢钠饱和溶液:制备CO 时除去HCl气体
2
【答案】B
【解析】A.皂化反应为油脂在碱性条件下的水解反应,A项正确;B.模拟侯氏制碱法应使用氯化钠饱和
溶液,B项错误;C.碳酸钠饱和溶液可以吸收乙醇,中和乙酸,降低酯的溶解度,C项正确:D.
NaHCO 可与HCl反应生成NaCl、CO 和水,因此碳酸氢钠饱和溶液可除去CO 中的HCl气体,D项正
3 2 2
确。答案选B。
8.(2024·山东泰安·一模)取一定体积的下列两种试剂(浓度均为 )进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是
A. 溶液、稀盐酸 B. 溶液、氨水
C. 溶液、溴水 D. 溶液、酸性 溶液
【答案】B
【解析】A.向 溶液中滴加稀盐酸,刚开始没有气泡,然后才产生气泡,向稀盐酸中滴加
溶液直接产生气泡,故A不符合题意;B. 溶液和氨水无论滴加顺序怎样,都会生成氢氧化铝沉
淀,故B符合题意;C.向 溶液中滴加溴水,溴水中的HBr和 反应生成二氧化碳气体,
溴水过量时溶液变为橙黄色,向溴水中滴加 溶液,溴水中的HBr和 反应生成二氧化碳气
体,溶液由橙黄色变为无色,故C不符合题意;D.向 溶液中滴加酸性 溶液,溶液由无色
变为红色,向酸性 溶液中滴加 溶液,溶液由红色变为无色,故D不符合题意;故选B。
9.(2024·湖南·模拟预测)向三支试管中分别加入稀盐酸、NaCl溶液和 溶液,然后分别向上述三
支试管中依次加入 溶液和稀硝酸。下列有关说法错误的是
A.稀盐酸、NaCl溶液和 溶液三种溶液的酸碱性互不相同
B.该实验可以证明不同物质间反应的离子方程式可能相同
C.在该实验的基础上,再追加一个焰色试验就可以将上述三种溶液鉴别出来
D.若不加入其他试剂,仅通过溶液间相互滴加不能鉴别出上述三种溶液
【答案】D
【解析】A.稀盐酸、NaCl溶液和 溶液分别呈酸性、中性和碱性,A正确;B.稀盐酸、氯化钠溶
液分别与硝酸银溶液反应均生成氯化银沉淀,离子方程式相同,则该实验可以证明不同物质间反应的离子
方程式可能相同,B正确;C.由于碳酸银能溶于硝酸,氯化银不能溶于硝酸,氯化钠的焰色显黄色,稀
盐酸无焰色,因此在该实验的基础上,再追加一个焰色试验就可以将上述三种溶液鉴别出来,C正确;
D.稀盐酸、NaCl溶液和 溶液可以通过相互滴加鉴别,将稀盐酸逐滴滴入碳酸钠溶液中,一段时
间后才有气泡产生,而将碳酸钠溶液滴入稀盐酸中,立即有气泡产生,NaCl溶液与稀盐酸或碳酸钠溶液互
滴均无明显现象,因此若不加入其他试剂,仅通过溶液间相互滴加能鉴别出上述三种溶液,D错误;故
选:D。
10.(2024·黑龙江双鸭山·模拟预测)某兴趣小组在实验室模拟侯氏制碱法制备 ,部分实验装置如
图所示,下列说法正确的是A.实验过程中向启普发生器中添加液体时,可以取下Ⅰ处胶塞加入
B.所用试剂有稀硫酸、浓硫酸、 、饱和食盐水、 、 、蒸馏水
C.开始实验时,应先打开活塞Ⅱ,再打开活塞Ⅲ
D.试剂d为冰水,以降低 的溶解度,促进晶体的析出
【答案】D
【分析】试剂a为盐酸,试剂b为碳酸钙,用于制取二氧化碳,试剂c为饱和碳酸氢钠溶液用于除去二氧
化碳中的HCl;然后将二氧化碳通入氨化的饱和食盐水中,反应生成碳酸氢钠,过量的氨气用水或硫酸溶
液吸收,且要防止倒吸,据此分析解答。
【解析】A.实验过程中向启普发生器中添加液体时,应从球形漏斗加入,A项错误;B.制备 应使用
稀盐酸不应使用稀硫酸,生成的 无需干燥, 和 用于制取 ,尾气中含有 ,可用
稀硫酸吸收,B项错误;C.因 溶解度大,开始实验时应先打开活塞Ⅲ,再打开活塞Ⅱ,C项错误;
D.反应结束后将锥形瓶放入冰水浴中可以降低 的溶解度,促进 晶体的析出,D项正
确;故选:D。
题型三 碱金属 焰色试验
11.(2024高三·全国·专题考试)碱金属元素是周期性表现得最鲜明和最规律的一族元素。下列说法正确
的是
A.单质都能浮在水面上,都能保存在煤油中
B.单质在空气中燃烧时,都生成过氧化物
C.单质都不能在自然界中稳定存在
D.单质都是强还原剂,其阳离子都具有强氧化性
【答案】C
【解析】A.Rb、Cs密度比水大,Li的密度比煤油小,A不正确;B.Li燃烧只能生成LiO,B不正确;
2
C.碱金属单质都是活泼金属,易与空气中氧气、水等发生反应,因此不能在自然界中稳定存在,故C正
确;D.碱金属单质是强还原剂,但其阳离子具有弱氧化性,D不正确;故选:C。
12.(23-24高三上·江西·阶段考试)第87号元素钫,它位于碱金属族,根据元素周期表结构及元素性质
变化趋势,下列关于碱金属某些元素原子结构和性质的判断,错误的是
①锂与水反应比钠剧烈 ②金属单质都可以密封保存在煤油中 ③钾的氧化物暴露在空气中易吸
收二氧化碳 ④锂的阳离子的最外层电子数和钠的相同 ⑤钫单质是强还原剂 ⑥钫在化合物中显+1价 ⑦钫单质的密度应该大于 ⑧钫单质有较高的熔点
A.①②④⑧ B.①②③⑦ C.③④⑤⑧ D.①③④⑥
【答案】A
【解析】①金属性: ,元素的金属性越强,对应的单质与水反应越剧烈,则钠与水反应比锂与水
反应剧烈,①错误;②锂的密度小于煤油的密度,若用煤油保存锂,则达不到隔绝空气和水的目的,②错
误;③钾的氧化物是碱性氧化物,在空气中易吸收二氧化碳,生成碳酸钾,③正确;④原子失去最外层电
子后,次外层变成最外层,故锂离子最外层有2个电子,钠离子最外层有8个电子,二者数目不等,④错
误;⑤钫属于碱金属,碱金属单质都具有强还原性,可作强还原剂,⑤正确;⑥碱金属元素原子最外层都
只有1个电子,在反应中容易失去这个电子显+1价,⑥正确;⑦碱金属单质的密度从上到下逐渐增大(K反
常),推测钫单质的密度应该大于铯的,密度大于 ,⑦正确;⑧碱金属单质的熔点较低且从上到下
熔点逐渐降低,所以钫单质的熔点很低,⑧错误。答案选A。
13.(23-24高三上·天津·期中)下列关于碱金属的说法中,正确的是
A.第ⅠA族元素叫碱金属元素 B.金属锂可以保存在煤油中
C.密度:Cs>Rb>K>Na>Li D.熔点:Li>Na>K>Rb>Cs
【答案】D
【解析】A.H为第ⅠA族元素,但不是碱金属,A错误;B.锂的密度比煤油小,不能保存在煤油中,应
该用石蜡保存,B错误;C.钠的密度比钾的密度要大,C错误;D.碱金属从上到下离子半径依次增大,
金属键强度减弱,所以熔点:Li>Na>K>Rb>Cs,D正确;综上所述答案为D。
14.(2024·湖北·一模)湖北盐业历史悠久,早在唐代已有零星的产盐记载。下列说法错误的是
A. 既可做调味品也可做防腐剂
B.焰色试验可用于区分 和
C.电解食盐水的产物可用于生产漂粉精
D.医疗上生理盐水是含0.9%的 溶液
【答案】B
【解析】A. 是食盐的主要成分,既可做调味品也可做防腐剂,故A正确;B. 和 焰色
试验均为黄色火焰,无法进行区分,故B错误;C.电解食盐水的产物为Cl、H、NaOH,Cl 可与石灰乳
2 2 2
生产漂粉精,故C正确;D.医疗上生理盐水是含0.9%的 溶液,故D正确;故选B。
15.(2024·辽宁鞍山·二模)下列实验操作及分析均正确的是
选项 实验操作 分析
防止杂质离子干扰实验现
A 焰色试验之前用硫酸清洗铂丝或铁丝
象
中和反应反应热测定时,将稀盐酸逐滴加入稀NaOH 缓慢加入盐酸确保反应完
B
溶液 全
C 配制溶液之前加热烘干容量瓶 防止定容时产生误差D 向酸性淀粉水解液中加入碘水检验是否有淀粉剩余 淀粉遇碘水显蓝色
【答案】D
【解析】A.硫酸为高沸点酸,不易挥发,在焰色试验之前用盐酸清洗铂丝或铁丝,不用硫酸,A错误;
B.中和反应反应热测定时,为了尽量减少热量的损失,应将稀盐酸迅速加入稀NaOH溶液,B错误;C.
配制一定物质的量浓度溶液之前容量瓶不需要干燥,不影响实验结果,C错误;D.淀粉遇碘单质显蓝
色,向酸性淀粉水解液中加入碘水,若变蓝色,说明淀粉没有完全水解,D正确;故答案为:D。
16.(2024·江苏·二模)实验室用如下方案测定 和 混合物的组成:称取一定质量样品溶解
于锥形瓶中,加入2滴指示剂 ,用标准盐酸滴定至终点时消耗盐酸 ;向锥形瓶中再加入2滴指示
剂 ,继续用标准盐酸滴定至终点,又消耗盐酸 。下列说法正确的是
A.指示剂 可依次选用甲基橙、酚酞
B.样品溶解后的溶液中:
C.滴定至第一次终点时的溶液中:
D.样品中 和 物质的量之比为
【答案】D
【分析】由题意可知,第一次滴定滴入的指示剂为酚酞,发生的反应为NaCO+HCl=NaHCO +NaCl,第二
2 3 3
次滴定滴入的指示剂为甲基橙,发生的反应为NaHCO +HCl=NaCl +CO ↑+H O,据此作答。
3 2 2
【解析】A.由分析可知,指示剂 可依次选用酚酞、甲基橙,故A错误;B.样品溶解后的溶液中,
并未知此时 和 的物质的量浓度比值关系,无法进行判断物料守恒关系,故B错误;C.第
一次滴定滴入的指示剂为酚酞,发生的反应为NaCO+HCl=NaHCO +NaCl,终点时溶液中含有的溶质是
2 3 3
NaHCO 、NaCl,根据电荷守恒可知 ,故C错误;
3
D.由方程式可知,(V —V)mL为原溶液中碳酸氢钠消耗盐酸的体积,加入的盐酸浓度是不变的,根据方
2 1
程式可知消耗盐酸的物质的量就等于 和 物质的量,则 和 物质的量之比为
,故D正确;故答案选D。
17.(2024·浙江·模拟预测)某研究小组利用 和 模拟工业制碱方法,实验流程如下:下列说法不正确的是
A.温度高于 , 分解加快导致 产率降低
B.操作Ⅲ中 可分解,所以操作Ⅰ中无需洗涤 固体
C.加入 固体有利于 晶体析出
D.步骤Ⅱ蒸发浓缩至溶液表面出现晶膜时停止加热
【答案】B
【分析】本题为工业制备碳酸钠的流程题,在饱和氯化钠溶液中加入碳酸氢铵固体,发生反应生成碳酸氢
钠和氯化铵,过滤后分别处理固体碳酸氢钠和氯化铵溶液,可以得到两种产品氯化铵和碳酸钠,以此解
题。
【解析】A.温度高于 , 会分解生成氨气、水和二氧化碳的量,减少了碳酸氢钠的量,最终
降低了碳酸钠的产率,A正确;B.操作Ⅲ中生成碳酸钠,其表面可能吸附氯化铵和氯化钠,氯化铵受热
会分解,但是氯化钠较稳定,则操作Ⅰ中还需洗涤 固体,B错误;C.食盐会降低氯化铵的溶解
度,则加入 固体有利于 晶体析出,C正确;D.蒸发浓缩至溶液表面出现晶膜时,停止加热,
防止析出的 因温度过高而分解,D正确;故选B。
18.(2024·重庆·模拟预测)常温下,分别向相同浓度的NaHCO 、NaCO 溶液中逐滴加入盐酸,滴加过
3 2 3
程中溶液的pH变化如下图所示。下列说法正确的是
A.曲线①表示盐酸滴入NaHCO 溶液的过程
3
B.d、e点水的电离程度:d>e
C.a点的K 大于d点的K
W W
D.b、c、e点均满足:
【答案】B
【解析】A. 相同浓度的 NaCO 和 NaHCO , Na CO 溶液碱性强, 曲线①表示盐酸滴入 Na₂CO₃溶液的过
2 3 3 2 3
程,A错误;B. e点的pH 小,酸性强,对水的抑制强,水的电离程度小,d、e点水的电离程度:d>e,B正确;C. 温度相同, K 相同,a点的K 等于d点的K ,C错误;
w w w
D. 电荷不守恒,阴离子中还有 Cl-,b、c、e点均满足
,D错误;故选B。
19.(23-24高三上·重庆·期中)已知氢化钠(NaH)可由氢气和钠在高温下化合形成,NaH遇水放出 ,下
列说法正确的是
A.取钠与氢气反应后的产物,加水若产生 ,即可证明产物为纯净的NaH
B.NaH与水反应产生的 ,通过盛有碱石灰的干燥管,再用向上排空气法收集
C.高温下NaH将四氯化钛( )还原成金属钛的原理为
D.NaH在无水条件下除去钢铁表面铁锈的原理为
【答案】D
【解析】A.由于2Na+2HO=2NaOH+H ↑,取钠与氢气反应后的产物,加水若产生 ,不能证明产物为
2 2
纯净的NaH,A错误;B.NaH与水反应产生的 ,通过盛有碱石灰的干燥管,H2的密度比空气的小,
应该用向下排空气法收集,B错误;C.高温下NaH将四氯化钛( )还原成金属钛的原理为
,C错误;D.NaH中H-具有强还原性,故NaH在无水条件下除去钢铁表
面铁锈的原理为 ,D正确;故答案为:D。
20.(2023·上海徐汇·模拟预测)金属钠及其化合物在人类生产、生活中起着重要作用。
(1)Na的轨道表示式为 。
(2)NaCl的熔点为800.8℃。工业上,采用电解熔融的NaCl和 混合盐,制备金属Na,电解的化学
方程式为: ,加入 的目的是 。
(3)采用空气和Na为原料可直接制备 。空气与熔融的金属Na反应前需依次通过的试剂为
、 (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
(4) 的电子式为 。
在25℃和101kPa时,Na与 反应生成 放出510.9kJ的热量,写出该反应的热化学方程式:
。
(5)向酸性 溶液中加入 粉末,观察到溶液褪色,发生如下反应。配平上述离子方程式 。
该反应说明 具有 (选填“氧化性”“还原性”或“漂白性”)。
(6)在密闭容器中,将 和bmol 固体混合物加热至250℃,充分反应后,若剩余固体为
和NaOH、排出气体为 和 时, 的取值范围为 。
【答案】(1)
(2)作助熔剂,降低NaCl的熔点,节省能耗
(3)c a
(4)
(5) 还原性
(6)
【解析】(1)Na为11号元素,基态Na原子的电子排布式为1s22s22p63s1,则其轨道表示式为
,故答案为: ;
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na,加入CaCl 时,580℃时NaCl即熔
2
融,所以加入CaCl 能降低NaCl的熔点,即CaCl 作助溶剂,降低NaCl的熔点,节省能耗,故答案为:作
2 2
助熔剂,降低NaCl的熔点,节省能耗;
(3)采用空气和Na为原料可直接制备NaO,空气中CO、水蒸气都能与金属Na反应,所以在反应前需
2 2 2
要将空气中的CO、水蒸气除去,CO 属于酸性氧化物,能和碱液反应,浓硫酸具有吸水性,所以空气与
2 2
熔融的金属Na反应前需依次通过NaOH溶液、浓硫酸,故答案为:c;a;
(4) 由钠离子和过氧根离子构成,过氧根离子中存在O-O键,则 的电子式为
;在25℃和101kPa时,Na与 反应生成 放出510.9kJ的热量,则反应的热化
学方程式为 ,故答案为: ;
;
(5)根据得失电子守恒和质量守恒配平方程式为 ,该
反应中, 为还原剂,说明 具有还原性,故答案为:
;还原性;
(6)残余的固体为NaCO 和NaOH,生成的气体为O 和HO,则有总反应式为
2 3 2 2, 2a-b>0,则a:b ,b-a>0,则a:b<1,则
a:b的取值范围为 ,故答案为: 。
21.(2024·安徽卷)青少年帮厨既可培养劳动习惯,也能将化学知识应用于实践。下列有关解释合理的是
A.清洗铁锅后及时擦干,能减缓铁锅因发生吸氧腐蚀而生锈
B.烹煮食物的后期加入食盐,能避免 长时间受热而分解
C.将白糖熬制成焦糖汁,利用蔗糖高温下充分炭化为食物增色
D.制作面点时加入食用纯碱,利用 中和发酵过程产生的酸
【答案】A
【解析】A.铁发生吸氧腐蚀时,正极上O 得电子结合水生成氢氧根离子,清洗铁锅后及时擦干,除去了
2
铁锅表面的水分,没有了电解质溶液,能减缓铁锅因发生吸氧腐蚀而生锈,A正确;B.食盐中含有碘酸
钾,碘酸钾受热不稳定易分解,因此烹煮食物时后期加入食盐,与NaCl无关,B错误;C.焦糖的主要成
分仍是糖类,同时还含有一些醛类、酮类等物质,蔗糖在高温下并未炭化,C错误;D.食用纯碱主要成
分为NaCO,制作面点时加入食用纯碱,利用了NaCO 中和发酵过程产生的酸,D错误;故答案选A。
2 3 2 3
22.(2023·天津卷)下列方法(试剂)中,无法鉴别 和 两种物质的是
A.焰色试验 B. 试纸 C.稀氨水 D.
【答案】C
【解析】A.钠元素、钡元素的焰色不同,可以用焰色试验鉴别碳酸钠和氯化钡,A不符合;B.NaCO
2 3
溶液显碱性,BaCl 溶液显中性,故可以用pH试纸检验NaCO 和BaCl ,B不符合;C.NaCO 溶液和
2 2 3 2 2 3
BaCl 溶液与氨水都不反应,都无现象,C符合;D.NaCO 溶液与NaSO 溶液不反应,BaCl 溶液与
2 2 3 2 4 2
NaSO 反应生成白色沉淀硫酸钡, D不符合;故答案为:C。
2 4
23.(2023·广东卷)部分含 或含 物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.可存在c→d→e的转化
B.能与 反应生成c的物质只有b
C.新制的d可用于检验葡萄糖中的醛基D.若b能与 反应生成 ,则b中含共价键
【答案】B
【分析】由图可知a、b、c对应物质分别为:钠、氧化钠(过氧化钠)、氢氧化钠或a、b、e 、d对应物
质分别为:铜、氧化亚铜、氧化铜、氢氧化铜。
【解析】A.由分析可知氢氧化钠和硫酸铜反应生成氢氧化铜,氢氧化铜受热分解生成氧化铜所以存在
c→d→e的转化,A合理;B.钠和氧化钠(过氧化钠)都能与 反应都能生成氢氧化钠,B不合理;
C.新制氢氧化铜可用于检验葡萄糖中的醛基,C合理;D.若b能与 反应生成 ,则b为过氧化
钠,结构中含共价键和离子键,D合理;故选B。
24.(2023·北京卷)离子化合物 和 与水的反应分别为① ;②
。下列说法正确的是
A. 中均有非极性共价键
B.①中水发生氧化反应,②中水发生还原反应
C. 中阴、阳离子个数比为 , 中阴、阳离子个数比为
D.当反应①和②中转移的电子数相同时,产生的 和 的物质的量相同
【答案】C
【解析】A.NaO 中有离子键和非极性键,CaH 中只有离子键而不含非极性键,A错误;B.①中水的化
2 2 2
合价不发生变化,不涉及氧化还原反应,②中水发生还原反应,B错误;C.NaO 由Na+和 组成.
2 2
阴、阳离子个数之比为1∶2,CaH 由Ca2+和H-组成,阴、阳离子个数之比为2∶1,C正确;D.①中每生成1
2
个氧气分子转移2个电子,②中每生成1个氢气分子转移1个电子,转移电子数相同时,生成氧气和氢气
的物质的量之比为1∶2,D错误;故选C。
25.(2023·浙江卷)物质的性质决定用途,下列两者对应关系不正确的是
A.铝有强还原性,可用于制作门窗框架
B.氧化钙易吸水,可用作干燥剂
C.维生素C具有还原性,可用作食品抗氧化剂
D.过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂
【答案】A
【解析】A.铝用于制作门窗框架,利用了铝的硬度大、密度小、抗腐蚀等性质,而不是利用它的还原
性,A不正确;B.氧化钙易吸水,并与水反应生成氢氧化钙,可吸收气体中或密闭环境中的水分,所以
可用作干燥剂,B正确;C.食品中含有的Fe2+等易被空气中的氧气氧化,维生素C具有还原性,且对人体
无害,可用作食品抗氧化剂,C正确;D.过氧化钠能与二氧化碳反应生成氧气,同时可吸收人体呼出的
二氧化碳和水蒸气,可作潜水艇中的供氧剂,D正确;故选A。
26.(2022·山东卷)实验室用基准 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐
酸滴定 标准溶液。下列说法错误的是A.可用量筒量取 标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制 标准溶液
C.应选用烧杯而非称量纸称量 固体
D.达到滴定终点时溶液显橙色
【答案】A
【分析】选甲基橙为指示剂,并以盐酸滴定NaCO 标准溶液,则应将NaCO 标准溶液置于锥形瓶中,将
2 3 2 3
待测盐酸置于酸式滴定管中,滴定终点时溶液由黄色变为橙色。
【解析】A.量筒的精确度不高,不可用量筒量取NaCO 标准溶液,应该用碱式滴定管或移液管量取
2 3
25.00 mL Na CO 标准溶液置于锥形瓶中,A说法错误;B.NaCO 溶液显碱性,盛放NaCO 溶液的容器
2 3 2 3 2 3
不能用玻璃塞,以防碱性溶液腐蚀玻璃产生有粘性的硅酸钠溶液而将瓶塞粘住,故应选用配带塑料塞的容
量瓶配制NaCO 标准溶液,B说法正确;C.NaCO 有吸水性且有一定的腐蚀性,故应选用烧杯而非称量
2 3 2 3
纸称量NaCO 固体,C说法正确;D.NaCO 溶液显碱性,甲基橙滴入NaCO 溶液中显黄色,当滴入最
2 3 2 3 2 3
后一滴盐酸时,溶液由黄色突变为橙色且半分钟之内不变色即为滴定终点,故达到滴定终点时溶液显橙
色,D说法正确;综上所述,本题选A。
27.(2022·浙江卷)下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏
【答案】A
【解析】A.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料,可用于制造晶体管、集成电
路等,而二氧化硅常用于制造光导纤维,A错误;B.钠的焰色反应为黄色,可用作透雾能力强的高压钠
灯,B正确;C.耐高温材料应具有高熔点的性质,氧化铝熔点高,可用作耐高温材料,C正确;D.石灰
石的主要成分为碳酸钙,石灰石-石膏法脱硫过程中发生反应:CaCO CaO+CO ↑,
3 2
SO +CaCO =CaSO +CO ,2CaSO+O =2CaSO ,得到了石膏,D正确;答案选A。
2 3 3 2 3 2 4
28.(2022·广东卷)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
【答案】B
【解析】A.向氢氧化钠溶液中通入过量的二氧化碳,碱可以转化成酸式盐,离子方程式为:CO+OH-=
2
,故A错误;B.氯气通入NaOH溶液中可以生成氯化钠和次氯酸钠两种盐,其离子方程式为:Cl+2OH-=Cl-+ClO-+H O,故B正确;C.钠的过氧化物为NaO,可以和水反应生成氢氧化钠,但在离子
2 2 2 2
方程式里NaO 不能拆成离子,故C错误;D.硅酸钠溶于水,在离子方程式里要写成离子,故D错误;
2 2
故选B。
29.(2022·全国卷)生活中处处有化学,下列叙述正确的是
A.HB铅笔芯的成分为二氧化铅 B.碳酸氢钠可做食品膨松剂
C.青铜和黄铜是不同结构的单质铜 D.焰火中红色来源于钠盐灼烧
【答案】B
【解析】A.铅笔芯的主要成分为石墨,不含二氧化铅,A错误;B.碳酸氢钠不稳定,受热易分解产生二
氧化碳,能使面团松软,可做食品膨松剂,B正确 ;C.青铜是在纯铜(紫铜)中加入锡或铅的合金,黄铜
为是由铜和锌所组成的合金,两者均属于混合物,不是铜单质,C错误;D.钠元素灼烧显黄色,D错
误;故选B。
30.(2021·海南卷)一次性鉴别等浓度的 、 、 三种溶液,下列方法不可行的是
A.测定 B.焰色试验
C.滴加 溶液 D.滴加饱和 溶液,微热
【答案】C
【解析】A. 溶液显中性, 溶液显酸性, 溶液显碱性,故可以用测定pH的方法鉴
别,故A正确;B. 的焰色试验中现象为透过蓝色钴玻璃为紫色, 的焰色试验中无现象,
的焰色试验中现象为黄色,故可以用焰色试验的方法鉴别,故B正确;C. 、 、
中只有 能与 反应有现象,故 和 不能鉴别,故C错误;D.2 +
CaCl2+2NH +2H O有刺激性气味气体产生, + =CaCO +2NaOH有白色沉淀产
3 2 3
生,而 不反应无现象,故可以鉴别,故D正确;故选C。