文档内容
第 03 讲 化学平衡常数及其相关计算
目录
01 考情透视·目标导航.........................................................................................................................2
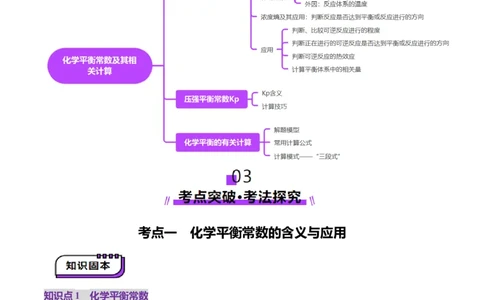
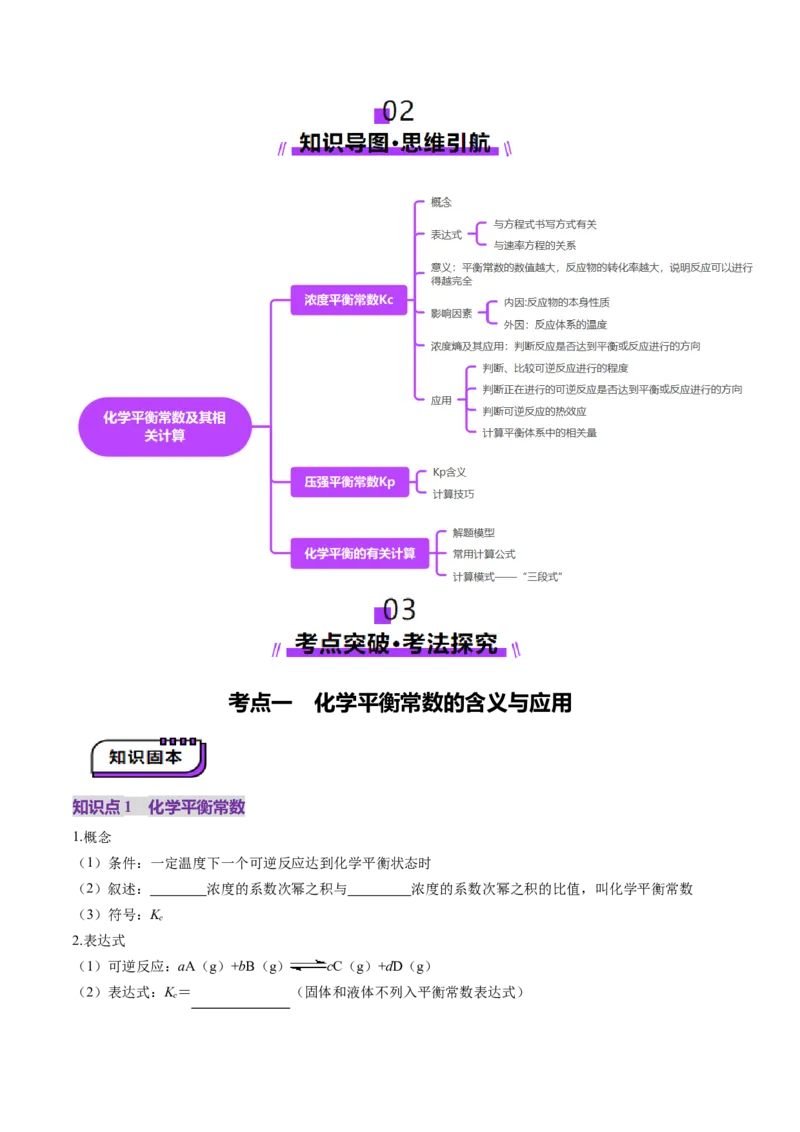
02 知识导图·思维引航.........................................................................................................................3
03 考点突破·考法探究.........................................................................................................................3
考点一 化学平衡常数的含义与应用.........................................................................................3
知识点1 化学平衡常数...........................................................................................................3
知识点2 化学平衡常数的应用...............................................................................................5
考向1 考查化学平衡常数的含义...........................................................................................6
考向2 考查化学平衡常数的应用...........................................................................................7
考点二 有关化学平衡的计算.....................................................................................................9
知识点1 三段式计算模式.......................................................................................................9
知识点2 有关化学平衡计算方法和技巧.............................................................................10
考向1 考查平衡常数的计算.................................................................................................12
考向2 考查转化率的计算.....................................................................................................14
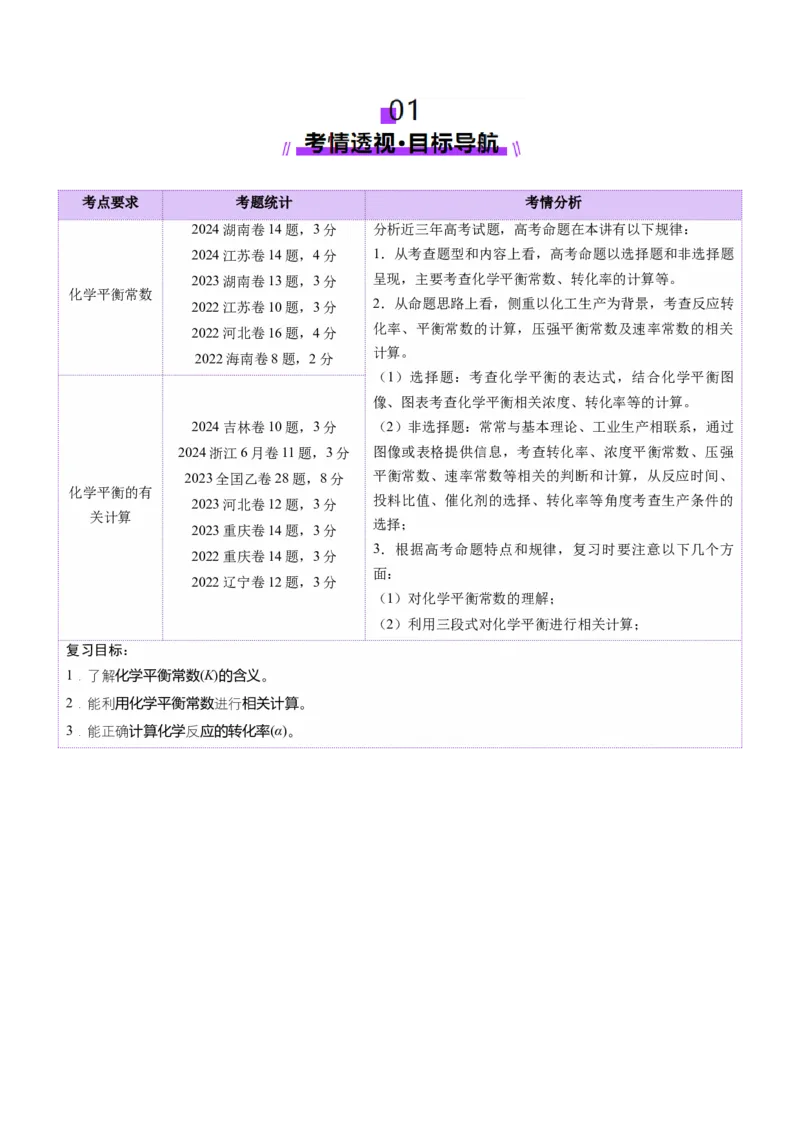
04 ........................................................................................................................................................16考点要求 考题统计 考情分析
2024湖南卷14题,3分 分析近三年高考试题,高考命题在本讲有以下规律:
2024江苏卷14题,4分 1.从考查题型和内容上看,高考命题以选择题和非选择题
2023湖南卷13题,3分 呈现,主要考查化学平衡常数、转化率的计算等。
化学平衡常数
2022江苏卷10题,3分 2.从命题思路上看,侧重以化工生产为背景,考查反应转
化率、平衡常数的计算,压强平衡常数及速率常数的相关
2022河北卷16题,4分
计算。
2022海南卷8题,2分
(1)选择题:考查化学平衡的表达式,结合化学平衡图
像、图表考查化学平衡相关浓度、转化率等的计算。
2024吉林卷10题,3分 (2)非选择题:常常与基本理论、工业生产相联系,通过
2024浙江6月卷11题,3分 图像或表格提供信息,考查转化率、浓度平衡常数、压强
2023全囯乙卷28题,8分 平衡常数、速率常数等相关的判断和计算,从反应时间、
化学平衡的有
投料比值、催化剂的选择、转化率等角度考查生产条件的
2023河北卷12题,3分
关计算
选择;
2023重庆卷14题,3分
3.根据高考命题特点和规律,复习时要注意以下几个方
2022重庆卷14题,3分
面:
2022辽宁卷12题,3分
(1)对化学平衡常数的理解;
(2)利用三段式对化学平衡进行相关计算;
复习目标:
1.了解化学平衡常数(K)的含义。
2.能利用化学平衡常数进行相关计算。
3.能正确计算化学反应的转化率(α)。考点一 化学平衡常数的含义与应用
知识点1 化学平衡常数
1.概念
(1)条件:一定温度下一个可逆反应达到化学平衡状态时
(2)叙述: 浓度的系数次幂之积与 浓度的系数次幂之积的比值,叫化学平衡常数
(3)符号:K
c
2.表达式
(1)可逆反应:aA(g)+bB(g) cC(g)+dD(g)
(2)表达式:K= (固体和液体不列入平衡常数表达式)
c(3)单位:
(4)平衡常数与书写方式的关系
①正逆反应平衡常数的关系是:K ·K =
c正 c逆
②化学计量数变成n倍,平衡常数变为 倍
③反应③=反应①+反应②,则:△H= ,K =
3 3
④反应③=反应①-反应②,则:△H= ,K =
3 3
1
⑤反应③=a×反应①-b ×反应②,则:△H= ,K =
3 3
(5)速率常数和平衡常数的关系
A.基元反应:a A(g)+b B(g) c C(g)+d D(g)
B.速率方程
①抽象化速率方程:笼统的正逆反应速率
v =k ·ca(A)·cb(B)、v =k ·cc(C)·cd(D)
正 正 逆 逆
②具体化速率方程:以具体物质表示的正逆反应速率
v =k ·ca(A)·cb(B)、v =k ·cc(C)·cd(D)
A正 正 C逆 逆
C.速率常数和平衡常数的关系
①抽象化:平衡条件 , = =
①具体化:平衡条件 , = × =
(4)升温对k 、k 的影响
正 逆
①放热反应:K值 ;k 值 ,k 值 , 变化更大
正 逆
②吸热反应:K值 ;k 值 ,k 值 , 变化更大
正 逆
3.意义
(1)对于同类型反应,平衡常数的大小反映了化学反应可能进行的 ;
(2)平衡常数的数值越 ,反应物的转化率 ,说明反应可以进行得越完全。
<10-
K值 10-5~105 >105
5
反应程
度
4.影响因素
(1)内因:反应物的 (某一具体反应)。
{放热反应:K值减小
¿¿¿¿
(2)外因:反应体系的 ,升高温度 。5.浓度熵:Q=
c
(1)浓度为任意时刻的浓度
(2)意义:Q越大,反应 向进行的程度越大
(3)应用:判断反应是否达到平衡或反应进行的方向
①Q>K,反应 向进行,v v
c 正 逆
②Q=K,反应达到平衡状态,v v
c 正 逆
③Q<K,反应 向进行,v v
c 正 逆
6.压强平衡常数K
p
(1)K 含义:在化学平衡体系中,用各气体物质的 替代浓度计算的平衡常数叫压强平衡常数。
p
(2)计算技巧:
第一步,根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度;
第二步,计算各气体组分的 或 ;
第三步,根据分压计算公式求出各气体物质的分压,某气体的分压= ;
第四步,根据平衡常数计算公式代入计算。例如,N(g)+3H(g) 2NH (g),压强平衡常数表达式为K
2 2 3 p
=。
知识点2 化学平衡常数的应用
1.判断、比较可逆反应进行的程度
一般来说,一定温度下的一个具体的可逆反应:
K值 正反应进行的程度 平衡时生成物浓度 平衡时反应物浓度 反应物转化率
越大
越小
【特别提醒】K值大小与反应程度的关系
K <10-5 10-5~105 >105
反应程度 很难进行 反应可逆 反应接近完全
2.判断正在进行的可逆反应是否达到平衡或反应进行的方向
对于可逆反应:mA(g)+nB(g) pC(g)+qD(g),浓度商Q=,则将浓度商和平衡常数作比较可判断可逆
c
反应所处的状态。
3.判断可逆反应的热效应
(1):;。
(2):;。
4.计算平衡体系中的相关量
根据相同温度下,同一反应的平衡常数不变,计算反应物或生成物的 、 、 等。
注意:计算时注意问题
①平衡量必须为平衡时的浓度②等体反应:可以用平衡时的物质的量代替平衡时的浓度
③恒压条件下:先计算平衡体积,再算平衡常数
【特别提醒】(1)计算平衡常数利用的是物质的平衡浓度,而不是任意时刻浓度,也不能用物质的量。
(2)固体和纯液体的浓度视为恒定常数,不出现在平衡常数表达式中。
如C(s)+HO(g) CO(g)+H(g),达到平衡后的K=。
2 2
(3)催化剂能加快化学反应速率,但对化学平衡无影响,也不会改变平衡常数的大小。
(4)一般K>105时,认为该反应基本进行完全;K<10-5时,一般认为该反应很难进行;而K在10-5~105反
应被认为是典型的可逆反应。
考向1 考查化学平衡常数的含义
例1(2024·江苏扬州·模拟预测)“碳达峰·碳中和”是我国社会发展的重大战略之一,CH 还原CO 是实
4 2
现“双碳”经济的有效途径之一,相关主要反应有:
Ⅰ:CH(g)+CO (g) 2CO(g)+2H(g) ΔH=+247kJ/mol,K
4 2 2 1 1
Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=+41kJ/mol,K
2 2 2 2 2
下列说法正确的是
A.反应Ⅰ的平衡常数K=
1
B.反应Ⅱ的ΔS<0
C.有利于提高CO 平衡转化率的条件是高温低压
2
D.该工艺每转化0.2mol CO 可获得0.4molCO
2
【易错提醒】平衡常数与书写方式的关系
①正逆反应平衡常数的关系是:K ·K =1;
c正 c逆
②化学计量数变成n倍,平衡常数变为n次方倍;
③反应③=反应①+反应②,则:△H=△H+△H,K =K ·K ;
3 1 2 3 1 2
④反应③=反应①-反应②,则:△H=△H-△H,K = ;
3 1 2 3
1 1
⑤反应③=a×反应①-b ×反应②,则:△H=a△H-b△H,K = ;
3 1 2 3
⑥固体和液体不列入平衡常数表达式。
【变式训练1】(23-24高三下·江苏连云港·期中)以CuZnOAl O 作催化剂发生反应2CHCHO(g)+H O(g)
2 3 3 2
C HOH(g)+CH COOH(g) ΔH<0,下列说法正确的是
2 5 3A.该反应的平衡常数K=
B.反应物的键能总和小于生成物的键能总和
C.该反应中每消耗1 mol H O(g),转移电子数约为6.02×1023
2
D.将C HOH移出一段时间后,v 增大
2 5 正
【变式训练2】(2024·江苏南京·一模) 含氯化合物在生产生活中应用广泛。舍勒发现将软锰矿和浓盐酸
混合加热可产生氯气,该方法仍是当今实验室制备氯气的主要方法之一,工业上以 为原料可制得
、 、 、 和 等。在催化剂 作用下,通过氧气直接氧化氯化氢制备氯气。该反应为
可逆反应,热化学方程式为 。对于反应
,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.其他条件相同,增大 , 的转化率减小
D.上述反应中消耗 ,转移电子的数目为
考向2 考查化学平衡常数的应用
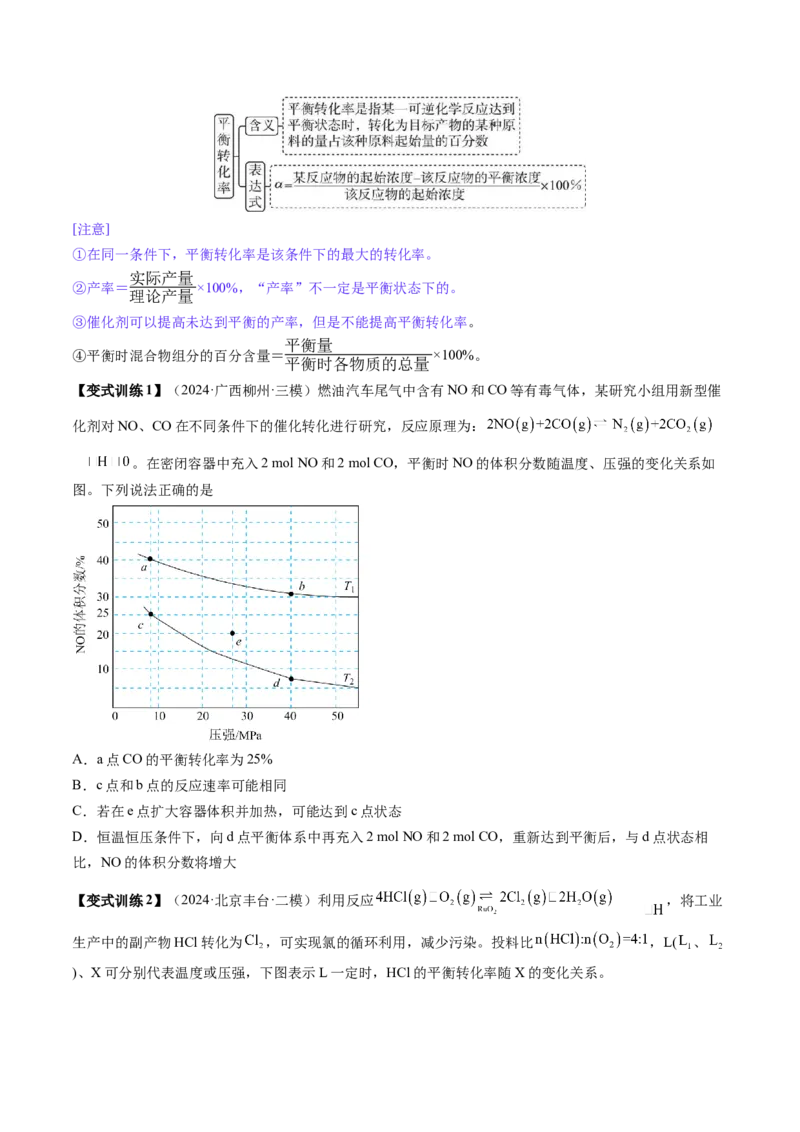
例2(23-24高三下·海南省直辖县级单位·开学考试) 转化为高附加值的产品是应对气候变化和能源高
速消耗的有效措施,反应 可实现 的资源化
利用,下列说法正确的是
A.温度升高, 增大, 减小
B.加入催化剂,反应速率加快,可提高 产率
C.恒温恒容,增大压强, 转化率增大,平衡常数增大
D.当密闭容器中二氧化碳的体积分数不变时说明该反应达到化学平衡状态
【易错提醒】应用化学平衡常数时应注意的四个问题
(1)化学平衡常数是在一定温度下一个反应本身固有的内在性质的定量体现。
(2)化学平衡常数只与温度有关,与反应物或生成物的浓度无关。
(3)反应物或生成物中有固体或纯液体存在时,其浓度可看作一个常数,而不计入平衡常数表达式中。
(4)化学平衡常数是指某一具体反应的平衡常数。若反应方向改变,则平衡常数改变;若化学方程式中
各物质的化学计量数等倍扩大或缩小,尽管是同一反应,平衡常数也会改变。
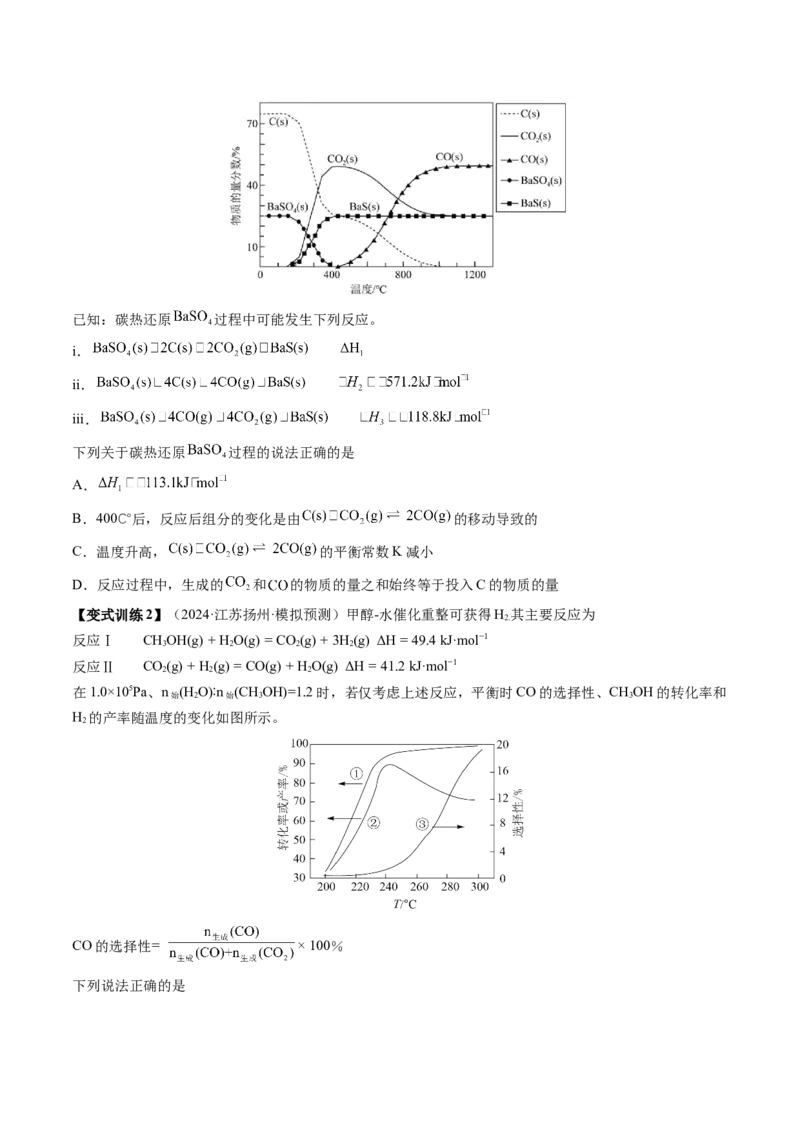
【变式训练1】(23-24高三下·重庆荣昌·开学考试)工业上利用碳热还原 制得 。进而生产各种
含钡化合物,温度对反应后组分的影响如图。已知:碳热还原 过程中可能发生下列反应。
i.
ii.
iii.
下列关于碳热还原 过程的说法正确的是
A.
B.400℃后,反应后组分的变化是由 的移动导致的
C.温度升高, 的平衡常数K减小
D.反应过程中,生成的 和 的物质的量之和始终等于投入C的物质的量
【变式训练2】(2024·江苏扬州·模拟预测)甲醇-水催化重整可获得H 其主要反应为
2.
反应Ⅰ CHOH(g) +HO(g) =CO(g)+3H(g) ΔH= 49.4 kJ·mol−1
3 2 2 2
反应Ⅱ CO(g)+H(g)=CO(g) +HO(g) ΔH=41.2 kJ·mol−1
2 2 2
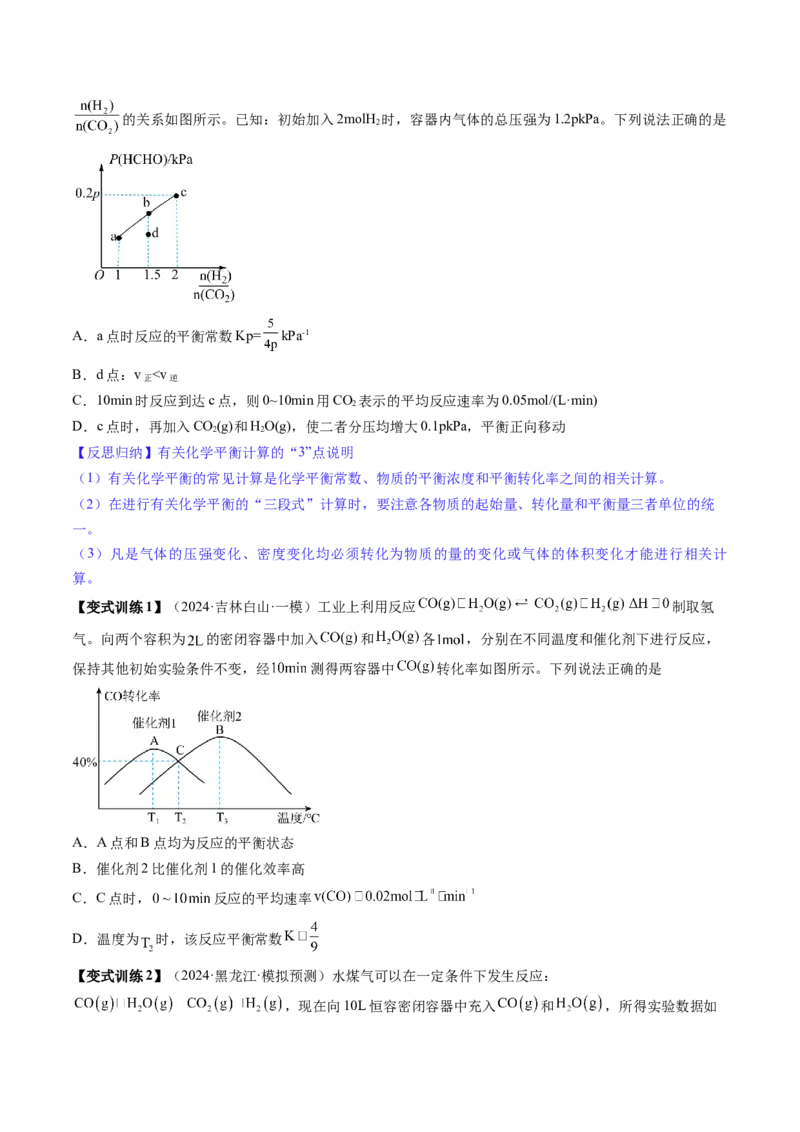
在1.0×105Pa、n (H O)∶n (CHOH)=1.2时,若仅考虑上述反应,平衡时CO的选择性、CHOH的转化率和
始 2 始 3 3
H 的产率随温度的变化如图所示。
2
CO的选择性= × 100%
下列说法正确的是A.一定温度下,增大 可提高CO的选择性
B.平衡时CHOH的转化率一定大于HO的转化率
3 2
C.图中曲线①表示平衡时H 产率随温度的变化
2
D.一定温度下,降低体系压强,反应Ⅰ的平衡常数增大
考点二 有关化学平衡的计算
知识点1 三段式计算模式
1.解题模型
2.“三段式”法思维建模
“三段式”法是有效解答化学平衡计算题的“万能钥匙”。解题时,要注意清楚条理地列出起始量、转化
量、平衡量,按题目要求进行计算,同时还要注意单位的统一。
1)分析三个量:起始量、变化量、平衡量。
2)明确三个关系
(1)对于同一反应物,起始量 变化量=平衡量。
(2)对于同一生成物,起始量 变化量=平衡量。
(3)各转化量之比等于各 的化学计量数之比。
3)计算方法:三段式法
化学平衡计算模式:对以下反应mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量浓度分别为a
mol/L、b mol/L,达到平衡后消耗A的物质的量浓度为mx mol/L。
mA(g)+nB(g) pC(g)+qD(g)
起始量(mol/L) a b 0 0
变化量(mol/L) mx nx px qx
平衡量(mol/L) a-mx b-nx px qx
则有①平衡常数:K= 。②A的平衡浓度:c(A)= mol·L-1。
③A的转化率:α(A)= ×100%,α(A)∶α(B)=∶=。
④A的体积分数:φ(A)= ×100%。
⑤平衡压强与起始压强之比:= 。
⑥混合气体的平均密度(混)= g·L-1。
⑦混合气体的平均摩尔质量= g·mol-1。
⑧生成物的产率:实际产量(指生成物)占理论产量的百分数。一般来讲,转化率越大,原料利用率越高,
产率越大。产率=×100%。
知识点2 有关化学平衡计算方法和技巧
1.化学平衡常数的计算
(1)根据化学平衡常数表达式计算
(2)依据化学方程式计算平衡常数
①同一可逆反应中,K ·K = 。
正 逆
②同一方程式中的化学计量数等倍扩大或缩小n倍,则新平衡常数K′与原平衡常数K间的关系是K′= 或
K′= 。
③几个可逆反应方程式相加,得总方程式,则总反应的平衡常数等于 。
④水溶液中进行的反应,必须拆成 再计算平衡常数。
2.转化率的计算
转化率(α)=×100%
3.常用的气体定律——气体状态方程:
条件 公式 文字叙述
同温同压
同温同容
同温同压同质量
4.压强平衡常数的计算技巧
(1)步骤
第一步,根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度;
第二步,计算各气体组分的物质的量分数或体积分数;
第三步,根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压强×该气体的体积分数(或物
质的量分数);
第四步,根据平衡常数计算公式代入计算。
例如,N(g)+3H(g) 2NH (g),压强平衡常数表达式为K =。
2 2 3 p
(2)计算K 的答题模板
p
计算K 的两套模板[以N(g)+3H(g) 2NH (g)为例]
p 2 2 3
模板1:N(g) + 3H(g) 2NH (g)(平衡时总压为p)
2 2 3 0n(始) 1 mol 3 mol 0
Δn 0.5 mol 1.5 mol 1 mol
n(平) 0.5 mol 1.5 mol 1 mol
p(X) p p p
0 0 0
K =
p
模板2:刚性反应器中
N(g)+ 3H(g) 2NH (g)
2 2 3
p(始) p 3p 0
0 0
Δp p′ 3p′ 2p′
p(平) p-p′ 3p-3p′ 2p′
0 0
K =
p
5.转化率大小变化分析技巧
判断反应物转化率的变化时,不要把平衡正向移动与反应物转化率提高等同起来,要视具体情况而定。常
见有以下几种情形:
反应类型 条件的改变 反应物转化率的变化
恒容时只增加反
反应物A的转化率减小,反应物B的转化率增大
应物A的用量
恒温恒压条件下 反应物转化率
有多种反应物的可逆 反应物A和B的转化率
m+n>p+q
反应:mA(g)+nB(g) 同等倍数地增大 均
pC(g)+qD(g) 反应物A、B的 恒温恒容 反应物A和B的转化率
m+n<p+q
量 条件下 均
反应物A和B的转化率
m+n=p+q
均
恒温恒压
只有一种反应物的可 反应物转化率
条件下
逆反应:mA(g) 增加反应物A的
m>n+p 反应物A的转化率
用量 恒温恒容
m<n+p 反应物A的转化率
nB(g)+pC(g) 条件下
m=n+p 反应物A的转化率
考向1 考查平衡常数的计算
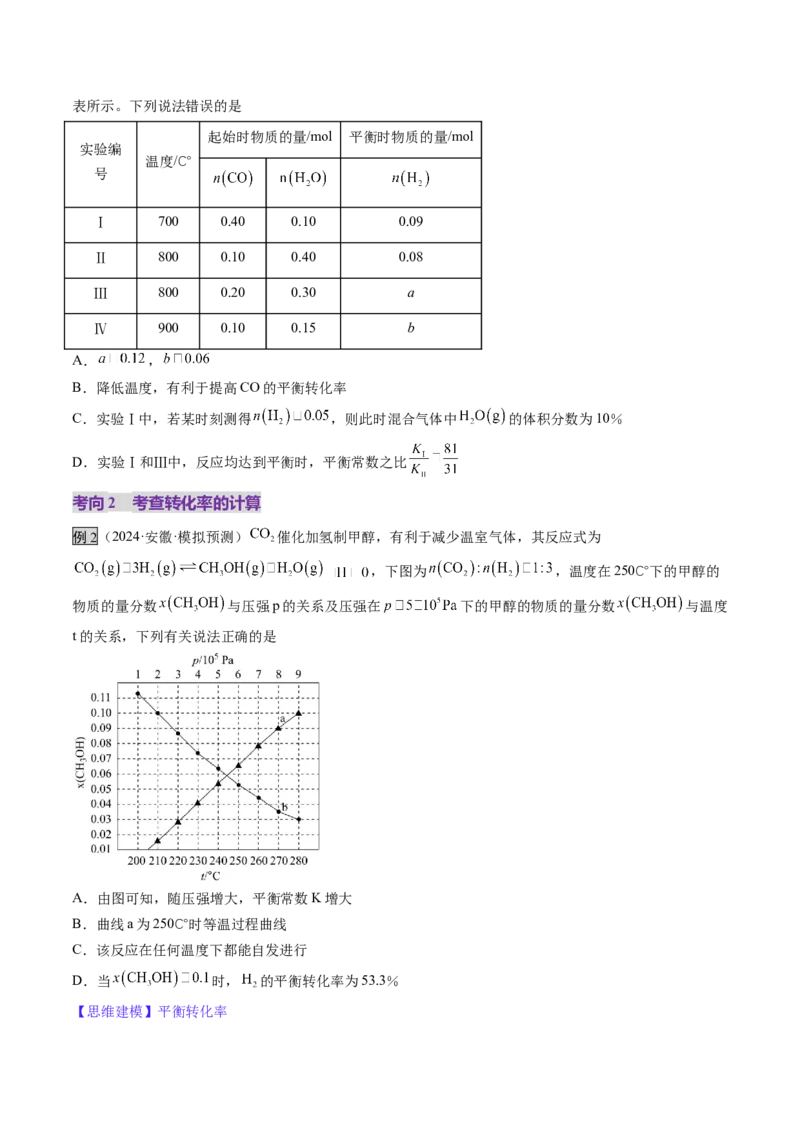
例1(23-24高三上·辽宁·期末)T℃时,向容积为2L的刚性容器中充入1molCO 和一定量的H 发生反
2 2
应:CO(g)+2H(g) HCHO(g)+H0(g),达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始
2 2 2的关系如图所示。已知:初始加入2molH 时,容器内气体的总压强为1.2pkPa。下列说法正确的是
2
A.a点时反应的平衡常数Kp= kPa-1
B.d点:v