文档内容
第三章 金属及其化合物
第08讲 铝、镁及其重要化合物
完卷时间:50分钟
可能用到的相对原子质量:O 16 Fe 56
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·广东惠州市·高三一模)下列关于物质的制备、生产的说法正确的是
A.用镁粉和空气反应制备
B.工业制取金属铝:电解熔融
C.实验室制取NH:可用浓硫酸干燥
3
D. 溶液与浓 混合制备HI
2.(2020·河北张家口市·高三一模)下列物质的用途描述正确的是
A.碳酸钠在医疗上是治疗胃酸过多的一种药剂
B.镁燃烧时发出耀眼的白光,可以用镁来制造照明弹和焰火等
C.明矾可以消毒杀菌,常用于净水
D.磁性氧化铁可用作红色油漆和涂料
3.(2021·江苏高三三模)下列氧化物的性质与用途具有对应关系的是
A. 具有漂白性,可用作溴蒸气的吸收剂
B.CaO具有碱性氧化物的性质,燃煤中加入CaO可以减少酸雨的形成
C. 是两性氧化物,可以用作防腐涂层
D.MgO熔融状态下能导电,可以用作耐火材料
4.(2020·浙江嘉兴市·高三一模)下列说法不正确的是
A.SO 使品红、溴水褪色的原因是它有漂白性
2
B.Mg着火不能用泡沫灭火器灭火
C.Al(OH) 胶体具有很强的吸附性,可以用来净水
3
D.新制Cu(OH) 悬浊液可用来检验牙膏中甘油的存在
2
5.(2020·广东中山市·中山纪念中学高三二模)向物质的量浓度均为1mol/L的HCl、AlCl、MgC1、
3 2
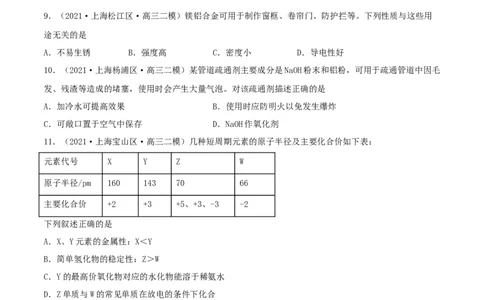
NHCl混合溶液中逐滴加入1mol/L的NaOH溶液,得到如图图像。下列有关说法正确的是 ( )
4A.沉淀的最大物质的量为2mol
B.c-d段会产生标况下22.4LNH
3
C.d-e段发生的反应为Al3++4OH-=AlO +2HO
2
D.滴加NaOH溶液过程中,微粒反应的先后顺序是H+、Al3+、Mg2+、NH 、Al(OH)
3
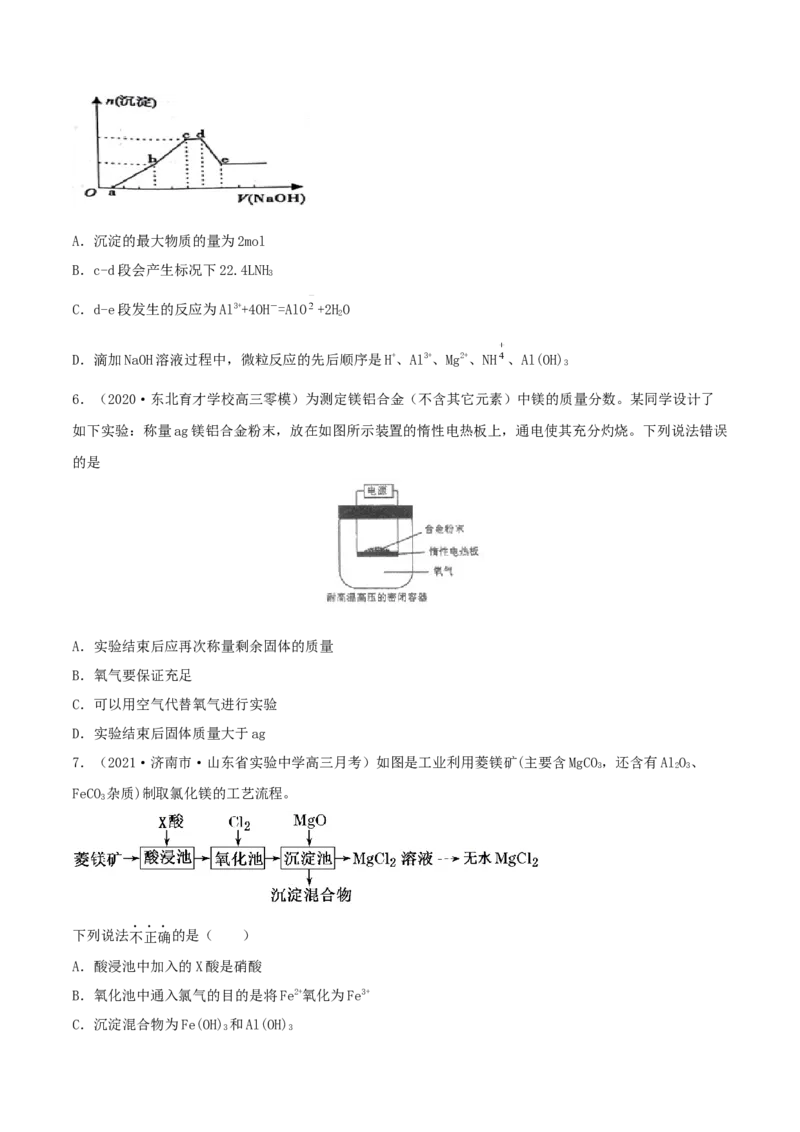
6.(2020·东北育才学校高三零模)为测定镁铝合金(不含其它元素)中镁的质量分数。某同学设计了
如下实验:称量ag镁铝合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧。下列说法错误
的是
A.实验结束后应再次称量剩余固体的质量
B.氧气要保证充足
C.可以用空气代替氧气进行实验
D.实验结束后固体质量大于ag
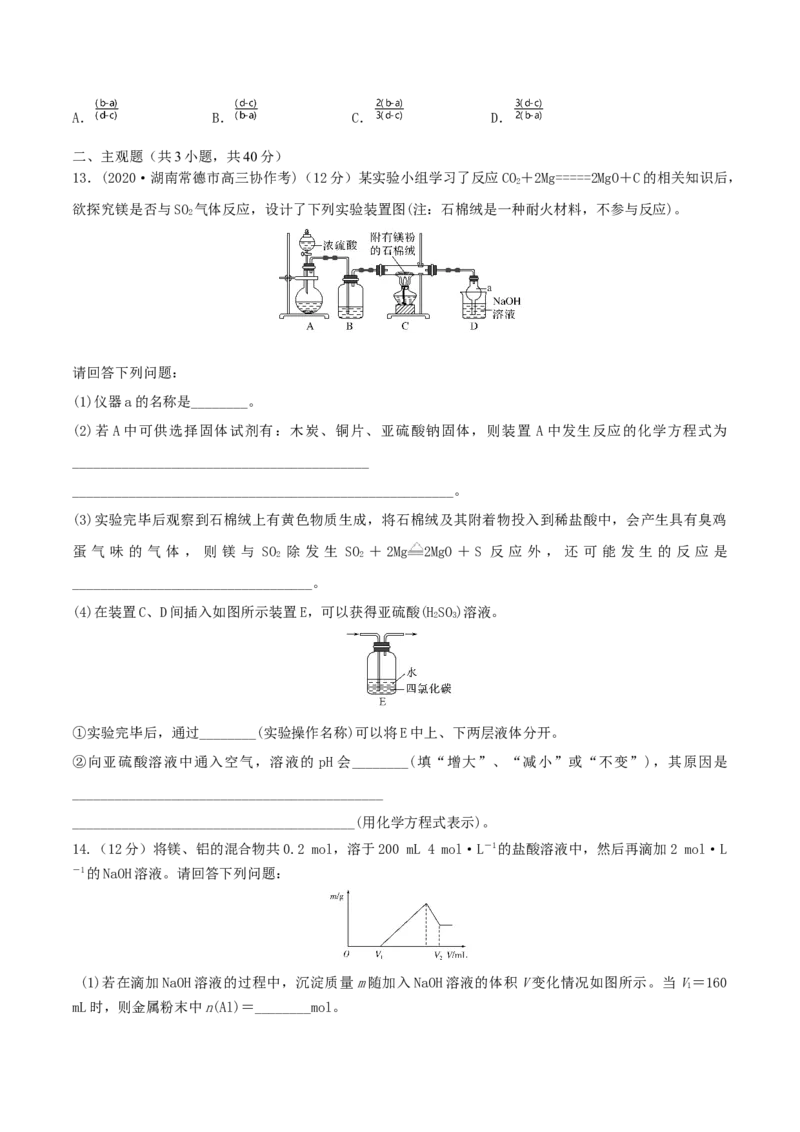
7.(2021·济南市·山东省实验中学高三月考)如图是工业利用菱镁矿(主要含MgCO,还含有AlO、
3 2 3
FeCO 杂质)制取氯化镁的工艺流程。
3
下列说法不正确的是( )
A.酸浸池中加入的X酸是硝酸
B.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
C.沉淀混合物为Fe(OH) 和Al(OH)
3 3D.在工业上常利用电解熔融氯化镁的方法制取金属镁
8.(2021·浙江宁波市·高三二模)下列说法正确的是
A. 、 、 都可以由相应单质在一定条件下直接化合得到
B.苯与浓溴水在光照下反应生成溴苯
C.硫在足量的氧气中燃烧生成
D.硫酸铝溶液中滴加过量氨水生成
9.(2021·上海松江区·高三二模)镁铝合金可用于制作窗框、卷帘门、防护拦等。下列性质与这些用
途无关的是
A.不易生锈 B.强度高 C.密度小 D.导电性好
10.(2021·上海杨浦区·高三二模)某管道疏通剂主要成分是NaOH粉末和铝粉,可用于疏通管道中因毛
发、残渣等造成的堵塞,使用时会产生大量气泡。对该疏通剂描述正确的是
A.加冷水可提高效果 B.使用时应防明火以免发生爆炸
C.可敞口置于空气中保存 D.NaOH作氧化剂
11.(2021·上海宝山区·高三二模)几种短周期元素的原子半径及主要化合价如下表:
元素代号 X Y Z W
原子半径/pm 160 143 70 66
主要化合价 +2 +3 +5、+3、-3 -2
下列叙述正确的是
A.X、Y元素的金属性:X<Y
B.简单氢化物的稳定性:Z>W
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.Z单质与W的常见单质在放电的条件下化合
12.(2010·上海浦东新区·高三二模)向用盐酸酸化的MgCl、FeCl 混合溶液中逐滴滴入NaOH(aq),生
2 3
成沉淀的质量与滴入NaOH(aq)的体积关系如图。原混合溶液中MgCl 与FeCl 的物质的量之比为
2 3A. B. C. D.
二、主观题(共3小题,共40分)
13.(2020·湖南常德市高三协作考)(12分)某实验小组学习了反应CO+2Mg=====2MgO+C的相关知识后,
2
欲探究镁是否与SO 气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
2
请回答下列问题:
(1)仪器a的名称是________。
(2)若A中可供选择固体试剂有:木炭、铜片、亚硫酸钠固体,则装置 A中发生反应的化学方程式为
__________________________________________
______________________________________________________。
(3)实验完毕后观察到石棉绒上有黄色物质生成,将石棉绒及其附着物投入到稀盐酸中,会产生具有臭鸡
蛋 气 味 的 气 体 , 则 镁 与 SO 除 发 生 SO + 2Mg 2MgO + S 反 应 外 , 还 可 能 发 生 的 反 应 是
2 2
__________________________________。
(4)在装置C、D间插入如图所示装置E,可以获得亚硫酸(HSO)溶液。
2 3
①实验完毕后,通过________(实验操作名称)可以将E中上、下两层液体分开。
②向亚硫酸溶液中通入空气,溶液的 pH会________(填“增大”、“减小”或“不变”),其原因是
____________________________________________
________________________________________(用化学方程式表示)。
14.(12分)将镁、铝的混合物共0.2 mol,溶于200 mL 4 mol·L-1的盐酸溶液中,然后再滴加2 mol·L
-1的NaOH溶液。请回答下列问题:
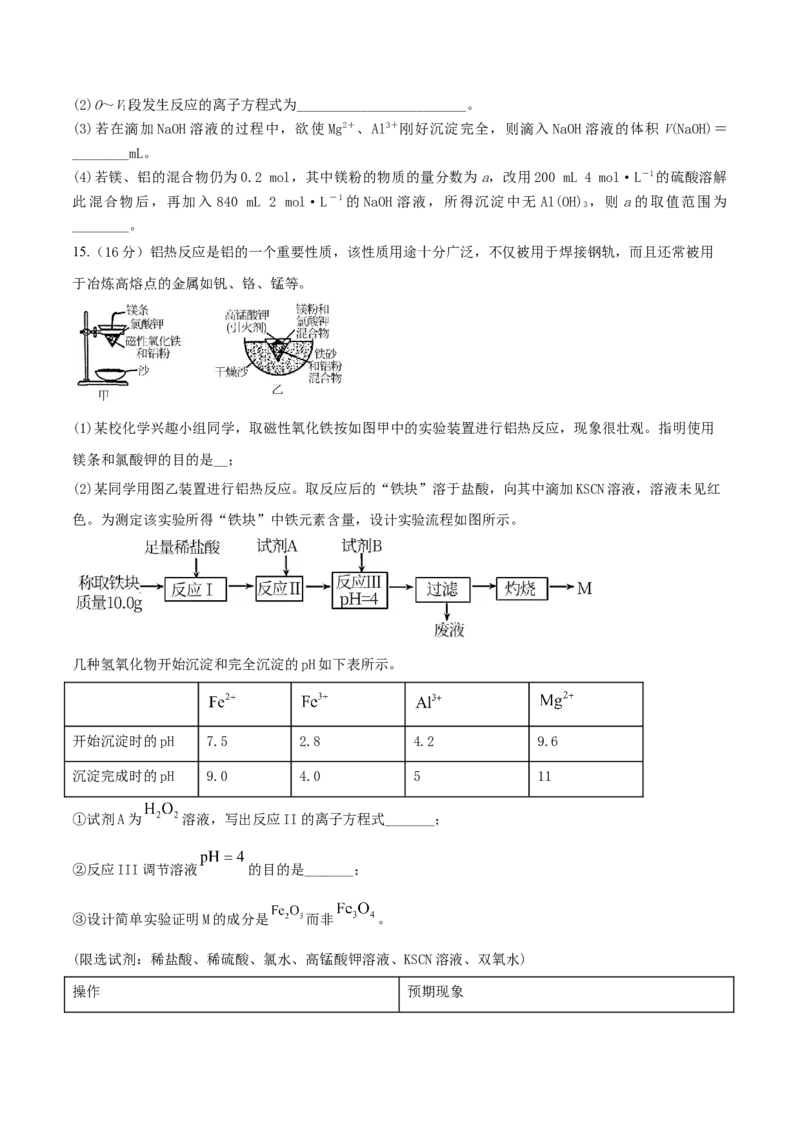
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示。当V=160
1
mL时,则金属粉末中n(Al)=________mol。(2)O~V段发生反应的离子方程式为________________________。
1
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=
________mL。
(4)若镁、铝的混合物仍为0.2 mol,其中镁粉的物质的量分数为a,改用200 mL 4 mol·L-1的硫酸溶解
此混合物后,再加入 840 mL 2 mol·L-1的 NaOH 溶液,所得沉淀中无 Al(OH) ,则a的取值范围为
3
________。
15.(16分)铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用
于冶炼高熔点的金属如钒、铬、锰等。
(1)某校化学兴趣小组同学,取磁性氧化铁按如图甲中的实验装置进行铝热反应,现象很壮观。指明使用
镁条和氯酸钾的目的是__;
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见红
色。为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示。
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
开始沉淀时的pH 7.5 2.8 4.2 9.6
沉淀完成时的pH 9.0 4.0 5 11
①试剂A为 溶液,写出反应II的离子方程式_______;
②反应III调节溶液 的目的是_______;
③设计简单实验证明M的成分是 而非 。
(限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水)
操作 预期现象取少量M固体于试管中,向其中加入_______,观察 固体完全溶解,溶液呈黄色
继续向上述溶液中滴入_______,振荡观察 _______;
④若最终红棕色粉未M的质量为12.0g,则该“铁块”的纯度是_______;