文档内容
第 09 讲 镁、铝及其重要化合物
考情分析 【夯基·必备基础知识梳理】
网络构建 知识点1 铝的性质
知识点2 氧化铝
考点一 镁及其化合物
知识点3 氢氧化铝
【夯基·必备基础知识梳理】
知识4 常见的铝盐
知识点1 镁的性质
知识5 数形结合与“铝三角”
知识点2 镁的氧化物MgO
【提升·必考题型归纳】
知识点3 镁的氢氧化物Mg(OH)
2
考向1 考查铝及其化合物的结构、性质及
知识点4 镁的其他化合物
其应用
【提升·必考题型归纳】
考向2 考查铝热反应及其应用
考向1 考查镁及其化合物的结构、性质及
考向3 考查铝及其化合物制备的工艺流程
应用
考向4 考查铝及其化合物与强酸、强碱反
考向2 考查镁及其化合物制备的工艺流程
应有关计算
考点二 铝及其化合物
真题感悟
考点要求 考题统计 考情分析
从近三年高考试题来看,铝、镁及其化合物的性
2023浙江1月卷12题,2分
镁、铝及其化 质与应用仍是高考的命题点。高考中一方面考查
2022浙江1月卷8题,2分
合物的性质与 铝及其化合物的性质在日常生活、生产中的应
2021浙江1月卷8题,2分
应用 用,另一方面以“铝三角”转化关系为载体,考
查图像分析和计算能力等。
预测新的一年高考可能会在选择题或化工流程图
镁、铝及其化 2023辽宁卷16题,3分 题中考查金镁、铝、氧化镁、氧化铝及氢氧化
合物的制备的 2022全国卷26题,1分 镁、氢氧化铝的性质与应用,如化学方程式或离
工艺流程 2021湖南卷6题,3分 子方程式的正误判断,或在化工流程图中考查铝
及其重要化合物的的转化或去除,题目难度中等
偏大。考点一 镁及其化合物
知识点1 镁的性质
1.镁的原子结构及存在
(1)镁的原子结构:镁元素在元素周期表中位于第______周期第______族,原子结构示意图为______。
镁是较活泼的金属,在金属活动性顺序中位于铝、锌、铁的前面。镁在化学反应中,能表现出较强的金属
性,即______电子的能力强,是常用的还原剂。
(2)镁的存在:镁蕴藏量丰富,在宇宙中含量第八,在地壳中含量丰度 2%。含镁矿物主要来自白云岩
[CaMg(CO )]、菱镁矿(MgCO )、水镁矿[Mg(OH) ]、光卤石(KCl·MgCl ·6H O)和橄榄石
3 2 3 2 2 2
[(Mg,Fe) SiO]等。海水、天然盐湖水也是含镁丰富的资源。
2 4
2.镁的物理性质
具有______色金属光泽的固体,密度、硬度均较小,熔点较低,有良好的导电、传热和延展性。
3.镁的化学性质
①与非金属反应
A.镁条在O 中燃烧,发出____________,生成______色固体物质,反应的化学方程式为2Mg+O 2MgO
2 2
B.镁条能与N 反应,化学方程式为____________________________________
2
【易错提醒】MgN 能与水剧烈反应生成Mg(OH) 沉淀,放出氨气,所以只能在干态下制取。
3 2 2
C.镁条能与Cl 反应,化学方程式为Mg+Cl MgCl
2 2 2
②与CO 反应:2Mg+CO 2MgO+C
2 2
③与HO反应:Mg+2HO Mg(OH) +H↑
2 2 2 2④与H+反应:Mg+2H+===Mg2++H↑
2
4.镁的用途
①制造信号弹和焰火;
②镁合金用于制造火箭、导弹和飞机的部件;
③氧化镁用于制耐高温材料;
④冶金工业上用作还原剂和脱氧剂。
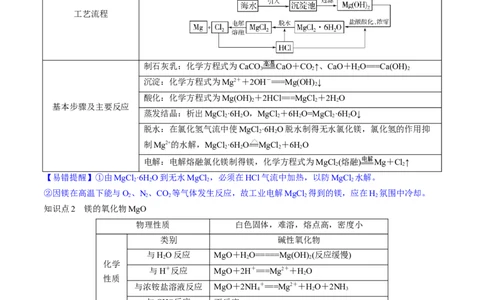
5.镁的工业制备——海水提镁
工艺流程
制石灰乳:化学方程式为CaCO CaO+CO↑、CaO+HO===Ca(OH)
3 2 2 2
沉淀:化学方程式为Mg2++2OH-===Mg(OH) ↓
2
酸化:化学方程式为Mg(OH) +2HCl===MgCl +2HO
2 2 2
基本步骤及主要反应
蒸发结晶:析出MgCl ·6H O,MgCl +6HO=MgCl ·6H O↓
2 2 2 2 2 2
脱水:在氯化氢气流中使MgCl ·6H O脱水制得无水氯化镁,氯化氢的作用抑
2 2
制Mg2+的水解,MgCl ·6H O MgCl +6HO
2 2 2 2
电解:电解熔融氯化镁制得镁,化学方程式为MgCl (熔融) Mg+Cl↑
2 2
【易错提醒】①由MgCl ·6H O到无水MgCl ,必须在HCl气流中加热,以防MgCl 水解。
2 2 2 2
②因镁在高温下能与O、N、CO 等气体发生反应,故工业电解MgCl 得到的镁,应在H 氛围中冷却。
2 2 2 2 2
知识点2 镁的氧化物MgO
物理性质 白色固体,难溶,熔点高,密度小
类别 碱性氧化物
与HO反应 MgO+HO=====Mg(OH) (反应缓慢)
2 2 2
化学
与H+反应 MgO+2H+===Mg2++HO
2
性质
与浓铵盐溶液反应 MgO+2NH +===Mg2++HO+2NH
4 2 3
与OH-反应 不反应
重要用途 制耐火、耐高温器材
知识点3 镁的氢氧化物Mg(OH)
2
物理性质 白色固体,难溶于水,溶解度小于碳酸镁
电离性 中强碱,悬浊液使酚酞变浅红:Mg(OH) Mg2++2OH-
2
与H+反应 Mg(OH) +2H+===Mg2++2HO
2 2
与OH-反应 不反应与铵盐浓溶液
Mg(OH) +2NH Cl===MgCl +2NH ·H O
2 4 2 3 2
反应
热稳定性 Mg(OH) =====MgO+HO
2 2
【易错提醒】碳酸镁水解生成氢氧化镁,反应的化学方程式:MgCO +HO Mg(OH) +CO↑,镁元素在
3 2 2 2
水垢中的存在形式是Mg(OH) 。
2
知识点4 镁的其他化合物
1.氯化镁:MgCl 可发生水解,由MgCl ·6H O制备MgCl 时,要在HCl的气氛中脱水,MgCl ·6H O
2 2 2 2 2 2
MgCl +6HO。
2 2
2.氮化镁:在水中剧烈水解,其反应的化学方程式为MgN +6HO===3Mg(OH) +2NH ↑,与酸反应生成
3 2 2 2 3
两种盐:MgN+8HCl===3MgCl +2NH Cl。
3 2 2 4
考向1 考查镁及其化合物的结构、性质及应用
例1.(2022·浙江舟山·舟山中学统考三模)关于镁的性质,下列说法错误的是
A.金属镁着火,可以用CO 灭火 B.镁是一种具有银白色光泽的金属
2
C.镁可以与热水反应生成氢气 D.镁可以与盐酸剧烈反应生成氢气
【变式训练】(2023·全国·高三专题练习)下列关于镁的叙述正确的是( )
A.镁在氮气中不能燃烧 B.镁与水不能反应释放出氢气
C.镁在氯气中燃烧会产生白烟 D.镁可在二氧化碳气体中燃烧,只生成白色固体
考向2 考查镁及其化合物制备的工艺流程
例2.(2022·浙江舟山·舟山中学校考模拟预测)菱镁矿(主要成分为 ,还含有少量 、 )制
备 的流程如图。下列说法正确的是
A.步骤(Ⅰ)得到的滤渣主要成分为 B.步骤(Ⅱ)发生的反应有2个
C.步骤(Ⅲ)操作可在蒸发皿中进行 D.滤液Y中加入足量氨水可得到白色沉淀
【变式训练】(2023·山东潍坊·统考二模)以水泥厂的废料(主要成分为 ,含少量
等杂质)为原料制备 的工艺流程如下:已知: 下列说法正确的是
A.为提高酸浸速率,可使用浓硫酸 B.试剂X可以是
C.滤渣为 D.操作a所得滤液经处理后可循环利用
考点二 铝及其化合物
知识点1 铝的性质
1.铝的原子结构和存在
(1)铝的原子结构:铝位于元素周期表第______周期______族,原子结构示意图为____________。
(2)铝的存在:自然界中的铝全部以______态的形式存在,地壳中铝含量位列金属第______位,以铝土
矿的形式存在,主要成分是Al O,含少量Fe O 和SiO。
2 3 2 3 2
2.金属铝的物理性质
银白色有金属光泽的固体,有良好的延展性、导电性和导热性等,密度较小,质地柔软。
3.金属铝的化学性质
①常温下,铝与氧气形成致密氧化膜,加热发生:4Al+3O 2Al O
2 2 3
②2Al+3Cl=====2AlCl
2 3
③常温铝遇氧化性酸——浓硫酸、浓硝酸钝化,与非氧化酸发生反应生成氢气:2Al+6H+===2Al3++3H↑
2
④2Al+2OH-+6HO===2[Al(OH) ]-+3H↑或2Al+2OH-+2HO===2AlO+3H↑
2 4 2 2 2
⑤2Al+Fe O=====2Fe+Al O
2 3 2 3
4.铝热反应
实验装置
①镁带剧烈燃烧,放出大量的热,并发出耀眼的白光,氧化铁与铝粉在较高
实验现象
温度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中
实验结论 高温下,铝与氧化铁发生反应,放出大量的热:Fe O+2Al=====2Fe+Al O
2 3 2 3
①制取熔点较高、活动性弱于Al的金属,如铁、铬、锰、钨等,
原理应用
3MnO +4Al=====3Mn+2Al O;
2 2 3②金属焊接,如野外焊接钢轨等
5.铝的制备和用途
(1)制备原理:铝土矿――→Al O――→Al,电解熔融Al O:2Al O(熔融)=====4Al+3O↑。
2 3 2 3 2 3 2
【特别提醒】工业上冶炼Al用电解熔融Al O 而不用AlCl 的原因:AlCl 是共价化合物,熔融态不导电。
2 3 3 3
(2)铝的用途:纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等,铝还用作还原剂。
6.铝与酸或碱反应生成H 的量的关系
2
2Al+6HCl===2AlCl +3H↑
3 2
2Al+2NaOH+6HO===2Na[Al(OH) ]+3H↑
2 4 2
(1)等质量的铝与足量的盐酸、氢氧化钠溶液分别反应:
①产生H 的物质的量相等。
2
②消耗H+、OH-的物质的量之比为n(H+)∶n(OH-)=3∶1。
(2)足量的铝分别与等物质的量的HCl和NaOH反应:
①消耗Al的物质的量之比为1∶3。
②生成H 的物质的量之比为1∶3。
2
(3)一定量的铝分别与一定量的盐酸、氢氧化钠溶液反应:
若产生氢气的体积比为<<1,则必定
①铝与盐酸反应时,铝过量而HCl不足。
②铝与氢氧化钠溶液反应时,铝不足而NaOH过量。
【易错警示】(1)常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝
与浓硫酸、浓硝酸不反应。
(2)铝与稀硝酸反应时生成的气体是NO而不是H。
2
(3)铝不但能与酸(H+)反应,还能够与碱溶液反应,表现为特殊性。2Al+2OH-+2HO===2AlO+3H↑。其
2 2
反应机理应为:铝先与强碱溶液中的水反应生成H 和Al(OH) ,然后Al(OH) 再与NaOH反应生成HO和
2 3 3 2
NaAlO ,反应中铝作还原剂,水作氧化剂,NaOH无电子得失。
2
(4)铝热反应是在高温状态下进行的置换反应,铝只能与排在金属活动性顺序其后的金属氧化物反应。铝不
能与MgO反应,铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
(5)Mg在CO 中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。同时镁与氮气反应
2
生成MgN。
3 2
知识点2 氧化铝
1.物理性质:______色固体,______溶于水,熔点很______。
2.化学性质——两性氧化物
①与酸反应:Al O+6H+===2Al3++3HO
2 3 2
②与碱反应:Al O+2OH-===2AlO+HO
2 3 2
【易错警示】这里的酸碱是指强酸、强碱。
3.用途:①作耐火材料②冶炼铝的原料
4.制备:Al(OH) 加热分解:2Al(OH) Al O+3HO
3 3 2 3 2知识点3 氢氧化铝
1.物理性质:______色______状______溶于水的固体,有较强的吸附性。
2.化学性质——两性氢氧化物
Al(OH) 的电离方程式为
3
(酸式电离)AlO+H++HO Al(OH) Al3++3OH-(碱式电离)
2 3
①与酸反应:Al(OH) +3H+===Al3++3HO
3 2
②与碱反应:Al(OH) +OH-===AlO+2HO
3 2
③受热分解:2Al(OH) Al O+3HO
3 2 3 2
【总结归纳】既能与酸反应又能与碱反应的物质:①弱酸的铵盐,如:NH HCO 、CHCOONH 、(NH )S
4 3 3 4 4 2
等;②弱酸的酸式盐,如:NaHCO 、KHS、NaHSO 等;③氨基酸;④铝及铝的氧化物、氢氧化物。
3 3
3.用途①制药 ②净水作用
4.制备Al(OH) 的三种方法
3
①向铝盐中加入氨水,离子方程式为Al3++3NH ·H O===Al(OH) ↓+3NH。
3 2 3
②NaAlO 溶液中通入足量CO,离子方程式为AlO+CO+2HO===Al(OH) ↓+HCO。
2 2 2 2 3
③可溶性铝盐和偏铝酸盐水溶液中混合:3AlO+Al3++6HO===4Al(OH) ↓。
2 3
知识4 常见的铝盐
1.明矾
1)硫酸铝钾是由两种不同的金属离子和一种酸根离子组成的复盐。
2)明矾的化学式为KAl(SO )·12H O,它是无色晶体,可溶于水,水溶液pH______7。
4 2 2
3)明矾净水的原理:明矾可以净水,其净水的原理是Al3++3HO Al(OH) (胶体)+3H+,Al(OH) 胶体
2 3 3
吸附水中的杂质形成沉淀而净水,使水澄清。
【易错警示】(1)AlO 、Al(OH) 是中学阶段接触的唯一与碱反应的金属氧化物和氢氧化物,经常应用到除
2 3 3
杂、计算题中,所以一定要熟记这两个反应的离子方程式。
(2)Al(OH) 具有两性,能溶于强酸(如盐酸)、强碱(如NaOH溶液),但不溶于弱酸(如HCO)、弱碱溶液(如
3 2 3
氨水)。
(3)由Al(OH) 的两式电离以及与酸和碱反应的离子方程式可知:与酸反应时相当于三元碱,与碱反应时相
3
当于一元酸。
(4)明矾净水只能除去水中的悬浮杂质,不能杀菌消毒,与氯气消毒原理不同。
2.AlCl 的结构与性质
3
1)AlCl 熔点、沸点都很低,且会升华,易溶于乙醚等有机溶剂,因为它是一种共价型化合物。熔化的
3
AlCl 不易导电,AlCl 晶体属于______晶体,故制备铝时不用AlCl 电解。
3 3 3
2) AlCl 的蒸汽或处于熔融状态时,都以AlCl 二聚分子形式存在。AlCl 二聚分子的形成原因是铝原子的
3 3 3
缺电子结构。AlCl 二聚分子结构示意图如图,其中每个铝原子均为sp 杂化,各有1条空的轨道,氯原子
3 3
处于以铝原子为中心的四面体的4个顶点位置。分子中有桥式氯原子存在,桥式氯原子在与其中一个铝原
子成σ键的同时,与另一个铝原子的空轨道发生配位,形成σ配位键。3)AlCl 能与Cl-生成AlCl -:AlCl (aq)+ Cl-(aq)=AlCl -(aq)
3 4 3 4
4)与Al Cl 类似,AlCl -、NaAlF、Al(OH) -中均存在配位键。
2 6 4 3 6 4
知识5 数形结合与“铝三角”
1.Al3+、Al(OH) 、[Al(OH) ]-之间的转化关系
3 4
(1)①Al3++3NH ·H O===Al(OH) ↓+3NH②Al3++3[Al(OH) ]-===4Al(OH) ↓③Al3++3OH-===Al(OH) ↓
3 2 3 4 3 3
(2)Al(OH) +3H+===Al3++3HO
3 2
(3)Al3++4OH-===[Al(OH) ]-
4
(4)[Al(OH)]-+4H+===Al3++4HO
4 2
(5)①[Al(OH) ]-+CO===Al(OH) ↓+HCO
4 2 3
②[Al(OH) ]-+H+===Al(OH) ↓+HO
4 3 2
(6)Al(OH) +OH-===[Al(OH) ]-
3 4
2.与Al(OH) 沉淀生成有关的图像分析
3
(1)可溶性铝盐溶液与NaOH溶液反应的图像(从上述转化关系中选择符合图像变化的离子方程式,下同)
可溶性铝盐溶液中逐滴加入NaOH NaOH溶液中逐滴加入可溶性铝盐
操作
溶液至过量 溶液至过量
立即产生白色沉淀→渐多→最多→ 无沉淀(有但即溶)→出现沉淀→渐
现象
渐少→消失 多→最多→沉淀不消失
图像
方程式 AB:(1)③ AB:(3)
序号 BD:(6) BC:(1)②
(2)偏铝酸盐溶液与盐酸反应的图像
操作 偏铝酸盐溶液中逐滴加入稀盐酸至过量 稀盐酸中逐滴加入偏铝酸盐溶液至过量
现象 立即产生白色沉淀→渐多→最多→渐少 无沉淀→出现沉淀→渐多→最多→沉淀不→消失 消失
图像
方程
AB:(5)② AB:(4)
式
BC:(2) BC:(1)②
序号
(3)突破Al(OH) 沉淀图像三个秘诀
3
①明晰横、纵坐标含义,然后通过曲线变化特点分析反应原理。
②掌握Al3+、Al(OH) 、AlO三者之间的转化比例:
3
③明晰Al3+溶液中加碱(OH-)的几种常见变形图像,如:
图A中,n(H+)∶n(Al3+)=2∶1。
图B中,若已知原溶液中含有Mg2+。则可推出:
n(Mg2+)∶n(Al3+)=1∶1。
图C中,若已知原溶液中含有H+和Mg2+,则可推导出:n(H+)∶n(Al3+)∶n(Mg2+)=2∶1∶1。
3.铝三角的应用
(1)选择制备Al(OH) 的最佳途径
3
①由Al3+制备Al(OH) ,宜用Al3+与氨水反应:
3
Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②由NaAlO 制备Al(OH) 宜用CO 与AlO反应:
2 3 2
2HO+AlO+CO===Al(OH) ↓+HCO
2 2 3
③从节约原料角度,由Al制备Al(OH) ,宜用Al制备Al3+,Al制备AlO,然后将二者混合:
3
Al3++3AlO+6HO===4Al(OH) ↓
2 3
(2)有关离子共存问题
①与Al3+不能大量共存的(阴)离子有:OH-、AlO、HS-、SiO、CO、HCO、SO等。
②与AlO不能大量共存的(阳)离子有:H+、Al3+、NH、Fe2+、Fe3+等。③AlO与HCO因发生(相对)强酸制弱酸的反应而不能共存。
(3)分析离子反应顺序
①向含有Al3+、NH、H+的混合溶液中逐滴加入NaOH溶液,反应顺序是:Ⅰ.H++OH-===HO;Ⅱ.Al3+
2
+3OH-===Al(OH) ↓(若先与NH反应,则生成的NH ·H O又使Al3+沉淀且生成NH);Ⅲ.NH+OH-
3 3 2
===NH ·H O[若先溶解Al(OH) ,则产生的AlO又与NH反应生成沉淀];Ⅳ.Al(OH) +OH-===AlO+
3 2 3 3
2HO。
2
②向含有AlO、CO、OH-的混合溶液中逐滴加入盐酸,反应顺序是:Ⅰ.OH-+H+===HO;Ⅱ.AlO+H+
2
+HO===Al(OH) ↓(AlO比CO先反应);Ⅲ.CO+H+===HCO;Ⅳ.HCO+H+===CO ↑+HO[HCO比
2 3 2 2
Al(OH) 先反应];Ⅴ.Al(OH) +3H+===Al3++3HO。
3 3 2
(4)有关Al(OH) 的计算
3
1)求产物Al(OH) 的量
3
①当n(OH-)≤3n(Al3+)时,n[Al(OH) ]=n(OH-);
3
②当3n(Al3+)