文档内容
第四章 非金属及其化合物
第11讲 碳、硅及无机非金属材料(精讲)
【考情分析】
本讲内容在高考中碳、硅及其化合物的知识单独考查的题目较少。常与晶体结构、元素周期律、化学
方程式及化工流程相结合,重在考查考生创新思维以及理论联系实际的能力。题型以选择题、推断题为主,
难度适中。
【核心素养分析】
1.变化观念与平衡思想:根据碳、硅的结构,预测在一定条件下碳、硅及其化合物可能发生的化学变化。
2.科学态度与社会责任:关注与碳、硅有关的热点问题(如光导纤维、硅电池、半导体材料),形成可持
续发展的意识;知道碳、硅及其化合物对社会发展的重大贡献。
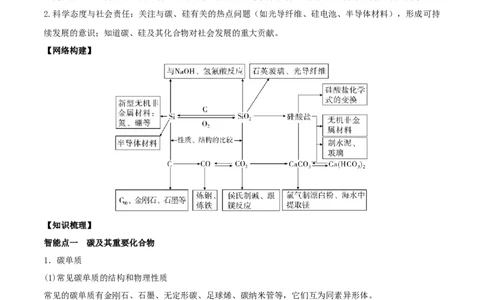
【网络构建】
【知识梳理】
智能点一 碳及其重要化合物
1.碳单质
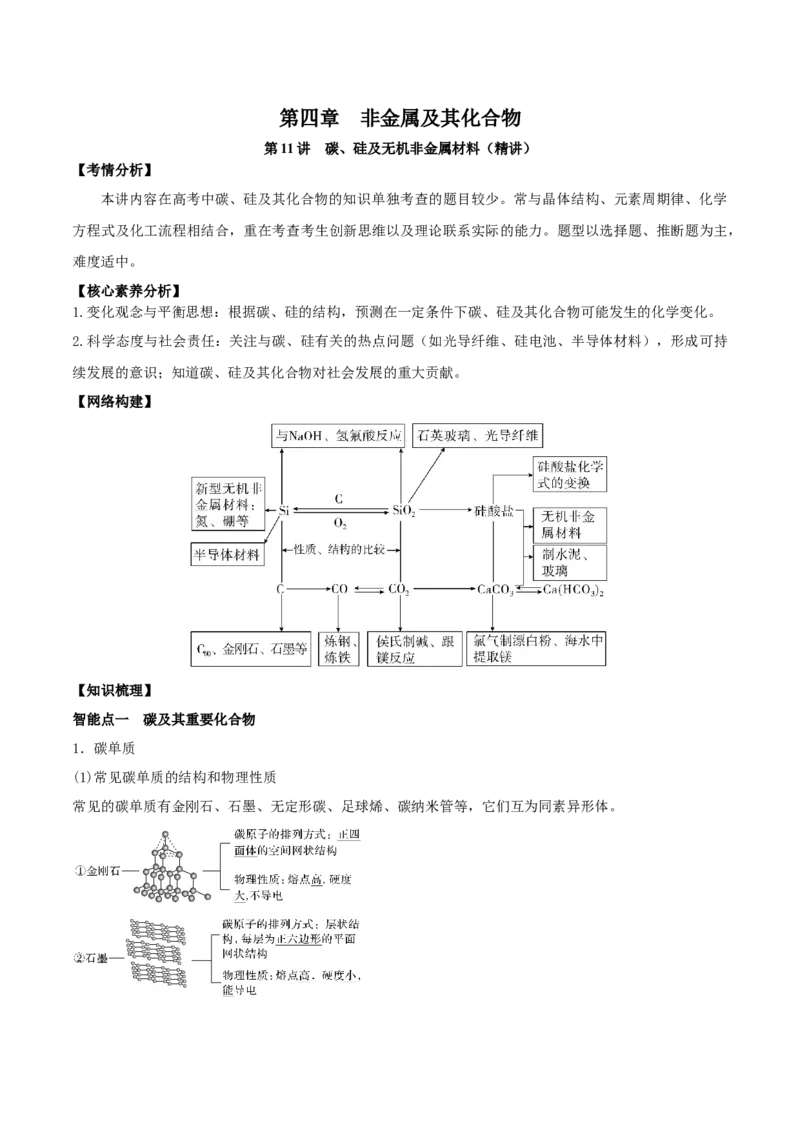
(1)常见碳单质的结构和物理性质
常见的碳单质有金刚石、石墨、无定形碳、足球烯、碳纳米管等,它们互为同素异形体。(2)化学性质
a.与O 的反应(用化学方程式表示):
2
①O 不足:2C+O=====2CO;
2 2
②O 充足:C+O=====CO。
2 2 2
b.与氧化物反应(用化学方程式表示):
①与CuO反应:2CuO+C 2Cu+CO↑;
2
②与FeO 反应:FeO+3C 2Fe+3CO↑;
2 3 2 3
③与CO 反应:CO+C 2CO;
2 2
④与水蒸气反应:C+HO(g) CO+H(制水煤气);
2 2
⑤与SiO 反应:SiO+2C Si+2CO↑(制粗硅);SiO+3C SiC+2CO↑(制金刚砂)
2 2 2
c.与强氧化性酸反应
①与浓硫酸反应:C+2HSO(浓) CO↑+2SO↑+2HO。
2 4 2 2 2
②与浓硝酸反应:C+4HNO(浓) CO↑+4NO↑+2HO。
3 2 2 2
(3)碳单质的用途:
①金刚石结构坚硬,作玻璃刻刀、机器钻头、装饰品等;
②石墨的细鳞片状结构质软、导电性、滑腻性、耐高温 铅笔芯、电极、润滑剂、坩埚;
③木炭和活性炭的疏松多孔的结构吸附性吸附食品色素、除臭、防毒面具、冰箱除味剂等;
④作燃料,用于家庭取暖、做饭等;
⑤作还原剂:冶炼金属,如冶炼金属铜、铁等。
2.CO和CO
2
(1)物理性质
色态味 密度(比空气) 水溶性 毒性
CO 无色、无 小 难溶 有
CO 味、气体 大 能溶 无
2
(2)化学性质
①CO具有较强的还原性,可以与O、金属氧化物等发生反应。
2
如与FeO 反应:FeO+3CO=====2Fe+3CO。
2 3 2 3 2
②CO 是典型的酸性氧化物,也具有氧化性。
2
a.酸性氧化物
①与水反应:CO +H O H CO
2 2 2 3
②与碱反应:CO 少量:CO +2NaOH===Na CO +H O;CO 足量:CO +NaOH===NaHCO
2 2 2 3 2 2 2 3
③与碱性氧化物反应:CO +CaO=CaCO
2 3④与Ca(ClO) 盐溶液反应:Ca(ClO) +CO +H O===CaCO ↓+2HClO(CO 少量);
2 2 2 2 3 2
Ca(ClO) +2CO +2H O===Ca(HCO ) +2HClO(CO 过量);
2 2 2 3 2 2
b.氧化性
①与C反应:CO+C 2CO;
2
②与Mg反应:2Mg+CO 2MgO+C
2
【特别提醒】溶液中通入CO 气体产生沉淀的问题:向BaCl 或CaCl 溶液中通入CO 气体,由于盐酸的酸性
2 2 2 2
比碳酸的强,不会产生BaCO 或CaCO 沉淀。
3 3
3.碳酸和碳酸盐
(1)碳酸
二元弱酸、不稳定,常用CO+HO代替HCO,但酸性比苯酚、次氯酸强。
2 2 2 3
(2)碳酸的正盐和酸式盐的比较
正盐(CO) 酸式盐(HCO)
溶解性 只有钾、钠、铵盐可溶 一般都可溶
热稳定性 正盐>酸式盐
溶液pH 同浓度:正盐>酸式盐
相互转化
CO HCO
4、碳元素在自然界中的循环
①CO 的主要来源:大量含碳燃料的燃烧。
2
②自然界消耗CO 的主要反应:
2
a.溶于江水、海水中:CO+HO HCO;
2 2 2 3
b.光合作用将CO 转化为O;
2 2
c.岩石的风化:CaCO +HO+CO===Ca(HCO)。
3 2 2 3 2
智能点二 硅及其化合物
1.硅
(1)硅的结构与物理性质
(2)化学性质a.常温
①与氢氟酸反应的化学方程式:Si+4HF===SiF ↑+2H ↑;
4 2
②与NaOH溶液反应的化学方程式:Si+2NaOH+H O===Na SiO +2H ↑;
2 2 3 2
③与F 反应的化学方程式:Si+2F ===SiF
2 2 4
b.高温
①与O 反应:Si+O SiO 。
2 2 2
②与Cl 反应:Si+Cl SiCl
2 2 4
(3)硅的工业制法
①原料:石英砂和焦炭
②制备:SiO+2C=====Si(粗)+2CO↑
2
③提纯:Si(粗)+2Cl SiCl ;SiCl +2H Si(纯)+4HCl
2 4 4 2
【特别提醒】①用焦炭还原SiO,产物是CO而不是CO。
2 2
②粗硅中含碳等杂质,与Cl 反应生成的SiCl 中含有CCl 等杂质,经过分馏提纯SiCl 后,再用H 还原,
2 4 4 4 2
得到高纯度硅。
(4)用途:半导体材料、太阳能电池、计算机芯片和耐酸设备等。
2.二氧化硅
(1)存在:硅石、石英、水晶、玛瑙、沙子等
(2)二氧化硅的结构特点
在SiO 晶体中,每个Si周围结合4个O,Si在中心,O在4个顶角;许多这样的 四面体又通
2
过顶角的O相连接,每个O为两个四面体所共有,即每个O与2个Si相结合。实际上,SiO 晶体是由Si
2
和O按1∶2的比例所组成的立体网状结构的晶体。由结构可知,二氧化硅的化学性质很稳定。
(3)物理性质:熔点高,硬度大,不溶于水
(4)化学性质:
a.酸性氧化物
①与碱反应:SiO +2NaOH===Na SiO +H O;
2 2 3 2
②与CaO碱性氧化物反应:SiO +CaO CaSiO
2 3
③与盐反应:SiO +Na CO Na SiO +CO ↑;SiO +CaCO CaSiO +CO ↑(工业制玻璃)
2 2 3 2 3 2 2 3 3 2
b.氧化性:
高温
①与碳反应:SiO
2
+2C Si+2CO↑(制粗硅);SiO
2
+3C SiC+2CO↑(制金刚砂);
②与Mg反应:4Mg+SiO 2MgSi+2MgO;MgSi+2H O=SiH ↑+2Mg(OH)(制硅化氢);
2 2 2 2 4 2c.特性:
与氢氟酸反应:SiO+4HF===SiF ↑+2H O
2 4 2
(5)用途
①水晶可用于电子工业的部件、光学仪器、工艺品
②SiO 是制光导纤维的重要原料
2
③较纯的石英用于制造石英玻璃
④石英砂用于制玻璃的原料及建筑材料
【特别提醒】(1)由于玻璃的成分中含有SiO,故实验室盛放碱液的试剂瓶用橡皮塞而不用玻璃塞。
2
(2)未进行磨砂处理的玻璃,在常温下是不易被强碱腐蚀的。
(3)因为氢氟酸腐蚀玻璃,与玻璃中的SiO 反应,所以氢氟酸不能用玻璃瓶保存,而应保存在塑料瓶或
2
铅皿中。
(4)SiO 是HSiO 的酸酐,但SiO 不与水反应,不能用SiO 直接与水作用制备HSiO。
2 2 3 2 2 2 3
3.硅酸
(1)物理性质:硅酸是一种白色胶状物质,不溶于水,能形成胶体。新制备的硅酸为透明、胶冻状,硅
酸经干燥脱水形成硅酸干凝胶——“硅胶”。
(2)化学性质:
a.弱酸性:硅酸的酸性很弱,比碳酸的酸性还弱,在与碱反应时只能与强碱反应。如 :
HSiO+2NaOH==Na SiO+2H O。
2 3 2 3 2
b.不稳定性:硅酸的热稳定性很差,受热分解为SiO 和HO:HSiO=====SiO+HO。
2 2 2 3 2 2
(3)制备:
由于SiO 不溶于水,所以硅酸是通过可溶性硅酸盐与其他酸反应制得的。
2
NaSiO+2HCl==H SiO↓+2NaCl,
2 3 2 3
NaSiO+CO +H O==H SiO↓+Na CO(证明酸性:HCO>HSiO)。
2 3 2 2 2 3 2 3 2 3 2 3
(4)用途:硅胶可作催化剂的载体和袋装食品、瓶装药品的干燥剂。
4.硅酸盐
(1)硅酸钠
①物理性质:白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显碱性。
②化学性质——与酸性较硅酸强的酸反应:
a.与盐酸反应的化学方程式:
NaSiO+2HCl===2NaCl+HSiO↓。
2 3 2 3
b.与CO 水溶液反应的化学方程式:
2
NaSiO+HO+CO===Na CO+HSiO↓。
2 3 2 2 2 3 2 3
③用途:黏合剂(矿物胶)、防腐剂和耐火阻燃材料。
【特别提醒】①NaSiO 的水溶液是一种黏合剂,是制备硅胶和木材防火剂等的原料;NaSiO 易与空气中
2 3 2 3
的CO、HO反应,要密封保存。
2 2
②可溶性碳酸盐、硅酸盐的水溶液呈碱性,保存该溶液的试剂瓶不能用玻璃塞,应用橡胶塞。(2)硅酸盐的氧化物表示法:
氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔开。
如硅酸钠(NaSiO)可表示为NaO·SiO,
2 3 2 2
长石(KAlSiO)可表示为KO·AlO·6SiO。
3 8 2 2 3 2
【特别提醒】(1)氧化物之间以“· ”隔开;(2)计量数配置出现分数应化为整数。硅酸盐改写为氧
化物形式时,各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。
当系数配置出现分数时一般应化为整数。如上例中 KAlSiO ,将 KO·AlO·3SiO ,要写成
3 8 2 2 3 2
KO·AlO·6SiO。
2 2 3 2
智能点三 无机非金属材料
1.传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
水泥 玻璃 陶瓷
主要原料 黏土、石灰石、石膏 石灰石、石英砂、纯碱 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
复杂的物理、化学变 主要反应:NaCO+SiO=====NaSiO+ 复杂的物理、化
变化 2 3 2 2 3
化过程 CO↑、CaCO+SiO=====CaSiO+CO↑ 学变化过程
2 3 2 3 2
硅酸三钙
(3CaO·SiO)
2
硅酸二钙
组成 硅酸钠、硅酸钙和二氧化硅 硅酸盐
(2CaO·SiO)
2
铝酸三钙
3CaO·AlO)
2 3
在工农业、科
用途 重要的建筑材料 制化学实验用的玻璃仪器、窗玻璃等 技、生活、实验
室中使用广泛
2.新型无机非金属材料,如高温结构陶瓷、光导纤维、生物陶瓷、压电陶瓷等。
材料类别 主要特性 示例 用途
高温结构陶 能承受高温,
氮化硅陶瓷 汽轮机叶片、轴承、永久性模具等
瓷 强度高
半导体陶瓷 具有电学特性 二氧化锡陶瓷 集成电路中的半导体
光学材料 具有光学特性 光导纤维 光缆通讯、医疗、照明等
生物陶瓷 具有生物功能 氧化铝陶瓷 人造骨骼、人造关节、接骨螺钉
智能点四 碳、硅及其化合物性质“反常”小结
(1)一般情况下,非金属元素单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金
刚石为自然界中硬度最大的物质。
(2)一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
(3)Si的还原性强于C,但C在高温下能还原出Si:SiO+2C=====Si+2CO↑。
2
(4)非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,
且放出氢气:Si+2NaOH+HO===NaSiO+2H↑。
2 2 3 2(5)非金属单质一般不与非氧化性酸反应,但硅能跟氢氟酸反应:Si+4HF===SiF↑+2H↑。
4 2
(6)一般情况下,碱性氧化物+酸―→盐+水,二氧化硅是酸性氧化物,却能与氢氟酸反应:SiO +
2
4HF===SiF↑+2HO(SiF 不属于盐,故SiO 不是两性氧化物)。
4 2 4 2
(7)一般情况下,无机酸能溶于水,但硅酸却难溶于水。
(8)一般情况下,较强酸+较弱酸的盐―→较弱酸+较强酸的盐(溶液中的反应)。
因碳酸的酸性强于硅酸,所以水玻璃在空气中易变质:NaSiO+HO+CO===NaCO+HSiO(胶体)。
2 3 2 2 2 3 2 3
但在高温下,可发生反应NaCO+SiO=====NaSiO+CO↑(CO 离开反应体系促进反应的正向进行)。
2 3 2 2 3 2 2
(9)一般情况下,金属(Na、K)能置换出水中的氢,但C在高温下也能置换出HO中的氢:C+HO(g)=====H
2 2 2
+CO。
(10)一般情况下,酸性氧化物与水反应生成相应的含氧酸,但二氧化硅不溶于水,也不与水反应。
智能点五 CO 与碱、盐溶液的反应规律
2
1、与碱溶液的反应
(1)反应原理
NaOH――→NaCO――→NaHCO
2 3 3
(2)反应后溶质成分的判断
x= 溶质成分
x≤1∶1 NaHCO
3
1∶12∶1 NaOH、NaCO
2 3
也可用数轴来表示:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===HSiO↓+NaCO
2 2 3 2 4 4 2 3
或CO+NaSiO+HO===HSiO↓+NaCO
2 2 3 2 2 3 2 3
当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===HSiO↓+2NaHCO
2 2 3 2 2 3 3
③CO+Ca(ClO)+HO===CaCO↓+2HClO
2 2 2 3
2、与盐溶液的反应
(1)CO 与盐溶液的常见反应
2
碳酸是一种弱酸,其酸性比盐酸、醋酸要弱,因此,盐酸、醋酸能与碳酸盐反应;其酸性又比硅酸、次氯
酸、苯酚、偏铝酸等强,因此,将CO 气体通入NaSiO 、NaClO、 、NaAlO 等盐溶液中,均能发生反
2 2 3 2
应而生成相应的弱酸和碳酸(氢)盐,这就是“强酸制弱酸”原理的应用。如:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===HSiO↓+NaCO
2 2 3 2 4 4 2 3
或CO+NaSiO+HO===HSiO↓+NaCO
2 2 3 2 2 3 2 3当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===HSiO↓+2NaHCO
2 2 3 2 2 3 3
③CO+Ca(ClO)+HO===CaCO↓+2HClO
2 2 2 3
当CO 过量时,发生反应如下:
2
2CO+Ca(ClO)+2HO===Ca(HCO)+2HClO
2 2 2 3 2
④CO+ +HO―→ +NaHCO
2 2 3
⑤CO+NaAlO+2HO===Al(OH)↓+NaHCO(CO 过量时)
2 2 2 3 3 2
CO+2NaAlO+3HO===2Al(OH)↓+NaCO(CO 少量时)
2 2 2 3 2 3 2
(2)注意事项
①“强酸制弱酸”是一个重要的化学反应规律,但不可认为弱酸就不能“制取”强酸。在某些条件下,当
弱酸的酸根阴离子被沉淀或被氧化后,H+就被“释放”出来,从而生成了强酸。如将HS通入CuSO 溶液中
2 4
或向氢硫酸中滴加氯水,均由氢硫酸这种弱酸生成了强酸:HS+CuSO===CuS↓+HSO(S2-与Cu2+结合成
2 4 2 4
难溶的CuS),HS+Cl===S↓+2HCl(S2-被氧化)。
2 2
②CO 与 溶液反应的产物与CO 的用量无关,都生成NaHCO,因为酸性HCO> >HCO。
2 2 3 2 3
③ CO 与 NaClO 溶液反应的产物与 CO 的量无关,也只能生成 NaHCO ,不能生成 NaCO ,因为酸性
2 2 3 2 3
HCO>HClO>HCO。
2 3
④CO、SO 通入CaCl 或BaCl 溶液均不反应,无沉淀产生。
2 2 2 2
【典例剖析】
高频考点1 考查碳及及其化合物性质和应用
例1、下列有关碳及其化合物的说法正确的是( )
A.CO 是导致酸雨的主要气体
2
B.CO和CO 组成元素相同,所以他们的化学性质相同
2
C.金刚石、石墨是碳的单质,而C 是碳的化合物
60
D.在高温条件下,碳能使CO 转变成CO
2
【解析】A.正常雨水的pH=5.6,就是溶有CO 的缘故,故CO 不是导致酸雨的主要气体,SO 和氮的氧化物
2 2 2
才是导致酸雨的主要气体,A错误;B.CO和CO 组成元素相同,但它们分子组成不同,故他们的化学性质
2
不相同,例如CO具有可燃性,CO 却不支持燃烧等,B错误;C.单质是指只含有一种元素的纯净物,故金
2
刚石、石墨是碳的单质,C 也是碳的单质,C错误;D.在高温条件下,碳能使CO 转变成CO,CO+C
60 2 2
2CO,D正确;故答案为:D。
【答案】D
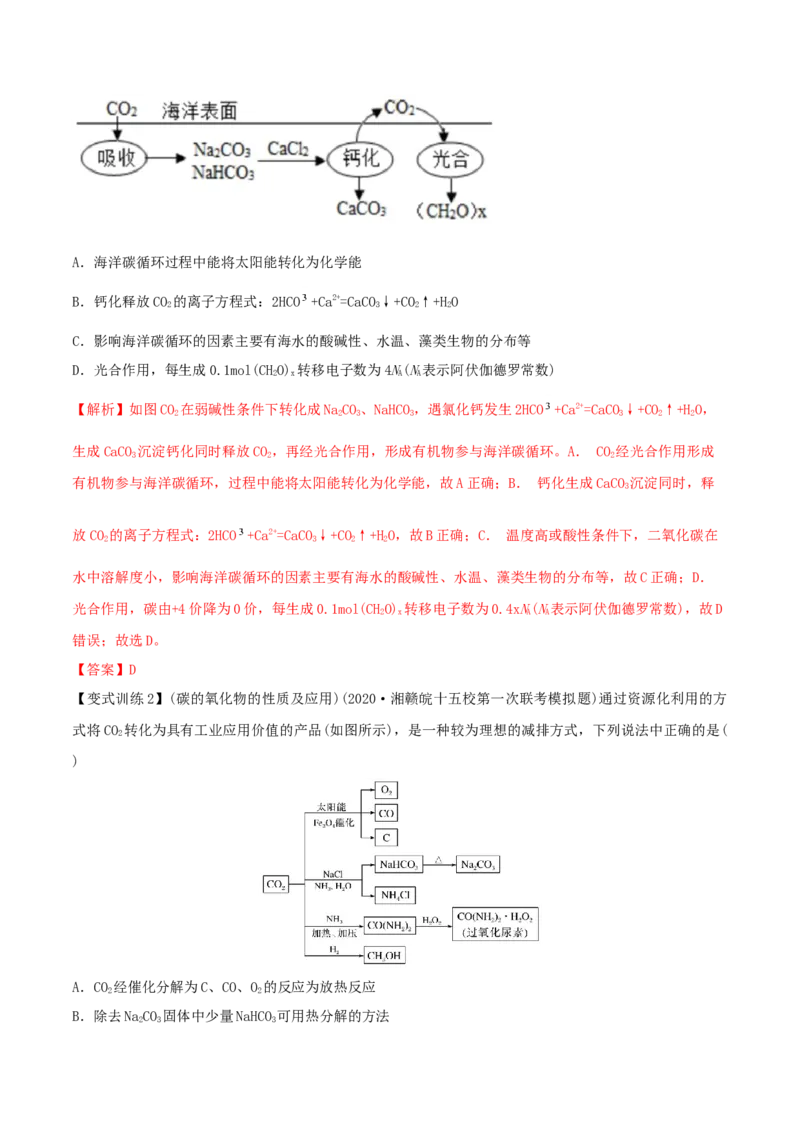
【变式训练1】(碳循环)(2021·福建高三三模)海洋碳循环是全球碳循环的重要组成部分,是影响全
球气候变化的关键控制环节。下图为海洋中碳循环的简单原理图。下列说法错误的是A.海洋碳循环过程中能将太阳能转化为化学能
B.钙化释放CO 的离子方程式:2HCO +Ca2+=CaCO↓+CO↑+HO
2 3 2 2
C.影响海洋碳循环的因素主要有海水的酸碱性、水温、藻类生物的分布等
D.光合作用,每生成0.1mol(CHO) 转移电子数为4N(N表示阿伏伽德罗常数)
2 x A A
【解析】如图CO 在弱碱性条件下转化成NaCO、NaHCO,遇氯化钙发生2HCO +Ca2+=CaCO↓+CO↑+HO,
2 2 3 3 3 2 2
生成CaCO 沉淀钙化同时释放CO,再经光合作用,形成有机物参与海洋碳循环。A. CO 经光合作用形成
3 2 2
有机物参与海洋碳循环,过程中能将太阳能转化为化学能,故A正确;B. 钙化生成CaCO 沉淀同时,释
3
放CO 的离子方程式:2HCO +Ca2+=CaCO↓+CO↑+HO,故B正确;C. 温度高或酸性条件下,二氧化碳在
2 3 2 2
水中溶解度小,影响海洋碳循环的因素主要有海水的酸碱性、水温、藻类生物的分布等,故C正确;D.
光合作用,碳由+4价降为0价,每生成0.1mol(CHO) 转移电子数为0.4xN(N表示阿伏伽德罗常数),故D
2 x A A
错误;故选D。
【答案】D
【变式训练2】(碳的氧化物的性质及应用)(2020·湘赣皖十五校第一次联考模拟题)通过资源化利用的方
式将CO 转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是(
2
)
A.CO 经催化分解为C、CO、O 的反应为放热反应
2 2
B.除去NaCO 固体中少量NaHCO 可用热分解的方法
2 3 3C.过氧化尿素和SO 都能使品红溶液褪色,其原理相同
2
D.由CO 和H 合成甲醇,原子利用率达100%
2 2
【解析】该反应应为吸热反应,A错误;碳酸氢钠受热易分解生成碳酸钠、水和二氧化碳,因此除去
NaCO 固体中少量NaHCO 可用热分解的方法,B正确;过氧化尿素使品红溶液褪色是利用它的强氧化性,
2 3 3
而二氧化硫使品红溶液褪色是利用它与品红化合生成不稳定的无色物质,原理不相同,C错误;由碳氧原
子个数比可知,二氧化碳与氢气合成甲醇的原子利用率不是100%,D错误。
【答案】B
高频考点2 考查硅及其化合物的性质和应用
例2.下列表述正确的是( )
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
②化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐,③提前建成的三峡大
坝使用了大量水泥,水泥是硅酸盐材料,④夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变
色眼镜来保护眼睛,⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④ C.③④⑤ D.③⑤
【解析】本题主要考查学生对身边常见的化学制品的了解情况。侧重考查学生应用化学知识解释和解决身
边化学问题的能力。人造刚玉主要成分为AlO,①错;玛瑙的主要成分是SiO;③水泥主要成分是硅酸盐,
2 3 2
正确;④变色眼镜镜片应是在普通硼酸盐玻璃中加入光敏物质AgBr等,并加入极少光敏化剂如CuO等制成,
故④错。综上所述,本题答案选D。
【答案】D
【拓展延伸】变色眼镜的玻璃片中含有少量溴化银和微量的氧化铜(作催化剂),当玻璃受到阳光照射时,
发生2AgBr 2Ag+Br 反应,而使玻璃由无色变成灰黑色,把玻璃放到暗处,又因发生2Ag+Br 2AgBr
2 2
反应,而使玻璃由灰黑色变成无色。在制造普通玻璃时常加入少量Cu O可使玻璃显红色。
2
【变式训练1】(二氧化硅的性质和用途)二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新
型材料等方面有着重要的用途。a~e是对①~⑤反应中SiO 所表现的化学性质或作用进行的判断,其中正
2
确的是( )
①SiO+2NaOH===Na SiO+HO
2 2 3 2
②SiO+2C=====Si+2CO↑
2
③SiO+4HF===SiF ↑+2HO
2 4 2
④NaCO+SiO=====NaSiO+CO↑
2 3 2 2 3 2
⑤SiO+3C=====SiC+2CO↑
2
a.反应①中SiO 作为玻璃的成分被消耗,用于刻蚀玻璃
2
b.反应②中SiO 表现出氧化性
2
c.反应③中SiO 表现出酸性氧化物的通性
2
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的道理e.反应⑤中SiO 未参加氧化还原反应
2
A.ace B.bde C.cde D.ab
【解析】通常用氢氟酸来刻蚀玻璃,与之对应的是反应③,反应①中SiO 表现出酸性氧化物的通性,a、c
2
判断错误;反应②是一个置换反应,其中二氧化硅被还原,表现出氧化性,b判断正确;反应④是一个复
分解反应,用难挥发的二氧化硅制取易挥发的二氧化碳,d判断正确;反应⑤中碳的化合价由0价变为-4
和+2价,硅的化合价和氧的化合价都没有改变,因此二氧化硅没有参加氧化还原反应,e判断正确。
【答案】B
【变式训练2】(硅酸盐的性质和表示方法)(2020·湖南怀化市高三期末)青石棉是一种致癌物质,是《鹿
特丹公约》中受限制的46种化学品之一,其化学式为NaFeSiO (OH) 。青石棉用稀硝酸处理时,还原产
2 5 8 22 2
物只有NO,下列说法不正确的是( )
A.青石棉是一种硅酸盐产品
B.青石棉中含有一定量的石英晶体
C.青石棉的化学组成可表示为NaO·3FeO·FeO·8SiO·HO
2 2 3 2 2
D.1 mol青石棉能还原1 mol HNO
3
【解析】硅酸盐指的是Si、O与其他化学元素结合而成的化合物的总称,根据青石棉的化学式可知,青石
棉是一种硅酸盐产品,故A说法正确;硅酸盐中不含有SiO ,因此青石棉中不含石英晶体,故B说法错误;
2
按 照 硅 酸 盐 写 成 氧 化 物 形 式 , 青 石 棉 的 化 学 式 组 成 用 氧 化 物 的 形 式 可 表 示 为
NaO·3FeO·FeO·8SiO·HO,故C说法正确;根据C选项分析,青石棉中含有+2价的铁,与硝酸发生
2 2 3 2 2
氧化还原反应,根据得失电子数目守恒可知,1 mol青石棉能还原1 mol HNO,故D说法正确。
3
【答案】B
高频考点3 考查无机非金属材料的分类和应用
例3.下列关于无机非金属材料的说法中不正确的是( )
A.传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料克服了传统无机非金属材料的许多缺点
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
【解析】无机非金属材料分为传统无机非金属材料和新型无机非金属材料两大类。传统无机非金属材料是
指我们常说的硅酸盐材料,包括玻璃、水泥、砖瓦、陶瓷等;新型无机非金属材料是指一些新型的具有特
殊结构和特殊功能的非硅酸盐型材料。新型无机非金属材料与传统无机非金属材料相比,具有许多优良性
能,如耐高温、耐磨损、耐酸碱腐蚀、具有压电效应、具有生物功能等。
【答案】D
【变式训练1】(传统无机非金属材料)陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与
化学有着密切的关系。下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
【答案】A
【解析】氧化铁为棕红色固体,瓷器的青色不可能来自氧化铁,故A错误;秦兵马俑是陶制品,陶制品是
由粘土或含有粘土的混合物经混炼、成形、煅烧而制成的,故B正确;陶瓷的主要原料是取之于自然界的
硅酸盐矿物,陶瓷的主要成分是硅酸盐,与水泥、玻璃等同属硅酸盐产品,故C正确;陶瓷的主要成分是
硅酸盐,硅酸盐的化学性质不活泼,具有不与酸或碱反应、抗氧化的特点,故D正确。
【变式训练2】(新型无机非金属材料)平昌冬奥会“北京8分钟”主创团队用石墨烯制作了-20 ℃能发
热4 h的智能服饰;用铝合金管材和碳纤维制作了高2.35 m、重量仅为10 kg的熊猫木偶,向世界展现了新
时代的中国形象。下列说法中,不正确的是( )
A.石墨烯是能导热的金属材料
B.铝合金是密度较小的金属材料
C.碳纤维是耐低温的无机非金属材料
D.新型材料种类多、用途广
【解析】石墨烯是无机非金属材料,A错误;铝合金是密度较小的金属材料,B正确;石墨烯可制作-20
℃能发热4 h的服饰,能耐低温,C正确;新型材料种类多、用途广,D正确。
【答案】A
高频考点4 考查CO 通入碱溶液中反应产物的判断及计算
2
例4.(2020·湘赣皖十五校第一次联考)往含0.2 mol NaOH和0.1 mol Ba(OH) 的混合溶液中持续稳定地通
2
入CO 气体6.72 L(标准状况下),则在这一过程中,下列有关溶液中离子总物质的量(n)随通入CO 气体体
2 2
积(V)的变化曲线中正确的是(离子水解忽略不计)( )
【解析】根据电离方程式:NaOH===Na++OH-,Ba(OH)===Ba2++2OH-可知,在含0.2 mol NaOH和0.1 mol
2
Ba(OH) 的混合溶液中离子的总物质的量为0.2 mol×2+0.1 mol×3=0.7 mol。标准状况下6.72 L CO 的
2 2
物质的量n(CO)==0.3 mol,把CO 气体通入混合溶液中,首先发生反应:Ba2++2OH-+CO===BaCO↓+
2 2 2 3
HO,当0.1 mol Ba(OH) 恰好反应完全时消耗0.1 mol CO(体积为2.24 L),此时离子的物质的量减少0.3
2 2 2mol,溶液中离子的物质的量为0.4 mol,排除D选项;然后发生反应:CO +2OH-===CO+HO,当0.2 mol
2 2
NaOH完全反应时又消耗0.1 mol CO(体积为2.24 L),消耗总体积为4.48 L,离子的物质的量又减少0.1
2
mol,此时溶液中离子的物质的量为0.7 mol-0.3 mol-0.1 mol=0.3 mol,排除A选项;继续通入0.1
mol CO 气体,发生反应:CO+HO+CO===2HCO,根据方程式可知:0.1 mol CO 反应,溶液中离子的物质
2 2 2 2
的量增加0.1 mol,此时溶液中离子的物质的量为0.3 mol+0.1 mol=0.4 mol,排除C选项,只有选项B
符合反应实际,故合理选项是B。
【答案】B
【变式训练】(2020·吉林模拟)将足量CO 通入KOH和Ca(OH) 的混合稀溶液中,生成沉淀的物质的量(n)
2 2
和通入CO 体积(V)的关系正确的是( )
2
【解析】CO 与KOH和Ca(OH) 都会反应,但存在着竞争,如果先与KOH反应,则反应后生成的KCO 立即会
2 2 2 3
与Ca(OH) 反应生成CaCO ,因此,可以看成CO 先与Ca(OH) 反应,所以通CO 后立即有CaCO 生成。第二
2 3 2 2 2 3
步还要判断CO 是先跟KOH反应还是先与生成的CaCO 反应,同样可以采用假设法判断,即如果先与CaCO
2 3 3
反应,则生成的Ca(HCO) 又会与KOH反应,因此是先与KOH反应,此过程生成沉淀的物质的量不变,当
3 2
KOH反应完全,CO 再与CaCO 反应,直至沉淀完全溶解,故选D。
2 3
【答案】D