文档内容
第 15 讲 化学反应的热效应
【化学学科素养】
变化观念与平衡思想:认识化学变化的本质是有新物质生成,并伴有能量的转化;能多角度、动态地
分析热化学方程式,运用热化学反应原理解决实际问题。
证据推理与模型认知:通过分析、推理等方法认识研究反应热的本质,建立盖斯定律模型。
科学态度与社会责任:赞赏化学对社会发展的重大贡献,具有可持续发展意识和绿色化学观念,能对
与化学有关的社会热点问题做出正确的价值判断。
【必备知识解读】
一、焓变、热化学方程式
1.反应热(焓变)
(1)概念:在恒压条件下进行的反应的热效应。
符号:ΔH。
单位:kJ·mol-1或kJ/mol。
(2)表示方法
吸热反应:ΔH>0;放热反应:ΔH<0。
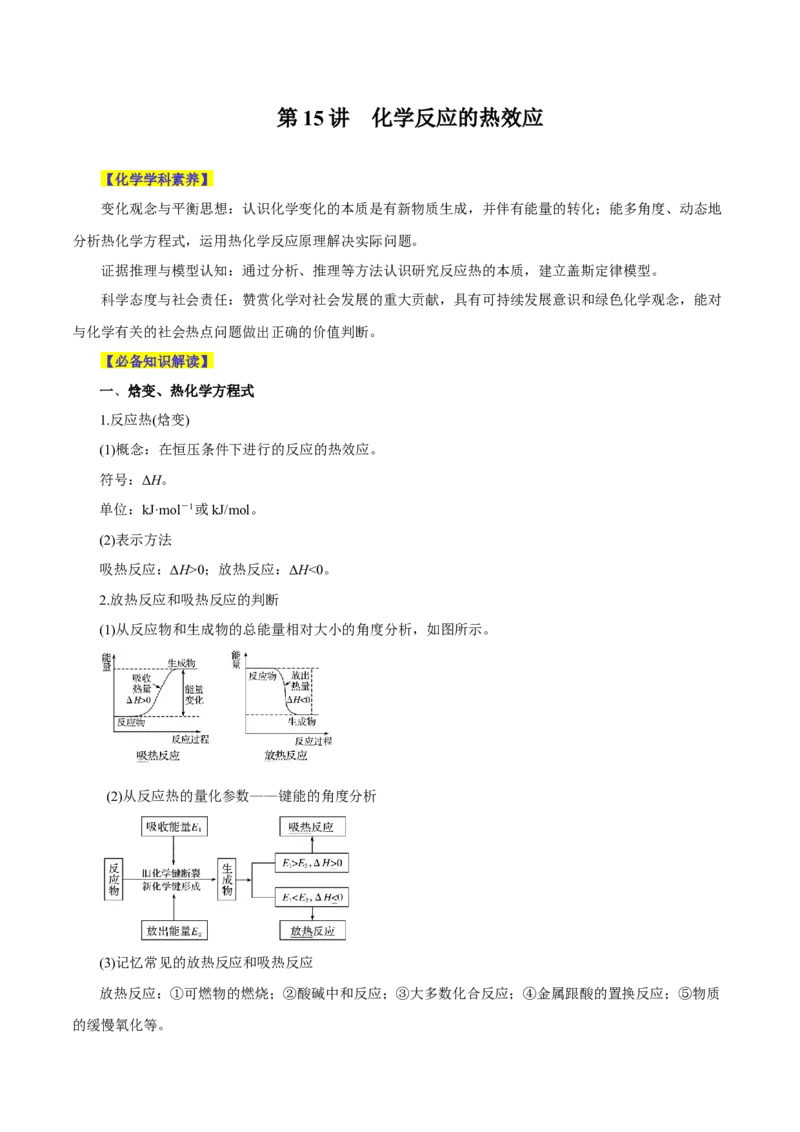
2.放热反应和吸热反应的判断
(1)从反应物和生成物的总能量相对大小的角度分析,如图所示。
(2)从反应热的量化参数——键能的角度分析
(3)记忆常见的放热反应和吸热反应
放热反应:①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的置换反应;⑤物质
的缓慢氧化等。吸热反应:①大多数分解反应;②盐的水解;③Ba(OH) ·8H O与NH Cl反应;④碳和水蒸气、C和
2 2 4
CO 的反应等。
2
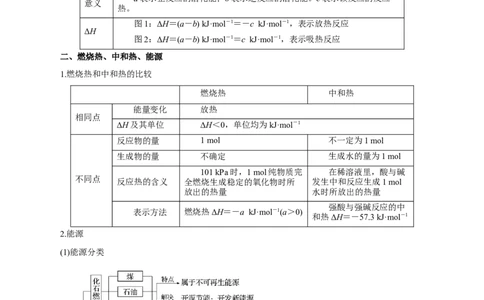
3.理解反应历程与反应热的关系
图示
a表示正反应的活化能;b表示逆反应的活化能。c表示该反应的反应
意义
热。
图1:ΔH=(a-b) kJ·mol-1=-c kJ·mol-1,表示放热反应
ΔH
图2:ΔH=(a-b) kJ·mol-1=c kJ·mol-1,表示吸热反应
二、燃烧热、中和热、能源
1.燃烧热和中和热的比较
燃烧热 中和热
能量变化 放热
相同点
ΔH及其单位 ΔH<0,单位均为kJ·mol-1
反应物的量 1 mol 不一定为1 mol
生成物的量 不确定 生成水的量为1 mol
101 kPa时,1 mol纯物质完 在稀溶液里,酸与碱
不同点
反应热的含义 全燃烧生成稳定的氧化物时所 发生中和反应生成1 mol
放出的热量 水时所放出的热量
强酸与强碱反应的中
表示方法 燃烧热ΔH=-a kJ·mol-1(a>0)
和热ΔH=-57.3 kJ·mol-1
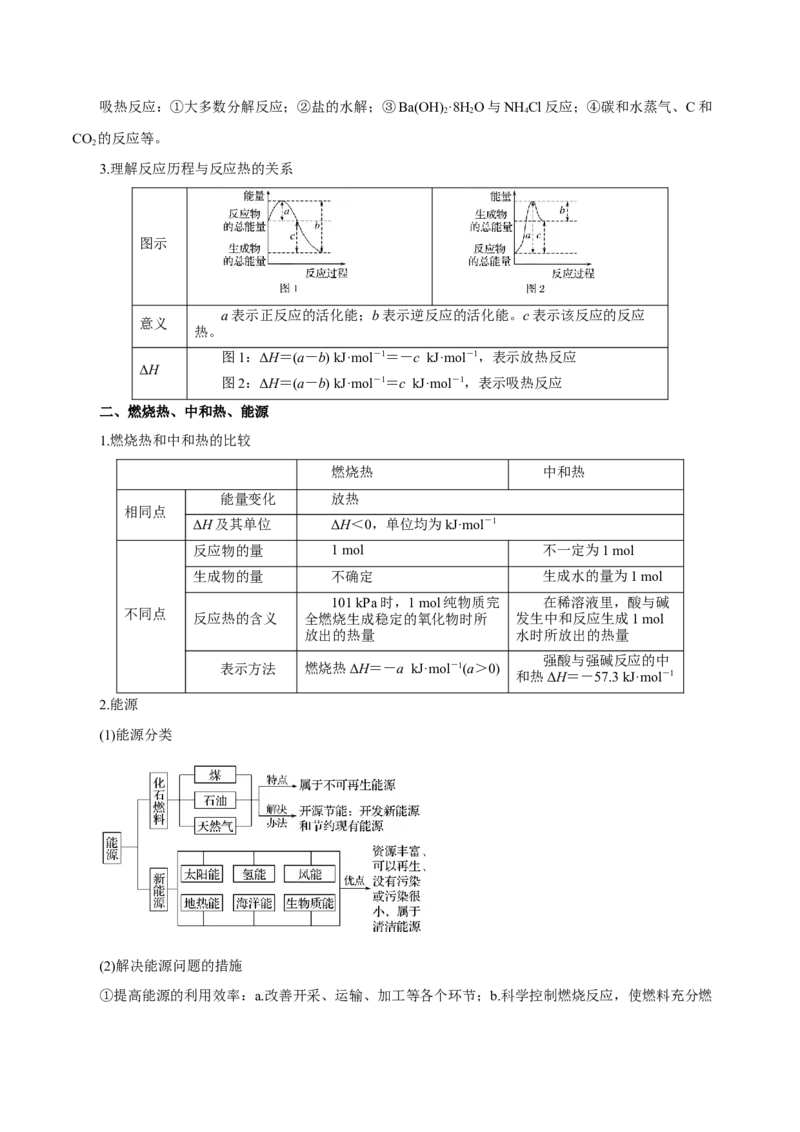
2.能源
(1)能源分类
(2)解决能源问题的措施
①提高能源的利用效率:a.改善开采、运输、加工等各个环节;b.科学控制燃烧反应,使燃料充分燃烧。
②开发新能源:开发资源丰富、可以再生、没有污染或污染很小的新能源。
【方法技巧】
(1)有关燃烧热的判断,一看是否以1 mol可燃物为标准,二看是否生成稳定氧化物。
(2)有关中和热的判断,一看是否以生成1 mol H O为标准,二看酸碱的强弱和浓度,应充分考虑弱
2
酸、弱碱,电离吸热,浓的酸碱稀释放热等因素。
三、盖斯定律及其应用
1.盖斯定律
(1)内容
对于一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的。即:化学反应的反应热只
与反应体系的始态和终态有关,而与反应的途径无关。
(2)意义
间接计算某些反应的反应热。
(3)应用
转化关系 反应热间的关系
aA――→B、A――→B ΔH=aΔH
1 2
A B ΔH=-ΔH
1 2
ΔH=ΔH+ΔH
1 2
2.利用盖斯定律计算反应热
(1)运用盖斯定律的技巧——“三调一加”
一调:根据目标热化学方程式,调整已知热化学方程式中反应物和生成物的左右位置,改写已知的热
化学方程式。
二调:根据改写的热化学方程式调整相应ΔH的符号。
三调:调整中间物质的化学计量数。
一加:将调整好的热化学方程式及其ΔH相加。
(2)运用盖斯定律的三个注意事项
①热化学方程式乘以某一个数时,反应热的数值必须也乘上该数。
②热化学方程式相加减时,物质之间相加减,反应热也必须相加减。
③将一个热化学方程式颠倒时,ΔH的“+”“-”随之改变,但数值不变。
3.反应热大小的比较
(1)看物质状态。物质的气、液、固三态转化时的能量变化如下:(2)看ΔH的符号。比较反应热大小时不要只比较ΔH数值的大小,还要考虑其符号。
(3)看化学计量数。当反应物与生成物的状态相同时,化学计量数越大,放热反应的ΔH越小,吸热反
应的ΔH越大。
(4)看反应的程度。对于可逆反应,参加反应的物质的量和状态相同时,反应的程度越大,热量变化越
大。
【关键能力拓展】
一、热化学方程式
(1)概念
表示参加反应物质的量和反应热的关系的化学方程式。
(2)意义
表明了化学反应中的物质变化和能量变化。
如:2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
表示:2 mol氢气和1 mol氧气反应生成2 mol液态水时放出571.6 kJ的热量。
(3)书写要求
①注明反应的温度和压强(25 ℃、101 kPa下进行的反应可不注明)。
②注明反应物和生成物的状态:固态(s)、液态(l)、水溶液(aq)、气态(g)。
③热化学方程式中各物质的化学计量数只表示物质的物质的量,而不表示分子个数(或原子个数),因
此可以写成分数。
④热化学方程式中不用“↑”和“↓”。
⑤由于ΔH与反应物的物质的量有关,所以热化学方程式中物质的化学计量数必须与ΔH相对应,如果
化学计量数加倍,则ΔH也要加倍。当反应向逆反应方向进行时,其反应热与正反应的反应热数值相等,
符号相反。
【方法技巧】
(1)焓变与反应发生的条件、反应进行是否彻底无关。
(2)催化剂能降低反应所需活化能,但不影响焓变的大小。
(3)在化学反应中,反应物各原子之间的化学键不一定完全断裂。
四、中和热的测定1.中和热的测定实验
(1)实验装置
(2)测定原理
ΔH=-
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;
n为生成HO的物质的量。
2
(3)注意事项
①泡沫塑料板和碎泡沫塑料(或纸条)的作用是保温。
②为保证酸完全中和,采取的措施是若采用的酸、碱浓度相等,可采用碱体积稍过量。
2.酸碱中和反应测定实验的注意事项
(1)为了保证0.50mol· L-1的盐酸完全被NaOH中和,采用0.55mol·L-1NaOH溶液,使碱稍稍过
量,因为过量的碱并不参加中和反应。(酸稍微过量也可以)
杨sir化学,侵权必究
(2)先后测量酸、碱及混合液的温度时,测定一种溶液后必须用水冲洗干净并用滤纸擦干。温度计
的水银球部分要完全浸入溶液中,且要稳定一段时间再记下读数。
(3)实验中所用的盐酸和氢氧化钠溶液配好后要充分冷却至室温,才能使用。
(4)操作时动作要快,尽量减少热量的散失。
杨sir化学,侵权必究
(5)实验时亦可选用浓度体积都不相同的酸碱溶液进行中和热的测定,但在计算时,应取二者中量
少的一种,因为过量的酸/碱并不参加中和反应。
(6)多次试验求平均值时,若有某一组的实验数据有明显偏差,应直接舍去。
(7)隔热层的作用是保温隔热,减少热量损失。
杨sir化学,侵权必究
三、反应热大小的比较
(1)直接比较法
①物质燃烧时,可燃物物质的量越大,燃烧放出的热量越多。
②等量的可燃物完全燃烧所放出的热量肯定比不完全燃烧所放出的热量多。
③生成等量的水时,强酸和强碱的稀溶液反应比弱酸和强碱或弱碱和强酸或弱酸和弱碱的稀溶液反应
放出的热量多。
④对于可逆反应,因反应不能进行完全,实际反应过程中放出或吸收的热量要小于相应热化学方程式
中的反应热数值。例如:2SO
2
(g)+O
2
(g) 2SO
3
(g) ΔH=-197 kJ·mol-1,表示2 mol SO
2
(g)和1 mol
O(g)完全反应生成2 mol SO (g)时,放出的热量为197 kJ,实际上向密闭容器中通入2 mol SO (g)和1 mol
2 3 2O(g),反应达到平衡后,放出的热量要小于197 kJ。
2
(2)盖斯定律比较法
①同一反应,生成物状态不同时
如A(g)+B(g)===C(g) ΔH<0
1
A(g)+B(g)===C(l) ΔH<0
2
C(g)===C(l) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
1 3 2 1 2 3
所以ΔH<ΔH。
2 1
②同一反应,反应物状态不同时
如S(g)+O(g)===SO (g) ΔH<0
2 2 1
S(s)+O(g)===SO (g) ΔH<0
2 2 2
S(g)===S(s) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
2 3 1 1 2 3
所以ΔH<ΔH。
1 2
【核心题型例解】
高频考点一 吸热反应和放热反应
例1.有关反应热效应的说法正确的是
A.大多数分解反应都是吸热反应 B.氧化还原反应都属于放热反应
C.有催化剂参与的反应是放热反应 D.有化学键断裂的反应是吸热反应
【答案】A
【解析】大多数化合反应是放热反应,大多数分解反应是吸热反应,A正确;氧化还原反应不一定是
放热反应,如碳与二氧化碳高温条件下反应生成一氧化碳为氧化还原反应,但属于吸热反应,B错误;催
化剂改变化学反应速率,不改变化学反应进行的程度,化学反应的吸放热与是否有催化剂参与无关,C错
误;
所有的化学反应均有化学键的断裂和生成,反应物断键吸收的热量比生成物成键放出的热量多,该反应为吸热反应,反之为放热反应,D错误;答案选A。
【变式探究】下列反应中属于吸热反应的是
A.氢氧化钠溶液与稀硫酸混合 B.甲烷燃烧
C.氢氧化钡晶体与氯化铵晶体混合搅拌 D.氧化钙溶于水
【答案】C
【解析】酸碱中和反应为放热反应,A不符合题意;燃烧反应为放热反应,B不符合题意;氢氧化钡
晶体与氯化铵晶体的反应是典型的吸热反应,C符合题意;氧化钙溶于水,放出大量热量,放热反应,D
不符合题意;故选C。
高频考点二 化学反应中的焓变
例2.(2022·浙江1月选考,18)相关有机物分别与氢气发生加成反应生成1 mol环己烷( )的能量变化
如图所示:
下列推理不正确的是( )
A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH<0,ΔH-ΔH>0,说明苯分子具有特殊稳定性
3 1 4 3
【答案】A【解析】2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比,但不能
1 2
是存在相互作用的两个碳碳双键,故A错误;ΔH<ΔH,即单双键交替的物质能量低,更稳定,说明单双
2 3
键交替的两个碳碳双键间存在相互作用,有利于物质稳定,故B正确;3ΔH<ΔH,说明苯分子中不存在
1 4
三个完全独立的碳碳双键,故C正确;ΔH-ΔH<0,ΔH-ΔH>0,说明苯分子具有特殊稳定性,故D
3 1 4 3
正确。
【变式探究】[2022·广东,19(1)②]Cr O 催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过程的
2 3
焓变为__________(列式表示)。【答案】(E-E)+ΔH+(E-E)
1 2 3 4
【解析】设反应过程中第一步的产物为M,第二步的产物为N,则X→M的ΔH=E-E,M→N的
1 1 2
ΔH=ΔH,N→Y的ΔH=E-E,根据盖斯定律可知,X(g)→Y(g)的焓变为ΔH+ΔH+ΔH=(E-E)+
2 3 3 4 1 2 3 1 2
ΔH+(E-E)。
3 4
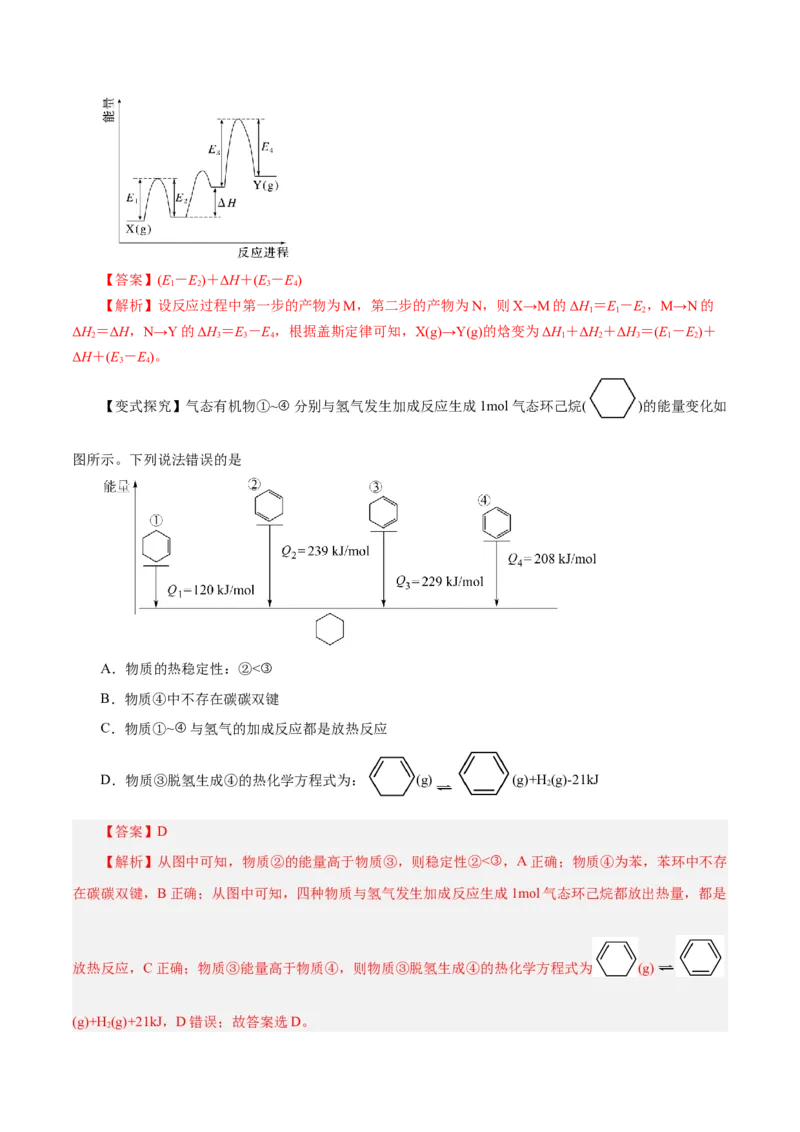
【变式探究】气态有机物①~④分别与氢气发生加成反应生成1mol气态环己烷( )的能量变化如
图所示。下列说法错误的是
A.物质的热稳定性:②<③
B.物质④中不存在碳碳双键
C.物质①~④与氢气的加成反应都是放热反应
D.物质③脱氢生成④的热化学方程式为: (g) (g)+H(g)-21kJ
2
【答案】D
【解析】从图中可知,物质②的能量高于物质③,则稳定性②<③,A正确;物质④为苯,苯环中不存
在碳碳双键,B正确;从图中可知,四种物质与氢气发生加成反应生成1mol气态环己烷都放出热量,都是
放热反应,C正确;物质③能量高于物质④,则物质③脱氢生成④的热化学方程式为 (g)
(g)+H(g)+21kJ,D错误;故答案选D。
2高频考点三 依据键能或能量变化图计算焓变
例3.(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
21
能量/ 249 39 10 0 0 -136 -242
8
可根据 计算出 中氧氧单键的键能为 。下列说法不正确的是
A. 的键能为
B. 的键能大于 中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:
D.
【答案】C
【解析】根据表格中的数据可知,H 的键能为218×2=436 ,A正确;由表格中的数据可知O
2 2
的键能为:249×2=498 ,由题中信息可知HO 中氧氧单键的键能为 ,则O 的键能
2 2 2
大于HO 中氧氧单键的键能的两倍,B正确;由表格中的数据可知HOO=HO+O,解离其中氧氧单键需要
2 2
的能量为249+39-10=278 ,HO 中氧氧单键的键能为 ,C错误;由表中的数据可知
2 2
的 ,D正确;故选C
【变式探究】(2021·浙江卷)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
热化学方程式 2H(g) + O (g)=2HO(g) ΔH= -482kJ·mol-1
2 2 2
则2O(g)=O (g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
【答案】D【解析】反应的ΔH=2(H-H)+(O-O)-4(H-O);-482kJ/mol=2×436kJ/mol+(O-O)-4×463kJ/mol,解得O-O
键的键能为498kJ/mol,2个氧原子结合生成氧气的过程需要释放能量,因此2O(g)=O (g)的ΔH=-498kJ/
2
mol。
【方法技巧】
1.熟记反应热ΔH的基本计算公式
ΔH=生成物的总能量-反应物的总能量
ΔH=反应物的总键能-生成物的总键能
2.常见1 mol物质中的化学键数目
1 mol CO 2 CH 4 N 2 H 4 (N—N、 SiO 2 金刚
P 石墨 S Si
4 石 8
物质 (CO) (C—H) N—H) (Si—O)
化学键 N—N:N
A
2N 4N 6N 4N 1.5N 2N 8N 2N
A A A A A A A A
数目 N—H:4N
A
【变式探究】将2 mol 和3 mol 置于密闭容器中,在250℃下只发生如下两个反应:
kJ/mol
kJ/mol
一段时间后, 和 恰好全部消耗,共放出303 kJ热量。
已知:部分化学键的键能如下表所示
化学键 (ClF中) ( 中)
键能/(kJ/mol) 157 243 248 X
则X的值为
A.172 B.202 C.238 D.258
【答案】A
【分析】根据反应热与键能的关系△H=∑D(反应物)−∑D(生成物),可求出a,以及用x把b表
示出来,然后根据化学方程式的计算可解。
【解析】根据反应热与键能的关系△H=∑D(反应物)−∑D(生成物),由题意Cl+F═2ClF ΔH
2 2 1
=akJ/mol;Cl+3F═2ClF ΔH=bkJ/mol可知;ΔH=(243+157−2×248)kJ/mol=−96kJ/mol,ΔH=
2 2 3 2 1 2
(243+3×157−2×3x)kJ/mol=(714−6x)kJ/mol,即a=−96,b=714−6x,设参与Cl+F═2ClF ΔH1=
2 2
akJ/mol的氯气物质的量为m,则消耗的氟气也为m,剩下的氯气和氟气正好按Cl+3F═2ClF ΔH=
2 2 3 2bkJ/mol的系数比反应,即 ,解之得,m=1.5mol,则有1.5mol×(−96kJ/mol)+0.5mol×
(714−6x)kJ/mol=303kJ,解之得x=172,故选A。
高频考点四 热化学方程式的书写
例4.胶状液氢(主要成分是 和 )有望用于未来的运载火箭和空间运输系统。实验测得:
时, 完全燃烧生成液态水,放出 热量; 完全燃烧生成液态水和 ,放出
的热量。下列热化学方程式的书写中正确的是
A.
B.
C.
D.
【答案】B
【解析】CH 燃烧为放热反应,ΔH<0,A项错误;1molCH 燃烧放出890.3kJ,反应放热且产生
4 4
HO(l),B项正确;CH 燃烧产生的HO(l),C项错误;ΔH单位错误应该为2H(g)+O(g)=2HO(l)
2 4 2 2 2 2
ΔH=−571.6kJ/mol,D项错误;故选B。
【方法技巧】
书写热化学方程式要“五查”
(1)查热化学方程式是否配平。
(2)查各物质的聚集状态是否正确。
(3)查ΔH的“+”“-”符号是否正确。
(4)查反应热的单位是否为kJ·mol-1。
(5)查反应热的数值与化学计量数是否对应。
【变式探究】25℃、101kPa 下,碳、氢气、甲烷和葡萄糖的燃烧热依次是
393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol。下列热化学方程式中,正确的是
A.C(s)+ O(g)=CO(g) △H=-393.5kJ/mol
2
B.2H(g)+O(g)=2HO(l) △H=+571.6kJ/mol
2 2 2C.CH(g)+2O(g)=CO (g)+2HO(g) △H=-890.3kJ/mol
4 2 2 2
D. C H O(s)+3O(g)=3CO (g)+3HO(l) △H=-1400 kJ/mol
6 12 6 2 2 2
【答案】D
【解析】C完全燃烧生成CO,生成CO反应热小于393.5kJ/mol,A项错误;氢气的燃烧热应是1mol
2
氢气完全燃烧放热285.8kJ,△H为负值,B项错误;CH 完全燃烧生成CO 和液态水,C项错误;0.5mol
4 2
C H O(s)完全燃烧放出1400kJ/mol的热量,热化学方程式为 C H O(s)+3O(g)=3CO (g)+3HO(l)
6 12 6 6 12 6 2 2 2
△H=-1400 kJ/mol,D项正确;答案选D。
高频考点五 中和反应热的测定
例5.将V mL 1.0 mol·L-1HCl溶液和V mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,
1 2
实验结果如图所示(实验中始终保持V+V=50)。下列叙述正确的是( )
1 2
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可转化为热能
C.NaOH溶液的浓度约为1.0 mol·L-1
D.该实验表明有水生成的反应都是放热反应
【答案】B
【解析】从表中分析可知当加入HCl溶液5 mL、NaOH溶液45 mL反应后温度为22 ℃,故实验时环
境温度低于22 ℃,A错;中和反应为放热反应,故该实验表明化学能可转化为热能,B对;加入HCl溶液
30 mL反应放热最多,应是酸碱正好中和,故c(NaOH)=1.0 mol·L-1×=1.5 mol·L-1,C错;中和反应有水
生成,但有水生成的反应不一定是放热反应,如H+CuO=====HO+Cu是吸热反应,D错。
2 2
【举一反三】利用如图所示装置测定中和热的实验步骤如下:①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55
mol·L-1 NaOH溶液,并用同一温度计测出其温度;③将 NaOH溶液倒入小烧杯中,设法使之混合均匀,
测定混合液最高温度。
回答下列问题:
(1)写出该反应的热化学方程式[生成1 mol H O(l)时的反应热为-57.3 kJ/mol]:
2
___________________________________________________________。
(2)为什么所用NaOH溶液要稍过量?
___________________________________________________________。
(3)倒入NaOH溶液的正确操作是__________(填字母)。
A.沿玻璃棒缓慢倒入
B.分三次倒入
C.一次迅速倒入
(4)使盐酸与NaOH溶液混合均匀的正确操作是______(填字母)。
A.用温度计小心搅拌
B.揭开泡沫塑料板用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒上下轻轻地搅动
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反
应,其反应热分别为ΔH、ΔH、ΔH,则ΔH、ΔH、ΔH 的大小关系为________________。
1 2 3 1 2 3
(6)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃
-1。为了计算中和热,某学生实验记录数据如下:
起始温度t/℃ 终止温度t/℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 23.6依据该学生的实验数据计算,该实验测得的中和热ΔH=________(结果保留一位小数)。
(7)________(填“能”或“不能”)用Ba(OH) 溶液和硫酸代替氢氧化钠溶液和盐酸,理由是
2
_____________________________________________________________________。
【解析】(2)在中和热的测定实验中为了确保一种反应物被完全中和,常常使加入的另一种反应物稍微
过量。(3)为了减少热量损失,NaOH溶液应该一次迅速倒入。(4)使盐酸与NaOH溶液混合均匀的正确操作
是用套在温度计上的环形玻璃搅拌棒上下轻轻地搅动。(5)稀氢氧化钠溶液和稀氢氧化钙溶液中溶质都完全
电离,它们的中和热相同,稀氨水中的溶质是弱电解质,它与盐酸反应时,一水合氨的电离要吸收热量,
故反应放出的热量要少一些(比较大小时,注意ΔH的正负号)。(6)取三次实验的平均值代入公式计算即
可。(7)硫酸与Ba(OH) 溶液反应生成BaSO 沉淀,沉淀的生成热会影响中和热的测定,故不能用Ba(OH)
2 4 2
溶液和硫酸代替氢氧化钠溶液和盐酸。
【答案】(1)HCl(aq)+NaOH(aq)===NaCl(aq)+HO(l) ΔH=-57.3 kJ·mol-1 (2)确保盐酸被完全中和
2
(3)C (4)D (5)ΔH =ΔH <ΔH (6)-51.8 kJ·mol-1 (7)不能 HSO 与Ba(OH) 反应生成BaSO 沉淀,沉
1 2 3 2 4 2 4
淀的生成热会影响中和热的测定
高频考点六 盖斯定律及其应用
例6.(2022·全国乙卷)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并
加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
③
计算 热分解反应④ 的 ________ 。
(2)较普遍采用的 处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利
用反应④高温热分解 。相比克劳斯工艺,高温热分解方法的优点是________,缺点是________。
【答案】(1)170 (2) 副产物氢气可作燃料 耗能高
【解析】
(1)已知:①2HS(g)+3O(g)=2SO (g)+2HO(g) ΔH=-1036kJ/mol
2 2 2 2 1
②4HS(g)+2SO (g)=3S(g)+4HO(g) ΔH=94kJ/mol
2 2 2 2 2
③2H(g)+O(g)=2HO(g) ΔH=-484kJ/mol
2 2 2 3
根据盖斯定律(①+②)×-③即得到2HS(g)=S(g)+2H(g)的
2 2 2
ΔH=(-1036+94)kJ/mol×+484kJ/mol=170 kJ/mol;
4
(2)根据盖斯定律(①+②)×可得2HS(g)+O(g)=S(g)+2HO(g)
2 2 2 2
ΔH=(-1036+94)kJ/mol×=-314kJ/mol,因此,克劳斯工艺的总反应是放热反应;根据硫化氢分解的
化学方程式可知,高温热分解方法在生成单质硫的同时还有氢气生成。因此,高温热分解方法的优点是:
可以获得氢气作燃料;但由于高温分解HS会消耗大量能量,所以其缺点是耗能高;
2
【变式探究】[2022·湖北,19(1)]已知:
①CaO(s)+H
2
O( l) Ca(OH)
2
(s) ΔH
1
=-65.17 kJ·mol-1
②Ca(OH)
2
(s ) Ca2+(aq)+2OH-(aq) ΔH
2
=-16.73 kJ·mol-1
③Al(s)+OH-(aq)+3HO(l)[Al(OH) ]-(aq)+H(g) ΔH=-415.0 kJ·mol-1
2 4 2 3
则CaO(s)+2Al(s)+7HO(l)===Ca2+(aq)+2[Al(OH) ]-(aq)+3H(g)的ΔH=_______kJ·mol-1。
2 4 2 4
【答案】-911.9
【解析】根据盖斯定律,①+②+2×③可得反应CaO(s)+2Al(s)+7HO(l)===Ca2+(aq)+2[Al(OH)]-
2 4
(aq)+3H(g),则ΔH=ΔH+ΔH+2ΔH=(-65.17 kJ·mol-1)+(-16.73 kJ·mol-1)+2×(-415.0 kJ·mol-1)=
2 4 1 2 3
-911.9 kJ·mol-1。
【变式探究】在一定条件下,Xe(g)与F(g)反应生成XeF (g)(n=2,4,6)的平衡气体。550K时主要为
2 n
XeF (g),850K时主要为XeF (g),高温时生成XeF (g)。其变转化关系如下:
6 4 2
下列说法不正确的是
A.∆H<0,∆H<0 B.∆H=∆H -∆H
1 5 3 5 4
C.∆H>0 D.∆H-∆H =∆H -∆H
3 1 3 4 6
【答案】C
【解析】大多数化合反应是放热反应,所以∆H<0,∆H<0,∆H<0,∆H<0,∆H<0,∆H<0,A正
1 2 3 4 5 6确;由Xe(g)→XeF (g),还有1个途径:Xe(g)→XeF (g)→XeF (g),根据盖斯定律,则有∆H=∆H +∆H ,B
6 4 6 5 4 3
正确;大多数化合反应是放热反应,所以∆H<0,∆H<0,∆H<0,∆H<0,∆H<0,∆H<0,C错误;由
1 2 3 4 5 6
Xe(g)→XeF (g),还有2个途径:Xe(g)→XeF (g)→XeF (g)∆H=∆H +∆H ,
6 4 6 4 3
Xe(g)→XeF (g)→XeF (g)∆H=∆H +∆H ,根据盖斯定律,则有
2 6 1 6
Xe(g)→XeF (g)→XeF (g)∆H=∆H +∆H =∆H +∆H ,即∆H-∆H =∆H -∆H ,D正确;故选C。
4 6 4 3 1 6 1 3 4 6
高频考点七 燃烧热和中和热
例7.(2022·海南卷)某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
回答问题:
(1)已知:电解液态水制备 ,电解反应的 。由此计算 的燃烧
热(焓) _______ 。
(2)已知: 的平衡常数(K)与反应温度(t)之间的关系如
图1所示。
若反应为基元反应,且反应的 与活化能(Ea)的关系为 。补充完成该反应过程的能量变化
示意图(图2)_______。【答案】(1)-286
(2)
【解析】
(1)电解液态水制备 ,电解反应的 ,由此可以判断,2mol 完
全燃烧消耗 ,生成液态水的同时放出的热量为572kJ ,故1mol 完全燃烧生成液态水放
出的热量为286kJ,因此, 的燃烧热(焓) -286 。
(2)由 的平衡常数(K)与反应温度(t)之间的关系图可
知,K随着温度升高而减小,故该反应为放热反应。若反应为基元反应,则反应为一步完成,由于反应的
与活化能(Ea)的关系为 ,由图2信息可知 =a ,则 a ,该反应
为放热反应,生成物的总能量小于反应物的,因此该反应过程的能量变化示意图为:。
【方法技巧】
(1)有关燃烧热的判断,一看是否以1 mol可燃物为标准,二看是否生成稳定氧化物。
(2)有关中和热的判断,一看是否以生成1 mol H O(l)为标准,二看酸碱的强弱和浓度,应充分考虑弱
2
酸、弱碱电离吸热,浓的酸碱稀释放热等因素。
【变式探究】下列热化学方程式中,ΔH能正确表示物质的燃烧热的是
A.
B.
C.
D.
【答案】A
【分析】燃烧热表示1mol可燃物完全燃烧生成稳定氧化物所放出的热量,表示燃烧热的热化学方程
式中可燃物为1mol,产物为稳定氧化物。
【解析】由热化学方程式可知,1mol一氧化碳完全燃烧生成二氧化碳放出283.0kJ的热量,ΔH能正确
表示一氧化碳的燃烧热,故A符合题意;一氧化碳不是稳定氧化物,ΔH不能正确表示碳的燃烧热,故B
不符合题意;气态水不是稳定氧化物,ΔH不能正确表示氢气的燃烧热,故C不符合题意;辛烷的物质的
量不是1mol,ΔH不能正确表示辛烷的燃烧热,故D不符合题意;综上所述答案为A。
【变式探究】化学反应中的能量变化,通常主要表现为热量的变化。下列相关表述正确的是
A.一定条件下,将 和 置于密闭容器中充分反应生成 放热 ,其热化学方
程式为:B.在 时, 完全燃烧生成液态水,放出 热量,表示氢气燃烧热的热化学方程式表
示为:
C.
D. 和 反应的中和热 ,则 和足量 反应的
【答案】B
【解析】 一定条件下,将 和 置于密闭容器中充分反应生成 放热 ,则I 和
2
H 反应生成1molHI(g)时放热大于akJ,放热焓变为负,则其热化学方程式I(g )+H (g) 2HI(g) H
2 2 2
<-2akJ•mol-1,故A错误;燃烧热是指在一定压强下,1 mol的可燃物完全燃烧生成稳⇌定的氧化△物的时候所
放出的热量;在 时, 完全燃烧生成液态水,放出 热量,表示氢气燃烧热的热化学方程
式表示为: ,B正确;硫蒸气的能量比等质量的固态硫能量高、
则等量的硫蒸汽燃烧生成二氧化硫气体比固态硫燃烧放出的热量多,焓变为负值时,放出热量越多,焓变
越小,则 ,故C错误; 和 反应
的中和热 ,硫酸和足量 反应生成硫酸钡沉淀和水,由于生成沉淀,也要放热,则
和足量 反应放出的热量大于盐酸和氢氧化钠反应1mol液态HO时放出的热量、即大
2
于57.3kJ,则 和足量 反应的 ,故D错误;答案选B。