文档内容
第 15 讲 化学反应的热效应
【学科核心素养】
变化观念与平衡思想:认识化学变化的本质是有新物质生成,并伴有能量的转化;能多角度、动态地
分析热化学方程式,运用热化学反应原理解决实际问题。
证据推理与模型认知:通过分析、推理等方法认识研究反应热的本质,建立盖斯定律模型。
科学态度与社会责任:赞赏化学对社会发展的重大贡献,具有可持续发展意识和绿色化学观念,能对
与化学有关的社会热点问题做出正确的价值判断。
【核心素养发展目标】
1.了解化学反应中能量转化的原因及常见的能量转化形式。
2.了解化学能与热能的相互转化,了解吸热反应、放热反应、反应热等概念。
3.了解热化学方程式的含义,能正确书写热化学方程式。
4.了解焓变(ΔH)与反应热的含义。
5.理解盖斯定律,并能运用盖斯定律进行有关反应焓变的计算。
6.了解能源是人类生存和社会发展的重要基础,了解化学在解决能源危机中的重要作用。
【知识点解读】
知识点一 焓变、热化学方程式
1.反应热(焓变)
(1)概念:在恒压条件下进行的反应的热效应。
符号:ΔH。
单位:kJ·mol-1或kJ/mol。
(2)表示方法
吸热反应:ΔH>0;放热反应:ΔH<0。
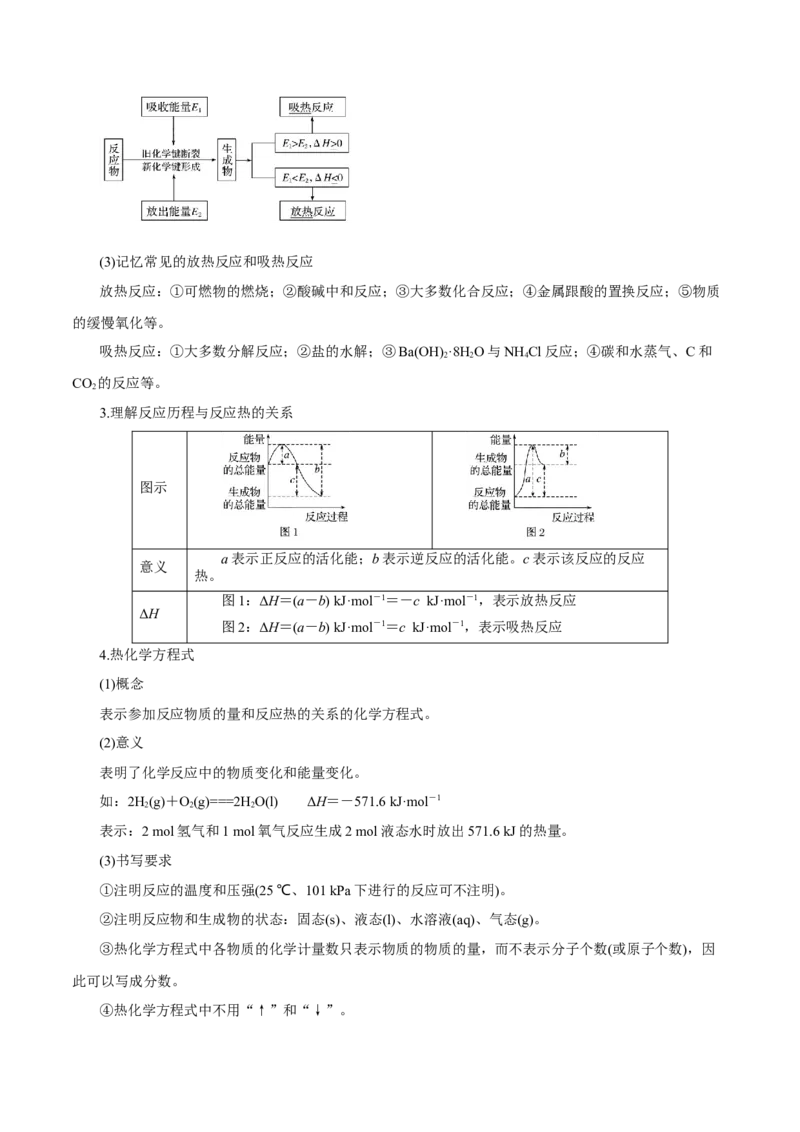
2.放热反应和吸热反应的判断
(1)从反应物和生成物的总能量相对大小的角度分析,如图所示。
(2)从反应热的量化参数——键能的角度分析(3)记忆常见的放热反应和吸热反应
放热反应:①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的置换反应;⑤物质
的缓慢氧化等。
吸热反应:①大多数分解反应;②盐的水解;③Ba(OH) ·8H O与NH Cl反应;④碳和水蒸气、C和
2 2 4
CO 的反应等。
2
3.理解反应历程与反应热的关系
图示
a表示正反应的活化能;b表示逆反应的活化能。c表示该反应的反应
意义
热。
图1:ΔH=(a-b) kJ·mol-1=-c kJ·mol-1,表示放热反应
ΔH
图2:ΔH=(a-b) kJ·mol-1=c kJ·mol-1,表示吸热反应
4.热化学方程式
(1)概念
表示参加反应物质的量和反应热的关系的化学方程式。
(2)意义
表明了化学反应中的物质变化和能量变化。
如:2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
表示:2 mol氢气和1 mol氧气反应生成2 mol液态水时放出571.6 kJ的热量。
(3)书写要求
①注明反应的温度和压强(25 ℃、101 kPa下进行的反应可不注明)。
②注明反应物和生成物的状态:固态(s)、液态(l)、水溶液(aq)、气态(g)。
③热化学方程式中各物质的化学计量数只表示物质的物质的量,而不表示分子个数(或原子个数),因
此可以写成分数。
④热化学方程式中不用“↑”和“↓”。⑤由于ΔH与反应物的物质的量有关,所以热化学方程式中物质的化学计量数必须与ΔH相对应,如果
化学计量数加倍,则ΔH也要加倍。当反应向逆反应方向进行时,其反应热与正反应的反应热数值相等,
符号相反。
【方法技巧】
(1)焓变与反应发生的条件、反应进行是否彻底无关。
(2)催化剂能降低反应所需活化能,但不影响焓变的大小。
(3)在化学反应中,反应物各原子之间的化学键不一定完全断裂。
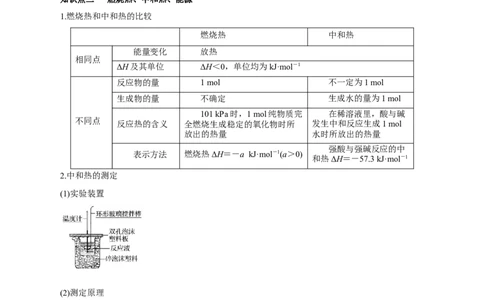
知识点二 燃烧热、中和热、能源
1.燃烧热和中和热的比较
燃烧热 中和热
能量变化 放热
相同点
ΔH及其单位 ΔH<0,单位均为kJ·mol-1
反应物的量 1 mol 不一定为1 mol
生成物的量 不确定 生成水的量为1 mol
101 kPa时,1 mol纯物质完 在稀溶液里,酸与碱
不同点
反应热的含义 全燃烧生成稳定的氧化物时所 发生中和反应生成1 mol
放出的热量 水时所放出的热量
强酸与强碱反应的中
表示方法 燃烧热ΔH=-a kJ·mol-1(a>0)
和热ΔH=-57.3 kJ·mol-1
2.中和热的测定
(1)实验装置
(2)测定原理
ΔH=-
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;
n为生成HO的物质的量。
2
(3)注意事项
①泡沫塑料板和碎泡沫塑料(或纸条)的作用是保温。
②为保证酸完全中和,采取的措施是若采用的酸、碱浓度相等,可采用碱体积稍过量。
3.能源(1)能源分类
(2)解决能源问题的措施
①提高能源的利用效率:a.改善开采、运输、加工等各个环节;b.科学控制燃烧反应,使燃料充分燃烧。
②开发新能源:开发资源丰富、可以再生、没有污染或污染很小的新能源。
【方法技巧】
(1)有关燃烧热的判断,一看是否以1 mol可燃物为标准,二看是否生成稳定氧化物。
(2)有关中和热的判断,一看是否以生成1 mol H O为标准,二看酸碱的强弱和浓度,应充分考虑弱酸、
2
弱碱,电离吸热,浓的酸碱稀释放热等因素。
知识点三 盖斯定律、反应热的计算与比较
1.盖斯定律
(1)内容
对于一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的。即:化学反应的反应热只
与反应体系的始态和终态有关,而与反应的途径无关。
(2)意义
间接计算某些反应的反应热。
(3)应用
转化关系 反应热间的关系
aA――→B、A――→B ΔH=aΔH
1 2
A B ΔH=-ΔH
1 2
ΔH=ΔH+ΔH
1 2
2.利用盖斯定律计算反应热
(1)运用盖斯定律的技巧——“三调一加”
一调:根据目标热化学方程式,调整已知热化学方程式中反应物和生成物的左右位置,改写已知的热
化学方程式。二调:根据改写的热化学方程式调整相应ΔH的符号。
三调:调整中间物质的化学计量数。
一加:将调整好的热化学方程式及其ΔH相加。
(2)运用盖斯定律的三个注意事项
①热化学方程式乘以某一个数时,反应热的数值必须也乘上该数。
②热化学方程式相加减时,物质之间相加减,反应热也必须相加减。
③将一个热化学方程式颠倒时,ΔH的“+”“-”随之改变,但数值不变。
3.反应热大小的比较
(1)看物质状态。物质的气、液、固三态转化时的能量变化如下:
(2)看ΔH的符号。比较反应热大小时不要只比较ΔH数值的大小,还要考虑其符号。
(3)看化学计量数。当反应物与生成物的状态相同时,化学计量数越大,放热反应的ΔH越小,吸热反
应的ΔH越大。
(4)看反应的程度。对于可逆反应,参加反应的物质的量和状态相同时,反应的程度越大,热量变化越
大。
【方法技巧】
(1)直接比较法
①物质燃烧时,可燃物物质的量越大,燃烧放出的热量越多。
②等量的可燃物完全燃烧所放出的热量肯定比不完全燃烧所放出的热量多。
③生成等量的水时,强酸和强碱的稀溶液反应比弱酸和强碱或弱碱和强酸或弱酸和弱碱的稀溶液反应
放出的热量多。
④对于可逆反应,因反应不能进行完全,实际反应过程中放出或吸收的热量要小于相应热化学方程式
中的反应热数值。例如:2SO
2
(g)+O
2
(g) 2SO
3
(g) ΔH=-197 kJ·mol-1,表示2 mol SO
2
(g)和1 mol
O(g)完全反应生成2 mol SO (g)时,放出的热量为197 kJ,实际上向密闭容器中通入2 mol SO (g)和1 mol
2 3 2
O(g),反应达到平衡后,放出的热量要小于197 kJ。
2
(2)盖斯定律比较法
①同一反应,生成物状态不同时
如A(g)+B(g)===C(g) ΔH<0
1
A(g)+B(g)===C(l) ΔH<0
2C(g)===C(l) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
1 3 2 1 2 3
所以ΔH<ΔH。
2 1
②同一反应,反应物状态不同时
如S(g)+O(g)===SO (g) ΔH<0
2 2 1
S(s)+O(g)===SO (g) ΔH<0
2 2 2
S(g)===S(s) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
2 3 1 1 2 3
所以ΔH<ΔH。
1 2
【典例剖析】
高频考点一 化学反应中能量变化探析
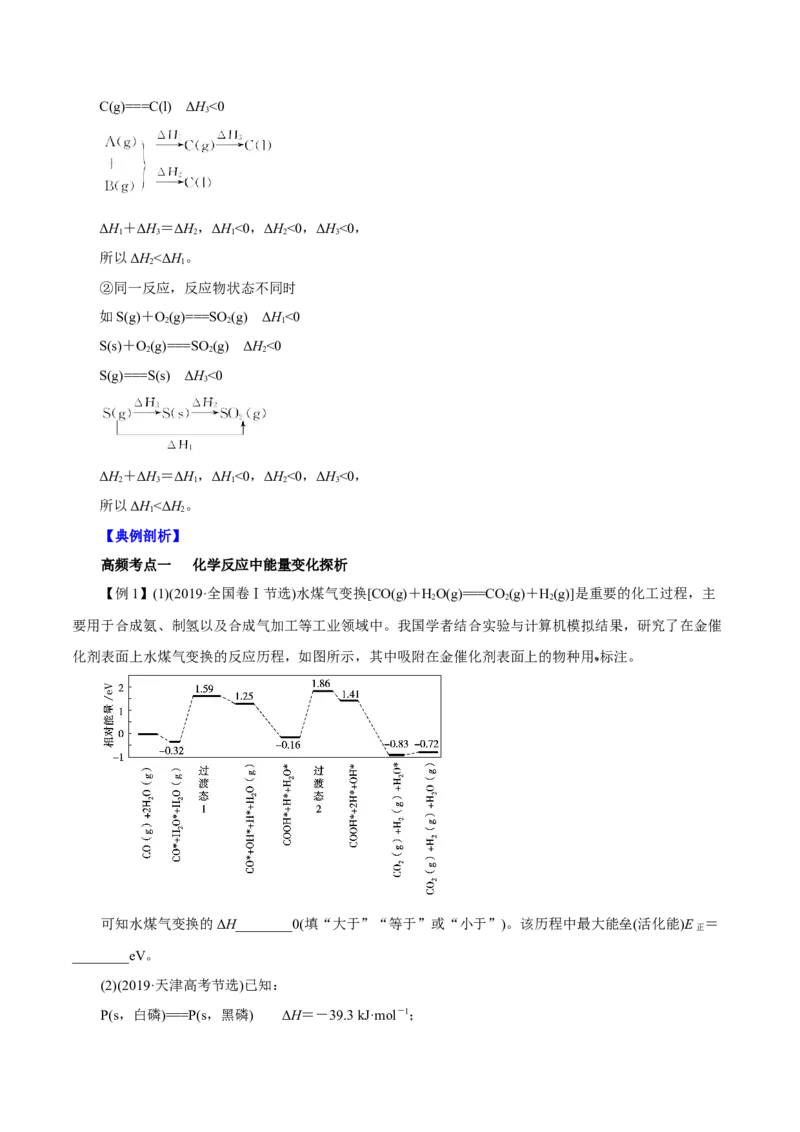
【例1】(1)(2019·全国卷Ⅰ节选)水煤气变换[CO(g)+HO(g)===CO (g)+H(g)]是重要的化工过程,主
2 2 2
要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催
化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。
可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E =
正
________eV。
(2)(2019·天津高考节选)已知:
P(s,白磷)===P(s,黑磷) ΔH=-39.3 kJ·mol-1;P(s,白磷)===P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是________。
(3)(2019·北京高考节选)已知反应器中还存在如下反应:
ⅰ.CH (g)+HO(g)===CO(g)+3H(g) ΔH
4 2 2 1
ⅱ.CO(g)+HO(g)===CO (g)+H(g) ΔH
2 2 2 2
ⅲ.CH (g)===C(s)+2H(g) ΔH
4 2 3
……
ⅲ为积炭反应,利用ΔH 和ΔH 计算ΔH 时,还需要利用________________________反应的ΔH。
1 2 3
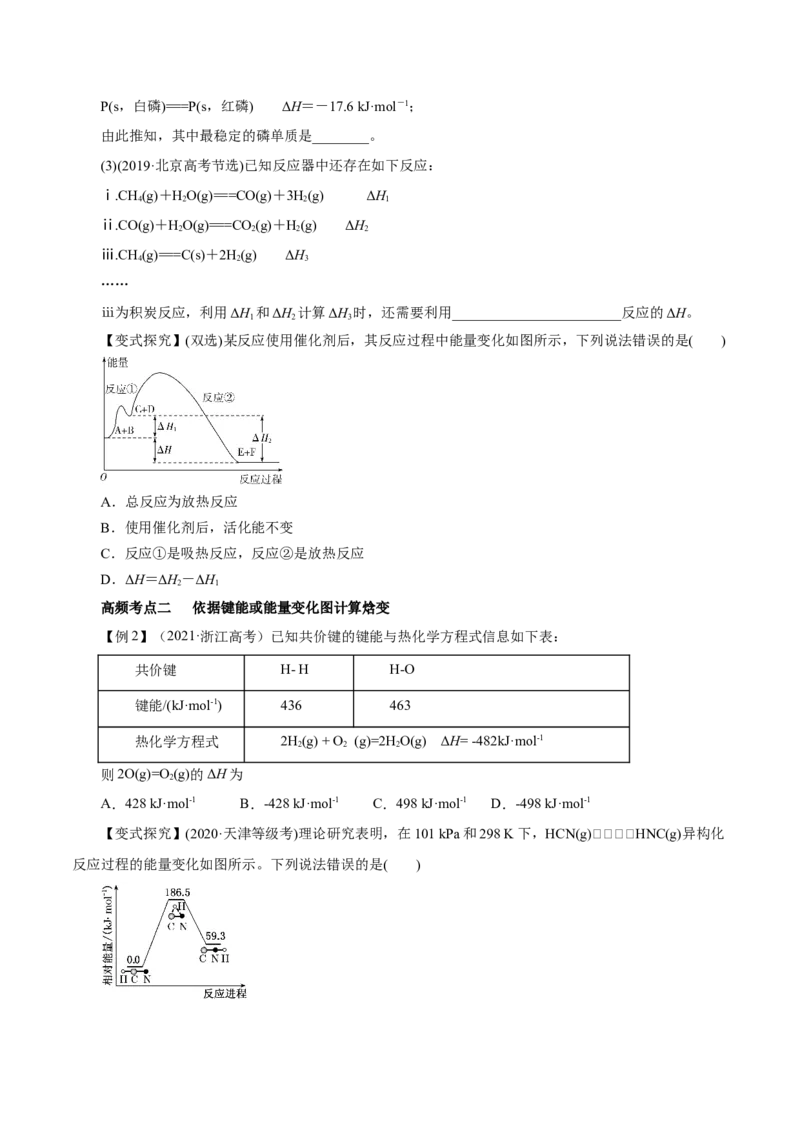
【变式探究】(双选)某反应使用催化剂后,其反应过程中能量变化如图所示,下列说法错误的是( )
A.总反应为放热反应
B.使用催化剂后,活化能不变
C.反应①是吸热反应,反应②是放热反应
D.ΔH=ΔH-ΔH
2 1
高频考点二 依据键能或能量变化图计算焓变
【例2】(2021·浙江高考)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
热化学方程式 2H(g) + O (g)=2HO(g) ΔH= -482kJ·mol-1
2 2 2
则2O(g)=O (g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
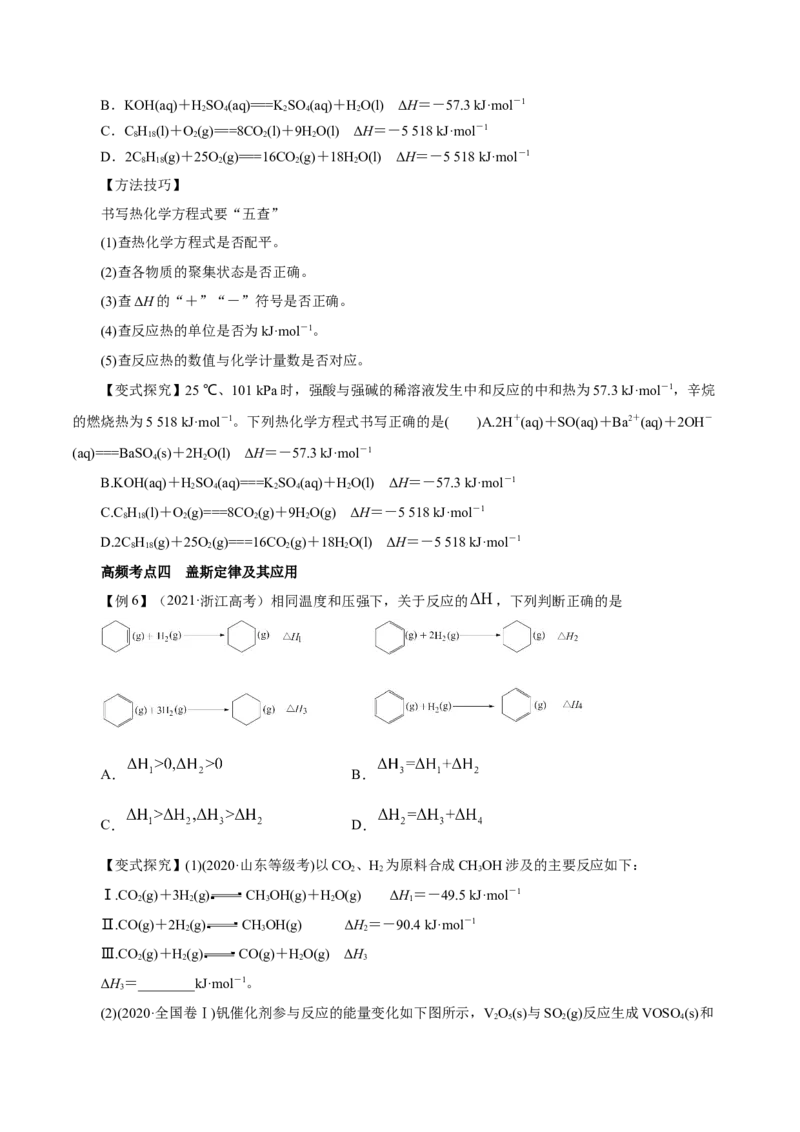
【变式探究】(2020·天津等级考)理论研究表明,在101 kPa和298 K下,HCN(g)HNC(g)异构化
反应过程的能量变化如图所示。下列说法错误的是( )A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
【变式探究】(2019·海南高考)根据图中的能量关系,可求得C—H键的键能为( )
A.414 kJ·mol-1 B.377 kJ·mol-1
C.235 kJ·mol-1 D.197 kJ·mol-1
【方法技巧】
1.熟记反应热ΔH的基本计算公式
ΔH=生成物的总能量-反应物的总能量
ΔH=反应物的总键能-生成物的总键能
2.常见1 mol物质中的化学键数目
1 mol CO 2 CH 4 N 2 H 4 (N—N、 SiO 2 金刚
P 石墨 S Si
4 石 8
物质 (CO) (C—H) N—H) (Si—O)
化学键 N—N:N
A
2N 4N 6N 4N 1.5N 2N 8N 2N
A A A A A A A A
数目 N—H:4N
A
【变式探究】(双选)根据如下能量关系示意图,判断下列说法正确的是( )
A.1 mol C(s)与1 mol O (g)的能量之和为393.5 kJ
2
B.反应2CO(g)+O(g)===2CO (g)中,生成物的总能量大于反应物的总能量
2 2
C.由C(s)→CO(g)的热化学方程式为2C(s)+O(g)===2CO(g) ΔH=-221.2 kJ·mol-1
2
D.热值指一定条件下单位质量的物质完全燃烧所放出的热量,则CO的热值为10.1 kJ·g-1
高频考点三 热化学方程式的书写
【例3】(双选)25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,辛烷
的燃烧热为5 518 kJ·mol-1。下列热化学方程式书写正确的是( )
A.2H+(aq)+SO(aq)+Ba2+(aq)+2OH-(aq)===BaSO (s)+2HO(l) ΔH=-57.3 kJ·mol-1
4 2B.KOH(aq)+HSO (aq)===K SO (aq)+HO(l) ΔH=-57.3 kJ·mol-1
2 4 2 4 2
C.C H (l)+O(g)===8CO (l)+9HO(l) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
D.2C H (g)+25O(g)===16CO (g)+18HO(l) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
【方法技巧】
书写热化学方程式要“五查”
(1)查热化学方程式是否配平。
(2)查各物质的聚集状态是否正确。
(3)查ΔH的“+”“-”符号是否正确。
(4)查反应热的单位是否为kJ·mol-1。
(5)查反应热的数值与化学计量数是否对应。
【变式探究】25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,辛烷
的燃烧热为5 518 kJ·mol-1。下列热化学方程式书写正确的是( )A.2H+(aq)+SO(aq)+Ba2+(aq)+2OH-
(aq)===BaSO (s)+2HO(l) ΔH=-57.3 kJ·mol-1
4 2
B.KOH(aq)+HSO (aq)===K SO (aq)+HO(l) ΔH=-57.3 kJ·mol-1
2 4 2 4 2
C.C H (l)+O(g)===8CO(g)+9HO(g) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
D.2C H (g)+25O(g)===16CO(g)+18HO(l) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
高频考点四 盖斯定律及其应用
【例6】(2021·浙江高考)相同温度和压强下,关于反应的 ,下列判断正确的是
A. B.
C. D.
【变式探究】(1)(2020·山东等级考)以CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.CO
2
(g)+3H
2
(g ) CH
3
OH(g)+H
2
O(g) ΔH
1
=-49.5 kJ·mol-1
Ⅱ.CO(g)+2H
2
(g ) CH
3
OH(g) ΔH
2
=-90.4 kJ·mol-1
Ⅲ.CO
2
(g)+H
2
(g ) CO(g)+H
2
O(g) ΔH
3
ΔH=________kJ·mol-1。
3
(2)(2020·全国卷Ⅰ)钒催化剂参与反应的能量变化如下图所示,VO(s)与SO (g)反应生成VOSO(s)和
2 5 2 4VO(s)的热化学方程式为_______________________________________。
2 4
【变式探究】(2020·浙江7月选考)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+H
2
O( l) HCO(aq)+OH-(aq) ΔH
2
OH-(aq)+H+(aq)===H O(l) ΔH
2 3
OH-(aq)+CHCOOH(aq)===CH COO-(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH<ΔH
1 2 1 2
C.ΔH<0 ΔH>0 D.ΔH>ΔH
3 4 3 4
【变式探究】[2019·高考全国卷Ⅲ,28(2)]近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢
的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。Deacon发明的直接氧
化法为4HCl(g)+O(g)===2Cl(g)+2HO(g),可按下列催化过程进行:
2 2 2
CuCl (s)===CuCl(s)+Cl(g) ΔH=+83 kJ·mol-1
2 2 1
CuCl(s)+O(g)===CuO(s)+Cl(g) ΔH=-20 kJ·mol-1
2 2 2
CuO(s)+2HCl(g)===CuCl (s)+HO(g) ΔH=-121 kJ·mol-1
2 2 3
则4HCl(g)+O(g)===2Cl(g)+2HO(g)的ΔH=________kJ·mol-1。
2 2 2
【举一反三】 [2019新课标Ⅲ节选]近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出
量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
Deacon直接氧化法可按下列催化过程进行:
CuCl (s)=CuCl(s)+ Cl(g) ΔH=83 kJ·mol− 1
2 2 1
CuCl(s)+ O(g)=CuO(s)+ Cl(g) ΔH=− 20 kJ·mol− 1
2 2 2
CuO(s)+2HCl(g)=CuCl (s)+HO(g) ΔH=− 121 kJ·mol− 1
2 2 3
则4HCl(g)+O (g)=2Cl (g)+2HO(g)的ΔH=_________ kJ·mol− 1。
2 2 2
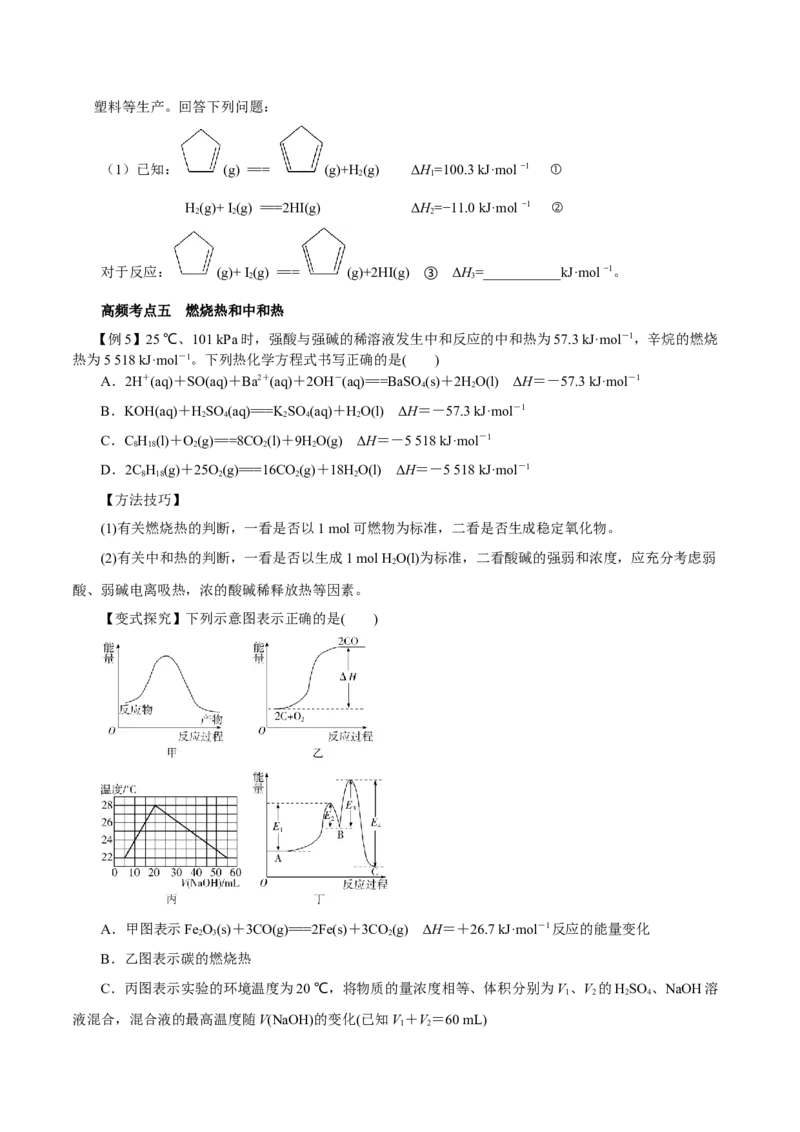
【举一反三】[2019新课标Ⅱ节选]环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知: (g) === (g)+H(g) ΔH=100.3 kJ·mol −1 ①
2 1
H(g)+ I (g) ===2HI(g) ΔH=−11.0 kJ·mol −1 ②
2 2 2
对于反应: (g)+ I (g) === (g)+2HI(g) ③ ΔH=___________kJ·mol −1。
2 3
高频考点五 燃烧热和中和热
【例5】25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,辛烷的燃烧
热为5 518 kJ·mol-1。下列热化学方程式书写正确的是( )
A.2H+(aq)+SO(aq)+Ba2+(aq)+2OH-(aq)===BaSO (s)+2HO(l) ΔH=-57.3 kJ·mol-1
4 2
B.KOH(aq)+HSO (aq)===K SO (aq)+HO(l) ΔH=-57.3 kJ·mol-1
2 4 2 4 2
C.C H (l)+O(g)===8CO (l)+9HO(g) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
D.2C H (g)+25O(g)===16CO (g)+18HO(l) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
【方法技巧】
(1)有关燃烧热的判断,一看是否以1 mol可燃物为标准,二看是否生成稳定氧化物。
(2)有关中和热的判断,一看是否以生成1 mol H O(l)为标准,二看酸碱的强弱和浓度,应充分考虑弱
2
酸、弱碱电离吸热,浓的酸碱稀释放热等因素。
【变式探究】下列示意图表示正确的是( )
A.甲图表示Fe O(s)+3CO(g)===2Fe(s)+3CO(g) ΔH=+26.7 kJ·mol-1反应的能量变化
2 3 2
B.乙图表示碳的燃烧热
C.丙图表示实验的环境温度为20 ℃,将物质的量浓度相等、体积分别为V、V 的HSO 、NaOH溶
1 2 2 4
液混合,混合液的最高温度随V(NaOH)的变化(已知V+V=60 mL)
1 2D.已知稳定性顺序:B<A<C,某反应由两步反应ABC 构成,反应过程中的能量变化曲线如丁图
【举一反三】利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55
mol·L-1 NaOH溶液,并用同一温度计测出其温度;③将 NaOH溶液倒入小烧杯中,设法使之混合均匀,
测定混合液最高温度。
回答下列问题:
(1)写出该反应的热化学方程式[生成1 mol H O(l)时的反应热为-57.3 kJ/mol]:
2
________________________________________________________________________。
(2)为什么所用NaOH溶液要稍过量?
________________________________________________________________________
________________________________________________________________________。
(3)倒入NaOH溶液的正确操作是__________(填字母)。
A.沿玻璃棒缓慢倒入
B.分三次倒入
C.一次迅速倒入
(4)使盐酸与NaOH溶液混合均匀的正确操作是______(填字母)。
A.用温度计小心搅拌
B.揭开泡沫塑料板用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒上下轻轻地搅动
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反
应,其反应热分别为ΔH、ΔH、ΔH,则ΔH、ΔH、ΔH 的大小关系为________________。
1 2 3 1 2 3
(6)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃
-1。为了计算中和热,某学生实验记录数据如下:
起始温度t/℃ 终止温度t/℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.22 20.2 20.4 23.4
3 20.5 20.6 23.6
依据该学生的实验数据计算,该实验测得的中和热ΔH=________(结果保留一位小数)。
(7)________(填“能”或“不能”)用Ba(OH) 溶液和硫酸代替氢氧化钠溶液和盐酸,理由是
2
_____________________________________________________________________。