文档内容
第十六讲 硫及其化合物
【基础巩固】
1.我国晋代《抱朴子》中描述了“丹砂(HgS)烧之成水银,积变又还成丹砂”。下列有关叙述正确的是(
)
A.“丹砂”和“水银”都是化合物
B.该描述中的反应是可逆反应
C.水银有恒定的体积膨胀系数,被用于制作温度计
D.“积变又还成丹砂”中的“还”可理解为“被还原”
2.如图是硫元素在自然界中的循环示意图,下列说法不正确的是( )
A.海水中的硫元素主要以S2-形式存在
B.煤中含有硫元素,燃煤中加入生石灰可脱硫
C.硫具有弱氧化性,和变价金属反应,通常将金属氧化成低价态
D.硫化氢溶于水得到氢硫酸,氢硫酸是弱酸,能与碱、碱性氧化物反应
3.下列关于鉴别1 mol·L-1稀硫酸和98%的浓硫酸的叙述正确的是( )
A.常温下测定两溶液的导电能力,导电能力强的是浓硫酸
B.常温下可以用铜片鉴别两种溶液
C.常温下不能用铝片鉴别两种溶液
D.两溶液敞口在空气中放置一段时间后质量明显增大的是浓硫酸
4.下列各物质在给定条件下通过一步反应就能实现所示转化的是( )
A.CuSO (aq)――→Cu(OH) (s)――→Cu O(s)
4 2 2
B.H S(g)――→SO (g)――→HSO (aq)
2 2 2 3
C.Fe(s)――→FeCl (s)――→Fe(OH) (s)
2 2
D.SO (g)――→NaSO (aq)――→NaSO (s)
2 2 3 2 3
5.(2021·山东卷)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法错误的是( )
2 3
A.吸收过程中有气体生成 B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高 D.中和后溶液中含NaSO 和NaHCO
2 3 3
6.(2022·石家庄模拟)根据SO 通入不同溶液中的实验现象,所得结论不正确的是( )
2
选项 溶液 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D 溴水 橙色褪去 SO 有还原性
2
7.(2022·广东省茂名市五校联盟高三联考)自然界中不同价态硫元素之间的转化如图所示,下列说法正确
的是( )
A.上图中,酸雨的含硫成分只有HSO ,由SO 溶于水生成
2 3 2
B.芒硝在浓硫酸中失水的过程体现了浓硫酸的脱水性
C.黄铁矿燃烧产生的尾气,与空气混合后通入碳酸钙的浆状物,可用来制备石膏
D.凝聚法是将SO 通入HS稀溶液中得到S胶体,该反应中氧化剂与还原剂的物质的量之比为2∶1
2 2
8.如表所示有关物质检验的实验结论正确的是( )
选项 实验操作及现象 实验结论
A 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 该溶液中一定含有SO
向某溶液中加入盐酸,将生成的气体通入品红溶液中,品红溶液褪
B 该溶液中一定含有SO
色
C 将某气体通入品红溶液中,品红溶液褪色 该气体一定是SO
2
将SO 通入NaCO 溶液中,生成的气体先通入足量的酸性KMnO 溶
D 2 2 3 4 说明酸性:HSO >HCO
液,再通入澄清石灰水中有浑浊产生 2 3 2 3
9.下图虚线框中的装置(试剂均足量)可用来检验浓硫酸与木炭粉在加热条件下反应所产生的所有气体产物,
其中供选择的试剂有无水硫酸铜、品红溶液、酸性高锰酸钾溶液、澄清石灰水四种试剂,下列说法正确的
是( )
A.物质甲可以是无水硫酸铜,也可以是变色硅胶、无水氯化钙等物质
B.丙中发生反应的离子方程式可能是SO +2OH-===SO+HO
2 2
C.乙和戊两种溶液都不宜用作尾气吸收装置中的试剂
D.如果将装置的连接顺序变为①③②,不影响检验10.已知2FeSO =====Fe O+SO ↑+SO ↑。下列有关操作、装置、原理及对现象的表述正确的是( )
4 2 3 2 3
A.用装置甲高温分解FeSO ,点燃酒精喷灯前应先向装置内通一段时间N
4 2
B.用装置乙可检验分解产生的SO ,现象是石蕊溶液先变红后褪色
2
C.用装置丙可检验分解产生的SO ,现象是产生白色沉淀
3
D.用装置丁可吸收尾气,避免污染环境
11.下图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.向溶液B中滴加KSCN溶液,溶液可能变为红色
B.溶液B转化为溶液C发生反应的离子方程式为4H++2Fe2++O===2Fe3++2HO
2 2
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
12.(2022·北京海淀区模拟)物质类别和核心元素的化合价是研究物质性质的两个重要视角。以硫及其化合物
与化合价变化为坐标的二维转化关系如图所示。
回答下列问题:
(1)图中 X 的电子式为________;其水溶液在空气中放置易变浑浊,写出反应的化学方程式:
_________________________________________________________________________。
该变化说明S的非金属性比O的________(填“强”或“弱”)。
(2)下列物质用于NaSO 的制备,从氧化还原反应的角度考虑,理论上有可能的是________(填字母)。
2 2 3
a.Na S+S b.Z+S c.Na SO +Y d.NaHS+NaHSO
2 2 3 3
(3)治理含CO、SO 的烟道气,以Fe O 为催化剂,将CO、SO 在380 ℃时转化为S和一种无毒气体,写出
2 2 3 2该反应的化学方程式:_______________________________________________________________。
13.某研究性学习小组在学习SO 的性质时,通过查阅文献、理性分析、实验验证与CO 的性质进行了比
2 2
较。试根据研究主题和过程,回答下列问题。
(1)水溶液的酸性
查阅文献知: 常温下,HSO 的电离常数K =1.2×10-2 ,K =6.3×10-3 ,HCO 的电离常数 K =
2 3 a1 a2 2 3 a1
4.4×10-7 ,K =4.7×10-11 。选用下面的药品和装置验证 HSO 和HCO 的酸性强弱,其连接顺序:
a2 2 3 2 3
A→___________________________________________________
(按气流方向用大写字母表示即可)。D装置的主要作用是______________________________。
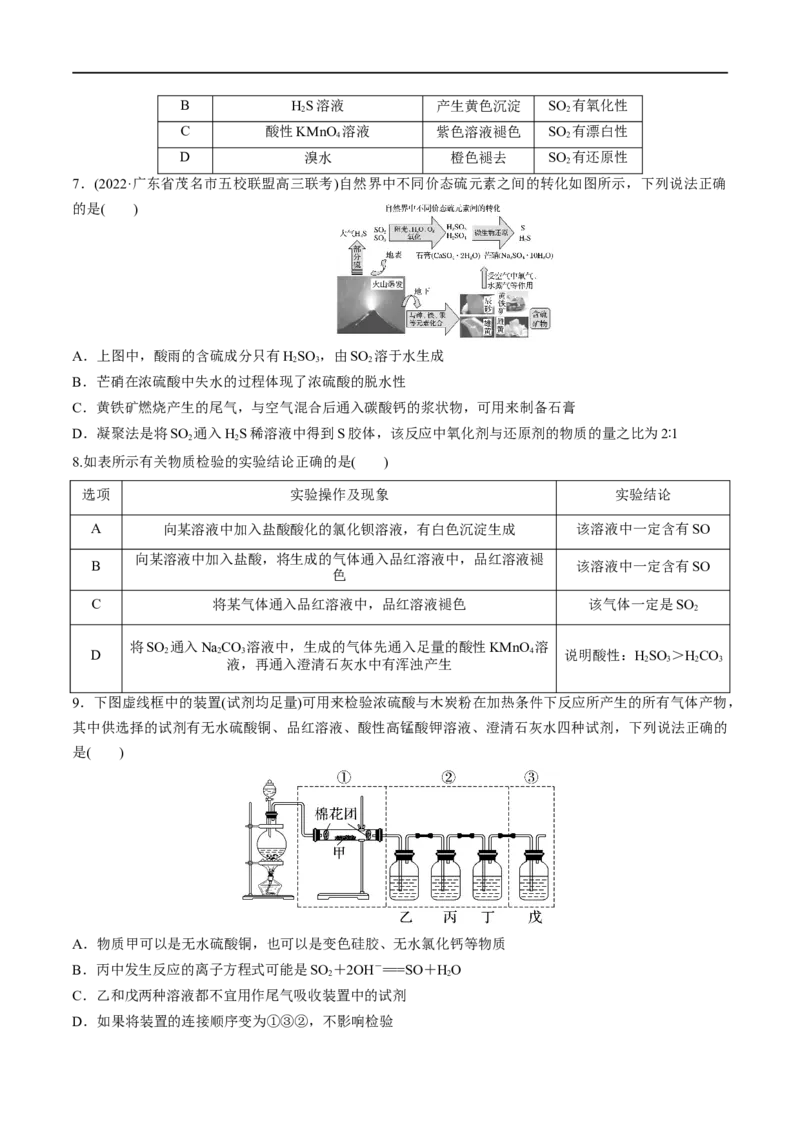
(2)二氧化硫的还原性
若按图示装置进行实验(部分固定装置未画出)。请你在实验前根据预设的操作,推测可能的实验现象及其
对应的原因。
预设的操作步骤 预期的实验现象 推测可能的原因
若将带火星的木条放在D SO 与NaO 反应无O 生成,可能发生反应
2 2 2 2
关闭弹簧夹2,打开弹簧
试管口处,木条不复燃 的化学方程式为①____________________
夹1,将浓硫酸注入三颈
若将带火星的木条放在D SO 与NaO 反应有O 生成,发生的反应:
2 2 2 2
烧瓶至浸没固体
试管口处,木条复燃 2SO +2NaO===2Na SO +O
2 2 2 2 3 2
关闭弹簧夹1,打开弹簧
E中②___________ E中反应的离子方程式③________________
夹2,残余气体进入E、F
F中④____________ F中反应为2OH- + SO ===SO+ HO
中 2 2
【拔高练习】
1.(2023春·河南洛阳·高三孟津县第一高级中学校考阶段练习)元素的价类二维图是我们学习元素及其化
合物、化合价相关知识的重要模型和工具,如图为铁元素的价类二维图,图中甲至庚均含铁元素。下列说
法正确的是A.在空气中加热丁,可实现丁→乙的转化
B.甲高温下与水蒸气的反应可实现甲乙的转化
C.己溶液是否含有 ,不能选用KSCN和新制的氯水检验
D.高铁酸根离子( )具有氧化性,可用于消毒, 与水反应最终可生成胶体,还可用作净水剂
2.(2023·陕西咸阳·统考二模)含硫化合物的反应具有多样性。下列反应的离子方程式书写错误的是
A.用NaSO 溶液吸收SO 废气:
2 3 2
B.海水提溴工艺中用SO 还原Br :
2 2
C.用Na
2
CO
3
溶液处理锅炉水垢中的CaSO
4
:CaSO
4
(s)+ (aq)⇌CaCO
3
(s)+ (aq)
D.用少量NaSO 溶液吸收水中的Cl:
2 2 3 2
3.(2023·江西·统考二模)N 为阿伏加德罗常数的值。硫及其化合物在生产、生活中有广泛应用。下列有
A
关叙述正确的是
A.6gSO 和SO 的混合物中含中子数为3N
2 3 A
B.32gS(如圈所示)中S原子形成共价键的数目为2N
8 A
C.1L0.5mol·L-1NaSO 溶液含阴离子总数小于0.5N
2 3 A
D.1molH S与适量O 完全反应转移电子数一定为2N
2 2 A
4.(2023·北京·高三专题练习) 和S均属于VIA族元素。下列关于Se及其化合物性质的比较不正确
的是
A.第一电离能: B.原子半径:Se