文档内容
第 16 讲 物质结构 原子核外电子排布
目录
考情分析 知识点2 能层和能级
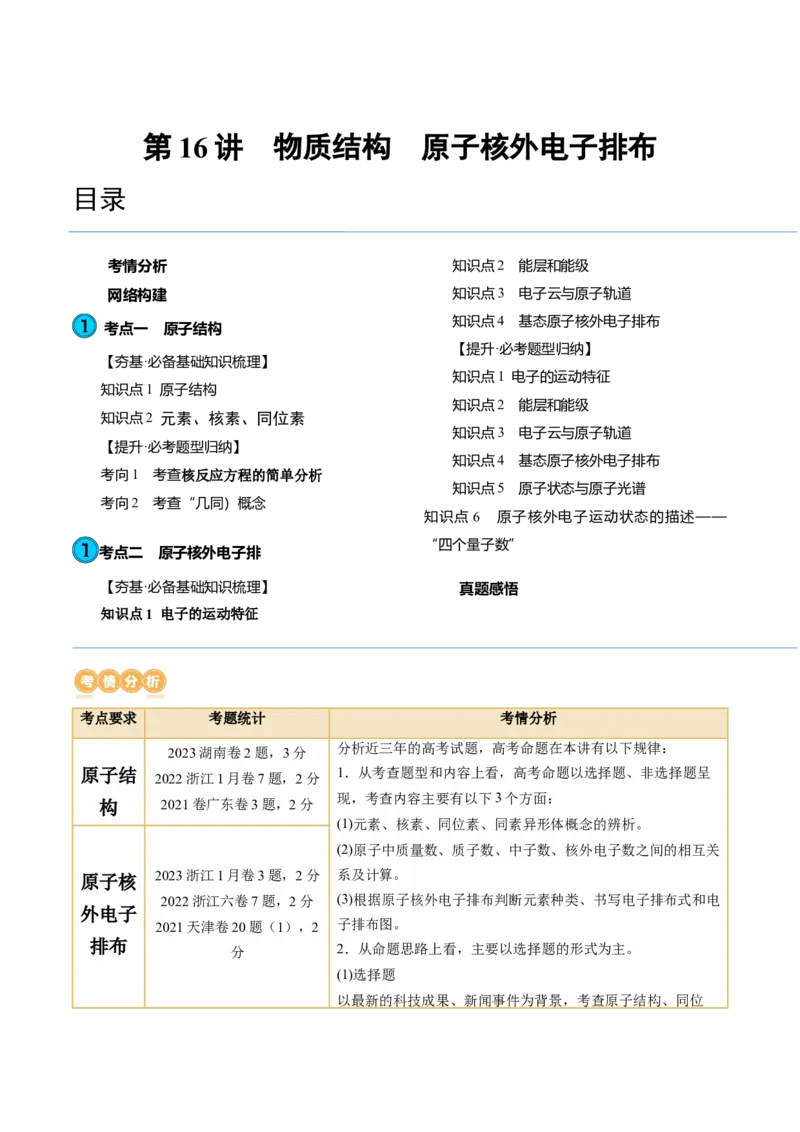
网络构建 知识点3 电子云与原子轨道
知识点4 基态原子核外电子排布
考点一 原子结构
【提升·必考题型归纳】
【夯基·必备基础知识梳理】
知识点1 电子的运动特征
知识点1 原子结构
知识点2 能层和能级
知识点2 元素、核素、同位素
知识点3 电子云与原子轨道
【提升·必考题型归纳】
知识点4 基态原子核外电子排布
考向1 考查核反应方程的简单分析
知识点5 原子状态与原子光谱
考向2 考查“几同)概念
知识点 6 原子核外电子运动状态的描述——
“四个量子数”
考点二 原子核外电子排
【夯基·必备基础知识梳理】 真题感悟
知识点1 电子的运动特征
考点要求 考题统计 考情分析
分析近三年的高考试题,高考命题在本讲有以下规律:
2023湖南卷2题,3分
原子结 1.从考查题型和内容上看,高考命题以选择题、非选择题呈
2022浙江1月卷7题,2分
现,考查内容主要有以下3个方面:
构 2021卷广东卷3题,2分
(1)元素、核素、同位素、同素异形体概念的辨析。
(2)原子中质量数、质子数、中子数、核外电子数之间的相互关
原子核
2023浙江1月卷3题,2分 系及计算。
2022浙江六卷7题,2分 (3)根据原子核外电子排布判断元素种类、书写电子排布式和电
外电子
2021天津卷20题(1),2 子排布图。
排布
分 2.从命题思路上看,主要以选择题的形式为主。
(1)选择题
以最新的科技成果、新闻事件为背景,考查原子结构、同位素、核素知识,核外电子排布表达式的正误判断。
(2)非选择题
直接考查电子排布式和电子排布图的书写,利用核外电子排布
推断元素等。
3.根据高考命题的特点和规律,复习时要注意以下几个方面:
(1)同位素和同素异形体的概念分析、原子构成微粒之间的关
系。
(2)原子结构及核外电子排布特性(全空、半充满、全充满的稳
定性)。
(3)规范化学术语的书写,重点掌握第四周期过渡元素的电子排
布式和电子排布图。
考点一 原子结构
知识点1 原子结构
1.原子的构成粒子
2.微粒之间的等式关系
1)质量关系:质量数(A)=质子数(Z)+中子数(N);
2)电性关系:
①原子中:质子数(Z)=核电荷数=核外电子数;
②阳离子的核外电子数=质子数-阳离子所带的电荷数,如Mg2+的核外电子数是10。
③阴离子的核外电子数=质子数+阴离子所带的电荷数,如Cl-的核外电子数是18。
3.微粒符号周围数字的含义【特别提醒】①原子中不一定都含有中子,如H中没有中子。
②电子排布完全相同的原子不一定是同一种原子,如互为同位素的各原子。
③易失去1个电子形成+1价阳离子的不一定是金属原子,如氢原子失去1个电子形成H+。
④形成稳定结构的离子最外层不一定是8个电子,如Li+为2个电子稳定结构。
知识点2 元素、核素、同位素
1.元素、核素、同位素的概念及相互关系
2.同位素的特征
①相同存在形态的同位素,化学性质几乎完全相同,物理性质不同。
②天然存在的同一元素各核素所占的原子百分数(丰度)一般不变。
3.同位素的“六同三不同”
4.常见的重要核素及其应用
核素 U C H(D) H(T) O
用途 核燃料 用于考古断代 制氢弹 示踪原子
5.元素、核素、同位素的联系与区别
①现行元素周期表已发现的元素有118种,由于同位素的存在,故核素的种数远大于118种。
②不同核素可能具有相同的质子数,如H、H;也可能具有相同的中子数,如C、O;也可能具有相同的质
量数,如C、N。
③同位素之间的转化,既不是物理变化也不是化学变化,是核反应。
④同位素之间可形成不同的同位素单质。如氢的三种同位素形成的单质有六种:H、D、T、HD、HT、
2 2 2
DT,他们的物理性质(如密度)有所不同,但化学性质几乎完全相同。
⑤同位素之间可形成不同的同位素化合物。如水分子有HO(普通水)、DO(重水)、TO(超重水)等。他们的
2 2 2
相对分子质量不同,物理性质(如密度)有所不同,但化学性质几乎完全相同。
6.相对原子质量
(1)原子(即核素)的相对原子质量:一个原子(即核素)的质量与一个12C质量的的比值。一种元素有几种同位素,就有几种不同核素的相对原子质量。
(2)元素的相对原子质量:是根据该元素各种天然同位素的相对原子质量按该元素各种天然同位素原子所占
的原子百分比算出的平均值。即:Ar(E)=Ar×a%+Ar×b%+Ar×c%+…,其中a%+b%+c%+…=1。
1 2 3
(3)核素的近似相对原子质量=该核素的质量数。
(4)元素的近似相对原子质量:是根据该元素各种天然同位素的质量数按该元素各种天然同位素原子所占的
原子百分比算出的平均值。即:Ar(E)=A×a%+A×b%+A×c%+…,其中a%+b%+c%+…=1。
1 2 3
7.核反应方程
①卢瑟福发现质子:N+He→O+H
②查德威克发现中子:Be+H→C+n
③铀核裂变反应:U+n→Kr+Ba+3n
④氘核与氚核聚变反应:H+H→He+n
考向1 核反应方程的简单分析
例1.(2023·全国·模拟预测)科学家利用 粒子(即氦核 )进行多种核反应: 、
。已知 和 都具有放射性,下列说法错误的是
A.X元素位于元素周期表的第二周期第ⅥA族
B. 和 互为同位素,化学性质相同
C. 、 都可作为示踪原子
D.核反应产生的能量可用于发电,属于化学能转化为电能
【答案】D
【解析】A.因为核反应过程中电子数不变,由题意可推出 ,所以X是O,位于元素周期表中第二周
期第ⅥA族,A正确;B.同位素的化学性质几乎相同,B正确;C.由于 、 都具有放射性,所以均
可作为示踪原子,C正确;D.核反应不属于化学反应的范畴,利用核反应产生的能量发电是将核能转化
为电能,D错误;故选D。
【变式训练】(2023·全国·统考模拟预测)已知核反应 Mg+ Cm→ Hs+5 n。下列说法正确的是
A. Hs与 Cm的中子数之差为21 B. Mg的原子结构示意图为
C. Cm和 Cm互为同素异形体 D.Cm位于元素周期表f区
【答案】D
【解析】A.根据质量守恒定律可知 ,则 的中子数为269﹣108=161,
的中子数为248﹣96=152,二者中子数之差为9,A项错误;B.Mg的原子序数为12, 的原子结构示意图为 ,B项错误;C. 和 互为同位素[提示:同一元素的不同核素互称为同位素],
C项错误;D.Cm为96号元素,基态Cm原子的核外电子排布式为 ,Cm位于元素周期表f
区,D项正确;故选D。
【思维建模】核反应方程分析思路
(1)质量数守恒:各微粒左上角数字之和在核反应前后相等;
(2)电荷数守恒:各微粒左下角数字之和(正电荷数)在核反应前后相等
例:碳14的β衰变:C→N+e
质量数守恒表达式:14=14+0;电荷数守恒表达式:6=7-1。
考向2 “几同”概念辨析
例2.(2023·天津河东·统考二模)下列叙述错误的是
A. 和 互为同系物 B. 和 互为同位素
C. 与 互为同素异形体 D.丙酸和甲酸乙酯互为同分异构体
【解析】A. 含有酚羟基,而 含有醇羟基,二者结构不相似,故不
互为同系物,A错误;B. 和 是质子数相同、中子数不同的原子,故互为同位素,B正确;C.
与 均为硫元素形成的不同单质,故互为同素异形体,C正确;D.丙酸即CHCHCOOH和甲酸乙酯即
3 2
HCOOCH CH,二者分子式相同而结构不同,故互为同分异构体,D正确;故答案为:A。
2 3
【答案】A
【变式训练】(2023·上海崇明·统考二模)科学家通过测定地球岩石和球粒陨石中 比例差异,为
月球起源“大撞击”假说提供了重要证据。25Mg与24Mg的说法正确的是
A.互为同素异形体 B.具有相同质量数
C.具有相似的化学性质 D.具有相同的中子数
【答案】C
【解析】A.25Mg与24Mg是质子数相同,中子数不同,两者互为同位素,故A错误;B.25Mg与24Mg两
者的质量数分别为25、24,故B错误;C.金属性的化学性质主要取决于最外层电子数,两者最外层电子
数相同,因此25Mg与24Mg两者具有相似的化学性质,故C正确;D.25Mg与24Mg两者的中子数分别为
13、12,故D错误。综上所述,答案为C。
考点二 原子核外电子排布
知识点1 电子的运动特征运动速度很快,与宏观物体的运动有极大不同:不能同时确定速度和位置,不能描绘动轨迹。
知识点2 能层和能级
(1)能层:根据多电子原子的核外电子的能量差异,将核外电子分成不同的能层,能层用n表示。n值越大,
能量越高。
(2)能级:
①根据多电子原子中同一能层电子能量的不同,将它们分成不同能级。
②能级用相应能层的序数和字母s、p、d、f组合在一起来表示,如n能层的能级按能量由低到高的顺序排
列为 n s 、 n p 、 n d 、 n f 等。
③能层序数等于该能层所包含的能级数,如第三能层有 3s 、 3p 、 3d 能级。
④s、p、d、f能级可容纳的电子数为1、3、5、7的二倍。
(3)能层、能级与其容纳的最多电子数之间的关系
能层(n) 一 二 三 四 五 六 七 …
符号 K L M N O P Q …
能级 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s … … … …
2 2 6 2 6 10 2 6 10 14 2 … … … …
容纳最多
电子数 2 8 18 32 …… … … 2n2
知识点3 电子云与原子轨道
(1)电子云:电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述。小黑点
越密,表示概率密度越大。由于核外电子的概率密度分布看起来像一片云雾,因而被形象地称作电子云。
(2)原子轨道:量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道。
能级符号 电子云形状 空间延伸方向
s 球形 一种
三种(相互垂直,分别相对
p 哑铃形
于x、y、z轴对称)
d / /
f / /
(3)轨道能量
①同能层的不同能级能量s