文档内容
第 17 讲 电解池 金属的腐蚀与防护
1.下列图示与对应的叙述相符的是
A.牺牲阳极的阴极保护法 B.粗铜的精炼 C.中和热的测定 D.未知浓度盐酸的滴定
【答案】B
【解析】A.A装置是利用电解原理防止钢闸门生锈,即外加电流的阴极保护法,其中钢闸门接外加
电源的负极、作阴极,发生得电子的还原反应,A错误;B.粗铜的精炼中粗铜作阳极,纯铜作阴极,B
正确;C.中和反应反应热的测定装置中,需要安装环形玻璃搅拌棒,以及烧杯空腔加入隔热材料等,C
错误;D.酸碱中和滴定中,NaOH为碱,应装在碱式滴定管中,D错误;故选B。
2.下列反应的电极反应式书写正确的是
A.钢铁发生吸氧腐蚀时,铁电极的电极反应式:
B.铅酸蓄电池放电时负极的电极反应式:
C.粗铜精炼时,与电源负极相连的电极的电极反应式:
D.碱性氢氧燃料电池负极的电极反应式:
【答案】D
【解析】A.钢铁发生吸氧腐蚀时,铁为负极,铁电极的电极反应式为Fe-2e-=Fe2+,故A错误;B.铅
酸蓄电池放电时,Pb为负极,负极的电极反应式: ,故B错误;C.粗铜精炼时,与
电源负极相连的电极为阴极,阴极反应式为 ,故C错误;D.碱性氢氧燃料电池,负极氢气失
电子生成水,负极的电极反应式为 ,故D正确;故选D。
3.下列有关金属的腐蚀与防护叙述正确的是A.铁管上镶嵌锌块,采用的是牺牲阳极法使铁不易被腐蚀
B.用锡焊接的铁质品,焊接处不易腐蚀
C.用铁电极电解饱和食盐水:
D.用外加电流法保护钢铁设备时,将设备连接电源正极
【答案】A
【解析】A.铁块上镶嵌锌块,锌金属活动性强于铁,作负极起到保护铁管的作用,采用的是牺牲阳
极的阴极保护法,A正确;B.铁的金属活动性强于锡,用锡焊接的铁制品,焊接处铁作负极较易被腐
蚀,B错误;C.用铁作电极电解饱和食盐水,阳极上铁失电子而不是氯离子失电子,C错误;D.用外加
电流法保护钢铁设备,设备连接电源负极,D错误;故选A。
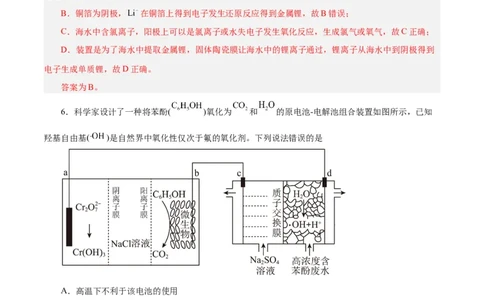
4.下列关于金属的电化学腐蚀与防护的说法正确的是
A.铜板打上铁铆 C.金属M比铁活 D.阴极的电极
B.钢闸门与电源的负极
钉后,铜板更易被腐 泼,电子由钢铁输水管 反应式为
相连,可防止钢闸门腐蚀
蚀 流出
【答案】B
【解析】A.铜板打上铁铆钉后,铁、铜与水膜形成原电池,铜做正极被保护,则铜板不易被腐蚀,
故A错误;B.钢闸门与电源的负极相连防止钢闸门腐蚀的方法为外加直流电源的阴极保护法,故B正
确;C.金属M比铁活泼,在潮湿的环境中M与铁构成原电池,M做负极被损耗,则电子由金属M流
出,故C错误;D.由图可知,与电源负极相连的铁管道为电解池的阴极,水在阴极得到电子发生还原反
应生成氢气和氢氧根离子,电极反应式为2HO+2e—=2OH—+H ↑,故D错误;故选B。
2 2
5.南京大学开发出一种以太阳能驱动的恒流电解装置,成功实现了从海水中提取金属锂,其工作原
理如图。下列说法不正确的是A.工作时的能量转化形式:太阳能→电能→化学能
B.铜箔为阴极, 在铜箔上发生氧化反应得到金属锂
C.阳极区可能有 和 生成
D.固体陶瓷膜可让海水中 选择性通过
【答案】B
【解析】A.该装置是先利用太阳能发电,然后电解海水生成锂,工作时的能量变化形式:太阳能→
电能→化学能,故A正确;
B.铜箔为阴极, 在铜箔上得到电子发生还原反应得到金属锂,故B错误;
C.海水中含氯离子,阳极上可以是氯离子或水失电子发生氧化反应,生成氯气或氧气,故C正确;
D.装置是为了海水中提取金属锂,固体陶瓷膜让海水中的锂离子通过,锂离子从海水中到阴极得到
电子生成单质锂,故D正确。
答案为B。
6.科学家设计了一种将苯酚( )氧化为 和 的原电池-电解池组合装置如图所示,已知
羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。下列说法错误的是
A.高温下不利于该电池的使用
B.电池工作一段时间后,NaCl溶液浓度保持不变
C.d电极的电极反应为:
D.相同时间内,c、d两极产生气体的体积比(相同条件下)为
【答案】B
【分析】该装置是原电池和电解池组合装置,左边是微生物燃料电池,右边是电解池,在原电池中苯
酚被氧化为二氧化碳,发生氧化反应是原电池的负极,重铬酸根离子被还原为Cr(OH) ,作正极,与b相
3连接的c是阴极发生还原反应,生成氢气,与a连接的d极为阳极,发生氧化反应,把废水中苯酚氧化成
二氧化碳除去。
【解析】A.由于用微生物做催化剂,不能在高温下进行,高温不利于该电池的使用,故A正确;
B.电池工作一段时间后,a侧产生的氢氧根离子和b侧产生的H+迁移到中间室生成水,导致NaCl浓
度降低,故B错误;
C.d为阳极,水失去电子发生氧化反应生成羟基自由和氢离子,故C正确;
D.c为阴极发生还原反应生成氢气,d极为阳极羟基自由基把苯酚氧化为二氧化碳,根据电子守恒,
28mol电子转移会产生14mol氢气和6molCO ,C HOH~28e-~6CO ~14H ,c、d两极产生气体的体积比(相
2 6 5 2 2
同条件下)为 ,故D正确;
答案选B。
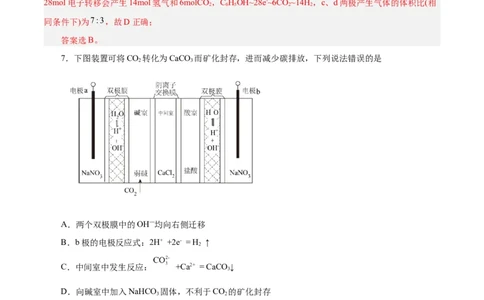
7.下图装置可将CO 转化为CaCO 而矿化封存,进而减少碳排放,下列说法错误的是
2 3
A.两个双极膜中的OH—均向右侧迁移
B.b极的电极反应式:2H+ +2e- = H ↑
2
C.中间室中发生反应: +Ca2+ = CaCO↓
3
D.向碱室中加入NaHCO 固体,不利于CO 的矿化封存
3 2
【答案】B
【分析】由图可知,与直流电源负极相连的电极a为电解池的阴极,水在阴极得到电子发生还原反应
生成氢气和氢氧根离子,双极膜中氢离子进入阴极室中与放电生成的氢氧根离子反应生成水,氢氧根离子
进入碱室,与通入的二氧化碳反应生成碳酸根离子;电极b为阳极,水在阳极失去电子发生氧化反应生成
氧气和氢离子,双极膜中氢氧根离子进入阳极室中中和放电生成的氢离子,氢离子进入酸室,导致阳离子
的电荷数大于阴离子,使得中间室中的氯离子进入酸室,碱室中的碳酸根离子进入中间室与溶液中钙离子
反应生成碳酸钙沉淀。【解析】A.由分析可知,两个双极膜中的氢氧根离子均向右侧迁移,故A正确;
B.由分析可知,电极b为阳极,水在阳极失去电子发生氧化反应生成氧气和氢离子,电极反应式为
2HO—4e—=O ↑+4H+,故B错误;
2 2
C.由分析可知,中间室中发生反应为碱室中的碳酸根离子进入中间室与溶液中钙离子反应生成碳酸
钙沉淀,离子方程式为 +Ca2+ = CaCO↓,故C正确;
3
D.向碱室中加入碳酸氢钠固体,碳酸氢钠与迁移至碱室的氢氧根离子反应,不利于二氧化碳与碱的
反应,导致二氧化碳难以矿化封存,故D正确;故选B。
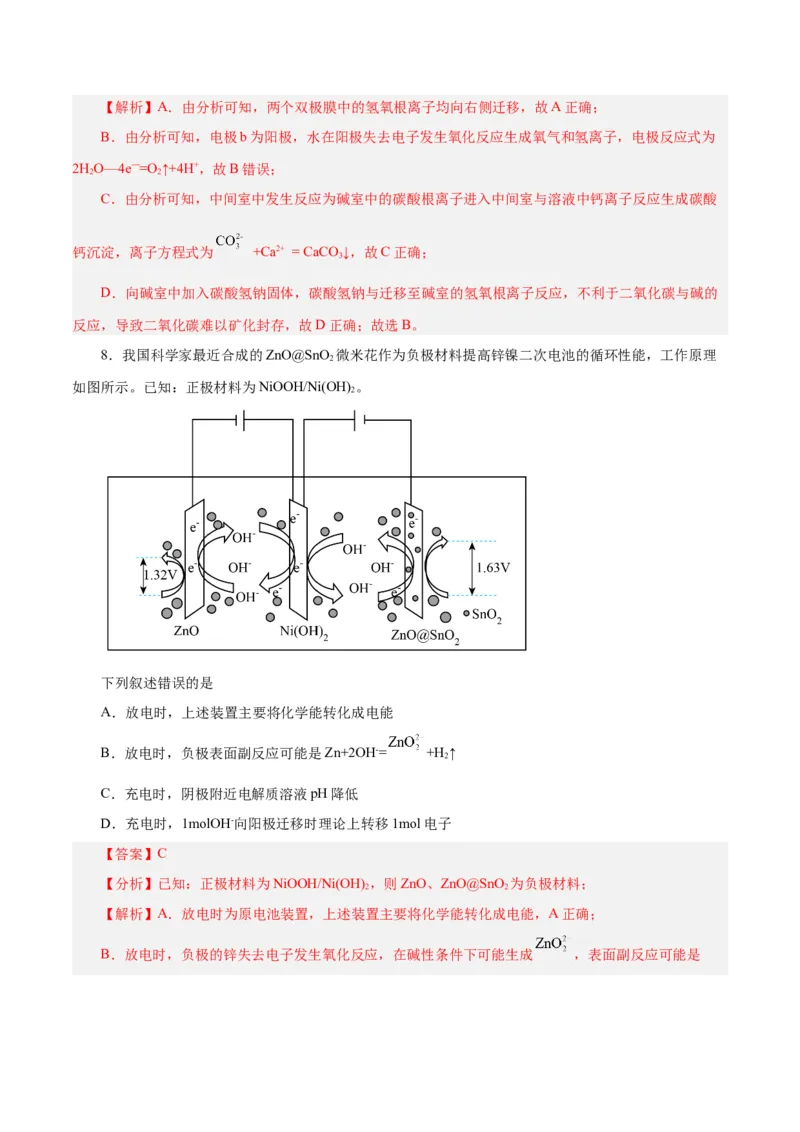
8.我国科学家最近合成的ZnO@SnO 微米花作为负极材料提高锌镍二次电池的循环性能,工作原理
2
如图所示。已知:正极材料为NiOOH/Ni(OH) 。
2
下列叙述错误的是
A.放电时,上述装置主要将化学能转化成电能
B.放电时,负极表面副反应可能是Zn+2OH-= +H ↑
2
C.充电时,阴极附近电解质溶液pH降低
D.充电时,1molOH-向阳极迁移时理论上转移1mol电子
【答案】C
【分析】已知:正极材料为NiOOH/Ni(OH) ,则ZnO、ZnO@SnO 为负极材料;
2 2
【解析】A.放电时为原电池装置,上述装置主要将化学能转化成电能,A正确;
B.放电时,负极的锌失去电子发生氧化反应,在碱性条件下可能生成 ,表面副反应可能是Zn+2OH-= +H ↑,B正确;
2
C.充电时,阴极的氧化锌得到电子发生还原反应,反应为 ,则附近电解质
溶液pH升高,C错误;
D.充电时,阳极的NiOOH失去电子发生氧化反应,反应为 ,则
1molOH-向阳极迁移时理论上转移1mol电子,D正确;故选C。
9.一种氯离子介导的电化学合成方法,能将乙烯高效清洁、选择性地转化为环氧乙烷,电化学反应
的具体过程如图所示。在电解结束后,将阴、阳极电解液输出混合,便可反应生成环氧乙烷。下列说法错
误的是
A.Ni电极与电源负极相连
B.阴极生成标况下22.4L气体,最终可制得2mol
C.工作过程中阴极附近pH增大
D.在电解液混合过程中会发生反应:HCl+KOH=KCl+H O
2
【答案】B
【分析】根据题给信息得乙烯在左室与HClO发生氧化还原反应,HClO由Cl 与HO反应生成,而由
2 2
转化生成 应发生在Pt电极上,即Pt电极为阳极,连接电源正极,Ni为阴极,连接电源负极。据此
分析解答。【解析】A.根据分析知,Ni为阴极,与电源负极相连,A正确;
B.阴极电极反应式为: ,阴极生成标况下22.4L气体时,电路上转移的电子
为2mol;阳极对应生成1molCl ,Cl 与水反应为可逆反应,生成的HClO小于1mol,被氧化的CH=CH 小
2 2 2 2
于1mol,因此可制得的环氧乙烷小于1mol,B错误;
C.工作过程中,阴极上水被电解生成氢气和氢氧根离子,因此阴极附近pH增大,C正确;
D.电解过程中,阳极生成的Cl 与水反应时生成HCl,阴极反应生成KOH,电解液混合时会发生以
2
下反应:HCl+KOH=KCl+H O,D正确;故选B。
2
10.下列说法正确的是
A.乙池中石墨电极表面有气泡产生,丙池中 向右侧 电极移动
B.甲池通入 的电极反应为
C.反应一段时间后,向乙池中加入一定量 固体能使 溶液恢复到原浓度
D.收集一段时间后丙池中两电极上产生的气体,左侧电极可能得到混合气体
【答案】D
【分析】由图可知,甲为原电池,甲醇通入极为负极,氧气通入极为正极,乙为电解池,石墨为阳
极,Ag为阴极,丙为电解池,左侧Pt电极为阳极,右侧Pt电极为阴极,据此作答。
【解析】A.乙池中石墨电极为阳极,溶液中氢氧根离子放电生成氧气,电极反应式为4OH--4e-
=O ↑+2H O,丙为电解池,阴离子向阳极(左侧Pt电极)移动,故A错误;
2 2
B.在燃料电池甲池中,负极是甲醇发生失电子的氧化反应,在碱性电解质下的电极反应为
CHOH-6e-+8OH-= +6H O,故B错误;
3 2
C.电解池乙池中,电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,故C错误;
D.丙池是电解池,左侧电极是阳极,开始生成氯气,电极反应式为2Cl--2e=Cl↑,当氯离子消耗完以
2后,电极继续生成氧气,电极反应式为4OH--4e-=O ↑+2H O,故左侧电极可能得到混合气体,故D正确;
2 2
故选D。
11.利用双阴极微生物燃料电池处理添加醋酸钠的含 废水,其工作原理如图(a)所示,双阴极通过
的电流相等,废水在电池中的运行模式如图(b)所示。
下列说法错误的是
A.X是阳离子交换膜
B.生成7 g N,理论上需要消耗20 g O
2 2
C.Ⅰ室的电极反应式为
D.理论上,Ⅱ室生成11 g CO 时,外电路通过1 mol电子
2
【答案】B
【分析】由图可知Ⅲ室中溶液进入Ⅰ室,则说明Ⅱ室中除了O 得到电子被还原为HO,还会发生反应
2 2
铵根离子被氧化为硝酸根离子;Ⅰ室、Ⅱ室、Ⅲ室分别发生还原反应、氧化反应、还原反应,Ⅰ室发生还
原反应,导致阳离子浓度增大,故X是阳离子交换膜,Y是阴离子交换膜,然后根据电子守恒,结合
m=n·M进行计算。
【解析】A.由图可知:Ⅰ室发生还原反应,反应变为N 逸出,导致左侧阳离子浓度增大,为维持平
2
衡,阳离子要通过X离子交换膜进入右侧,故X离子交换膜为阳离子交换膜,A正确;
B.7 g N 的物质的量为n(N )= =0.25 mol,根据电子转移守恒可知在Ⅲ室消耗O2的物质的量
2 2
是n(O )= =0.625 mol,在Ⅲ室发生反应 +2O = +2H O,发生该反应消耗O 的物质的
2 2 2 2
量为0.25 mol×2×2=1 mol,故共消耗O 的物质的量为n(O )=0.625 mol+1 mol=1.625 mol,其质量为
2 2
m(O )=1.625 mol×32 g/mol=52 g,B错误;
2
C.根据图示可知在Ⅰ室 得到电子被还原为N,电极反应式为: ,
2C正确;
D.Ⅱ室发生氧化反应,电极反应式为:CHCOO- -8e-+2H O=2CO↑+7H+。每反应产生2 mol CO 气
3 2 2 2
体,转移8 mol电子,反应产生11 g CO 气体的物质的量是0.25 mol,则转移电子的物质的量为n(e-)=0.25
2
mol×4=1 mol ,D正确;故选B。
12.目前可采用“双极膜组”电渗析法淡化海水,同时获得副产品A和B,模拟工作原理如图所示。
M和N为离子交换膜,在直流电作用下,双极阴阳膜(BP)复合层间的 解离成 和 ,作为 和
的离子源。下列说法正确的是
A.X电极为阴极,电极反应式为2HO+2e-=2OH-+H ↑
2 2
B.M为阳离子交换膜,N为阴离子交换膜,BP膜的作用是选择性通过Cl-和Na+
C.每生成5.6L气体a,理论上获得副产品A和B各0.5mol
D.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH)
【答案】D
【分析】由BP双极膜中H+、OH-移动方向可知:X电极为电解池的阳极,电极反应式为:2 +2e-
=Cl,Y电极为阴极,电极反应式为:2H++2e-=H ,电解总反应为: ,精制食
2 2
盐水中钠离子经过M离子交换膜移向产品A室,与BP双极膜中转移过来的氢氧根结合生成氢氧化钠,所
以M膜为阳离子交换膜,盐室中氯离子经过N离子交换膜移向产品B室,与BP双极膜中转移过来的氢离
子结合生成氯化氢,所以N为阴离子交换膜。
【解析】A.由图中氢氧根移动方向可知X电极为阳极,电极反应式为:2 +2e-=Cl,A错误;
2
B.由题意可知,精制食盐水中钠离子经过M离子交换膜移向产品A室,与BP双极膜中转移过来的
氢氧根结合生成氢氧化钠,所以M膜为阳离子交换膜,盐室中氯离子经过N离子交换膜移向产品B室,
与BP双极膜中转移过来的氢离子结合生成氯化氢,所以N为阴离子交换膜,BP双极膜的作用是选择性通
过氢离子和氢氧根离子,B错误;C.阳极反应式为:2 +2e-=Cl,电路中每生成标况下5.6L气体氯气,其物质的量为0.25mol,转移
2
电子0.5mol,理论上获得副产品A(氢氧化钠溶液)和B(氯化氢溶液)各0.5mol,需标明标准状况,C
错误;
D.“双极膜组”电渗析法从氯化钠溶液中获得酸(HCl)和碱(NaOH),由此可知:也可从M溶液
制备相应的酸(HX)和碱(MOH),D正确;故选D。
13.近日,中国科学院大连化学物理研究所团队利用固体氧化物(γ–Al O)电解质实现了乙烷电化学脱
2 3
氢制乙烯,其工作原理如图所示。下列说法正确的是
A.a为电源的负极
B.M极电极反应式为C H+2e-=C H+2H+
2 6 2 4
C.每生成0.5molC H,N极消耗标准状况下11.2LCO
2 4 2
D.每生成56gCO,电路中转移电子的物质的量为2mol
【答案】C
【解析】A.M电极乙烷发生氧化反应生成乙烯,M为阳极,a为电源的正极,故A错误;
B.M极乙烷失电子发生氧化反应生成乙烯,反应式为C H-2e-+O2-=C H+2H O,故B错误;
2 6 2 4 2
C.阳极发生反应C H-2e-+O2-=C H+2H O,阴极发生反应CO+2e-=CO+O2-,每生成0.5molC H,转
2 6 2 4 2 2 2 4
移1mol电子,N极消耗0.5molCO,标准状况下的体积为11.2LCO,故C正确;
2 2
D.阴极发生反应CO+2e-=CO+O2-,每生成56gCO,电路中转移电子的物质的量为
2
,故D错误;故选C。
14.科研团队开创了海水原位直接电解制氢的全新技术(如图所示)。该研究的关键点是利用海水侧和
电解质 侧的水蒸气压力差使海水自发蒸发,并以蒸汽形式通过透气膜扩散到电解质侧重新液化,即
“液-气-液”水迁移机制,为电解提供淡水。下列叙述错误的是A.直接电解海水存在阳极易腐蚀问题
B.液态水、阴离子分别不能通过膜a、膜b
C.铅酸蓄电池做电源时, 电极与N电极相连
D.电解过程中,阴极区溶液 可能不变
【答案】B
【分析】由图可知,在电解过程中M极OH-放电失去电子生成O,N极HO得到电子生成H,则M
2 2 2
为阳极,电极方程式为:4OH--4e-=O ↑+2H O,N为阴极,电极方程式为:2HO+2e-=H ↑+2OH-,阳极区
2 2 2 2
OH-浓度减小,为保证KOH浓度较高形成水蒸气压力差,阴极产生的OH-需要经过离子交换膜b进入阳
极,膜b为阴离子交换膜,以此解答。
【解析】A.海洋环境中的盐度、温度、溶解氧等因素会影响金属材料的化学反应,导致其受到腐
蚀,直接电解海水存在阳极易腐蚀问题,故A正确;
B.由题意可知,海水自发蒸发,并以蒸汽形式通过透气膜扩散到电解质侧重新液化,液态水不能通
过膜a,膜b为阴离子交换膜,阴离子能通过膜b,故B错误;
C.铅酸蓄电池做电源时,Pb为负极,应该与阴极N电极相连,故C正确;
D.电解过程中,阴极区电极方程式为2HO+2e-=H ↑+2OH-,生成的OH-进入阳极区,阴极区溶液
2 2
可能不变,故D正确;故选B。
15.通过NO协同耦合反应,实现了NO的电催化歧化,并同时合成了双氮产物( 和硝酸盐)是实现
可持续固氮的一种极具潜力的方法,装置如图。下列说法正确的是A.电解液E为阳极电解液,呈酸性
B.电极B的电极反应:
C.中间层的 、 分别透过选择性离子膜向A、B极迁移
D.若电解一段时间后,取两极所有产物于溶液中反应,可得硝酸盐和硝酸
【答案】D
【分析】由图可知,A极氮元素价态降低得电子,故A极为阴极,电极反应式为NO+5H++5e-
=NH+H O,B极为阳极,电极反应式为NO+2H O-3e-=NO +4H+,据此分析解答。
3 2 2
【解析】A.根据以上分析,A极为阴极,电极反应式为NO+5H++5e-=NH+H O,则电解液E为阴极
3 2
电解液,呈酸性,故A错误;
B.B极为阳极,电极反应式为NO+2H O-3e-= NO +4H+,故B错误;
2
C.由两极反应式可知,阳极区产生氢离子,阴极区消耗氢离子,故中间层的OH-、H+分别透过选择
性离子膜向B、A极迁移,故C错误;
D.由图可知,A极NO→NH ~5e-,B极NO→NO ~3e-,根据电子得失守恒,电解一段时间后,取
3
两极所有产物于溶液中反应,可得硝酸盐和硝酸,故D正确;
故选D。
16.工业上电解MnSO 溶液制备Mn和MnO 的工作原理如图所示,下列说法错误的是
4 2A.电流由钛电极经MnSO 溶液流向不锈钢电极
4
B.阳极反应式为Mn2+—2e—+2H O=MnO +4H+
2 2
C.离子交换膜为阳离子交换膜
D.当电路中有2mole-转移时,生成55gMn
【答案】C
【分析】由图可知,该装置为电解池,与直流电源负极相连的不锈钢电极为阴极,锰离子在阴极得到
电子发生还原反应生成锰,电极反应式为Mn2++2e—=Mn,钛电极为阳极,锰离子在阳极失去电子发生氧化
反应生成二氧化锰,电极反应式为Mn2+—2e—+2H O=MnO +4H+,溶液中硫酸根离子由阴极区经阴离子交
2 2
换膜进入阳极区。
【解析】A.由分析可知,不锈钢电极为阴极,钛电极为阳极,则内电路中电流由钛电极经硫酸锰溶
液流向不锈钢电极,故A正确;
B.由分析可知,钛电极为阳极,锰离子在阳极失去电子发生氧化反应生成二氧化锰,电极反应式为
Mn2+—2e—+2H O=MnO +4H+,故B正确;
2 2
C.由分析可知,不锈钢电极为阴极,钛电极为阳极,电解时溶液中硫酸根离子由阴极区经阴离子交
换膜进入阳极区,故C错误;
D.由分析可知,不锈钢电极为阴极,锰离子在阴极得到电子发生还原反应生成锰,电极反应式为
Mn2++2e—=Mn,则当电路中有2mole-转移时,阴极生成锰质量为1mol×55g/mol=55g,故D正确;
故选C。
17.镍—镉电池是一种新型的封闭式体积小的可充电电池。其工作原理如下图所示,下列说法不正确
的是A.放电时a极为负极
B.放电时a极的反应:
C.充电时b极接外接电源正极
D.用该电池电解足量的饱和食盐水,电路中通过0.2mol ,阴极生成0.2gH
2
【答案】B
【分析】根据化合价升降,左室元素化合价升高,失去电子,作负极,右室元素化合价降低,得到电
子,作正极。
【解析】A.根据图中信息电子从左转移到右边,因此放电时a极为负极,b极为正极,故A正确;
B.根据图中负极Cd变为Cd(OH) ,则放电时a极的反应为 ,故B错误;
2
C.放电时b极为正极,充电时b极接外接电源正极,故C正确;
D.用该电池提供的电能电解饱和食盐水,阴极反应式为2HO+2e-=H +2OH-,电路中通过0.2mole-,
2 2
则阴极生成氢气物质的量为0.1mol,质量为0.2g,故D正确。
综上所述,答案为B。
18.微生物电化学产甲烷法能将电化学法和生物还原法有机结合,装置如图所示(左侧 转化
为 和 ,右侧 和 转化为 )。有关说法正确的是
A.电源a端为负极
B.该方法能实现二氧化碳零排放
C.b电极的反应为:D.外电路中每通过 ,与a相连的电极将产生
【答案】C
【分析】左侧 转化为 和 ,发生氧化反应,故左侧为电解池阳极;右侧 和 转化
为 ,发生还原反应,右侧为阴极。
【解析】A.根据分析可知,左侧为阳极,则电源a端为正极,A错误;
B.电解池总反应为CHCOO-+H+=CH +CO ,故该方法不能实现二氧化碳零排放,B错误;
3 4 2
C.b极二氧化碳得电子与氢离子反应生成甲烷和水,故电极反应式为 ,
C正确;
D.a极电极反应式为2HO+CHCOO--8e-=2CO +7H+,外电路中每通过 ,与a相连的电极在标
2 3 2
准状态下将产生 ,D错误;答案选C。
19.当今社会的主题之一:发展经济,节能减排。而燃料电池因其无污染,且原料来源广可再生被人
们青睐,广泛应用于生产、生活、科学研究中,现有如下图所示装置,所有电极均为Pt,请按要求回答下
列问题:
(1)甲装置是 (填“原电池”或“电解池”),写出a极的电极反应 。
(2)乙池中c极的电极反应 。
(3)当b极消耗标准状况下的O112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积
2
保持不变,此时乙池中的pH= 。
(4)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许
某些离子通过,则A出口导出的溶液溶质为 (写化学式),M为 离子交换膜(填“阴”或“阳”)。
【答案】(1) 原电池 CHOH-6e-+8OH-= +6H O
3 2
(2)2H O-4e-=O ↑+4H+
2 2
(3)1
(4) O 阴
2
【分析】从图中可以看出,CHOH为燃料,装置甲为燃料电池,装置乙和丙为电解池。其中a极为负
3
极,b极为正极,c极为阳极,d极为阴极,丙池中左侧电极为阳极,右侧电极为阴极。
【解析】(1)甲装置是原电池,a极CHOH失电子产物与电解质反应,生成 等,电极反应为
3
CHOH-6e-+8OH-= +6H O。(2)乙池中,c极的HO失电子生成H+、O,电极反应为2HO-4e-
3 2 2 2 2
=O ↑+4H+。
2
(3)当b极消耗标准状况下的O112mL时,n(e-)= =0.02mol,若乙中硫酸铜溶液的体积是
2
200mL,阳极2HO-4e-=O ↑+4H+,阴极Cu2++2e-=Cu,假若电解前后溶液体积保持不变,此时乙池中,H+
2 2
——e-,则n(H+)=0.02mol,c(H+)= =0.1mol/L,pH=1。(4)丙池中,左侧电极(阳极)发生反应
2HO-4e-=O ↑+4H+,则 透过离子交换膜M向左移动,则A出口导出的溶液溶质为O,M为阴离子交
2 2 2
换膜。
20.回答下列问题:
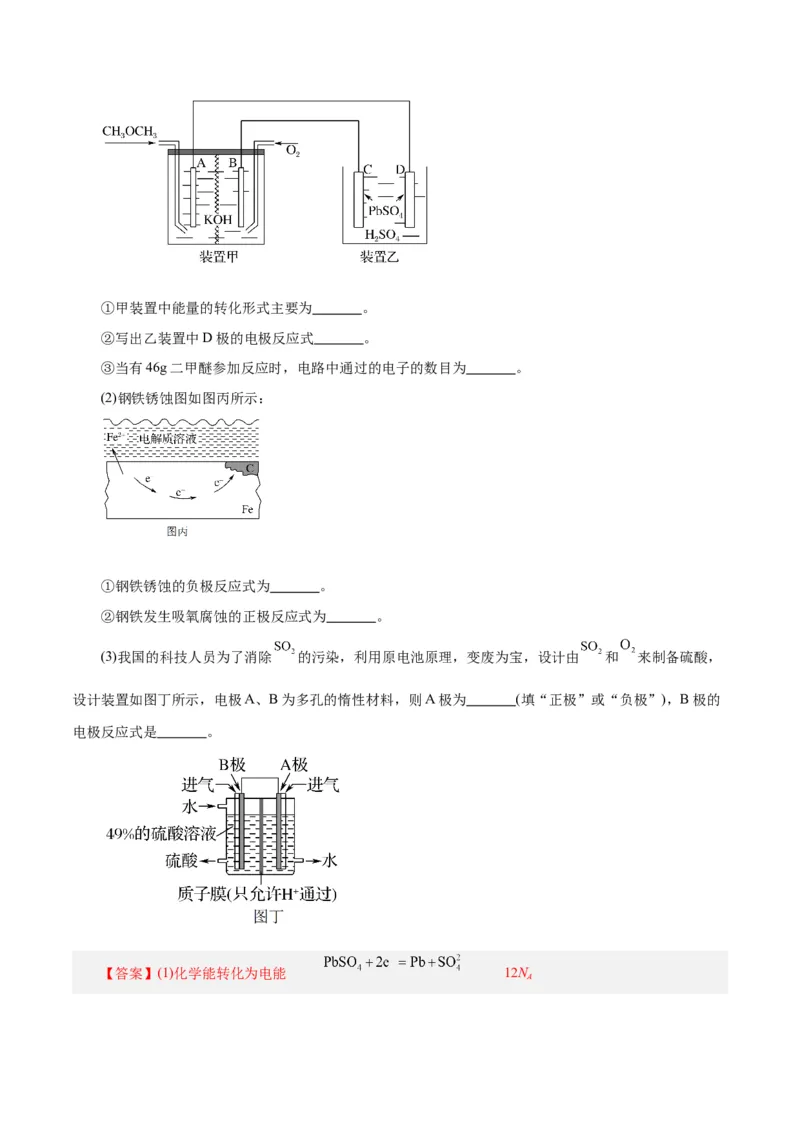
(1)图中甲装置为 碱性燃料电池,其电极均为 电极,装置乙中,C、D电极为 电极,其
表面均覆盖着 ,其电解液为稀 溶液。①甲装置中能量的转化形式主要为 。
②写出乙装置中D极的电极反应式 。
③当有46g二甲醚参加反应时,电路中通过的电子的数目为 。
(2)钢铁锈蚀图如图丙所示:
①钢铁锈蚀的负极反应式为 。
②钢铁发生吸氧腐蚀的正极反应式为 。
(3)我国的科技人员为了消除 的污染,利用原电池原理,变废为宝,设计由 和 来制备硫酸,
设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为 (填“正极”或“负极”),B极的
电极反应式是 。
【答案】(1)化学能转化为电能 12N
A(2)
(3)正极
【解析】(1)由图可知,装置甲为二甲醚燃料电池,通入二甲醚的A电极为负极,通入氧气的B电
极为正极,装置乙为电解池,与负极相连的D电极为阴极,与正极相连的C电极为阳极;
①由分析可知,装置甲为化学能转化为电能的二甲醚燃料电池;
②装置乙为电解池,与负极相连的D电极为阴极,硫酸铅在阴极得到电子发生还原反应生成铅和硫酸
根离子,电极反应式为 ;
③由分析可知,通入二甲醚的A电极为负极,二甲醚碱性条件下在负极失去电子发生氧化反应生成碳
酸根离子和水,电极反应式为CHOCH +16OH--12e-=2CO +11HO,则当有46g二甲醚参加反应时,
3 3 2
电路中通过的电子的数目为 ×12×N mol—1=12N ;
A A
(2)①钢铁锈蚀时,铁做原电池的负极,碳为正极,铁在负极失去电子发生氧化反应生成亚铁离
子,电极反应式为 ;
②钢铁发生吸氧腐蚀时,铁做原电池的负极,碳为正极,水分子作用下,氧气在正极得到电子发生还
原反应生成氢氧根离子,电极反应式为 ;
(3)由图可知,该装置为原电池,通入氧气的A电极为正极,通入二氧化硫的B电极为负极,水分
子作用下,二氧化硫在负极失去电子发生氧化反应生成硫酸根离子和氢离子,电极反应式为
。