文档内容
第 18 讲 化学反应速率
1.了解化学反应速率的概念和定量表示方法。
2.了解反应活化能的概念,了解催化剂的重要作用。
3.理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,能用相关理论解释其一般规律。
4.了解化学反应速率的调控在生活、生产和科学研究领域中的重要作用。
【核心素养分析】
变化观念与平衡思想:能认识化学反应速率是变化的,知道化学反应速率与外界条件有关,并遵循一
定规律;能多角度。动态地分析化学反应速率,运用化学反应原理解决实际问题。
证据推理与模型认知:建立观点、结论和证据之间的逻辑关系,知道可以通过分析、推理等方法认识
化学反应速率的本质特征及其相互关系,建立模型。能运用模型解释化学现象,揭示现象的本质和规律。
科学探究与创新意识:能发现和提出有关化学反应速的有探究价值的问题;通过控制变量来探究影响
化学反应速率的外界条件。
知识点一 化学反应速率的概念及计算
1.化学反应速率
2.化学反应速率计算的万能方法——三段式法
对于反应mA(g)+nB(g) pC(g)+qD(g),起始时A的浓度为a mol·L-1,B的浓度为b mol·L-1,反应进行至ts时,A消耗了x mol·L-1,则化学反应速率可计算如下:
1
mA(g)+nB(g) pC(g)+qD(g)
起始/(mol·L-1) a b 0 0
转化/(mol·L-1) x
t/(mol·L-1) a-x b-
1
则:v(A)= mol·L-1·s-1,v(B)= mol·L-1·s-1,
v(C)= mol·L-1·s-1,v(D)= mol·L-1·s-1。
3.化学反应速率与化学计量数的关系
对于已知反应mA(g)+nB(g)===pC(g)+qD(g),其化学反应速率可用不同的反应物或生成物来表示,
当单位相同时,化学反应速率的数值之比等于化学计量数之比,即v(A)∶v(B)∶v(C)∶v(D)=
m∶n∶p∶q。
如一定温度下,在密闭容器中发生反应:3A(g)+B(g) 2C(g)。已知v(A)=0.6 mol·L-1·s-1,则
v(B)=0.2 mol·L-1·s-1,v(C)=0.4 mol·L-1·s-1。
4.化学反应速率的大小比较
(1)归一法
将同一反应中的不同物质的反应速率转化成同一单位、同一种物质的反应速率,再进行速率的大小比
较。
(2)比值法
将各物质表示的反应速率转化成同一单位后,再除以对应各物质的化学计量数,然后对求出的数值进
行大小排序,数值大的反应速率快。如反应mA(g)+nB(g)===pC(g)+qD(g),若>,则反应速率A>B。
知识点二 影响化学反应速率的因素
1.影响化学反应速率的因素
(1)内因
反应物本身的性质是主要因素。如相同条件下Mg、Al与稀盐酸反应的速率大小关系为Mg>Al。
(2)外因(只改变一个条件,其他条件不变)【特别提醒】
①改变固体或纯液体的量对化学反应速率无影响。
②浓度、温度、压强发生变化或加入催化剂时,正、逆反应速率均增大或减小,如升高温度,不论是
放热反应还是吸热反应,化学反应速率均加快。
(3)反应体系条件改变对反应速率的影响
①恒温时:体积缩小――→压强增大――→浓度增大――→反应速率增大。
②恒温恒容时:
a.充入气体反应物――→总压强增大――→浓度增大――→反应速率增大。
b.充入“惰性气体”――→总压强增大,但各气体分压不变―→各物质的浓度不变―→反应速率不
变。
③恒温恒压时:充入“惰性气体”――→体积增大――→各反应物浓度减小――→反应速率减小。
总之,压强改变而对反应速率产生的影响是因为压强改变会引起浓度变化,从而对反应速率产生影响。
2.理论解释——有效碰撞理论
(1)活化分子、活化能、有效碰撞
①活化分子:能够发生有效碰撞的分子。
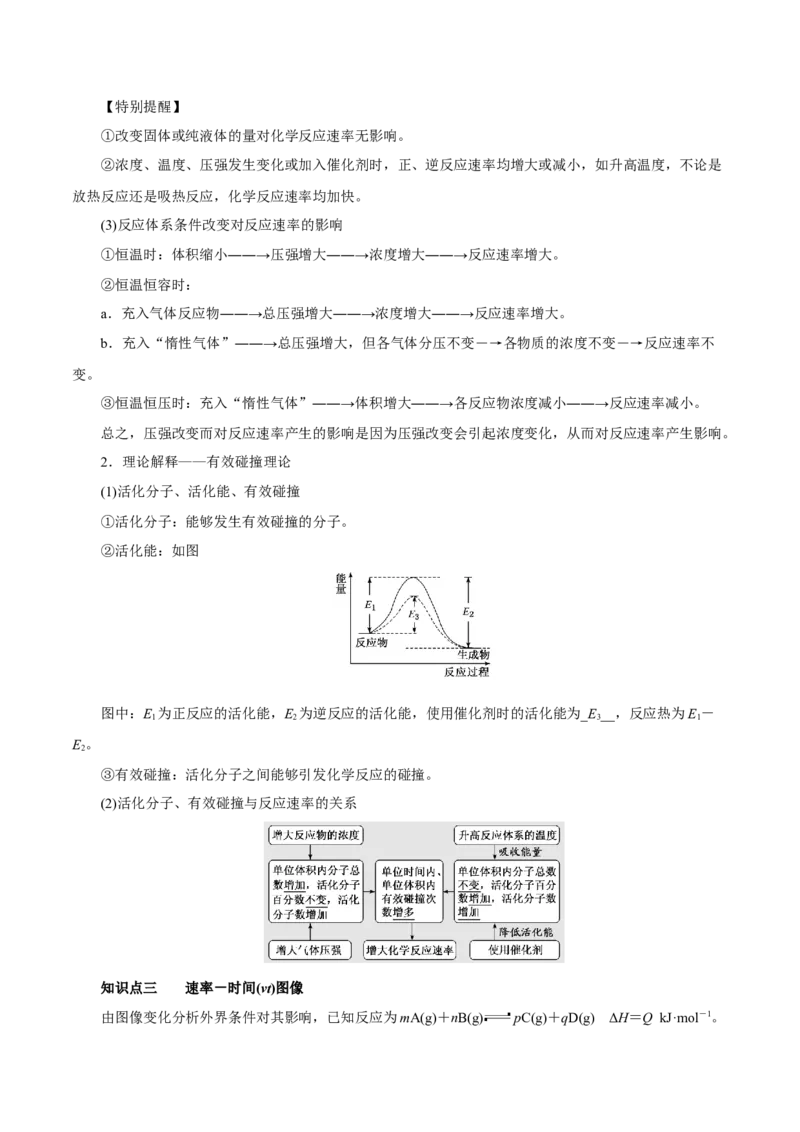
②活化能:如图
图中:E 为正反应的活化能,E 为逆反应的活化能,使用催化剂时的活化能为_E__,反应热为E-
1 2 3 1
E。
2
③有效碰撞:活化分子之间能够引发化学反应的碰撞。
(2)活化分子、有效碰撞与反应速率的关系
知识点三 速率-时间(vt)图像
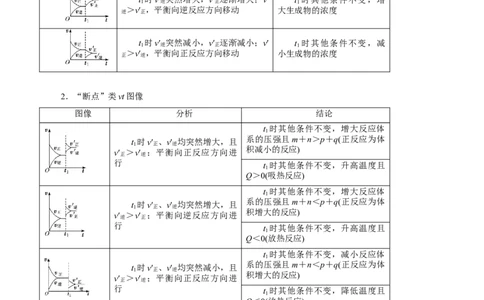
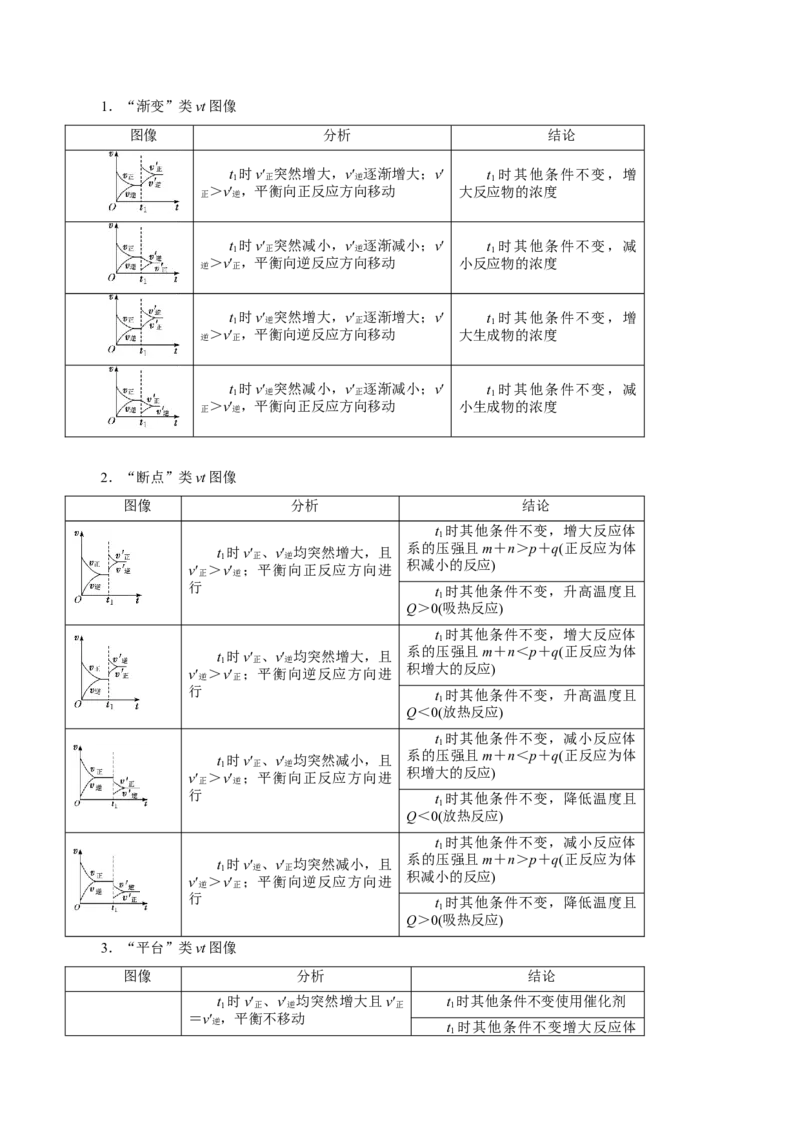
由图像变化分析外界条件对其影响,已知反应为mA(g)+nB(g ) pC(g)+qD(g) ΔH=Q kJ·mol-1。1.“渐变”类vt图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增大;v′ t 时其他条件不变,增
1 正 逆 1
>v′ ,平衡向正反应方向移动 大反应物的浓度
正 逆
t 时v′ 突然减小,v′ 逐渐减小;v′ t 时其他条件不变,减
1 正 逆 1
>v′ ,平衡向逆反应方向移动 小反应物的浓度
逆 正
t 时v′ 突然增大,v′ 逐渐增大;v′ t 时其他条件不变,增
1 逆 正 1
>v′ ,平衡向逆反应方向移动 大生成物的浓度
逆 正
t 时v′ 突然减小,v′ 逐渐减小;v′ t 时其他条件不变,减
1 逆 正 1
>v′ ,平衡向正反应方向移动 小生成物的浓度
正 逆
2.“断点”类vt图像
图像 分析 结论
t 时其他条件不变,增大反应体
1
t 时v′ 、v′ 均突然增大,且
系的压强且m+n>p+q(正反应为体
1 正 逆
v′ >v′ ;平衡向正反应方向进
积减小的反应)
正 逆
行 t 时其他条件不变,升高温度且
1
Q>0(吸热反应)
t 时其他条件不变,增大反应体
1
t 时v′ 、v′ 均突然增大,且
系的压强且m+n<p+q(正反应为体
1 正 逆
v′ >v′ ;平衡向逆反应方向进
积增大的反应)
逆 正
行 t 时其他条件不变,升高温度且
1
Q<0(放热反应)
t 时其他条件不变,减小反应体
1
t 时v′ 、v′ 均突然减小,且
系的压强且m+n<p+q(正反应为体
1 正 逆
v′ >v′ ;平衡向正反应方向进
积增大的反应)
正 逆
行 t 时其他条件不变,降低温度且
1
Q<0(放热反应)
t 时其他条件不变,减小反应体
1
t 时v′ 、v′ 均突然减小,且
系的压强且m+n>p+q(正反应为体
1 逆 正
v′ >v′ ;平衡向逆反应方向进
积减小的反应)
逆 正
行 t 时其他条件不变,降低温度且
1
Q>0(吸热反应)
3.“平台”类vt图像
图像 分析 结论
t 时v′ 、v′ 均突然增大且v′ t 时其他条件不变使用催化剂
1 正 逆 正 1
=v′ ,平衡不移动
逆 t 时其他条件不变增大反应体
1系的压强且m+n=p+q(反应前后
气体体积无变化)
t 时其他条件不变,减小反应
t 时v′ 、v′ 均突然减小且v′ 1
1 正 逆 正 体系的压强且m+n=p+q(反应前
=v′ ,平衡不移动
逆 后气体体积无变化)
高频考点一 化学反应速率
【例1】(2022·北京卷) 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①
完成之后,以 为载气,以恒定组成的 混合气,以恒定流速通入反应器,单位时间流出气体各
组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
下列说法不正确的是
A. 反应①为 ;反应②为
B. , 比 多,且生成 速率不变,可能有副反应
C. 时刻,副反应生成 的速率大于反应②生成 速率
D. 之后,生成 的速率为0,是因为反应②不再发生
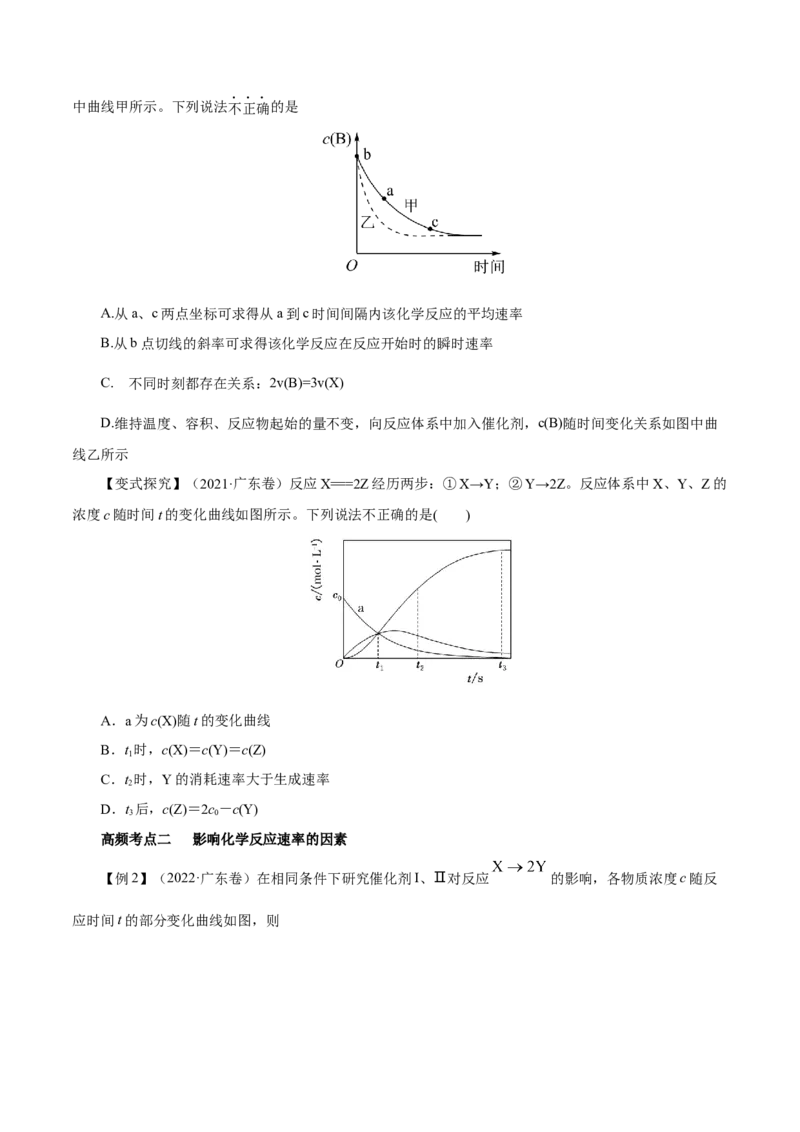
【变式探究】(2022·浙江卷)在恒温恒容条件下,发生反应A(s)+2B(g)3X(g),c(B)随时间的变化如图中曲线甲所示。下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
在
C. 不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲
线乙所示
【变式探究】(2021·广东卷)反应X===2Z经历两步:①X→Y;②Y→2Z。反应体系中X、Y、Z的
浓度c随时间t的变化曲线如图所示。下列说法不正确的是( )
A.a为c(X)随t的变化曲线
B.t 时,c(X)=c(Y)=c(Z)
1
C.t 时,Y的消耗速率大于生成速率
2
D.t 后,c(Z)=2c-c(Y)
3 0
高频考点二 影响化学反应速率的因素
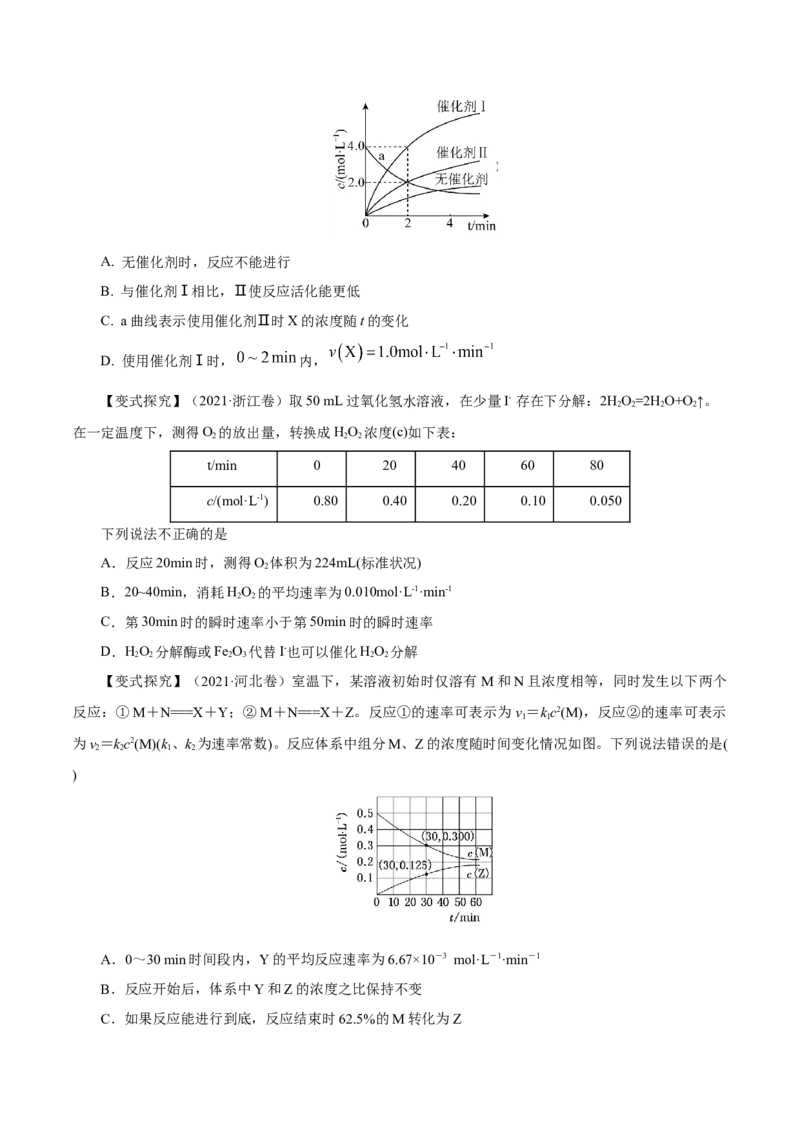
【例2】(2022·广东卷)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反
应时间t的部分变化曲线如图,则A. 无催化剂时,反应不能进行
B. 与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C. a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D. 使用催化剂Ⅰ时, 内,
【变式探究】(2021·浙江卷)取50 mL过氧化氢水溶液,在少量I- 存在下分解:2HO=2H O+O↑。
2 2 2 2
在一定温度下,测得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A.反应20min时,测得O 体积为224mL(标准状况)
2
B.20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C.第30min时的瞬时速率小于第50min时的瞬时速率
D.HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
【变式探究】(2021·河北卷)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个
反应:①M+N===X+Y;②M+N===X+Z。反应①的速率可表示为v =kc2(M),反应②的速率可表示
1 1
为v=kc2(M)(k、k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图。下列说法错误的是(
2 2 1 2
)
A.0~30 min时间段内,Y的平均反应速率为6.67×10-3 mol·L-1·min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为ZD.反应①的活化能比反应②的活化能大
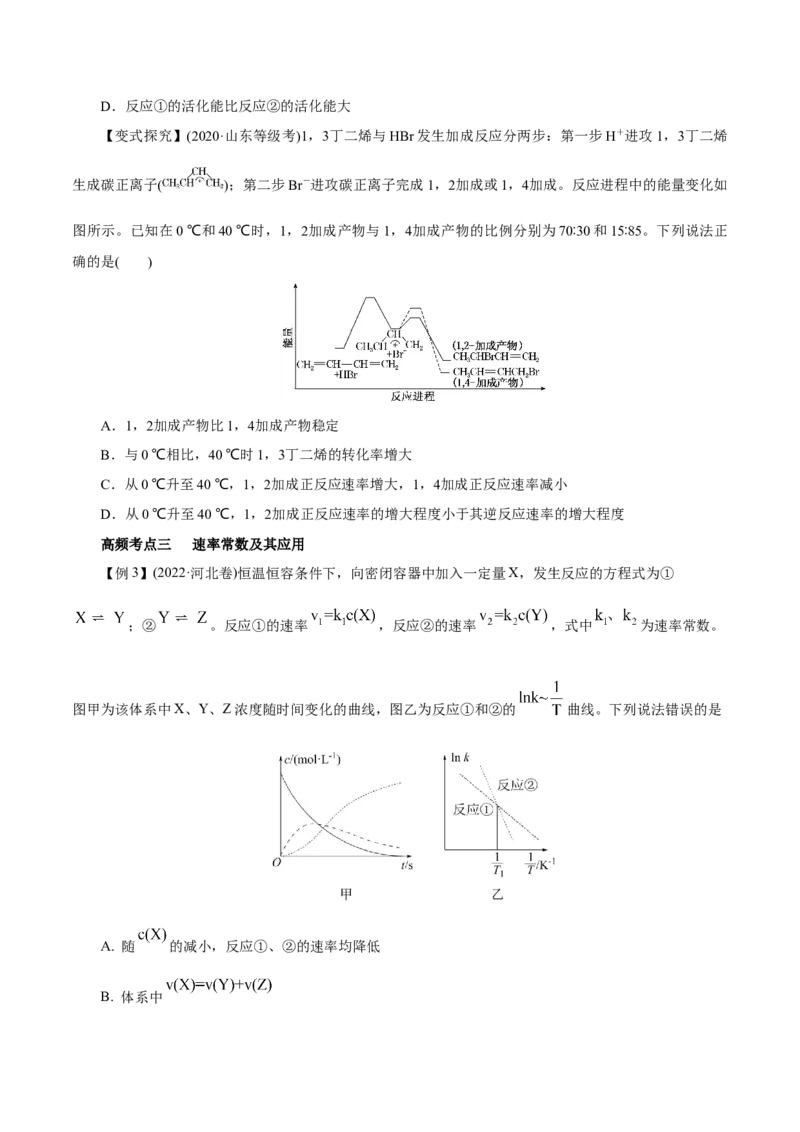
【变式探究】(2020·山东等级考)1,3丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3丁二烯
生成碳正离子( );第二步Br-进攻碳正离子完成1,2加成或1,4加成。反应进程中的能量变化如
图所示。已知在0 ℃和40 ℃时,1,2加成产物与1,4加成产物的比例分别为70∶30和15∶85。下列说法正
确的是( )
A.1,2加成产物比1,4加成产物稳定
B.与0 ℃相比,40 ℃时1,3丁二烯的转化率增大
C.从0 ℃升至40 ℃,1,2加成正反应速率增大,1,4加成正反应速率减小
D.从0 ℃升至40 ℃,1,2加成正反应速率的增大程度小于其逆反应速率的增大程度
高频考点三 速率常数及其应用
【例3】(2022·河北卷)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①
;② 。反应①的速率 ,反应②的速率 ,式中 为速率常数。
图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是
A. 随 的减小,反应①、②的速率均降低
B. 体系中C. 欲提高Y的产率,需提高反应温度且控制反应时间
D. 温度低于 时,总反应速率由反应②决定
【变式探究】[2020·全国卷Ⅱ,28(2)]高温下,甲烷生成乙烷的反应如下:2CH――→C H+H。反应
4 2 6 2
在初期阶段的速率方程为:r=k× ,其中k为反应速率常数。
①设反应开始时的反应速率为r,甲烷的转化率为α时的反应速率为r,则r=________ r。
1 2 2 1
②对于处于初期阶段的该反应,下列说法正确的是________。
A.增加甲烷浓度,r增大
B.增加H 浓度,r增大
2
C.乙烷的生成速率逐渐增大
D.降低反应温度,k减小
【方法技巧】
1.速率常数含义
速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同的浓度条件下,可
用速率常数大小来比较化学反应的反应速率。
化学反应速率与反应物浓度(或浓度的次方)成正比,而速率常数是其比例常数,在恒温条件下,速率
常数不随反应物浓度的变化而改变。因此,可以应用速率方程求出该温度下任意浓度时的反应速率。
2.速率方程
一定温度下,化学反应速率与反应物浓度以其计量数为指数的幂的乘积成正比。
对于反应:aA+bB===gG+hH
则v=kca(A)·cb(B)(其中k为速率常数)。
如:①SO Cl SO +Cl v=kc(SO Cl)
2 2 2 2 1 2 2
②2NO 2NO+O v=kc2(NO )
2 2 2 2
③2H+2NO N+2HO v=kc2(H )·c2(NO)
2 2 2 3 2
3.速率常数的影响因素
温度对化学反应速率的影响是显著的,速率常数是温度的函数,同一反应,温度不同,速率常数将有
不同的值,但浓度不影响速率常数。
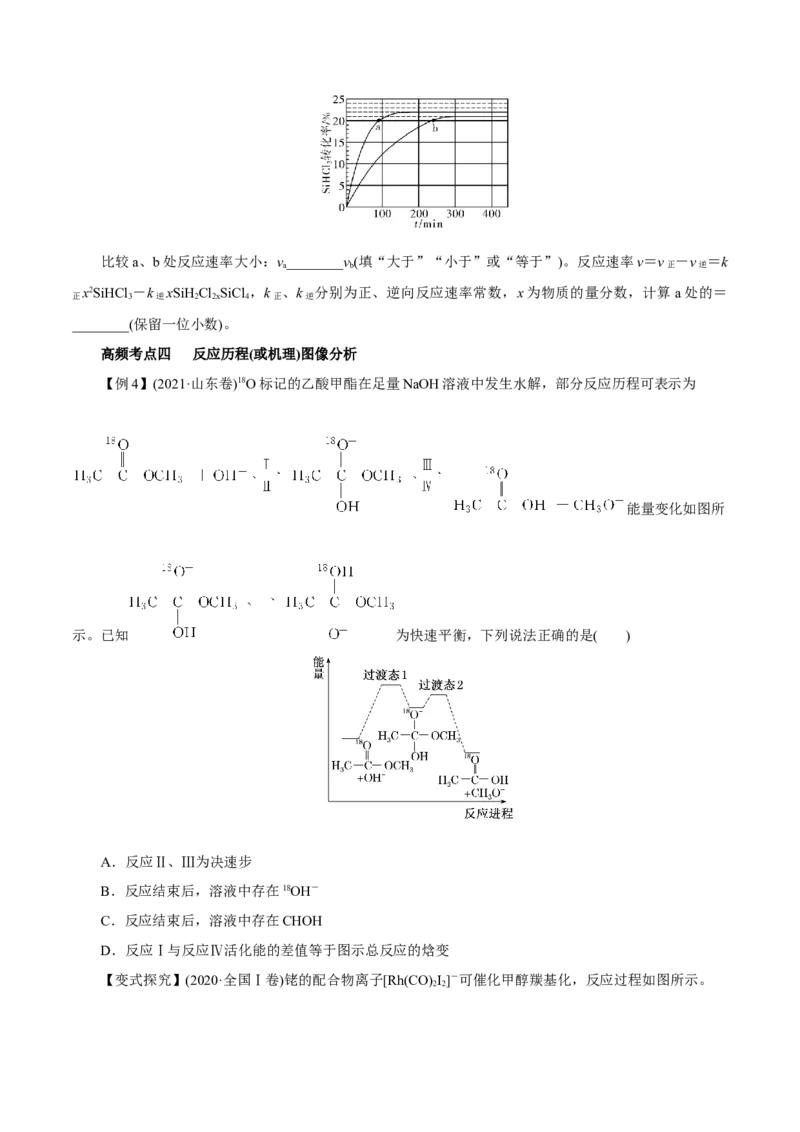
【变式探究】(2018·全国卷Ⅲ) 三氯氢硅(SiHCl )是制备硅烷、多晶硅的重要原料。对于反应
3
2SiHCl (g)===SiH Cl(g)+SiCl (g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl 的
3 2 2 4 3
转化率随时间变化的结果如图所示。比较a、b处反应速率大小:v________v(填“大于”“小于”或“等于”)。反应速率v=v -v =k
a b 正 逆
x2SiHCl -k xSiHCl SiCl ,k 、k 分别为正、逆向反应速率常数,x为物质的量分数,计算a处的=
正 3 逆 2 2x 4 正 逆
________(保留一位小数)。
高频考点四 反应历程(或机理)图像分析
【例4】(2021·山东卷)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为
能量变化如图所
示。已知 为快速平衡,下列说法正确的是( )
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CHOH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
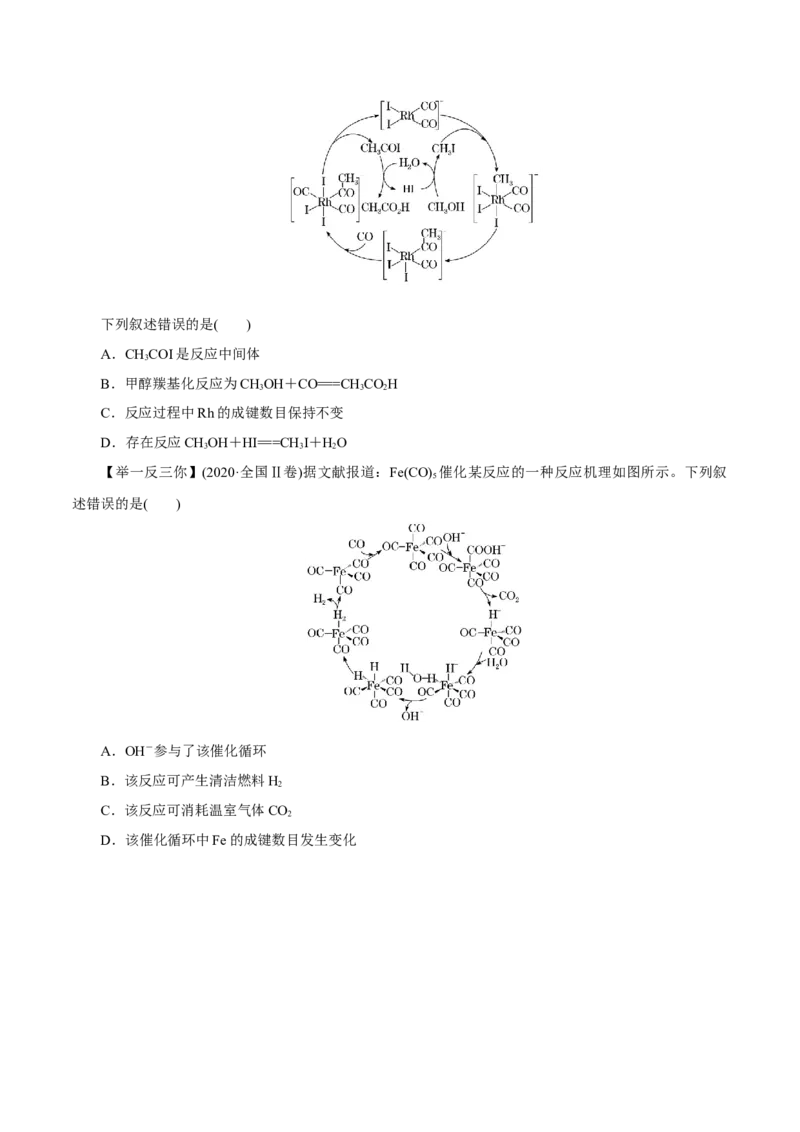
【变式探究】(2020·全国Ⅰ卷)铑的配合物离子[Rh(CO) I]-可催化甲醇羰基化,反应过程如图所示。
2 2下列叙述错误的是( )
A.CHCOI是反应中间体
3
B.甲醇羰基化反应为CHOH+CO===CH COH
3 3 2
C.反应过程中Rh的成键数目保持不变
D.存在反应CHOH+HI===CH I+HO
3 3 2
【举一反三你】(2020·全国Ⅱ卷)据文献报道:Fe(CO) 催化某反应的一种反应机理如图所示。下列叙
5
述错误的是( )
A.OH-参与了该催化循环
B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO
2
D.该催化循环中Fe的成键数目发生变化