文档内容
第 4 讲 氧化还原反应的概念和规律
[复习目标] 1.了解氧化还原反应的概念。2.会用“单、双线桥”分析电子转移的方向和数
目。3.掌握氧化性、还原性强弱的比较及价态规律的应用。
考点一 氧化还原反应及相关概念
1.氧化还原反应
(1)判断依据:反应前后有元素的________发生变化。
(2)本质:____________(得失或偏移)。
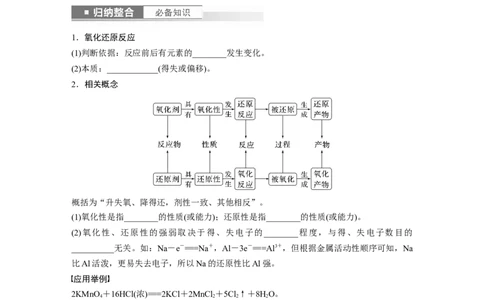
2.相关概念
概括为“升失氧、降得还,剂性一致、其他相反”。
(1)氧化性是指________的性质(或能力);还原性是指________的性质(或能力)。
(2)氧化性、还原性的强弱取决于得、失电子的________程度,与得、失电子数目的
__________无关。如:Na-e-===Na+,Al-3e-===Al3+,但根据金属活动性顺序可知,Na
比Al活泼,更易失去电子,所以Na的还原性比Al强。
应用举例
2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO。
4 2 2 2
上述反应中,氧化剂是______,还原剂是________,氧化产物是__________,还原产物是
________,KMnO 发生__________反应,HCl 发生________反应,盐酸表现的性质是
4
________性和________性;生成1 mol Cl 时转移电子数目为__________,被氧化的HCl的
2
物质的量是________ mol。
3.氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价,②画箭头(反应物指向生成物),③算数目,④说变化。
用双线桥法标出MnO 与浓盐酸加热反应的电子转移的方向和数目:
2
________________________________________________________________________。归纳 。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标
“得”“失”字样。
用单线桥法标出铜和浓硝酸反应的电子转移的方向和数目:
________________________________________________________________________。
归纳 。
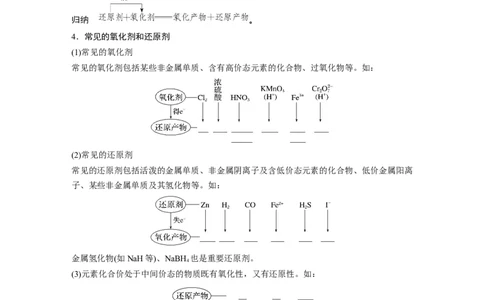
4.常见的氧化剂和还原剂
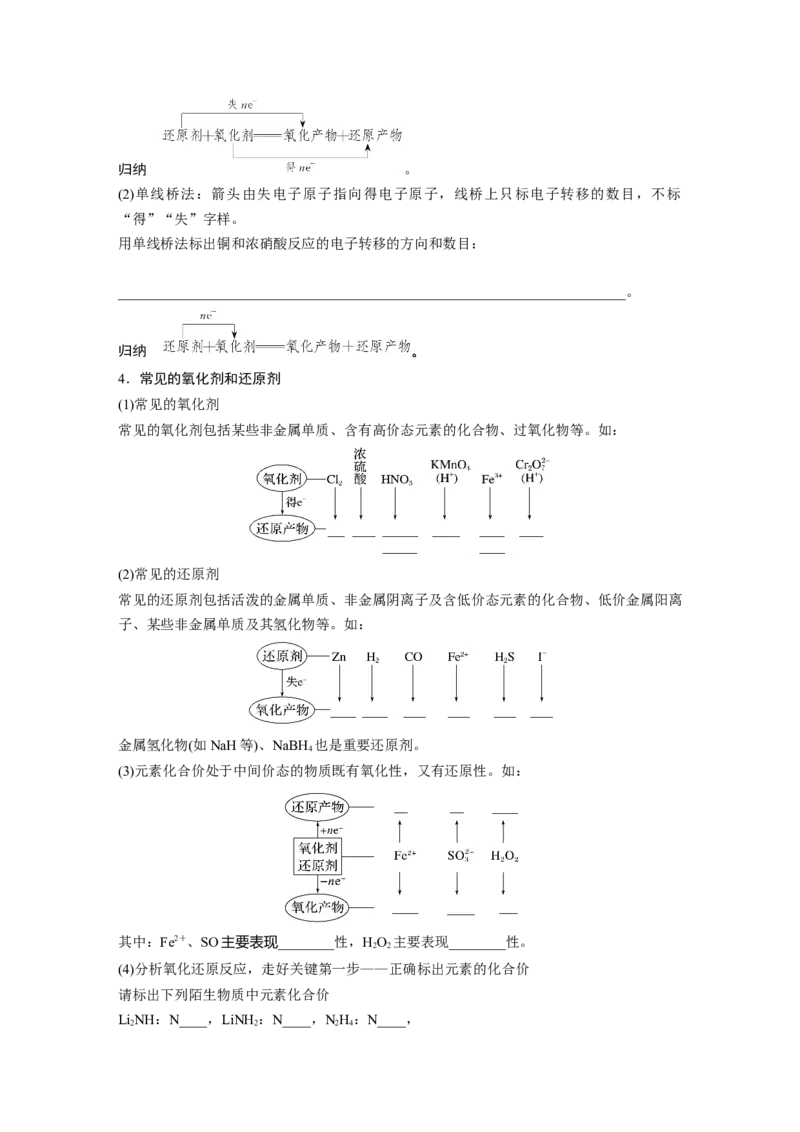
(1)常见的氧化剂
常见的氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
(2)常见的还原剂
常见的还原剂包括活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离
子、某些非金属单质及其氢化物等。如:
金属氢化物(如NaH等)、NaBH 也是重要还原剂。
4
(3)元素化合价处于中间价态的物质既有氧化性,又有还原性。如:
其中:Fe2+、SO主要表现________性,HO 主要表现________性。
2 2
(4)分析氧化还原反应,走好关键第一步——正确标出元素的化合价
请标出下列陌生物质中元素化合价
LiNH:N____,LiNH:N____,NH:N____,
2 2 2 4NaSO:S____,SO:S____,C O:C____,
2 2 3 2 2
HCN:C____、N____,BH:B____、H____,CuH:Cu____、H____,MnO(OH):
Mn____,FePO :Fe____,CrO:Cr____,KFeO :Fe____,LiFePO :Fe____,CuFeS :
4 2 4 4 2
Fe____。
5.氧化还原反应与四种基本反应类型的关系
分析下列四个化学反应:
A.2Na+2HO===2NaOH+H↑
2 2
B.2HClO=====2HCl+O↑
2
C.4NH +5O=====4NO+6HO
3 2 2
D.4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
其中属于区域“1”的是______(填字母,下同),属于区域“2”的是______,属于区域
“3”的是______,属于区域“4”的是______。
1.在氧化还原反应中,非金属单质不一定是氧化剂( )
2.某元素从游离态变为化合态,则该元素一定被还原( )
3.有单质参加或生成的化学反应不一定是氧化还原反应( )
4.氧化还原反应中的反应物不是氧化剂就是还原剂( )
5.氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原( )
一、氧化还原反应概念的考查
1.(2023·长沙模拟)关于反应5KSO +2MnSO +8HO===2KMnO +8HSO +4KSO 的说
2 2 8 4 2 4 2 4 2 4
法不正确的是( )
A.KSO 发生还原反应
2 2 8
B.KMnO 是氧化产物
4
C.消耗3.6 g H O时,转移0.25 mol电子
2
D.氧化剂和还原剂的物质的量之比是2∶5
二、双线桥、单线桥表示法
2.氢化钠(NaH)广泛应用于工业生产。
(1)氢化钠(NaH)中氢元素的化合价为_______________________________________________。
(2)写出NaH与HO反应的化学方程式,并用“双线桥”标出电子转移的方向和数目:
2________________________________________________________________________
________________________________________________________________________,
氧化产物和还原产物的物质的量之比为____________________________________________。
(3)在高温下氢化钠(NaH)可将四氯化钛(TiCl )还原成金属钛,该反应的化学方程式为
4
________________________________________________________________________
________________________________________________________________________。
3.已知NaBH 与水反应的化学方程式为NaBH +2HO===NaBO +4H↑
4 4 2 2 2
回答下列问题:
(1)用“单线桥”标出电子转移的方向和数目:
________________________________________________________________________,
氧化剂:____________,还原剂:____________。
(2)若生成标准状况下4.48 L H ,则转移电子的物质的量为________。
2
考点二 氧化还原反应的强弱规律及价态规律
(一)强弱规律
1.氧化性、还原性强弱的比较方法
(1)根据化学方程式判断
氧化剂(氧化性)+还原剂(还原性)===还原产物+氧化产物
氧化性:氧化剂____氧化产物;
还原性:还原剂____还原产物。
(2)根据相同条件下产物的价态高低判断
如2Fe+3Cl=====2FeCl ;Fe+S=====FeS,则氧化性:Cl____S。
2 3 2
(3)根据反应条件、浓度大小及反应的剧烈程度判断
反应条件要求越低,浓度越大,反应越剧烈,对应物质的氧化性或还原性越强。
应用举例
1.MnO +4HCl(浓)=====MnCl +Cl↑+2HO,2KMnO +16HCl(浓)===2KCl+2MnCl +
2 2 2 2 4 2
5Cl↑+8HO,可判断氧化性:KMnO ____MnO 。
2 2 4 2
2.下列各组物质:①Cu与HNO 溶液 ②Cu与FeCl 溶液 ③Zn与HSO 溶液 ④Fe与
3 3 2 4
FeCl 溶液 ⑤Cl 与NaOH溶液 ⑥Fe与HNO 溶液
3 2 3
⑦Fe与HSO 溶液 ⑧Na与O
2 4 2
(1)由于浓度不同而发生不同氧化还原反应的是______________________(填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是________________________。
(3)氧化还原反应不受浓度、温度影响的是__________________________________________。2.氧化性、还原性强弱的比较规律
(1)氧化性
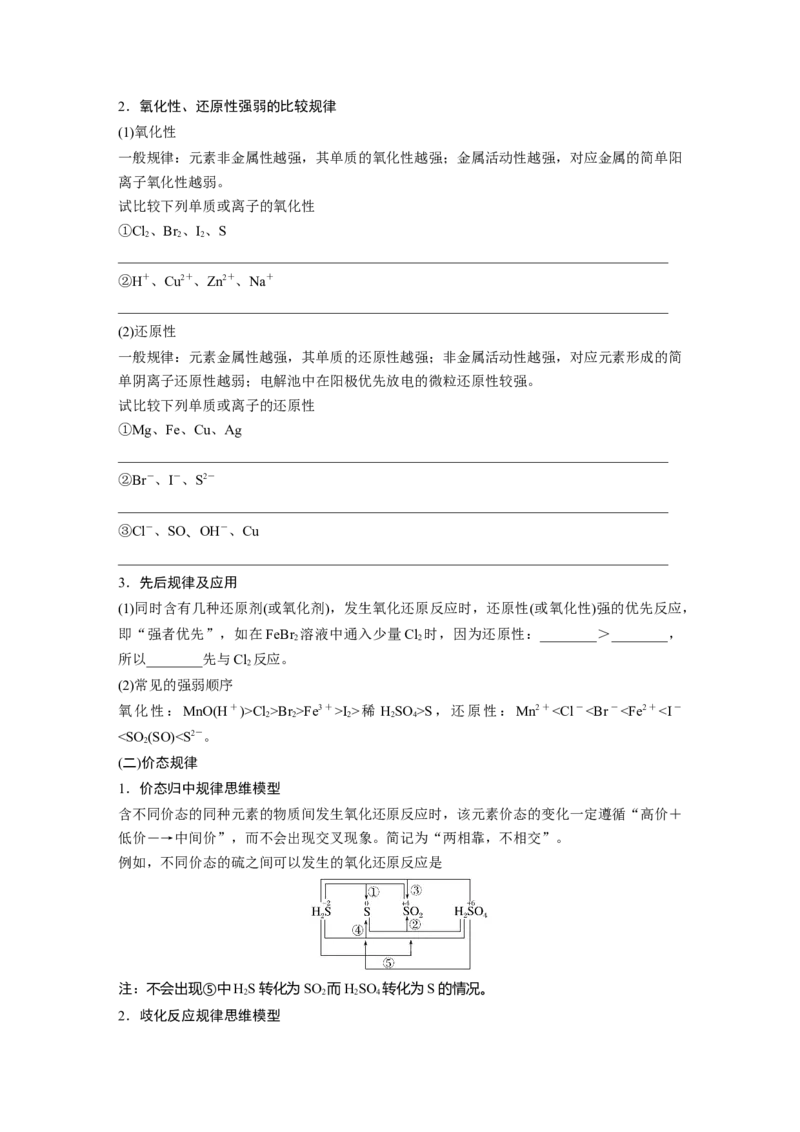
一般规律:元素非金属性越强,其单质的氧化性越强;金属活动性越强,对应金属的简单阳
离子氧化性越弱。
试比较下列单质或离子的氧化性
①Cl、Br 、I、S
2 2 2
______________________________________________________________________________
②H+、Cu2+、Zn2+、Na+
______________________________________________________________________________
(2)还原性
一般规律:元素金属性越强,其单质的还原性越强;非金属活动性越强,对应元素形成的简
单阴离子还原性越弱;电解池中在阳极优先放电的微粒还原性较强。
试比较下列单质或离子的还原性
①Mg、Fe、Cu、Ag
______________________________________________________________________________
②Br-、I-、S2-
______________________________________________________________________________
③Cl-、SO、OH-、Cu
______________________________________________________________________________
3.先后规律及应用
(1)同时含有几种还原剂(或氧化剂),发生氧化还原反应时,还原性(或氧化性)强的优先反应,
即“强者优先”,如在FeBr 溶液中通入少量Cl 时,因为还原性:________>________,
2 2
所以________先与Cl 反应。
2
(2)常见的强弱顺序
氧化性:MnO(H+)>Cl >Br >Fe3+>I >稀 HSO >S,还原性:Mn2+Fe3+>Ag+ B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe3+
2.已知I-、Fe2+、SO 、Cl-和H O 均有还原性,它们在酸性溶液中还原性的强弱顺序为
2 2 2
Cl-<Fe2+<HO<I-<SO ,则下列反应不能发生的是( )
2 2 2
A.2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
B.I+SO +2HO===HSO +2HI
2 2 2 2 4
C.HO+HSO ===SO ↑+O↑+2HO
2 2 2 4 2 2 2
D.2Fe2++Cl===2Fe3++2Cl-
2
3.根据反应事实判断性质的强弱。
①向Co O 固体中滴加浓盐酸,有黄绿色气体生成
2 3
②将氯气通入碘水中,溶液褪色生成两种酸(HCl和HIO )
3
则Cl 、HIO 、Co O 的氧化性由强到弱的顺序:_____________________;HCl、CoCl 、I
2 3 2 3 2 2
的还原性由强到弱的顺序:____________________________________________。4.实验室制备高铁酸钾(K FeO)并探究其性质。
2 4
(1)制备KFeO 的反应为3Cl+2Fe(OH) +10KOH===2KFeO+6KCl+8HO,由此得出氧化
2 4 2 3 2 4 2
性:Cl________(填“>”或“<”)FeO。
2
(2)K FeO 的性质探究:用KOH溶液将紫色KFeO 固体溶出,得到紫色KFeO 溶液。取少
2 4 2 4 2 4
量该溶液,滴加盐酸,有Cl 产生。
2
该实验表明Cl 和FeO的氧化性强弱关系与(1)相反,原因是___________________________。
2
二、价态规律的应用
5.氯气跟氢氧化钾溶液在一定条件下发生如下反应:Cl +KOH―→KX+KY+HO(未配
2 2
平),KX在一定条件下能自身反应:KX―→KY+KZ(未配平,KY与KZ的物质的量之比为
1∶3),以上KX、KY、KZ均是含氯元素的一元酸的钾盐,由以上条件推知在KX中氯元素
的化合价是( )
A.+1 B.+3 C.+5 D.+7
6.K35ClO 晶体与含有H37Cl的浓盐酸反应生成Cl,化学方程式为KClO+6HCl(浓)===KCl
3 2 3
+3Cl↑+3HO,该反应生成氯气的摩尔质量为________。
2 2
7.已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G―→Q+NaCl
②Q+HO――→X+H
2 2
③Y+NaOH―→G+Q+HO
2
④Z+NaOH―→Q+X+HO
2
这五种化合物中Cl元素化合价由低到高的顺序是________________。
1.(2020·山东,2)下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋
B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒
D.大气中NO 参与酸雨形成
2
2.(2020·北京,3)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl C.NO D.NaO
2 2 2
3.(2022·辽宁,6)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶
液恢复棕色;加入CCl ,振荡,静置,液体分层。下列说法正确的是( )
4
A.褪色原因为I 被Fe还原
2
B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈
D.溶液恢复棕色的原因为I-被氧化
4.(2022·浙江6月选考,10)关于反应NaSO+HSO ===NaSO +S↓+SO ↑+HO,下列
2 2 3 2 4 2 4 2 2说法正确的是( )
A.HSO 发生还原反应
2 4
B.NaSO 既是氧化剂又是还原剂
2 2 3
C.氧化产物与还原产物的物质的量之比为2∶1
D.1 mol Na SO 发生反应,转移4 mol电子
2 2 3
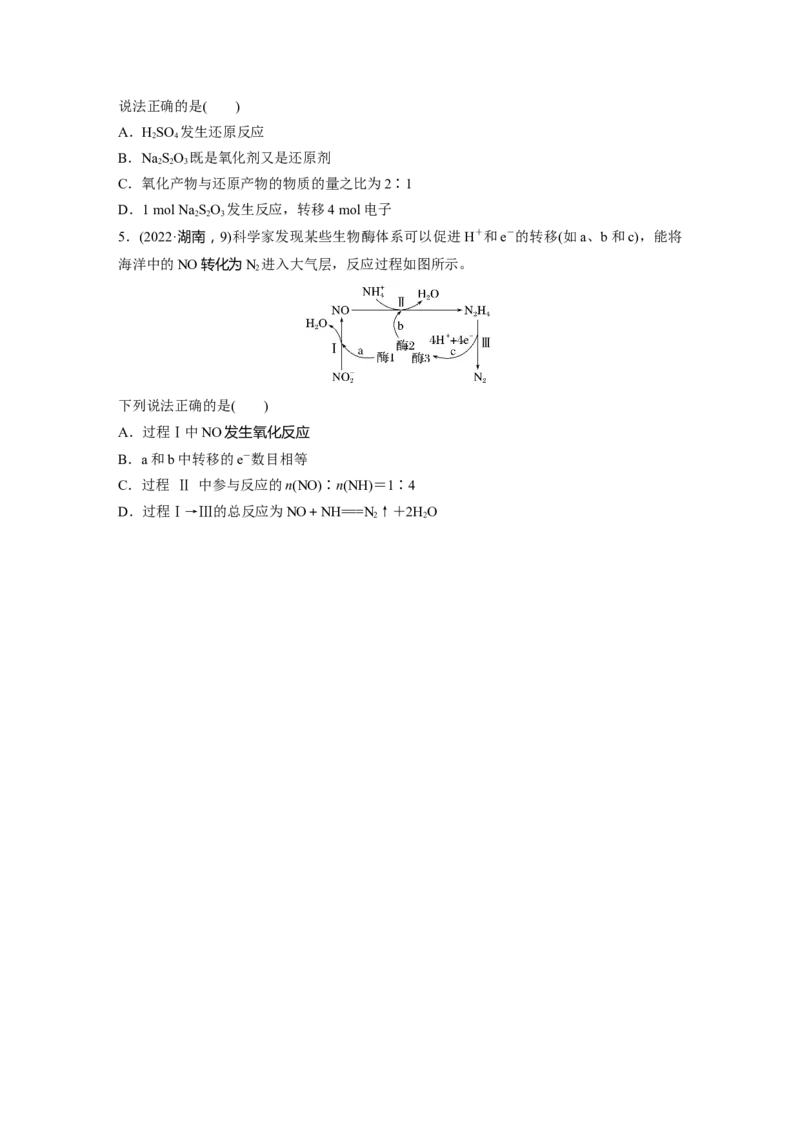
5.(2022·湖南,9)科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将
海洋中的NO转化为N 进入大气层,反应过程如图所示。
2
下列说法正确的是( )
A.过程Ⅰ中NO发生氧化反应
B.a和b中转移的e-数目相等
C.过程 Ⅱ 中参与反应的n(NO)∶n(NH)=1∶4
D.过程Ⅰ→Ⅲ的总反应为NO+NH===N↑+2HO
2 2