文档内容
1.一定条件下,硝酸铵受热分解的化学方程式(未配平)为NH NO ―→HNO+N↑+HO,
4 3 3 2 2
下列说法错误的是( )
A.配平后HO的化学计量数为6
2
B.NH NO 既是氧化剂又是还原剂
4 3
C.该反应既是分解反应也是氧化还原反应
D.氧化产物和还原产物的物质的量之比为5∶3
2.把图2中的物质补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平)。
对该氧化还原反应的离子方程式,下列说法不正确的是( )
A.IO是氧化剂,具有氧化性
B.氧化性:MnO>IO
C.氧化剂和还原剂的微粒个数之比为5∶2
D.若有2个Mn2+参加反应,则转移10个电子
3.钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三
铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到
130 ℃反应。其过程可以用如下化学方程式表示,下列说法不正确的是( )
①3Fe+NaNO +5NaOH===3NaFeO+HO+NH ↑
2 2 2 2 3
②NaFeO+NaNO +HO―→NaFe O+NH ↑+NaOH(未配平)
2 2 2 2 2 2 4 3
③NaFeO+NaFe O+2HO===Fe O+4NaOH
2 2 2 2 4 2 3 4
A.碱性条件下,NaNO 的氧化性比NaFeO、NaFe O 都强
2 2 2 2 2 4
B.反应①、②是氧化还原反应,③不是氧化还原反应
C.反应②配平后,HO的化学计量数是6
2
D.整个反应过程中,每有16.8 g Fe参加反应转移0.8 mol电子
4.工业上常用绿矾(FeSO ·7H O)处理工业废水中含有的重铬酸根离子(CrO),反应的化学方
4 2 2
程式为FeSO +KCr O +HSO ―→Fe (SO ) +Cr (SO ) +HO+KSO (未配平),下列有关
4 2 2 7 2 4 2 4 3 2 4 3 2 2 4
说法正确的是( )
A.每有1 mol K Cr O 参加反应,转移3 mol电子
2 2 7
B.KCr O 中铬元素的化合价为+7价
2 2 7
C.参与反应的Fe2+与Cr O物质的量之比为6∶1
2D.FeSO 是氧化剂
4
5.已知反应:①SO +2Fe3++2HO―→SO+2Fe2++W;
2 2
②Cr O+aFe2++bH+―→Cr3++Fe3++HO (未配平)
2 2
下列有关说法正确的是( )
A.方程式①中W为4OH-
B.还原性强弱:SO >Fe2+
2
C.a=6,b=7
D.反应Cr O+3SO +2H+===2Cr3++3SO+HO不能发生
2 2 2
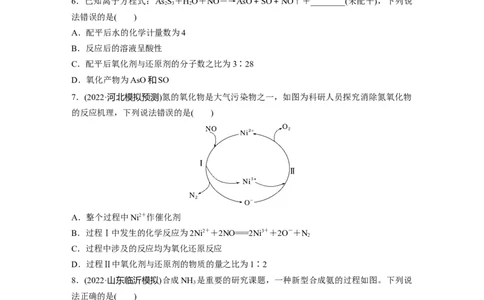
6.已知离子方程式:As S +HO+NO―→AsO+SO+NO↑+________(未配平),下列说
2 3 2
法错误的是( )
A.配平后水的化学计量数为4
B.反应后的溶液呈酸性
C.配平后氧化剂与还原剂的分子数之比为3∶28
D.氧化产物为AsO和SO
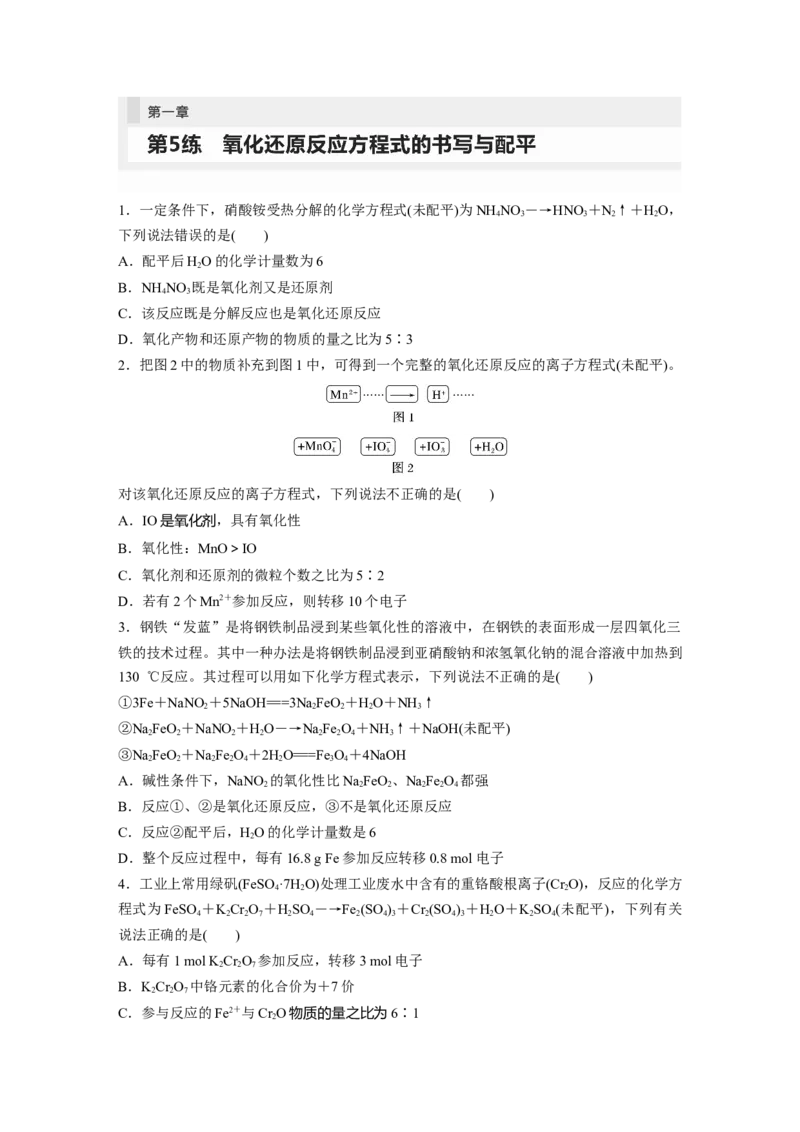
7.(2022·河北模拟预测)氮的氧化物是大气污染物之一,如图为科研人员探究消除氮氧化物
的反应机理,下列说法错误的是( )
A.整个过程中Ni2+作催化剂
B.过程Ⅰ中发生的化学反应为2Ni2++2NO===2Ni3++2O-+N
2
C.过程中涉及的反应均为氧化还原反应
D.过程Ⅱ中氧化剂与还原剂的物质的量之比为1∶2
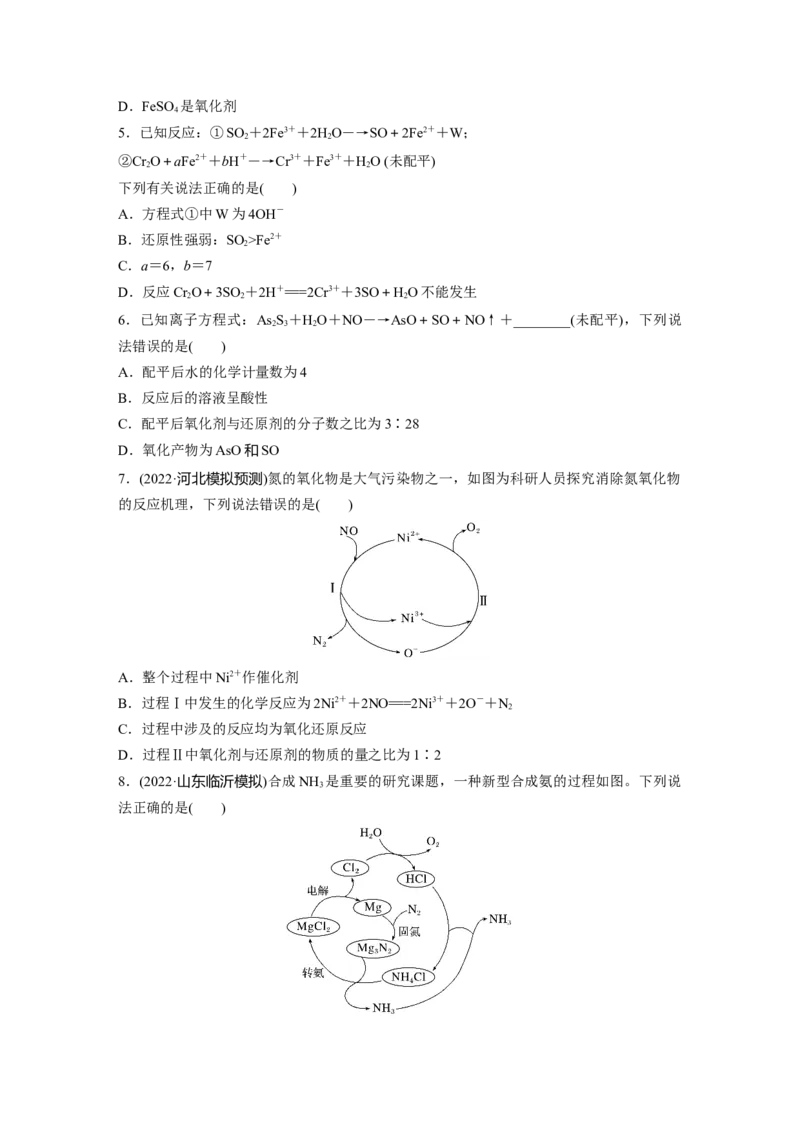
8.(2022·山东临沂模拟)合成NH 是重要的研究课题,一种新型合成氨的过程如图。下列说
3
法正确的是( )A.“转氨”过程属于人工固氮
B.合成过程中所涉及反应均为氧化还原反应
C.若用HO代替NH Cl进行转化,从体系中分离出NH 更容易
2 4 3
D.该合成氨过程中,参加反应的N 与HO的物质的量之比为1∶3
2 2
9.(2023·济南质检)向某FeBr 溶液中通入1.12 L(标准状况)的Cl ,测得溶液中c(Br-)=3c(Cl
2 2
-)=0.3 mol·L-1。反应过程中溶液的体积变化忽略不计。则下列说法正确的是( )
A.原溶液的浓度为0.1 mol·L-1
B.反应后溶液中c(Fe3+)=0.1 mol·L-1
C.反应后溶液中c(Fe3+)=c(Fe2+)
D.原溶液中c(Br-)=0.4 mol·L-1
10.(2022·吉林模拟)64 g铜粉投入一定量浓硝酸中,随着铜粉的溶解,反应生成的气体颜色
逐渐变浅,当铜粉完全溶解后共收集到由 NO 和NO组成的混合气体22.4 L(标准状况下),
2
则混合气体中NO的体积为( )
A.11.2 L B.33.6 L C.22.4 L D.44.8 L
11.(2022·浙江模拟)已知酸性KMnO 溶液能被NaSO 溶液还原成Mn2+而使溶液褪色。欲
4 2 3
使20.00 mL 1.00×10-2 mol·L-1酸性KMnO 溶液恰好褪色,需消耗25.00 mL Na SO 溶液,
4 2 3
则该NaSO 溶液的物质的量浓度(单位:mol·L-1)为( )
2 3
A.2.00×10-2 B.3.00×10-2
C.4.00×10-2 D.5.00×10-2
12.(2022·山东模拟)玻璃仪器内壁残留的硫单质可用热NaOH溶液洗涤除去,发生如下反应:
①3S+6NaOH=====2NaS+ NaSO + 3HO
2 2 3 2
②(x-1)S+NaS=====NaS (x=2~6)
2 2 x
③S+NaSO =====NaSO
2 3 2 2 3
下列说法正确的是( )
A.反应①②③中,硫单质的作用相同
B.反应①中,每消耗1 mol硫单质转移4 mol电子
C.0.96 g硫单质与a mL 2 mol·L-1热NaOH溶液恰好完全反应,只生成NaS和NaSO ,
2 2 3
则a=60
D.1.28 g硫单质与10 mL 2 mol·L-1热NaOH溶液恰好完全反应,只生成NaS 和NaSO ,
2 x 2 2 3
则x=5
13.根据信息完成下列方程式。
(1)KMnO 氧化废水中Mn2+生成MnO 的离子方程式为_____________________________。
4 2
(2)NaAlH 与水发生氧化还原反应的化学方程式为__________________________________。
4
(3)在酸性条件下,NaClO 可发生反应生成NaCl并释放出ClO ,该反应的离子方程式为
2 2
________________________________________________________________________。
(4)PbO 可 由 PbO 与 次 氯 酸 钠 溶 液 反 应 制 得 , 反 应 的 离 子 方 程 式 为
2_______________________。
(5)NaClO 溶液与 Ag 反应的产物为 AgCl、NaOH 和 O ,该反应的化学方程式为
2
________________________________________________________________________。
(6)在45~50 ℃时向CuCl悬浊液中持续通入空气,得到碱式氯化铜[Cu (OH) Cl·3H O],该
2 2 2 2
反应的化学方程式为___________________________________________________。
14.锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO )制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4
Ⅰ.制备
(1)写出铝热法还原MnO 制备锰的化学方程式:_____________________________________。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度 SO 的烟气,可用
2
以下方法处理。
方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO
2
进行脱硫的化学方程式: __________________________________________。
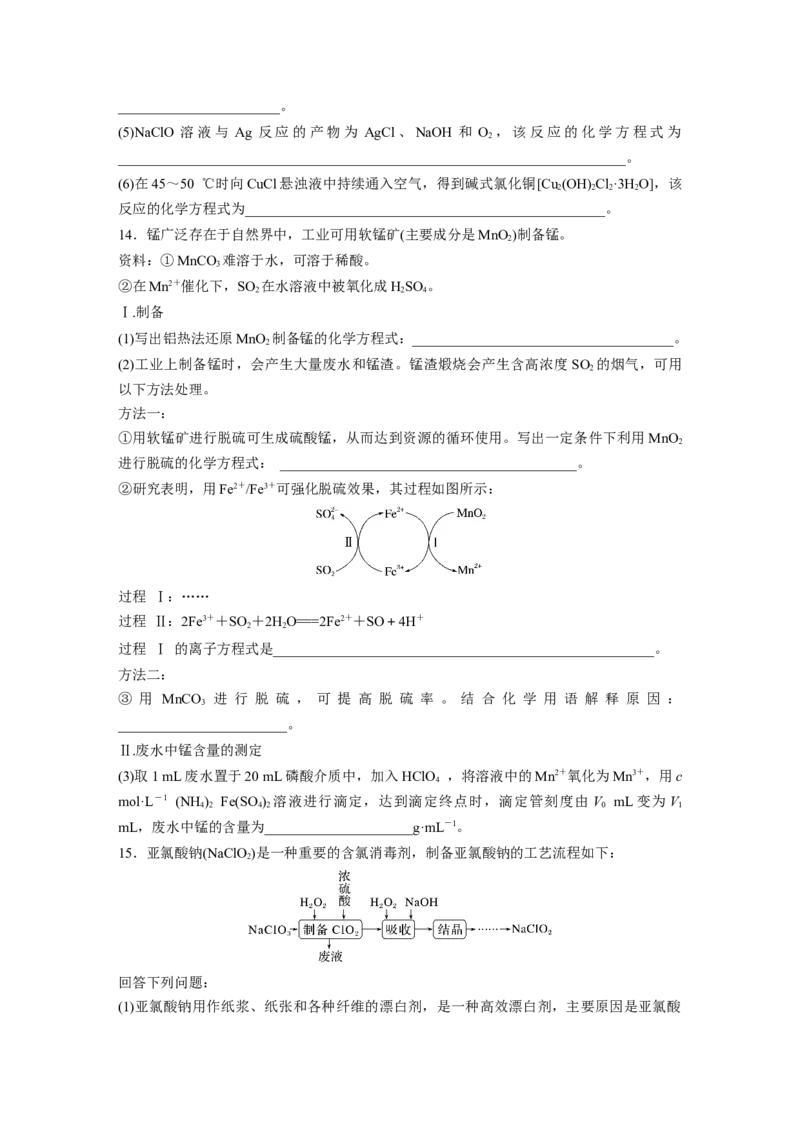
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如图所示:
过程 Ⅰ:……
过程 Ⅱ:2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
过程 Ⅰ 的离子方程式是______________________________________________________。
方法二:
③ 用 MnCO 进 行 脱 硫 , 可 提 高 脱 硫 率 。 结 合 化 学 用 语 解 释 原 因 :
3
________________________。
Ⅱ.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO ,将溶液中的Mn2+氧化为Mn3+,用c
4
mol·L-1 (NH ) Fe(SO ) 溶液进行滴定,达到滴定终点时,滴定管刻度由 V mL变为V
4 2 4 2 0 1
mL,废水中锰的含量为_____________________g·mL-1。
15.亚氯酸钠(NaClO)是一种重要的含氯消毒剂,制备亚氯酸钠的工艺流程如下:
2
回答下列问题:
(1)亚氯酸钠用作纸浆、纸张和各种纤维的漂白剂,是一种高效漂白剂,主要原因是亚氯酸钠具有________性。
(2)制备 ClO 气体的化学方程式为 2NaClO +HO +HSO ===2ClO ↑+O↑+NaSO +
2 3 2 2 2 4 2 2 2 4
2HO ; 制 备 时 可 用 S 代 替 HO , 写 出 该 反 应 的 离 子 方 程 式 :
2 2 2
___________________________。
(3)测定某亚氯酸钠样品的纯度:准确称取亚氯酸钠样品m g,加入适量蒸馏水和过量的碘
化钾晶体,再滴入适量稀硫酸(发生反应:ClO+4I-+4H+===2I +Cl-+2HO),配成250
2 2
mL待测液。移取25.00 mL待测液于锥形瓶中,加几滴淀粉溶液,用 c mol·L-1的NaSO
2 2 3
标准溶液进行滴定,消耗NaSO 标准溶液V mL (已知:I+2SO===2I-+SO)。
2 2 3 2 2 4
①移取25.00 mL待测液的仪器的名称是________________。
②该样品中NaClO 的质量分数为__________(用含m、c、V的代数式表示);在滴定操作正
2
确无误的情况下,此实验测得结果偏高,其可能的原因是_________________________。