文档内容
物质及其变化
第 1 讲 物质的分类及转化
课 程 标 准 知 识 建 构
1.认识元素可以组成不同种类的物质,根据物质的组
成和性质可以对物质进行分类。
2.认识同类物质具有相似的性质,在一定条件下各
类物质可以相互转化。
3.认识胶体是一种常见的分散系。
一、物质的组成和分类
(一)物质的组成
1.物质的组成
宏观上物质是由元素组成的,微观上物质是由分子、原子或离子等微观粒子
构成的。
2.元素与物质的组成
(1)元素:具有相同核电荷数的一类原子的总称。
(2)元素的存在形态
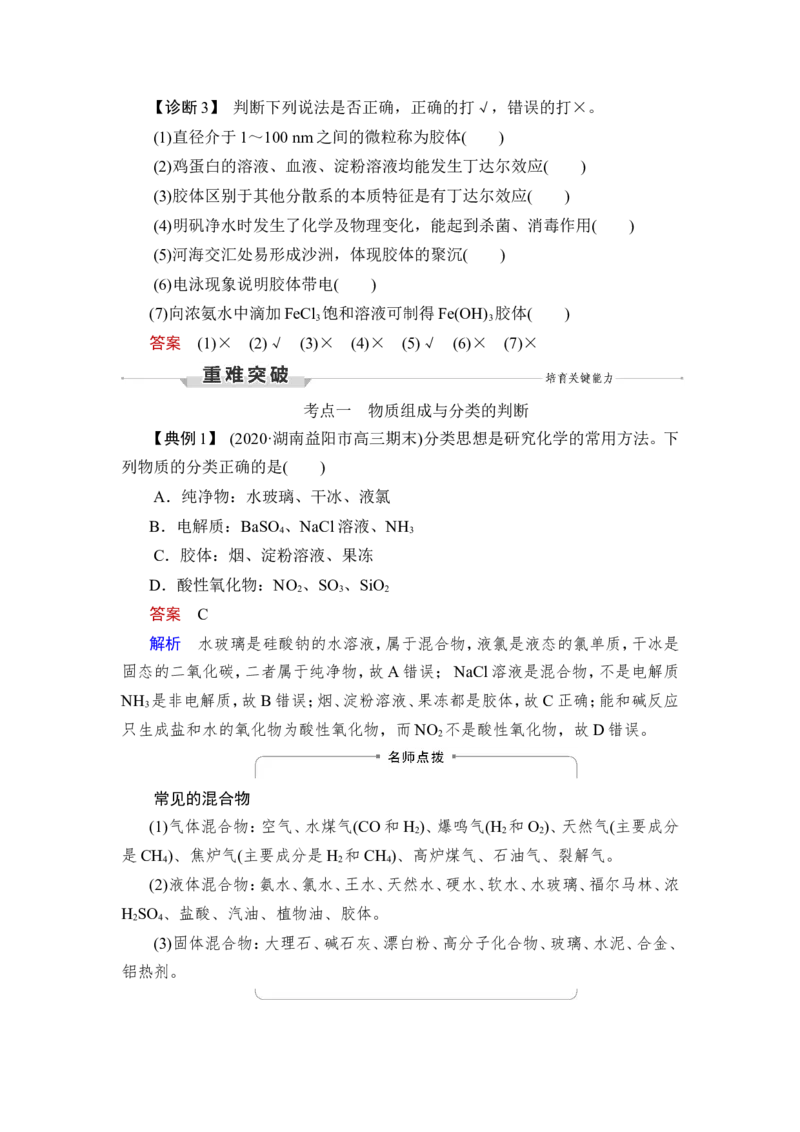
3.微粒与物质的构成4.同素异形体
(1)概念:由同种元素形成的不同单质。
(2)常见同素异形体:金刚石与 石墨、 C 、碳纳米管等,O 与O ,白磷与红磷,
60 2 3
单斜硫与 斜方硫 ( 正交硫 )等。
(3)性质特点:物理性质差别较大,同素异形体之间的转化属于化学变化。
5.纯净物与混合物
(1)纯净物:由同种单质或化合物组成的物质。
(2)混合物:由几种不同的单质或化合物组成的物质。
(3)纯净物和混合物的区别
纯净物 混合物
有固定的组成和结构 无固定的组成和结构
有一定的熔、沸点 无一定的熔、沸点
保持一种物质的性质 保持原有物质各自的性质
(二)物质的分类
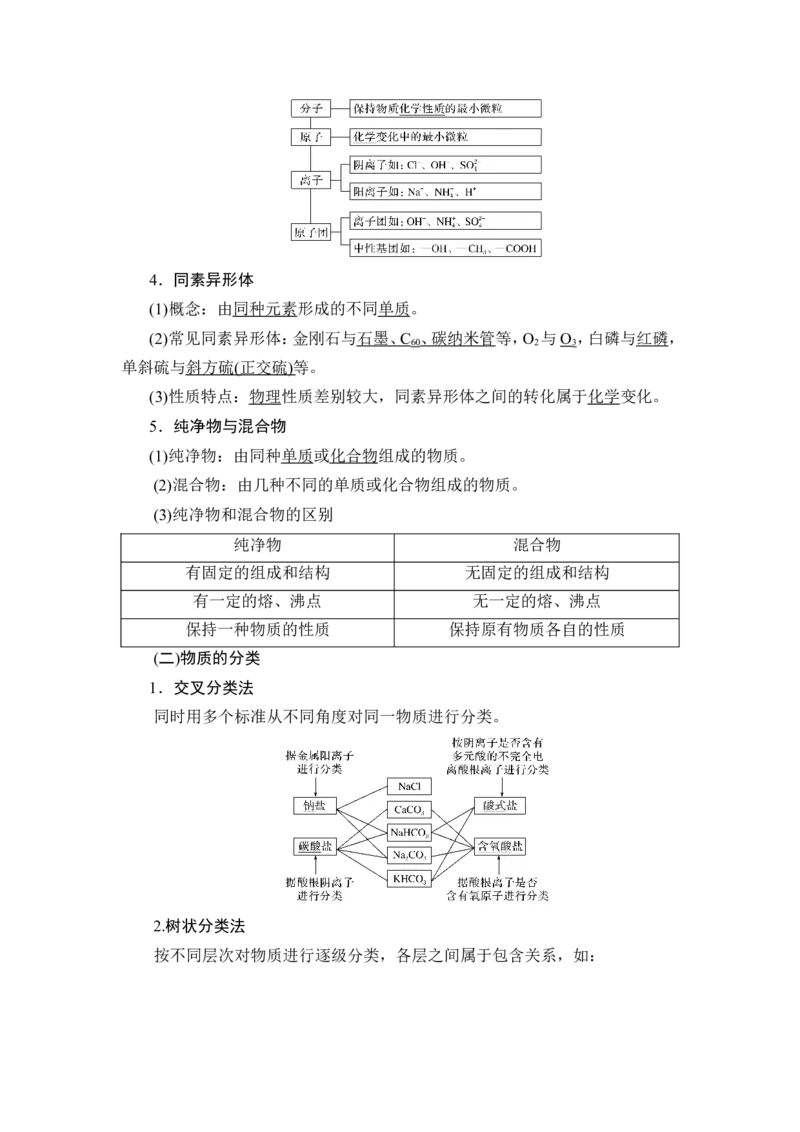
1.交叉分类法
同时用多个标准从不同角度对同一物质进行分类。
2.树状分类法
按不同层次对物质进行逐级分类,各层之间属于包含关系,如:【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)Na、NaCl、SiO 、H SO 都称为分子式( )
2 2 4
(2)含有金属元素的离子不一定是阳离子( )
(3)某物质经科学测定只含有一种元素,不可以断定该物质一定是一种纯净
物( )
(4)只由一种元素的阳离子与另一种元素的阴离子组成的物质一定为纯净物(
)
(5)能与酸反应的氧化物,一定是碱性氧化物( )
(6)CO 和NO 均能与H O反应生成酸,故二者都是酸性氧化物( )
2 2 2
(7)纯碱属于碱,硫酸氢钠、碳酸氢钠属于酸式盐( )
答案 (1)× (2)√ (3)√ (4)× (5)× (6)× (7)×
二、物质的性质和变化
1.物理变化和化学变化
宏观 有新物质生成的是化学变化,反之是物理变化
有旧化学键断裂,同时有新化学键形成的是化学变化;只有化学
微观 键断裂或生成的过程不是化学变化,如NaCl晶体的熔化和溶液
中晶体的析出
化学变化中一定伴随着物理变化,但物理变化过程中一般没有
二者关系
化学变化。
2.化学反应的分类
化学反应
3.常见物质间的转化
(1)单质、氧化物、酸(或碱)和盐的转化关系(2)应用实例:
写出上述反应的化学方程式并指明反应类型:
① 2HCl + Fe == =FeCl + H ↑,置换反应;
2 2
② 6HCl + Fe O == =2FeCl + 3H O,复分解反应;
2 3 3 2
③ 2HCl + CaCO == =CaCl + H O + CO ↑,复分解反应;
3 2 2 2
④ HCl + NaOH == =NaCl + H O,复分解反应。
2
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)用铂丝蘸取Na SO 溶液进行焰色试验是化学变化( )
2 4
(2)232Th转化成233U是化学变化( )
(3)Na CO ·10H O的风化是物理变化( )
2 3 2
(4)用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐不涉及化学变化( )
(5)有化学键断裂的变化一定是化学变化( )
(6)CO还原CuO的反应属于置换反应( )
(7)用CCl 萃取溴水中的溴属于物理变化( )
4
答案 (1)× (2)× (3)× (4)√ (5)× (6)× (7) √
三、分散系 胶体
1.分散系
(1)概念
把一种(或几种)物质分散在另一种物质中所得到的体系。
(2)分类
标准:分散质微粒的直径大小。
(3)三种分散系的比较
分散系 溶液 胶体 浊液单个小分子或 高分子或多个分 巨大数目的分子
分散质粒子
离子 子的集合体 集合体
分散质粒子直径 小于 1_nm 1 ~ 100_nm 大于 100_nm
外观 均一、透明 均一 不均一、不透明
稳定性 稳定 较稳定 不稳定
性
能否透过滤纸 能 能 不能
质
能否透过半透膜 能 不能 不能
鉴别 无丁达尔效应 有丁达尔效应 静置分层或沉淀
2.胶体
(1)胶体的分类
气溶胶 雾、云、烟
按分散剂
液溶胶 Fe(OH) 胶体、蛋白质溶液
3
状态
固溶胶 烟水晶、有色玻璃
分散质粒子是很多小分子或离子的集合体,如Fe(OH)
3
粒子胶体
按分散质 胶体
分子胶体 分散质粒子是高分子化合物,如淀粉溶液、蛋白质溶液
(2)胶体的性质及应用
(3)Fe(OH) 胶体的制备
3
①图示
②操作:向沸水中逐滴加入FeCl 饱和溶液,继续煮沸至液体呈红褐色,停止
3
加热,即制得Fe(OH) 胶体。
3
③制备原理:FeCl + 3H O ===== Fe(OH) ( 胶体 ) + 3HCl 。
3 2 3【诊断3】 判断下列说法是否正确,正确的打√,错误的打×。
(1)直径介于1~100 nm之间的微粒称为胶体( )
(2)鸡蛋白的溶液、血液、淀粉溶液均能发生丁达尔效应( )
(3)胶体区别于其他分散系的本质特征是有丁达尔效应( )
(4)明矾净水时发生了化学及物理变化,能起到杀菌、消毒作用( )
(5)河海交汇处易形成沙洲,体现胶体的聚沉( )
(6)电泳现象说明胶体带电( )
(7)向浓氨水中滴加FeCl 饱和溶液可制得Fe(OH) 胶体( )
3 3
答案 (1)× (2)√ (3)× (4)× (5)√ (6)× (7)×
考点一 物质组成与分类的判断
【典例1】 (2020·湖南益阳市高三期末)分类思想是研究化学的常用方法。下
列物质的分类正确的是( )
A.纯净物:水玻璃、干冰、液氯
B.电解质:BaSO 、NaCl溶液、NH
4 3
C.胶体:烟、淀粉溶液、果冻
D.酸性氧化物:NO 、SO 、SiO
2 3 2
答案 C
解析 水玻璃是硅酸钠的水溶液,属于混合物,液氯是液态的氯单质,干冰是
固态的二氧化碳,二者属于纯净物,故A错误; NaCl溶液是混合物,不是电解质
NH 是非电解质,故B错误;烟、淀粉溶液、果冻都是胶体,故C正确;能和碱反应
3
只生成盐和水的氧化物为酸性氧化物,而NO 不是酸性氧化物,故D错误。
2
常见的混合物
(1)气体混合物:空气、水煤气(CO和H )、爆鸣气(H 和O )、天然气(主要成分
2 2 2
是CH )、焦炉气(主要成分是H 和CH )、高炉煤气、石油气、裂解气。
4 2 4
(2)液体混合物:氨水、氯水、王水、天然水、硬水、软水、水玻璃、福尔马林、浓
H SO 、盐酸、汽油、植物油、胶体。
2 4
(3)固体混合物:大理石、碱石灰、漂白粉、高分子化合物、玻璃、水泥、合金、
铝热剂。【对点练1】 (物质的分类)下列物质的分类正确的是( )
选项 碱 酸 盐 碱性氧化物 酸性氧化物
A Na CO H SO NaOH SO CO
2 3 2 4 2 2
B NaOH HCl NaCl Na O NO
2 2
C KOH HNO CaCO CaO Mn O
3 3 2 7
D NaOH HCl CaF Na O SO
2 2 2 2
答案 C
解析 Na CO 、NaOH、SO 依次为盐、碱、酸性氧化物,A项错误; NO 不是
2 3 2 2
酸性氧化物,B项错误;Na O 不是碱性氧化物,D项错误。
2 2
【对点练2】 (生活中物质的分类)下列说法中正确的有( )
①面粉中禁止添加CaO 、过氧化苯甲酰等增白剂,CaO 属于碱性氧化物,也
2 2
属于离子化合物,其阴、阳离子个数比为1∶1 ②国产大飞机——C919使用的
碳纤维是一种新型的无机非金属材料 ③“浮梁巧烧瓷,颜色比琼玖”,描述的
是我国驰名于世的陶瓷,陶瓷是一种硅酸盐产品 ④“青蒿一握,以水二升渍,绞
取汁”,该过程属于物理变化 ⑤使用含钙离子浓度较大的地下水洗衣服,肥皂去
污能力减弱
A.2个 B.3个
C.4个 D.5个
答案 C
解析 ①碱性氧化物是和酸反应生成盐和水的氧化物,过氧化钙属于过氧化
物,不是碱性氧化物,其阴、阳离子个数比为1∶1,故错误;②国产大飞机——
C919使用的碳纤维是一种新型的无机非金属材料,故正确;③“浮梁巧烧瓷,颜
色比琼玖”,描述的是我国驰名于世的陶瓷,陶瓷是一种硅酸盐产品,故正确;
④“青蒿一握,以水二升渍,绞取汁”,该过程利用萃取原理,属于物理变化,故正
确;⑤含钙离子浓度较大的地下水与高级脂肪酸钠反应会生成高级脂肪酸钙沉淀
去污能力减弱,故正确。正确的个数为4个,答案选C。
有关氧化物的几个“不一定”
(1)碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物,如
Mn O 为酸性氧化物。
2 7
(2)酸性氧化物不一定是非金属氧化物,如Mn O ;非金属氧化物也不一定是
2 7
酸性氧化物,如CO、NO。(3)酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱,如SiO 、
2
Fe O 。
2 3
考点二 物质性质与变化的分析
【典例2】 (2020·福建福州市高三期末《) 本草纲目》卷七石碱条: “彼人采蒿
蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面”,则下列说
法正确的是( )
A.文中的“灰”,指的是草木灰(主要成分K CO )
2 3
B.“发面”是利用了“灰”的不稳定性
C.“以水淋汁,久则凝淀如石”的过程是萃取
D.该物质用来浣衣、去垢的过程涉及氧化还原反应
答案 A
解析 “彼人采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,
亦去垢发面”,说明“石碱”易溶于水,能洗去油脂,能发面,作为发酵剂。植物烧
成的灰中的成分主要为碳酸盐,成分来自植物烧成的灰中的成分,文中的“灰”,
指的是草木灰(主要成分K CO ),故A正确;发面,能作为发酵剂,故B错误;
2 3
“以水淋汁,久则凝淀如石”的过程是溶解和结晶,故C错误;该物质用来浣衣、
去垢的过程不涉及氧化还原反应,涉及水解等过程,故D错误。
【对点练3】 (物质变化类型的判断)下列各组变化中,前者是物理变化,后者
是化学变化的是( )
A.碘的升华、石油的分馏
B.NH Cl溶液除铁锈、食盐水导电
4
C.蛋白质溶液中加入饱和(NH ) SO 溶液、蓝色的胆矾在常温下变白
4 2 4
D.热的饱和KNO 溶液降温析出晶体、二硫化碳洗涤试管内壁上的硫
3
答案 C
解析 A项涉及的都是物理变化;B项中涉及的都是化学变化;D项中涉及
的都是物理变化。
【对点练4】 (双选)(物质的性质及应用)(2020·海南省高三模拟一)下列有关
物质的性质与用途具有对应关系的是( )
A.NH HCO 受热易分解,可用作化肥
4 3
B.稀硫酸具有酸性,可用于除去铁锈
C.SO 具有漂白性,可用于纸浆漂白
2D.Al O 具有两性,可用于电解冶炼铝
2 3
答案 BC
解析 NH HCO 受热易分解和用作化肥无关,可以用作化肥是因为含有氮元
4 3
素,A项错误;铁锈的主要成分为Fe O ,硫酸具有酸性可以和Fe O 反应,具有对
2 3 2 3
应关系,B项正确;二氧化硫的漂白原理是二氧化硫与有色物质化合成不稳定的
无色物质,C项正确;电解冶炼铝,只能说明熔融氧化铝能导电,是离子化合物,
与其具有两性无关,D项错误。
【对点练5】 (化学反应类型的判断)(2020·河南濮阳市高三二模)中国医药学
是一个伟大的宝库。古代制取下列药物过程中未发生氧化还原反应的是( )
《本草纲目》:制取“玄明 以芒硝于风日中消尽水气,自成轻
A
粉”(Na SO ) 飘白粉也
2 4
以铁筋穿作窍,以绳子穿之;用净瓷
《通玄秘术》:制取“华盖丹”(醋酸
B 瓮子盛米醋1斗,将铅片子悬排于
铅)
瓮子口……
《本草蒙筌》:制取“灵砂”(硫化 水银一两,硫黄六铢,先炒作青砂
C
汞) 头,后入水火炉抽之……
《本草图经》:制取“铁华粉”(醋酸 以铁拍做段片,置醋糟中,积久衣
D
亚铁) 生……
答案 A
解析 用芒硝制硫酸钠的反应为:Na SO ·10H O===Na SO +10H O↑,没有
2 4 2 2 4 2
发生元素化合价的升降,不是氧化还原反应,A符合题意;用净瓷瓮子盛米醋1斗,
将铅片子悬排于瓮子口,即将铅的单质转化为醋酸铅,铅的化合价升高,是氧化
还原反应,B不符合题意;水银一两,硫黄六铢,来制硫化汞,硫和汞的化合价改
变了,是氧化还原反应,C不符合题意;以铁拍做段片,置醋糟中,积久衣生制醋
酸亚铁,铁的化合价升高,是氧化还原反应,D不符合题意。
物质变化中的“三馏”、“四色”、“五解”和“十六化”
物理变化 化学变化
三馏 蒸馏、分馏 干馏
四色 焰色试验 显色反应、颜色反应、指示剂变色反应
五解 潮解 分解、电解、水解、裂解
十六化
熔化、汽化、液 氧化、风化、钝化、催化、皂化、歧化、硝化、酯化、裂化、升华 化、油脂的硬化、煤的气化、煤的液化
考点三 胶体的性质和应用
【典例3】 (2020·广东广州市高三期末)下列现象或应用中,不涉及胶体性质
的是( )
A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
B.清晨,在茂密的树林中,常可以看到从枝叶间透过的光柱
C.用半透膜分离淀粉和食盐的混合液
D.肾功能衰竭等疾病引起的血液中毒,可用血液透析进行治疗
答案 A
解析 氯化铁溶液中逐滴加入NaOH溶液,会产生红褐色沉淀,不涉及胶体
性质,故A正确;清晨的雾属于胶体,看到从枝叶间透过的道道光柱就是胶体具
有的丁达尔效应,涉及胶体性质,故B错误;食盐溶液中溶质粒子能通过半透膜,
淀粉溶液属于胶体,胶体中的分散质粒子不能通过,可以用半透膜来分离,涉及
胶体性质,故C错误;血液透析涉及胶体性质,故D错误。
(1)胶体区别于其他分散系的本质特征是分散质粒子的直径大小(1~100
nm)。
(2)区分胶体和溶液两种分散系的最简便的方法是利用丁达尔效应。
(3)胶粒不是胶体,是分散质,一般是大量难溶物(分子)的聚集体或高分子(淀
粉、蛋白质)。
(4)胶体不带电荷,胶体粒子因吸附离子往往带有电荷,但淀粉胶体的胶体粒
子不带电荷。
【对点练6】 (胶体的组成和性质)FeCl 溶液、Fe(OH) 胶体、Fe(OH) 浊液是三
3 3 3
种重要的分散系,下列叙述中不正确的是( )
A.Fe(OH) 胶体区别于其他分散系的本质特征是分散质微粒的直径在 1~
3
100 nm之间
B.分别用一束光透过三种分散系,只有Fe(OH) 胶体具有丁达尔效应
3
C.三种分散系的颜色都相同,且均能与盐酸反应,具有吸附性
D.三种分散系中分散质微粒直径大小不同
答案 C解析 FeCl 溶液为棕黄色,不能与盐酸反应,且不具有吸附性,Fe(OH) 胶体
3 3
Fe(OH) 浊液均为红褐色,Fe(OH) 浊液不具有吸附性,C项不正确。
3 3
【对点练7】 (胶体的性质及应用)下列关于胶体的性质与应用的说法错误的
是( )
A.明矾净水利用的是胶体的吸附性
B.胶体区别于其他分散系的本质特征是丁达尔效应
C.胶粒不能透过半透膜,血液透析利用半透膜将有害物质移出体外
D.静电除尘器除去空气或工厂废气中的飘尘,是利用胶体粒子的带电性而
加以除去
答案 B
解析 明矾中铝离子水解为氢氧化铝胶体,氢氧化铝胶体具有吸附性,A项
正确;胶体区别于其他分散系的本质特征是分散质粒子直径不同,B项错误;血
液属于胶体,可利用半透膜提纯胶体,C项正确;胶体粒子带电,静电除尘器吸附
带电的飘尘,使之发生电泳而除去,D项正确。
【对点练8】 (胶体的制备)
(1)实验室制取Fe(OH) 胶体的方法是______________________________。
3
有关反应的化学方程式为________________________________________。
(2)可以利用________证明Fe(OH) 胶体已经制成。
3
(3)可以利用________来提纯Fe(OH) 胶体。证明Fe(OH) 胶体与Cl-已完全
3 3
分离的实验方法是______________________________________。
答案 (1)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,然后向烧杯中
逐滴滴加饱和FeCl 溶液,并继续煮沸至液体呈透明的红褐色即得Fe(OH) 胶体
3 3
FeCl +3H O=====Fe(OH) (胶体)+3HCl
3 2 3
(2)丁达尔效应
(3)半透膜袋 将半透膜袋再浸入另一份蒸馏水中,片刻后取出半透膜袋,向
蒸馏水中滴入AgNO 溶液,无白色沉淀产生,证明Fe(OH) 胶体与Cl-已完全分
3 3
离
(1)胶体具有介稳性的主要原因是胶体粒子可以通过吸附而带有电荷,且同
种胶体粒子的电性相同。
(2)掌握净水剂及其作用原理
胶体粒子具有较大的表面积,吸附能力强,能在水中吸附悬浮固体或毒素形成沉淀,从而达到净化水的目的。KAl(SO ) ·12H O、FeCl ·6H O等物质被称为净
4 2 2 3 2
水剂,其形成胶体的化学原理是Al3+、Fe3+发生水解反应分别生成Al(OH) 胶体、
3
Fe(OH) 胶体。
3
微专题5 传统文化中的化学物质及变化
中华优秀传统文化中的化学知识
1.中国古代化学工艺简介
(1)烧制陶器。陶瓷是传统的硅酸盐材料,它的基本原料是黏土。釉料中主要
含有一些金属及其化合物,在高温烧制时金属及其化合物发生了不同的氧化还原
反应,产生不同颜色的物质。
(2)青铜的冶炼。冶炼青铜的过程较复杂,大致为先把选好的矿石加入熔剂,
再放在炼炉内,燃木炭熔炼,等火候成熟,弃去炼渣得初铜。初铜经提炼才能获得
纯净的红铜。红铜加锡、铅熔成合金,即是青铜。
(3)造纸。以我国古书《天工开物》卷中所记载之竹纸制造方法为例,作为介绍
古时以竹子造纸之步骤如下:
①斩竹漂塘。目的:利用天然微生物分解并洗去竹子之青皮。
②煮徨足火:放入“徨”桶内与石灰一道蒸煮。目的:是利用石灰的碱性脱脂
杀死微生物等。
③舂臼:把上述处理的竹子,放入石臼中打烂,形同泥面。
④荡料入帘:将被打烂之竹料倒入水槽内,并以竹帘在水中荡料,竹料成为薄
层附于竹帘上面。
⑤覆帘压纸,透火焙干。
(4)黑火药。主要成分:硝酸钾、木炭和硫黄。反应原理:2KNO +S+
3
3C===K S+N ↑+3CO ↑
2 2 2
(5)酿酒。第一步用米曲霉、黑曲霉、黄曲霉等将淀粉水解,称为糖化;第二步
由酵母菌再将葡萄糖发酵产生酒精。发酵后的混合料经过蒸馏,得到白酒和酒糟
(6)染色。染色是一个很古老的工艺,即用染料使物品着色。
2.常考经典史籍材料归纳
(1)《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油。
(2)《黄白第十六》中“曾青涂铁,铁赤如铜”,其“曾青”是可溶性铜盐。
(3)《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的
碱是K CO 。
2 3(4)《天工开物》中“凡石灰经火焚炼为用”里的“石灰”指的是CaCO 。
3
(5)《本草经集注》中区分硝石(KNO )和朴消(Na SO )的方法:“以火烧之,紫
3 2 4
青烟起,乃真硝石也”这是利用了“焰色试验”。
(6)《梦溪笔谈器用》中“古人以剂钢为刃,柔铁为茎干,不尔则多断折”的
“剂钢”是指铁的合金。
(7《) 本草图经》中“绿矾形似朴消(Na SO ·10H O)而绿色,取此物置于铁板上,
2 4 2
聚炭,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金汁者是真也。 ”中的
绿矾是FeSO ·7H O描述了绿矾受热分解的现象。
4 2
3.解答传统文化问题的四个步骤
【案例1】 以传统文化为依托,考查物质组成和性质
(2021·1月广东学业水平选择考适应性测试,1)书法是中华文化之瑰宝,“无色而
具画图的灿烂,无声而有音乐的和谐”,书法之美尽在笔墨纸砚之间(如图所示的
王羲之的“平安贴”)。下列关于传统文房四宝的相关说法正确的是( )
A.墨汁是一种水溶液B.宣纸是合成高分子材料
C.砚石的成分与水晶相同
D.制笔用的狼毫主要成分是蛋白质
答案 D
解析 A.墨汁中分散质粒子直径在1至100纳米之间,属于胶体,故A错误;B.宣
纸的主要成分是天然纤维素,不是合成高分子材料,故B错误;C.水晶的主要成
分是二氧化硅,而砚石的成分为无机盐,故C错误;D.狼毫为动物的毛,主要成分
为蛋白质,故D正确。
【案例2】 以传统文化为依托,考查物质变化和反应
(2021·1月广东学业水平选择考适应性测试,2)“古诗文经典已融入中华民族的
血脉”下列诗文中隐含化学变化的是( )
A.月落乌啼霜满天,江枫渔火对愁眠
B.掬月水在手,弄花香满衣
C.飞流直下三千尺,疑是银河落九天
D.举头望明月,低头思故乡
答案 A
解析 A.渔火为物质燃烧发的光,燃烧属于化学变化,A符合题意;B.“掬月水在
手”为光线的反射,“弄花香满衣”为分子的扩散,均为物理变化,B与题意不符
C.“飞流直下三千尺”,为水的自由落体运动,为物理变化,C与题意不符;D.“举
头望明月”,月光为反射的太阳光,为物理变化,D与题意不符。
【案例3】 以传统文化为依托,考查实验操作
(2020·课标全国Ⅱ)北宋沈括《梦溪笔谈》中记载: “信州铅山有苦泉,流以
为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有
关叙述错误的是( )
A.胆矾的化学式为CuSO
4
B.胆矾可作为湿法冶铜的原料
C.“熬之则成胆矾”是浓缩结晶过程
D.“熬胆矾铁釜,久之亦化为铜”是发生了置换反应
答案 A
解析 胆矾的化学式为CuSO ·5H O,A项错误;湿法冶铜的原理是CuSO +
4 2 4
Fe===FeSO +Cu,即胆矾可作为湿法冶铜的原料,B项正确;CuSO 溶液经熬制
4 4可以得到胆矾,是CuSO 溶液浓缩结晶的过程,C项正确;熬胆矾的铁釜中发生
4
的反应为CuSO +Fe===FeSO +Cu,属于置换反应,D项正确。
4 4
1.(2020·河南许昌、济源、平顶山三市二次联考)磁山(在今河北省邯郸市武
安)是我国四大发明之一指南针的发源地。据《古矿录》记载:《明史地理志》称:
“磁州武安县西南有磁山,产磁铁石。”文中的磁铁石的主要化学成分应该是(
)
A.Fe O B.FeO
2 3
C.Fe O D.Fe(OH)
3 4 3
答案 C
解析 根据题干信息可知磁铁石应具有磁性,Fe O 、FeO、Fe(OH) 都不具有
2 3 3
磁性,Fe O 俗称磁铁,具有磁性,所以磁铁矿的主要成分主要为Fe O ,故答案为
3 4 3 4
C。
2.(2020·陕西高三联考)《本草纲目》中的“石碱”条目下写道:“采蒿蓼之
属……晒干烧灰,以原水淋汁……久则凝淀如石……浣衣发面,甚获利也。”下
列说法中错误的是( )
A.“石碱”的主要成分易溶于水
B.“石碱”俗称烧碱
C.“石碱”可用作洗涤剂
D.“久则凝淀如石”的操作为结晶
答案 B
解析 由“以原水淋汁”可以看出,“石碱”的主要成分易溶于水,故A正
确; “采蒿蓼之属……晒干烧灰”,草木灰的成分是碳酸钾,故B错误;碳酸钾溶
液呈碱性,可用作洗涤剂,故C正确; “以原水淋汁……久则凝淀如石”是从碳
酸钾溶液中得到碳酸钾晶体,操作为蒸发结晶,故D正确。
3.(2020·重庆市二诊)中华文化源远流长、博大精深。下列有关蕴含的化学知
识的说法中,不正确的是( )
A.《周礼》中记载沿海古人“煤饼烧蛎房成灰”,“灰”的主要成分是CaO
B.刘禹锡《浪淘沙》诗句“千淘万漉虽辛苦,吹尽黄沙始到金。”“淘”、
“漉”相当于分离提纯操作中的“过滤”
C.《天工开物》有言“世间丝、麻、裘、褐皆具素质”,“丝、麻”的主要成分都
是蛋白质D.《本草经集注》记载“以火烧之,紫青烟起,云是真硝石(硝酸钾)也”,钾的
焰色试验为紫色
答案 C
解析 “煤饼烧蛎房成灰”,“蛎房”为牡蛎壳,即贝壳,贝壳的主要成分为
碳酸钙,CaCO 灼烧生成CaO和CO ,所以“灰”的主要成分是CaO,A选项正
3 2
确; “千淘万漉虽辛苦,吹尽黄沙始到金”指淘金要经过千遍万遍的过滤,只有
淘尽了泥沙才能得到黄金,所以其中的“淘”“漉”相当于分离提纯操作中的
“过滤”,B选项正确; “麻”的主要成分为纤维素,“丝”的主要成分为蛋白质,
C选项错误;硝石为硝酸钾,含有钾元素,钾的焰色试验颜色为紫色,灼烧产生紫
色火焰,D选项正确。
4.(2020·陕西渭南市富平县第一次摸底考试)“爆竹声中一岁除,春风送暖入
屠苏。千门万户曈曈日,总把新桃换旧符。 ”是王安石的作品《元日》,其中的
“屠苏”是一种酒。下列说法错误的是( )
A.黑火药是由硫黄、硝石和木炭按照一定比例混合而成
B.“屠苏”中不含非电解质
C.爆竹爆炸发生了化学变化
D.早期的桃符大都是木质的,其主要成分纤维素可以发生水解反应
答案 B
解析 黑火药是由硫黄、硝石和木炭按照一定比例混合而成,故 A正确;
“屠苏”是药酒,含有酒精,酒精是非电解质,故B错误;爆竹爆炸生成新物质,
发生了化学变化,故C正确;早期的桃符大都是木质的,含有纤维素,纤维素是多
糖,在一定条件下能发生水解,故D正确。
5.(2020·福建南平市高三质检)2020年春节期间举行的《中国诗词大会》第五
季精彩纷呈,体现了中国诗词博大精深,下列诗词分析错误的是( )
A.“弄风柳絮疑成雪,满地榆钱买得春”中的“柳絮”和棉花的成分均含
纤维素
B.“日暮汉宫传蜡烛,轻烟散入五侯家”中的“蜡烛”是高级脂肪酸酯,也
是高分子化合物
C.“炎炎日正午,灼灼火俱燃”中的“炎炎”体现自然界中太阳能与热能的
转化
D.“煮豆持作羹,漉鼓以为汁”中的“漉鼓”涉及的基本操作是过滤
答案 B解析 “柳絮”和棉花的主要成分均为纤维素,A正确;高级脂肪酸酯不属
于高分子化合物,B错误;“炎炎”体现了太阳能转化为热能,C正确;由“漉鼓
以为汁”可知,“漉鼓”涉及过滤,D正确。
1.(2020·7月浙江选考,6)下列说法不正确的是( )
A.天然气是不可再生能源
B.用水煤气可合成液态碳氢化合物和含氧有机物
C.煤的液化属于物理变化
D.火棉是含氮量高的硝化纤维
答案 C
解析 煤、石油、天然气是不可再生能源,A项正确;水煤气的主要成分是CO
和H ,用水煤气可以合成甲醇等含氧有机物,B项正确;煤的液化是在一定条件
2
下将固体煤炭转化为液体燃料的过程,煤的液化属于化学变化,C项错误;火棉
是含氮量高的硝化纤维,D项正确。
2.(2020·浙江1月选考,3)下列属于有机物,又是电解质的是( )
A.己烷 B.乙酸
C.葡萄糖 D.纯碱
答案 B
解析 有机物通常指含有碳元素的化合物,或碳氢化合物及其衍生物的总称
(二氧化碳、碳酸、碳酸盐、金属碳化物、碳酸氢盐除外)。电解质是在水溶液中或熔
融状态下都能导电的化合物。己烷、乙酸、葡萄糖属于有机物,而纯碱即碳酸钠属
于无机物,不符合题意,故D项错误;己烷和葡萄糖在水溶液中或熔融状态下都
不能导电,属于非电解质,故A项和C项错误。乙酸在水溶液能导电,为电解质,
故B项正确。答案选B。
3.(2020·课标全国Ⅰ)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙
醚、75%乙醇、含氯消毒剂、过氧乙酸(CH COOOH)、氯仿等均可有效灭活病毒。
3
对于上述化学药品,下列说法错误的是( )
A.CH CH OH能与水互溶
3 2
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
答案 D解析 乙醇易溶于水,能与水以任意比例互溶,A项正确;次氯酸钠具有强氧
化性,能通过氧化灭活病毒,B项正确;由过氧乙酸的结构简式(CH COOOH)可知
3
其相对分子质量为76,C项正确;氯仿的化学式为CHCl ,化学名称是三氯甲烷,
3
D项错误。
4.(2020·课标全国Ⅲ)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千
年色彩依然,其中绿色来自孔雀石颜料[主要成分为Cu(OH) ·CuCO ],青色来自
2 3
蓝铜矿颜料[主要成分为Cu(OH) ·2CuCO ]。下列说法错误的是( )
2 3
A.保存《千里江山图》需控制温度和湿度
B.孔雀石、蓝铜矿颜料不易被空气氧化
C.孔雀石、蓝铜矿颜料耐酸耐碱
D.Cu(OH) ·CuCO 中铜的质量分数高于Cu(OH) ·2CuCO
2 3 2 3
答案 C
解析 Cu(OH) 和CuCO 在高温时均易分解,在潮湿的空气中会有微量溶解,
2 3
因此保存《千里江山图》需控制温度和湿度,A项正确;孔雀石和蓝铜矿颜料中的
Cu元素均为+2价,处于Cu元素的最高价态,因此孔雀石、蓝铜矿颜料不易被空
气氧化,B项正确;Cu(OH) 和CuCO 均能与强酸发生反应,C项错误;Cu(OH) 中
2 3 2
Cu的质量分数为65.3%,CuCO 中Cu的质量分数为51.6%,因此Cu(OH) ·CuCO
3 2 3
中铜的质量分数高于Cu(OH) ·2CuCO 中铜的质量分数,D项正确。
2 3
5.(2019·课标全国Ⅱ)“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商
隐的著名诗句,下列关于该诗句中所涉及物质的说法错误的是( )
A.蚕丝的主要成分是蛋白质
B.蚕丝属于天然高分子材料
C.“蜡炬成灰”过程中发生了氧化反应
D.古代的蜡是高级脂肪酸酯,属于高分子聚合物
答案 D
解析 蚕丝的主要成分是蛋白质,A项正确;蚕丝属于天然高分子化合物,B
项正确;“蜡炬成灰”是指蜡烛燃烧,这属于氧化反应,C项正确。在古代蜡烛通
常由动物油脂制成,动物油脂的主要成分为高级脂肪酸酯,其不属于高分子聚合
物,D项错误。
6.(2019·天津理综)化学在人类社会发展中发挥着重要作用,下列事实不涉
及化学反应的是( )
A.利用废弃的秸秆生产生物质燃料乙醇B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物
D.利用反渗透膜从海水中分离出淡水
答案 D
解析 利用废弃的秸秆生产乙醇的过程中,秸秆中的纤维素水解生成葡萄糖
葡萄糖再转化成乙醇,A项不符合题意;利用石油生产塑料、化纤等高分子材料
的过程中,发生加聚反应或缩聚反应,B项不符合题意;利用基本的化学原料生
产化学合成药物的过程中,发生了化学反应,C项不符合题意;利用反渗透膜从
海水中分离出淡水,属于物理变化,D项符合题意。
7.(2019·浙江4月选考)下列属于碱的是( )
A.C H OH B.Na CO
2 5 2 3
C.Ca(OH) D.Cu (OH) CO
2 2 2 3
答案 C
解析 C H OH属于醇,Na CO 属于盐,Ca(OH) 属于碱,Cu (OH) CO 属于碱
2 5 2 3 2 2 2 3
式盐,故选C。
8.(2019·海南卷)我国古代典籍中有“石胆……浅碧色,烧之变白色者真”的
记载,其中石胆是指( )
A.CuSO ·5H O B.FeSO ·7H O
4 2 4 2
C.ZnSO ·7H O D.KAl(SO ) ·12H O
4 2 4 2 2
答案 A
解析 ZnSO ·7H O俗名皓矾,是白色固体、KAl(SO ) ·12H O俗名明矾,是白
4 2 4 2 2
色固体,与“石胆……浅碧色“不相符,可排除C、D选项;FeSO ·7H O俗名绿矾
4 2
是绿色固体,在空气中加热失去结晶水得到绛红色粉末Fe (SO ) ,与”烧之变白
2 4 3
色“不相符,可排除B选项;CuSO ·5H O俗名蓝矾或胆矾,是蓝色固体,在空气
4 2
中加热失去结晶水得到白色粉末CuSO ,与“石胆……浅碧色,烧之变白色”相
4
符合,故A正确。
一、选择题(每小题只有一个选项符合题意)
1.(2020·7月浙江选考,4)下列物质对应的组成不正确的是( )
A.干冰:CO B.熟石灰:CaSO ·2H O
2 4 2
C.胆矾:CuSO ·5H O D.小苏打:NaHCO
4 2 3
答案 B解析 干冰的组成为CO ,A项正确;熟石灰的组成为Ca(OH) ,B项错误;胆
2 2
矾的组成为CuSO ·5H O,C项正确;小苏打的组成为NaHCO ,D项正确。
4 2 3
2.(2020·贵阳摸底考试)下列物质与类别不对应的是( )
A B C D
物质 小苏打 食用油 淀粉 “84”消毒液
类别 碱 油脂(酯类) 天然高分子化合物 混合物
答案 A
解析 小苏打是NaHCO ,属于盐,物质与类别不对应,A项符合题意;食用
3
油是油脂,油脂属于酯类,物质与类别对应,B项不符合题意;淀粉是天然高分子
化合物,物质与类别对应,C项不符合题意;“84”消毒液的有效成分是次氯酸钠,
属于混合物,物质与类别对应,D项不符合题意。
3.下列变化中,前者是物理变化,后者是化学变化,且都有明显颜色变化的
是( )
A.打开盛装NO的集气瓶;冷却NO 气体
2
B.用冰水混合物冷却SO 气体;加热氯化铵晶体
3
C.木炭吸附NO 气体;将氯气通入品红溶液中
2
D.向品红溶液中加入Na O ;向FeCl 溶液中滴加KSCN溶液
2 2 3
答案 C
解析 A项,前者发生化学反应:2NO+O ===2NO ;B项,冷却SO 气体没有
2 2 3
颜色变化,加热氯化铵晶体分解产生HCl和NH ,发生的是化学变化,没有明显
3
颜色变化;D项,前者为Na O 的氧化性漂白为化学变化。
2 2
4.(2020·河北衡水中学高三联考)下列厨房中的常见物质溶于相应溶剂后,
不能形成胶体的是( )
A.淀粉溶于水中 B.鸡蛋清溶于水中
C.豆浆加入水中 D.食醋溶于水中
答案 D
解析 A项淀粉溶液为胶体;B、C项均为蛋白质溶液,都是胶体;D项食醋溶
于水中形成溶液,不是胶体,选D。
5.(2021·安徽合肥市高三调研检测)化学与人类生活、生产密切相关。下列说
法正确的是( )
A.84消毒液和医用酒精均可用来消毒,两者混合效力更强
B.丝绸的主要成分是纤维素,在酸性条件下可以水解C.从石墨中剥离出的石墨烯薄片能导电,故石墨烯是电解质
D.中国天眼FAST用到的碳化硅是一种新型无机非金属材料
答案 D
解析 84消毒液的有效成分为NaClO,具有强氧化性,和医用酒精混合使用
时C H OH和NaClO会发生氧化还原反应,降低消毒效果,A项错误;丝绸的主
2 5
要成分为蛋白质,B项错误;石墨烯为单质,不是电解质,C项错误;碳化硅的熔
点高、硬度大,是一种新型无机非金属材料,D项正确。
6.(2020·陕西渭南市富平县第一次摸底考试)分类法是研究化学的一种重要
方法,下列乙中的物质与甲的分类关系匹配的是( )
选项 甲 乙
A 干燥剂 浓硫酸、石灰石、无水氯化钙
B 混合物 空气、石油、干冰
C 空气质量检测物质 氮氧化物、二氧化硫、PM2.5
D 酸性氧化物 三氧化硫、一氧化碳、二氧化硅
答案 C
解析 石灰石是碳酸钙,不具有吸水性,故不能做干燥剂,故A错误;干冰是
固体二氧化碳,属于纯净物,故B错误;氮氧化物能导致光化学烟雾、二氧化硫能
导致酸雨、PM2.5能导致雾霾,故氮氧化物、二氧化硫、PM2.5均能导致空气污染,
均是空气质量检测物质,故C正确;CO不是酸性氧化物,故D错误。
7.(2020·海南海口市一中高三三模)以下关于胶体的说法不正确的是( )
A.胶体粒子能透过滤纸,但不能透过半透膜
B.Fe(OH) 胶体粒子具有较大的表面积,具有吸附性,能吸附阳离子,故在电
3
场作用下会产生电泳现象
C.向Fe(OH) 胶体中逐滴滴入稀硫酸,会先出现红褐色沉淀然后沉淀消失
3
D.Fe(OH) 胶体无色透明,能产生丁达尔效应
3
答案 D
解析 胶体粒子的大小介于滤纸和半透膜的孔径之间,能透过滤纸,但不能
透过半透膜,A项正确;Fe(OH) 胶体粒子具有较大的表面积,具有吸附性,能吸
3
附阳离子,故在电场作用下会定向移动产生电泳现象,B项正确;向Fe(OH) 胶体
3
中逐滴滴入稀硫酸,会先聚沉,岀现红褐色沉淀,然后沉淀被硫酸溶解而消失,C
项正确;Fe(OH) 胶体呈红褐色,D项错误。
3
8.(2020·山东烟台质检)某学习兴趣小组讨论辨析以下说法,其中说法正确的是( )
①通过化学变化可以实现16O与18O间的相互转化 ②煤的气化与液化都是
物理变化 ③碱性氧化物一定是金属氧化物 ④只由一种元素组成的物质一
定为纯净物
⑤石墨和C 是同素异形体 ⑥糖类、蛋白质、油脂属于天然高分子化合物
60
A.③⑤⑥ B.①②
C.③⑤ D.①③④
答案 C
解析 ①同位素之间的转化不是化学变化,错误;②煤的气化与液化都是化
学变化,错误;④只由一种元素组成的物质不一定为纯净物,例如氧气和臭氧的
混合物等,错误;⑥糖类中的单糖和二糖、油脂等均不是高分子化合物,错误,答
案选C。
9.化学与人类的生活、生产密切相关,下列说法中正确的是( )
A.蚕丝和棉花的组成元素相同,结构不同,因而性质不同
B.埃博拉病毒可用乙醇、次氯酸钠溶液、双氧水消毒,其消毒原理相同
C.纯碱属于碱类,谷氨酸钠(C H NO Na,味精)属于盐类
5 8 4
D.压缩天然气(CNG)、液化石油气(LPG)的主要成分是烃类,是城市推广的
清洁燃料
答案 D
解析 A项,蚕丝的主要成分为蛋白质,棉花的主要成分为纤维素;B项,乙
醇不具有氧化性;C项,纯碱属于盐;D项,天然气的主要成分为甲烷,液化石油
气的主要成分有丙烷、丙烯、丁烷和丁烯等。
10.下列说法不正确的是( )
A.利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液
B.将饱和FeCl 溶液滴入沸水中,继续煮沸至溶液呈红褐色即生成氢氧化铁
3
胶体
C.用过滤法可以除去Fe(OH) 胶体中的FeCl
3 3
D.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
答案 C
解析 胶体微粒能通过滤纸,不能用过滤提纯胶体。
11.以工业副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵[(NH ) S O ]和氧
4 2 2 8
化铁红颜料,其主要流程如下:下列叙述正确的是( )
A.用一束光照射(NH ) S O 溶液,会产生丁达尔效应
4 2 2 8
B.H 、CO 、Fe O 、FeCO 均属于非电解质
2 2 2 3 3
C.NH HCO 是酸式盐,既能与酸反应,又能与碱反应
4 3
D.室温下,FeSO 溶液、NH HCO 溶液的pH均小于7
4 4 3
答案 C
解析 溶液中分散质微粒直径小于10-9 m,不能产生丁达尔效应,A错误;
Fe O 、FeCO 属于电解质,H 属于单质,既不是电解质也不是非电解质,B错误;
2 3 3 2
FeSO 属于强酸弱碱盐,水解后溶液均显酸性,NH ·H O电离常数大于H CO 的,
4 3 2 2 3
NH HCO 溶液呈碱性,D错误。
4 3
12.科学家将水置于足够强的电场中,在20 ℃时水分子瞬间凝固可形成
“暖冰”。某兴趣小组做如图所示实验,发现烧杯中酸性KMnO 溶液褪色,且有
4
气泡产生。将酸性KMnO 溶液换成FeCl 溶液,烧杯中溶液颜色无变化,但有气
4 3
泡产生。则下列说法正确的是( )
A.20 ℃时,水凝固形成“暖冰”所发生的变化是化学变化
B.“暖冰”是水置于足够强的电场中形成的混合物
C.烧杯中液体为FeCl 溶液时,产生的气体为Cl
3 2
D.该条件下H 燃烧的产物中可能含有一定量的H O
2 2 2
答案 D
解析 水凝固形成“暖冰”的过程中只有水的状态发生了变化,没有生成新
物质,故所发生的变化是物理变化,A项错误;“暖冰”是在20 ℃时水分子瞬间
凝固的产物,B项错误;酸性KMnO 溶液褪色,说明H 燃烧生成了具有还原性的
4 2
物质,该物质被氧化产生气体,故有气泡产生,结合元素守恒,推测该物质为
H O ,H O 在Fe3+的作用下分解产生O ,故将酸性KMnO 溶液换成FeCl 溶液,
2 2 2 2 2 4 3溶液颜色不变化,但有气泡产生,C项错误,D项正确。
二、非选择题(本题包括3小题)
13.零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是
CaO。
(1)CaO属于________(填字母,下同)。
A.酸 B.碱
C.盐 D.纯净物 E.化合物 F.金属氧
化物 G.非金属氧化物 H.碱性氧化物 I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、CaO等物质划分为一类。该同学的分类依据
为________。
A.酸 B.碱
C.氧化物 D.干燥剂
(3)CaO可作干燥剂的理由是_________________________________(用化学
方程式表示)。
(4)CaO还可以跟哪些类别的物质发生化学反应?请列举两例并填表。
物质类别 化学方程式
(5)小纸袋中的物质能否长期持续地作干燥剂?________。
答案 (1)DEFH (2)D
(3)CaO+H O===Ca(OH)
2 2
(4)酸 CaO+2HCl===CaCl +H O 酸性氧化物 CaO+SO ===CaSO
2 2 2 3
(5)不能
解析 (1)CaO 属于纯净物、化合物、金属氧化物、碱性氧化物,答案为
DEFH。
(2)浓硫酸、NaOH固体、CaO都可作干燥剂。
(3)CaO 与 水 反 应 生 成 氢 氧 化 钙 , 反 应 的 化 学 方 程 式 为 CaO +
H O===Ca(OH) ,可作干燥剂。
2 2
(4)CaO属于碱性氧化物能与水反应生成碱;能与酸反应生成盐和水;能与酸
性氧化物反应生成盐。
(5)当CaO与H O反应完全后,不再具有干燥作用。
2
14.铜器久置于空气中会和空气中的水蒸气、CO 、O 作用产生“绿锈”,该
2 2“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu (OH) CO ],“铜绿”能跟
2 2 3
酸反应生成铜盐、CO 和 H O。某同学利用下述系列反应实现了“铜→铜绿
2 2
→……→铜”的转化。
铜――→铜绿――→A――→Cu(OH) ――→B――→Cu
2
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:
_____________________________________________________________。
(3)写出④、⑤的化学方程式:
④______________________________________________________;
⑤______________________________________________________。
(4)上述转化过程中属于化合反应的是________(填序号,下同),属于复分解
反应的是________,属于分解反应的是________。
答案 (1)盐、铜盐、碱式盐(或碳酸盐)
(2)Cu (OH) CO +4HCl===2CuCl +3H O+CO ↑
2 2 3 2 2 2
(3)Cu(OH) =====CuO+H O
2 2
CuO+H =====Cu+H O
2 2
(4)① ②③ ④
15.某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取
少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的
FeCl 溶液。继续煮沸至液体呈透明的红褐色。反应原理为 FeCl +
3 3
3H O=====Fe(OH) (胶体)+3HCl。
2 3
(1)判断胶体的制备是否成功,可利用胶体的______________________。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观
察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果
没有观察到______________________________________________________,
其原因是____________________________________________________。
② 乙 同 学 在 实 验 中 没 有 使 用 蒸 馏 水 , 而 是 用 自 来 水 , 结 果 会
_______________________________________________________________,
原因是_____________________________________________________。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会
____________________________________________________________,
原因是_____________________________________________________。(3)丁同学按要求制备了Fe(OH) 胶体,但是他又向Fe(OH) 胶体中逐滴加入
3 3
了稀H SO 溶液,结果出现了一系列变化。
2 4
①先出现红褐色沉淀,原因是__________________________________。
②随后沉淀溶解,此反应的离子方程式是_________________________。
答案 (1)丁达尔效应
(2)①红褐色液体 FeCl 溶液浓度太小,生成的Fe(OH) 太少 ②生成红褐
3 3
色沉淀 自来水中含有电解质,胶体发生聚沉 ③生成红褐色沉淀 长时间加热
使胶体发生聚沉
(3)①电解质H SO 使Fe(OH) 胶体聚沉而产生沉淀
2 4 3
②Fe(OH) +3H+===Fe3++3H O
3 2
解析 (2)①若用稀FeCl 溶液,则水解产生的Fe(OH) 的量太少,看不到红褐
3 3
色液体;②自来水中含有较多的电解质,使胶体发生聚沉;③长时间加热使胶体
发生聚沉。(3)加入稀H SO 后,Fe(OH) 胶体会发生聚沉而产生红褐色沉淀,随后
2 4 3
H SO 会与Fe(OH) 发生中和反应,使沉淀溶解。
2 4 3