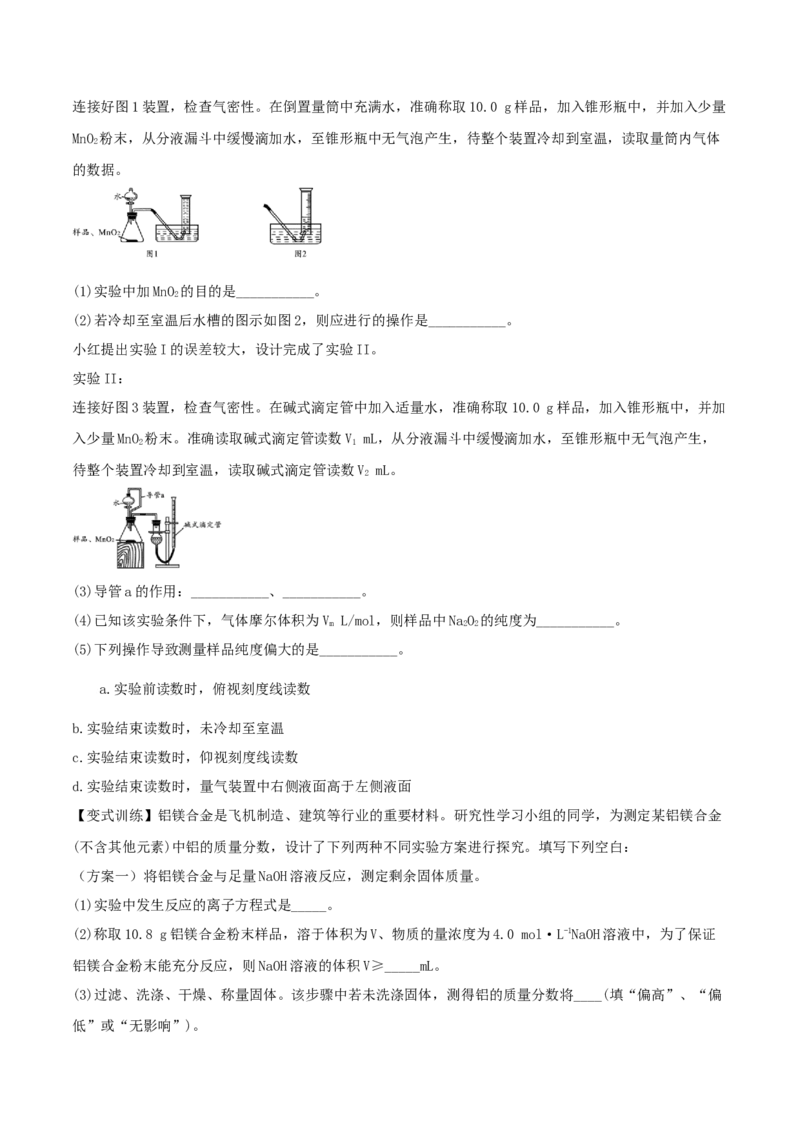文档内容
第 1 讲 物质的量 气体摩尔体积(精讲)
【考情分析】
本讲为高考命题热点,分值6分,题型以选择题为主,试题以物质的组成和结构、弱电解质电离、可
逆反应、氧化还原反应为载体,综合考查基本概念、基本理论、化学计算。可能会从考查气体摩尔体积的
使用条件、物质结构、弱电解质电离、可逆反应、氧化还原反应中电子转移等相关内容命题,解题时注意
题设中的陷阱,构建好解题模型。
【核心素养分析】
1.宏观辨识与微观探析:认识物质的量是联系宏观物质和微观粒子的重要工具,能从宏观和微观相结合的
视角分析与解决实际问题。
2.证据推理与模型认知:在有关物质的最计算过程中,通过分析、推理等理解计算的方法,建立阿伏加德
罗常数、气体摩尔体积等题目解答的模型。
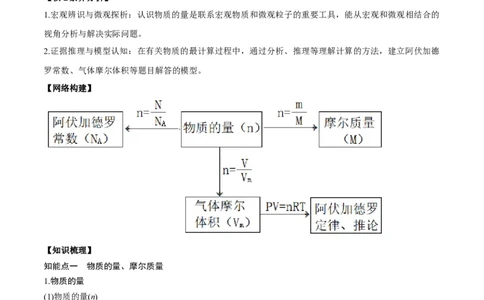
【网络构建】
【知识梳理】
知能点一 物质的量、摩尔质量
1.物质的量
(1)物质的量(n)
表示含有一定数目粒子的集合体的物理量,单位为摩尔(mol)。
(2)物质的量的规范表示方法:
(3)阿伏加德罗常数(N )
A
0.012 kg 12C中所含的碳原子数为阿伏加德罗常数,其数值约为6.02×1023,单位为mol-1。公式:N =。
A
【易错提醒】(1)物质的量只能衡量微观粒子,必须指明具体粒子的种类或化学式,故摩尔后面应为确切的
微粒名称;如1 mol氢(不确切)和1 mol大米(宏观物质)皆为错误说法。(2)物质的量是物理量,摩尔是物质的量的单位,不是物理量。
(3)6.02×1023是个纯数值,没有任何物理意义,而阿伏加德罗常数(N )是指1 mol任何微粒所含的粒子数,
A
它与0.012 kg12C所含的碳原子数相同,数值约为6.02×1023。
2.摩尔质量
(1)单位物质的量的物质所具有的质量。常用的单位是 g·mol-1。公式:M=。
(2)数值:以 g·mol-1为单位时,任何粒子的摩尔质量在数值上都等于该粒子的相对分子(原子)质量。
【易错提醒】(1)物质的量是计量微观粒子“集体”的物理量,只适用于微观粒子(即分子、原子、离子、
质子、中子、电子等),不适用于宏观物质。
(2)摩尔质量、相对原子(或分子)质量的含义不同,不是同一个物理量。二者单位也不同,摩尔质量的单
位是g·mol-1或kg·mol-1,相对原子(或分子)质量的单位为1,当摩尔质量以g·mol-1为单位时,二者
在数值上相等。
(3)对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态而变化。
知能点二 气体摩尔体积 阿伏加德罗定律
1.影响物质体积大小的因素
①粒子的大小(物质的本性);②粒子间距的大小(由温度与压强共同决定);③粒子的数目(物质的量的大小)。
2.气体摩尔体积
(1)含义:单位物质的量的气体所占的体积,符号为V ,标准状况下,V 约为 22.4_L·mol-1。
m m
(2)常用单位:L/mol(或L·mol-1)。
(3)数值:在标准状况下(指温度为0℃,压强为101 kPa)约为22.4 L·mol-1。
(4)基本关系式:n===
(5)影响因素:气体摩尔体积的数值不是固定不变的,它决定于气体所处的温度和压强。
【特别提醒】气体摩尔体积(22.4 L·mol-1)应用的“五大误区”
(1)使用“条件”是标准状况,即0 ℃、101 kPa,而不是常温、常压。
(2)使用对象必须是气体物质,可以是单一气体,也可以是混合气体。标准状况下不是气体而又常在题中出
现的物质有:水、苯、SO 、HF、CCl 、己烷、CS、CHCl 、Br 、乙醇等。
3 4 2 3 2
(3)标准状况下的气体摩尔体积约为22.4 L·mol-1,其他条件下V 一般不是22.4 L·mol-1。
m
(4)22.4 L气体,在标准状况下的物质的量是1 mol,在非标准状况下,可能是1 mol,也可能不是1 mol。
(5)物质的质量、物质的量一定时,所含微粒数与物质处于何种条件无关。如常温常压下32 g O 所含的原
2
子数目是2N 。注意不要形成定势思维,看到“常温常压”就排除选项。
A
3.阿伏加德罗定律及其推论
(1)阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体,含有相同数目的粒子(或气体的物质
的量相同)。
注:可总结为:“三同”定“一同”,即同温、同压下,同体积的任何气体具有相同的分子数。
(2)阿伏加德罗定律的推论(以下用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质量,V为体积,T为热力学温度)
条件 推论公式 语言叙述
T、p相同 = 同温、同压下,气体的体积与其物质的量成正比
T、V相同 = 温度、体积相同的气体,其压强与其物质的量成正比
T、p相同 = 同温、同压下,气体的密度与其摩尔质量(或相对分子质量)成正比
T、p、m相
= 同温同压下,相同质量的任何气体的体积与它们的摩尔质量成反比
同
T、V、m相
= 同温同体积时,相同质量的任何气体的压强与它们的摩尔质量成反比
同
T、p、V相 同温同压下,同体积的任何气体的质量比等于它们的摩尔质量之比,
==
同 也等于它们的密度之比
【方法技巧】
1、记忆方法:三正比、二反比、一连比。
2、应用阿伏加德罗定律推论时可通过pV=nRT及n=、ρ=导出。
【典例剖析】
高频考点一 物质的量 摩尔质量
例1、(2018·全国卷Ⅲ)下列叙述正确的是( )
A.24 g镁与27 g铝含有相同的质子数
B.等质量的氧气和臭氧,电子数相同
C.1 mol重水与1 mol水中,中子数比为2∶1
D.1 mol乙烷和1 mol乙烯,化学键数目相同
【变式训练】下列有关叙述正确的是()
A.1 mol任何物质都含有6.02×1023个分子
B.硫酸的摩尔质量为98 g
C.2 mol H O是1 mol H O摩尔质量的2倍
2 2
D.摩尔是物质的量的单位
高频考点二 气体摩尔质量及相对分子质量的计算
例2、按要求解答问题
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为_______,可能是_______
气体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为_______。
(3)CO和CO 的混合气体18 g,完全燃烧后测得CO 体积为11.2 L(标准状况),则
2 2
①混合气体在标准状况下的密度是_______g·L-1。②混合气体的平均摩尔质量是_______ g·mol-1。
【变式训练】同温同压下,相同体积的两种气体A、B的质量比为22:17,若A气体为CO,则B气体可能
2
是
A.NH B.HS C.SO D.O
3 2 2 2
高频考点三 有关气体分压的计算
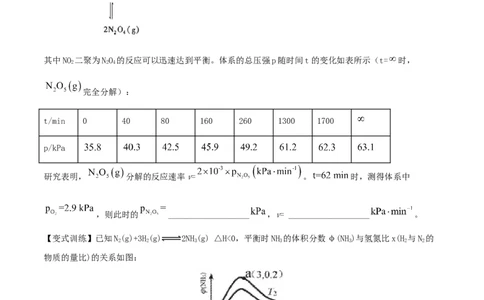
例3.F.Daniels等曾利用测压法在刚性反应器中研究了 时 分解反应:
其中NO 二聚为NO 的反应可以迅速达到平衡。体系的总压强p随时间t的变化如表所示(t= 时,
2 2 4
完全分解):
t/min 0 40 80 160 260 1300 1700
p/kPa
研究表明, 分解的反应速率v= 。 时,测得体系中
,则此时的 ___________________ ,v= ___________________ 。
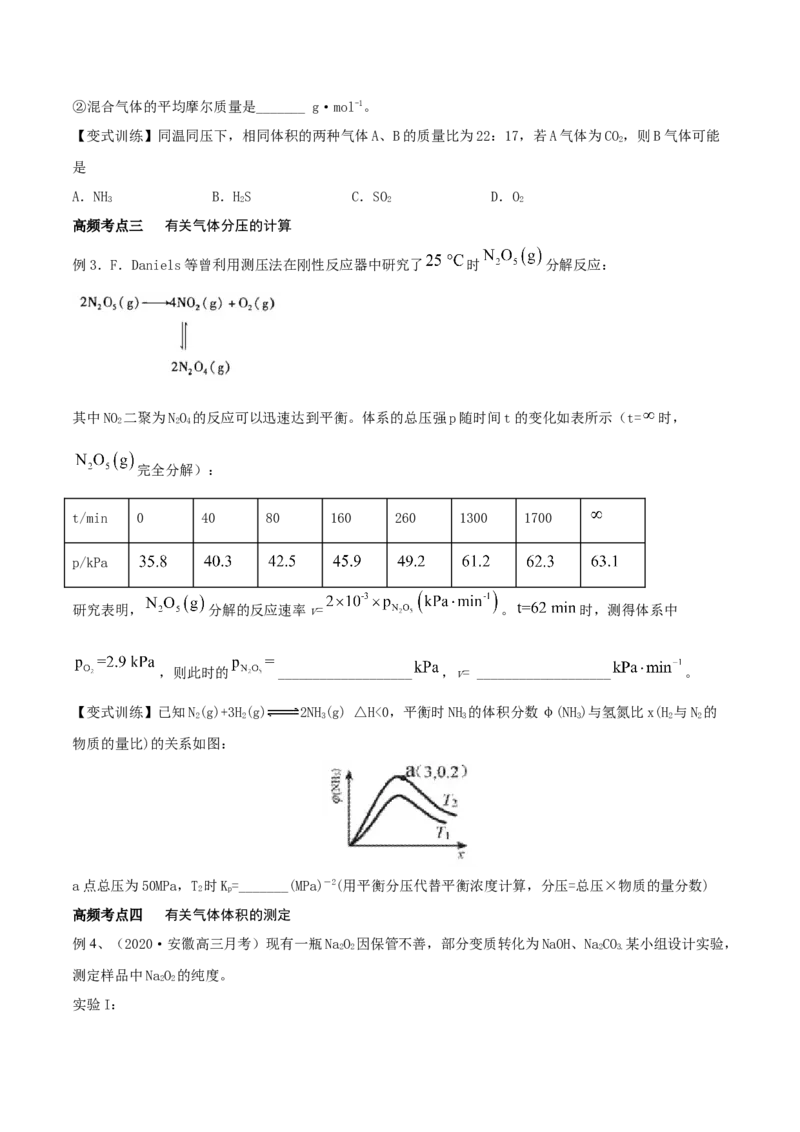
【变式训练】已知N(g)+3H(g) 2NH(g) △H<0,平衡时NH 的体积分数φ(NH)与氢氮比x(H 与N 的
2 2 3 3 3 2 2
物质的量比)的关系如图:
a点总压为50MPa,T 时K=_______(MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
2 p
高频考点四 有关气体体积的测定
例4、(2020·安徽高三月考)现有一瓶NaO 因保管不善,部分变质转化为NaOH、NaCO 某小组设计实验,
2 2 2 3.
测定样品中NaO 的纯度。
2 2
实验I:连接好图1装置,检查气密性。在倒置量筒中充满水,准确称取10.0 g样品,加入锥形瓶中,并加入少量
MnO 粉末,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,待整个装置冷却到室温,读取量筒内气体
2
的数据。
(1)实验中加MnO 的目的是___________。
2
(2)若冷却至室温后水槽的图示如图2,则应进行的操作是___________。
小红提出实验I的误差较大,设计完成了实验II。
实验II:
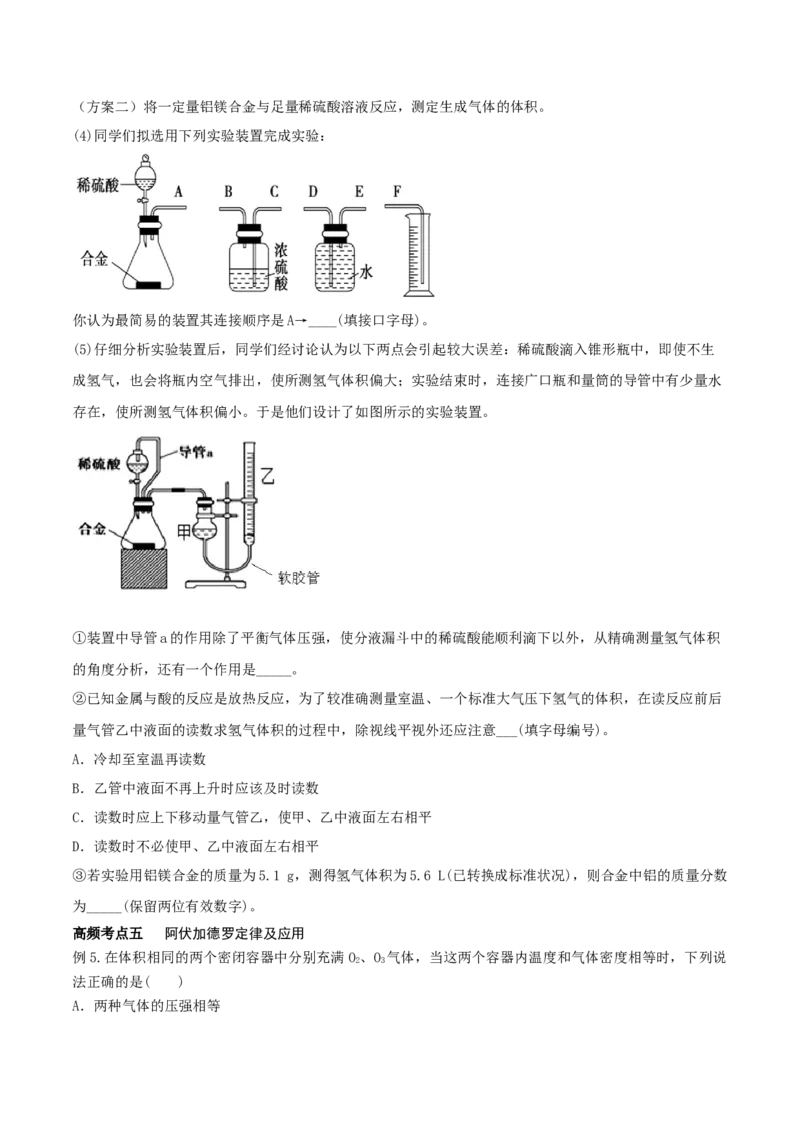
连接好图3装置,检查气密性。在碱式滴定管中加入适量水,准确称取10.0 g样品,加入锥形瓶中,并加
入少量MnO 粉末。准确读取碱式滴定管读数V mL,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,
2 1
待整个装置冷却到室温,读取碱式滴定管读数V mL。
2
(3)导管a的作用:___________、___________。
(4)已知该实验条件下,气体摩尔体积为V L/mol,则样品中NaO 的纯度为___________。
m 2 2
(5)下列操作导致测量样品纯度偏大的是___________。
a.实验前读数时,俯视刻度线读数
b.实验结束读数时,未冷却至室温
c.实验结束读数时,仰视刻度线读数
d.实验结束读数时,量气装置中右侧液面高于左侧液面
【变式训练】铝镁合金是飞机制造、建筑等行业的重要材料。研究性学习小组的同学,为测定某铝镁合金
(不含其他元素)中铝的质量分数,设计了下列两种不同实验方案进行探究。填写下列空白:
(方案一)将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
(1)实验中发生反应的离子方程式是_____。
(2)称取10.8 g铝镁合金粉末样品,溶于体积为V、物质的量浓度为4.0 mol·L-1NaOH溶液中,为了保证
铝镁合金粉末能充分反应,则NaOH溶液的体积V≥_____mL。
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得铝的质量分数将____(填“偏高”、“偏
低”或“无影响”)。(方案二)将一定量铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。
(4)同学们拟选用下列实验装置完成实验:
你认为最简易的装置其连接顺序是A→____(填接口字母)。
(5)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生
成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水
存在,使所测氢气体积偏小。于是他们设计了如图所示的实验装置。
①装置中导管a的作用除了平衡气体压强,使分液漏斗中的稀硫酸能顺利滴下以外,从精确测量氢气体积
的角度分析,还有一个作用是_____。
②已知金属与酸的反应是放热反应,为了较准确测量室温、一个标准大气压下氢气的体积,在读反应前后
量气管乙中液面的读数求氢气体积的过程中,除视线平视外还应注意___(填字母编号)。
A.冷却至室温再读数
B.乙管中液面不再上升时应该及时读数
C.读数时应上下移动量气管乙,使甲、乙中液面左右相平
D.读数时不必使甲、乙中液面左右相平
③若实验用铝镁合金的质量为5.1 g,测得氢气体积为5.6 L(已转换成标准状况),则合金中铝的质量分数
为_____(保留两位有效数字)。
高频考点五 阿伏加德罗定律及应用
例5.在体积相同的两个密闭容器中分别充满O 、O 气体,当这两个容器内温度和气体密度相等时,下列说
2 3
法正确的是( )
A.两种气体的压强相等B.O 比O 的质量小
2 3
C.两种气体的分子数目相等
D.两种气体的氧原子数目相等
【变式训练】一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024
个原子组成,下列有关说法中不正确的是( )
A.该温度和压强可能是标准状况
B.标准状况下该纯净物若为气态,其体积约是22.4 L
C.每个该气体分子含有2个原子
D.若O 在该条件下为气态,则1 mol O 在该条件下的体积也为30 L
2 2
高频考点六 有关阿伏加德罗常数的考查
例6.(2019·全国卷Ⅱ,8)已知N是阿伏加德罗常数的值,下列说法错误的是( )
A
A.3 g 3He含有的中子数为1N
A
B.1 L 0.1 mol·L-1磷酸钠溶液含有的 数目为0.1 N
PO3− A
4
C.1 mol KCrO 被还原为Cr3+转移的电子数为6N
2 2 7 A
D.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13N
A
【变式训练】(2021·河北衡水中学一模)N表示阿伏加德罗常数的值。下列说法错误的是( )
A
A.标准状况下,11.2 L正丁烷所含极性键的数目为5N
A
B.常温常压下,1 mol O 中含有的中子数为44N
Na18 2 A
2
C.1 L pH均为2的盐酸和醋酸溶液,氢离子数均为0.01N
A
D.64 g铜与足量硫粉加热充分反应,转移电子数为2N
A