文档内容
专题 9 原子结构、分子结构与性质的基础考查
1.Cu Sn S 属于三元化合物,是一种重要的半导体和非线性光学材料,具有杰出的热学、
a b c
光学和机械等性质,因而备受人们的广泛关注。回答下列问题:
Cu Sn S 中Cu元素有+1和+2两种价态,从结构上分析基态Cu+、Cu2+中________更稳定,
a b c
原因是_____________________________;其中Cu2+可与CN-形成配离子[Cu(CN) ]2-,1
4
mol该配离子中含有σ键的物质的量为______mol。
2.氮元素在地球上含量丰富,氮及其化合物在工农业生产和生活中有着重要作用。
尿素[CO(NH)]的合成揭开了人工合成有机物的序幕。其中各组成元素(氢除外,下同)电负
2 2
性最弱的是________(填元素名称),第一电离能由小到大的顺序为________(填元素符号),
氮原子价层电子的轨道表示式为________。
3.钛被视为继铁、铝之后的第三金属,也有人说“21世纪将是钛的世纪”,钛和钛的化合
物在航天、化工、建筑、医疗中都有着广泛的用途。
回答下列问题:
(1)基态钛原子核外有________种能量不同的电子,其能量最高的电子所在的能级符号为
________________________________________________________________________。
(2)Ti(BH) 是一种储氢材料,可由TiCl 和LiBH 反应制得。
4 3 4 4
①Ti(BH) 中所含元素电负性由小到大的顺序为
4 3
________________________________________________________________________。
②TiCl 与SiCl 互为等电子体,TiCl 的空间结构为_______________________________。
4 4 4
③LiBH 由Li+和BH构成,BH中B原子的杂化类型是________________。
4
④LiBH 存在________________(填字母)。
4
A.离子键 B.共价键
C.金属键 D.配位键
E.氢键
4.蛋白质中含有C、H、O、N、S等元素,食物中的铁主要以三价铁与蛋白质和羧酸结合
成络合物的形式存在。
(1)在蛋白质中涉及的碳、氮、氧元素电负性由小到大的顺序是____________;三价铁离子
的价层电子排布式为______________,从原子结构的理论解释 Fe3+比 Fe2+稳定:
______________。
(2)KSCN是检验Fe3+的试剂之一,SCN-的空间结构为______________,1 mol SCN-中含有
π键的数目为______________。
(3)FeCl 晶体易溶于水、乙醇,受热易气化,而FeF 晶体的熔点高于1 000 ℃,试解释两种
3 3
化合物熔点差异较大的原因:________________________________________________
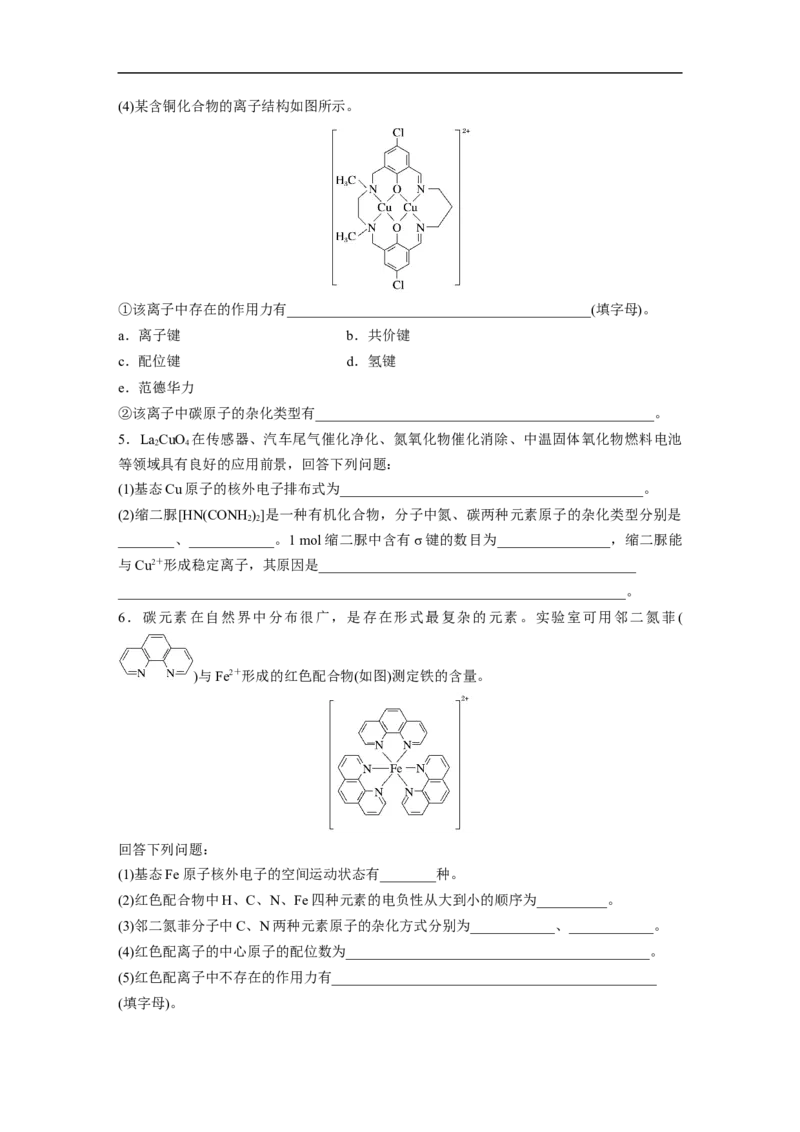
________________________________________________________________________。(4)某含铜化合物的离子结构如图所示。
①该离子中存在的作用力有___________________________________________(填字母)。
a.离子键 b.共价键
c.配位键 d.氢键
e.范德华力
②该离子中碳原子的杂化类型有________________________________________________。
5.LaCuO 在传感器、汽车尾气催化净化、氮氧化物催化消除、中温固体氧化物燃料电池
2 4
等领域具有良好的应用前景,回答下列问题:
(1)基态Cu原子的核外电子排布式为___________________________________________。
(2)缩二脲[HN(CONH )]是一种有机化合物,分子中氮、碳两种元素原子的杂化类型分别是
2 2
________、____________。1 mol缩二脲中含有σ键的数目为________________,缩二脲能
与Cu2+形成稳定离子,其原因是_____________________________________________
________________________________________________________________________。
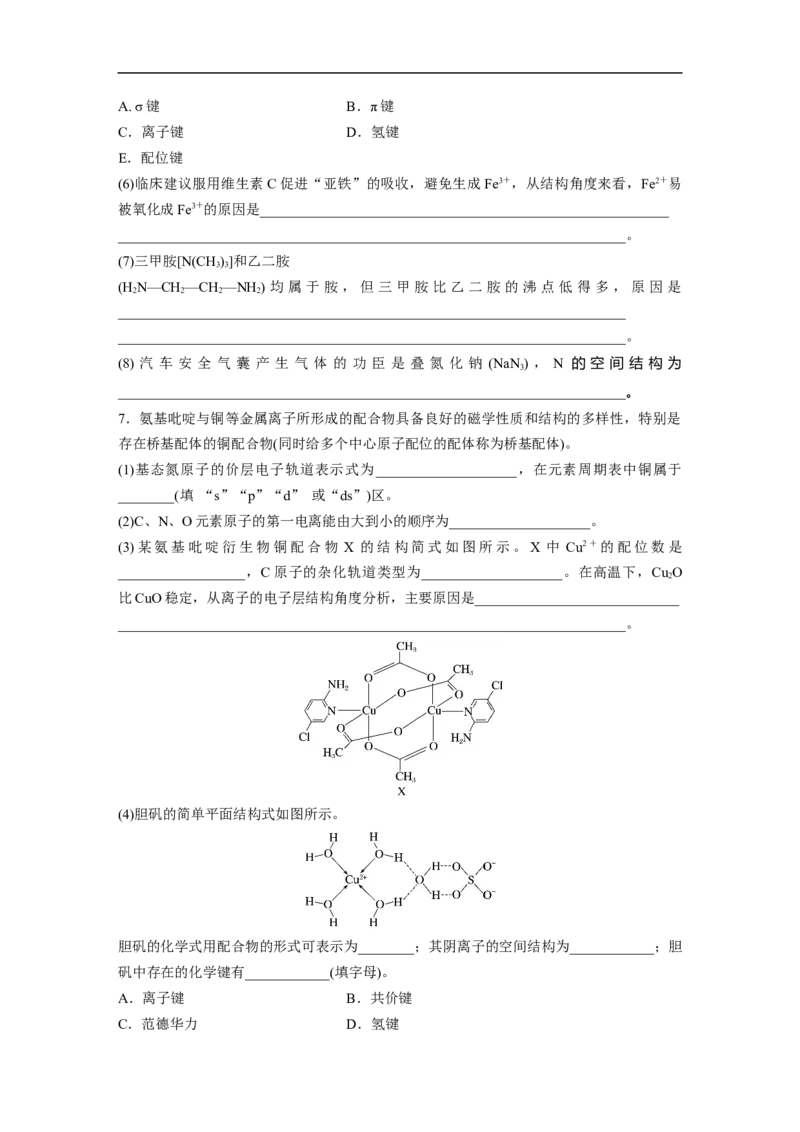
6.碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮菲(
)与Fe2+形成的红色配合物(如图)测定铁的含量。
回答下列问题:
(1)基态Fe原子核外电子的空间运动状态有________种。
(2)红色配合物中H、C、N、Fe四种元素的电负性从大到小的顺序为__________。
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为____________、____________。
(4)红色配离子的中心原子的配位数为___________________________________________。
(5)红色配离子中不存在的作用力有______________________________________________
(填字母)。A. σ键 B.π键
C.离子键 D.氢键
E.配位键
(6)临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易
被氧化成Fe3+的原因是__________________________________________________________
________________________________________________________________________。
(7)三甲胺[N(CH )]和乙二胺
3 3
(H N—CH —CH—NH )均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
2 2 2 2
________________________________________________________________________
________________________________________________________________________。
(8) 汽 车 安 全 气 囊 产 生 气 体 的 功 臣 是 叠 氮 化 钠 (NaN ) , N 的 空 间 结 构 为
3
________________________________________________________________________。
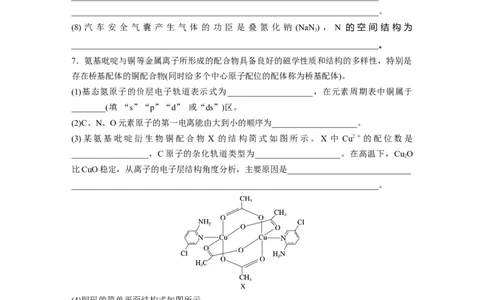
7.氨基吡啶与铜等金属离子所形成的配合物具备良好的磁学性质和结构的多样性,特别是
存在桥基配体的铜配合物(同时给多个中心原子配位的配体称为桥基配体)。
(1)基态氮原子的价层电子轨道表示式为____________________,在元素周期表中铜属于
________(填 “s”“p”“d” 或“ds”)区。
(2)C、N、O元素原子的第一电离能由大到小的顺序为____________________。
(3)某氨基吡啶衍生物铜配合物 X 的结构简式如图所示。X 中 Cu2+的配位数是
__________________,C原子的杂化轨道类型为____________________。在高温下,Cu O
2
比CuO稳定,从离子的电子层结构角度分析,主要原因是_____________________________
________________________________________________________________________。
(4)胆矾的简单平面结构式如图所示。
胆矾的化学式用配合物的形式可表示为________;其阴离子的空间结构为____________;胆
矾中存在的化学键有____________(填字母)。
A.离子键 B.共价键
C.范德华力 D.氢键E.配位键
8.铁、钛、镁等金属及其化合物有广泛用途。回答下列问题:
(1)基态Ti原子的价层电子的轨道表示式是________,基态Fe原子共有________种不同能级
的电子。
(2)某含钛半夹心结构催化剂R能催化乙烯、丙烯等的聚合,其结构如图所示:
①组成 R 的元素中,电负性最大的是__________(填元素符号),氧原子的杂化方式是
________。
②R中含有的化学键有________(填字母)。
A.π键 B.σ键
C.离子键 D.配位键
E.金属键