文档内容
第 20 讲 化学反应速率
第一部分:高考真题感悟
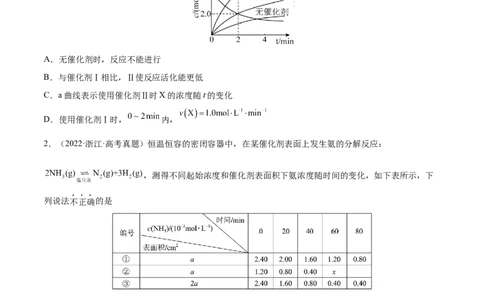
1.(2022·广东·高考真题)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时
间t的部分变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
2.(2022·浙江·高考真题)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
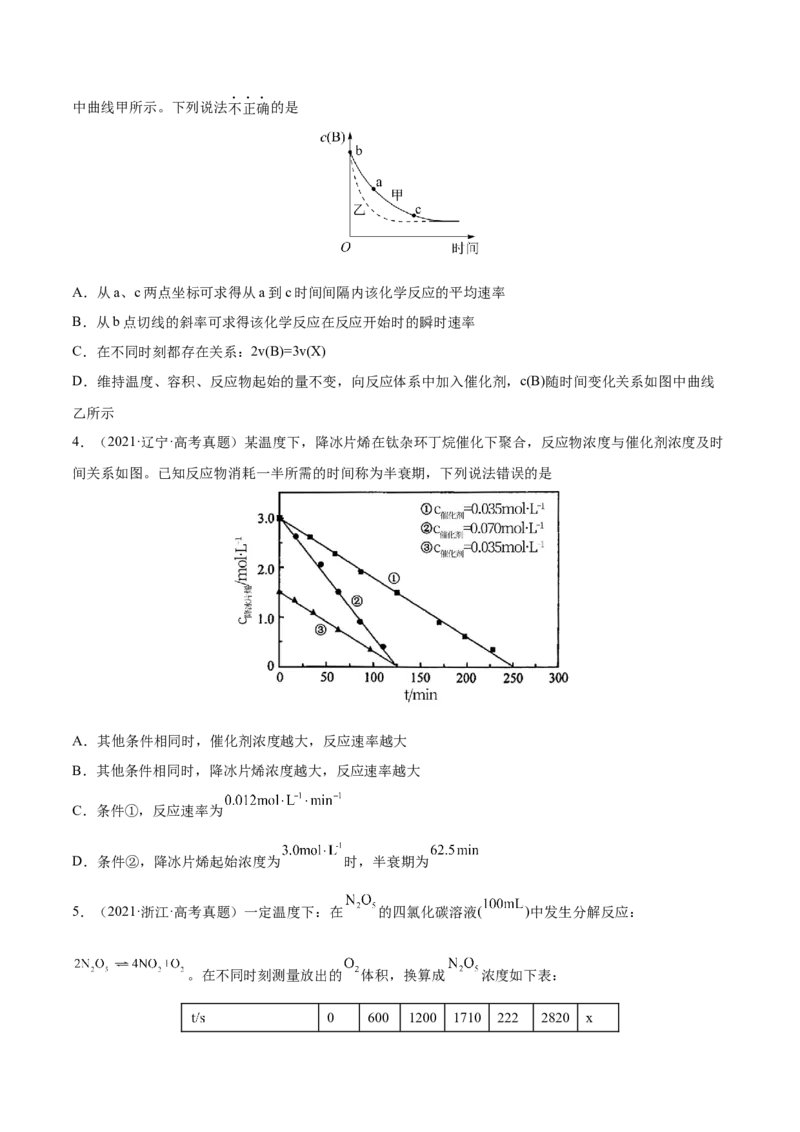
3.(2022·浙江·高考真题)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化如图中曲线甲所示。下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线
乙所示
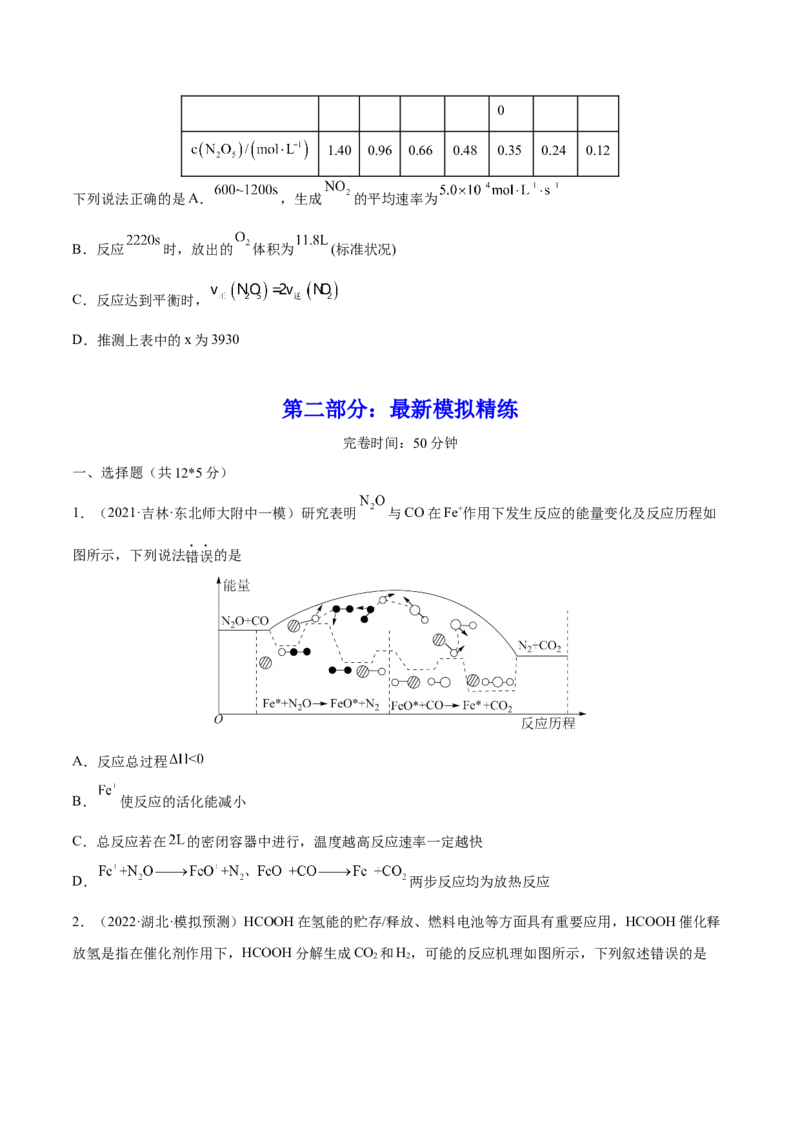
4.(2021·辽宁·高考真题)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时
间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为
D.条件②,降冰片烯起始浓度为 时,半衰期为
5.(2021·浙江·高考真题)一定温度下:在 的四氯化碳溶液( )中发生分解反应:
。在不同时刻测量放出的 体积,换算成 浓度如下表:
0 600 1200 1710 222 2820 x0
1.40 0.96 0.66 0.48 0.35 0.24 0.12
下列说法正确的是A. ,生成 的平均速率为
B.反应 时,放出的 体积为 (标准状况)
C.反应达到平衡时,
D.推测上表中的x为3930
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(共12*5分)
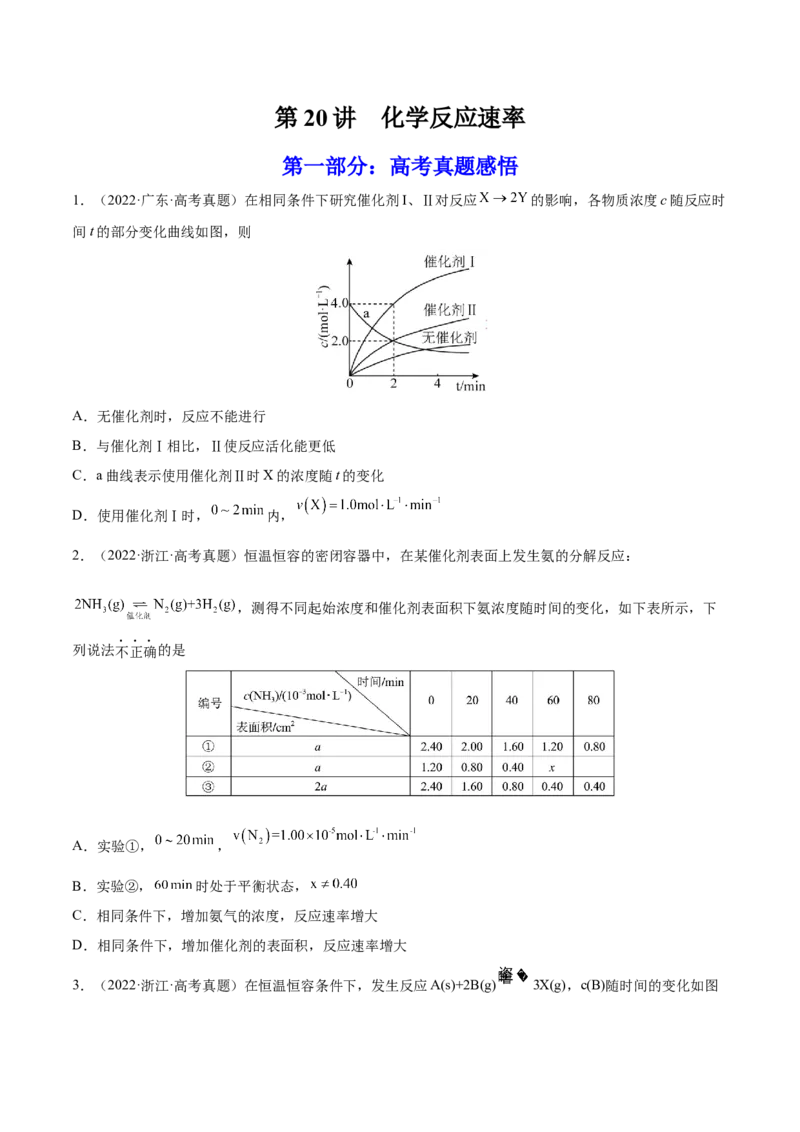
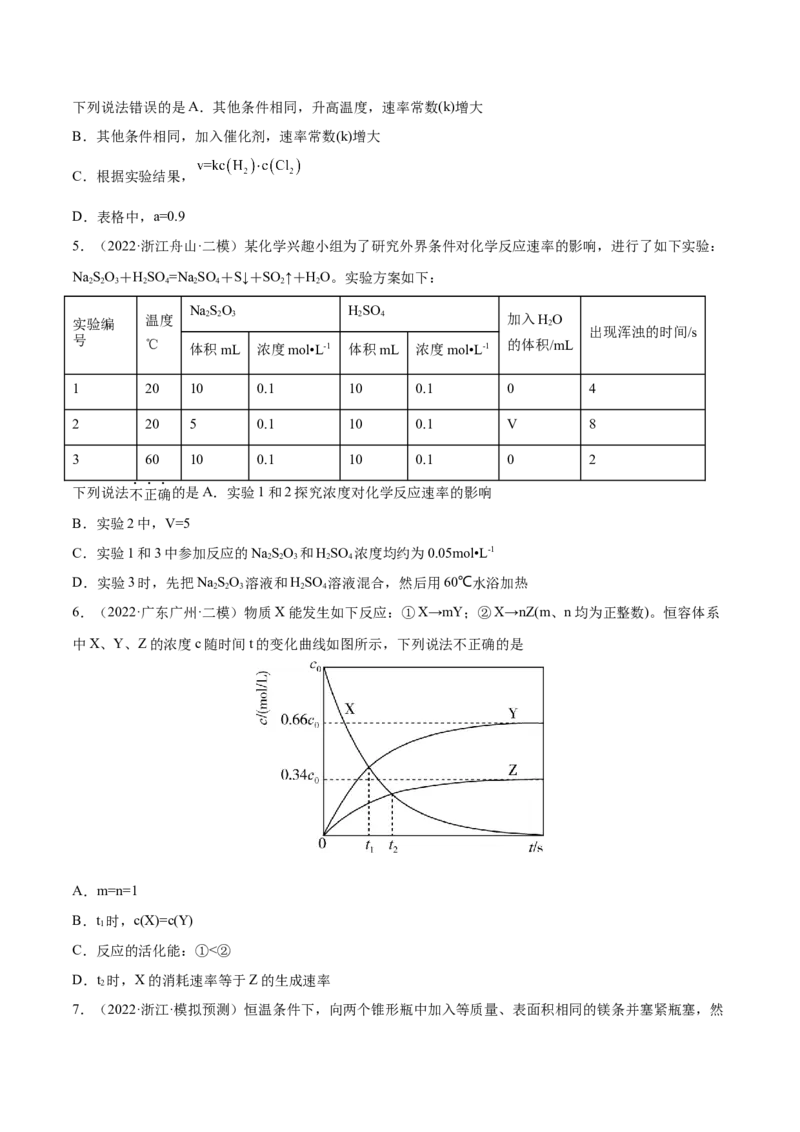
1.(2021·吉林·东北师大附中一模)研究表明 与CO在Fe+作用下发生反应的能量变化及反应历程如
图所示,下列说法错误的是
A.反应总过程
B. 使反应的活化能减小
C.总反应若在 的密闭容器中进行,温度越高反应速率一定越快
D. 两步反应均为放热反应
2.(2022·湖北·模拟预测)HCOOH在氢能的贮存/释放、燃料电池等方面具有重要应用,HCOOH催化释
放氢是指在催化剂作用下,HCOOH分解生成CO 和H,可能的反应机理如图所示,下列叙述错误的是
2 2A.该过程的总反应为HCOOH CO↑+H ↑
2 2
B.其他条件不变时,在HCOOH溶液中加入适量HCOOK溶液可提高反应速率
C.催化过程中涉及非极性共价键的断裂和形成
D.HCOOD催化释氢反应除生成CO 外,还生成了HD
2
3.(2022·北京·模拟预测)臭氧分解2O 3O 的反应历程包括以下反应:
3 2
反应①:O 3 →O 2 +O• (快) ⇌
反应②:O+O•→2O (慢)
3 2
大气中的氯氟烃光解产生的氯自由基(Cl•)能够催化O 分解,加速臭氧层的破坏。下列说法正确的是
3
A.活化能:反应①>反应②
B.O 分解为O 的速率主要由反应②决定
3 2
C.Cl•主要参与反应①,改变O 分解的反应历程
3
D.Cl•参与反应提高了O 分解为O 的平衡转化率
3 2
4.(2022·河北省唐县第一中学模拟预测)一定条件下,反应 的速率方程为
,k为速率常数(只与温度、催化剂、接触面积有关,与浓度无关),m、n是反应级数,
可以是整数、分数。
实验测得速率与浓度关系如表所示:
实验 速率
① 0.10 0.10 v
② 0.20 0.10 2v
③ 0.20 0.40 4v
④ 0.40 a 12v下列说法错误的是A.其他条件相同,升高温度,速率常数(k)增大
B.其他条件相同,加入催化剂,速率常数(k)增大
C.根据实验结果,
D.表格中,a=0.9
5.(2022·浙江舟山·二模)某化学兴趣小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
NaSO+HSO =Na SO +S↓+SO ↑+HO。实验方案如下:
2 2 3 2 4 2 4 2 2
NaSO HSO
实验编 温度 2 2 3 2 4 加入H 2 O
出现浑浊的时间/s
号 ℃
体积mL 浓度mol•L-1 体积mL 浓度mol•L-1
的体积/mL
1 20 10 0.1 10 0.1 0 4
2 20 5 0.1 10 0.1 V 8
3 60 10 0.1 10 0.1 0 2
下列说法不正确的是A.实验1和2探究浓度对化学反应速率的影响
B.实验2中,V=5
C.实验1和3中参加反应的NaSO 和HSO 浓度均约为0.05mol•L-1
2 2 3 2 4
D.实验3时,先把NaSO 溶液和HSO 溶液混合,然后用60℃水浴加热
2 2 3 2 4
6.(2022·广东广州·二模)物质X能发生如下反应:①X→mY;②X→nZ(m、n均为正整数)。恒容体系
中X、Y、Z的浓度c随时间t的变化曲线如图所示,下列说法不正确的是
A.m=n=1
B.t 时,c(X)=c(Y)
1
C.反应的活化能:①<②
D.t 时,X的消耗速率等于Z的生成速率
2
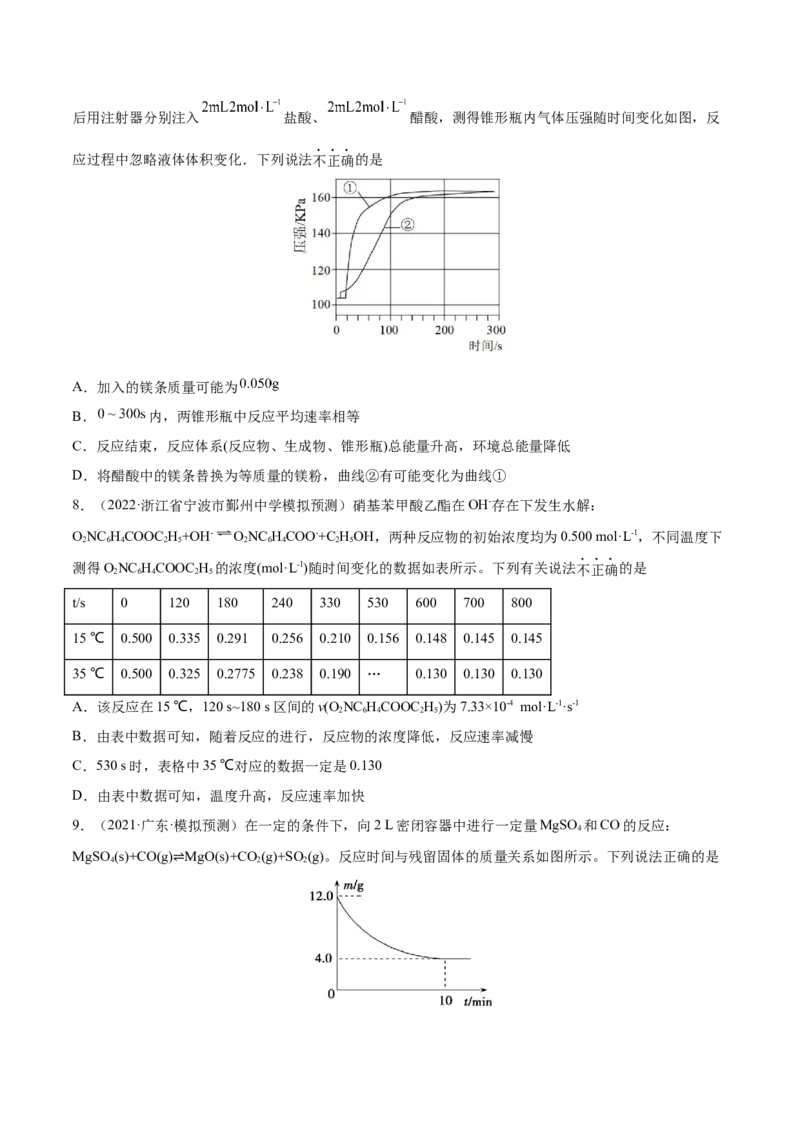
7.(2022·浙江·模拟预测)恒温条件下,向两个锥形瓶中加入等质量、表面积相同的镁条并塞紧瓶塞,然后用注射器分别注入 盐酸、 醋酸,测得锥形瓶内气体压强随时间变化如图,反
应过程中忽略液体体积变化.下列说法不正确的是
A.加入的镁条质量可能为
B. 内,两锥形瓶中反应平均速率相等
C.反应结束,反应体系(反应物、生成物、锥形瓶)总能量升高,环境总能量降低
D.将醋酸中的镁条替换为等质量的镁粉,曲线②有可能变化为曲线①
8.(2022·浙江省宁波市鄞州中学模拟预测)硝基苯甲酸乙酯在OH-存在下发生水解:
ONC HCOOC H+OH- ONC HCOO-+C HOH,两种反应物的初始浓度均为0.500 mol·L-1,不同温度下
2 6 4 2 5 2 6 4 2 5
测得ONC HCOOC H 的浓度(mol·L-1)随时间变化的数据如表所示。下列有关说法不正确的是
2 6 4 2 5
t/s 0 120 180 240 330 530 600 700 800
15 ℃ 0.500 0.335 0.291 0.256 0.210 0.156 0.148 0.145 0.145
35 ℃ 0.500 0.325 0.2775 0.238 0.190 … 0.130 0.130 0.130
A.该反应在15 ℃,120 s~180 s区间的v(O NC HCOOC H)为7.33×10-4 mol·L-1·s-1
2 6 4 2 5
B.由表中数据可知,随着反应的进行,反应物的浓度降低,反应速率减慢
C.530 s时,表格中35 ℃对应的数据一定是0.130
D.由表中数据可知,温度升高,反应速率加快
9.(2021·广东·模拟预测)在一定的条件下,向2 L密闭容器中进行一定量MgSO 和CO的反应:
4
MgSO (s)+CO(g) MgO(s)+CO (g)+SO(g)。反应时间与残留固体的质量关系如图所示。下列说法正确的是
4 2 2
⇌A.升高温度时,正反应速率增大,逆反应速率减小
B.随着反应的进行,混合气体的平均相对分子质量增大
C.增加硫酸镁的质量时,正反应速率增大
D.在0~10 min内,v(CO)=0.01 mol·L-1·min-1
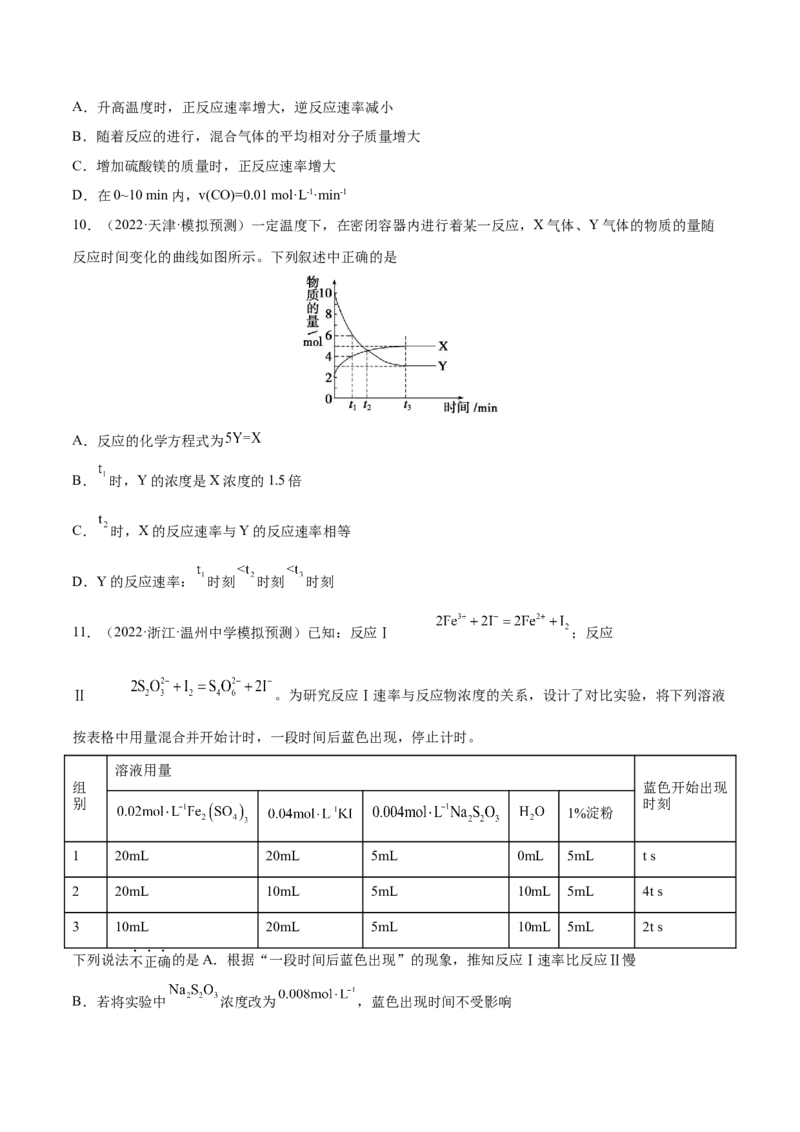
10.(2022·天津·模拟预测)一定温度下,在密闭容器内进行着某一反应,X气体、Y气体的物质的量随
反应时间变化的曲线如图所示。下列叙述中正确的是
A.反应的化学方程式为
B. 时,Y的浓度是X浓度的1.5倍
C. 时,X的反应速率与Y的反应速率相等
D.Y的反应速率: 时刻 时刻 时刻
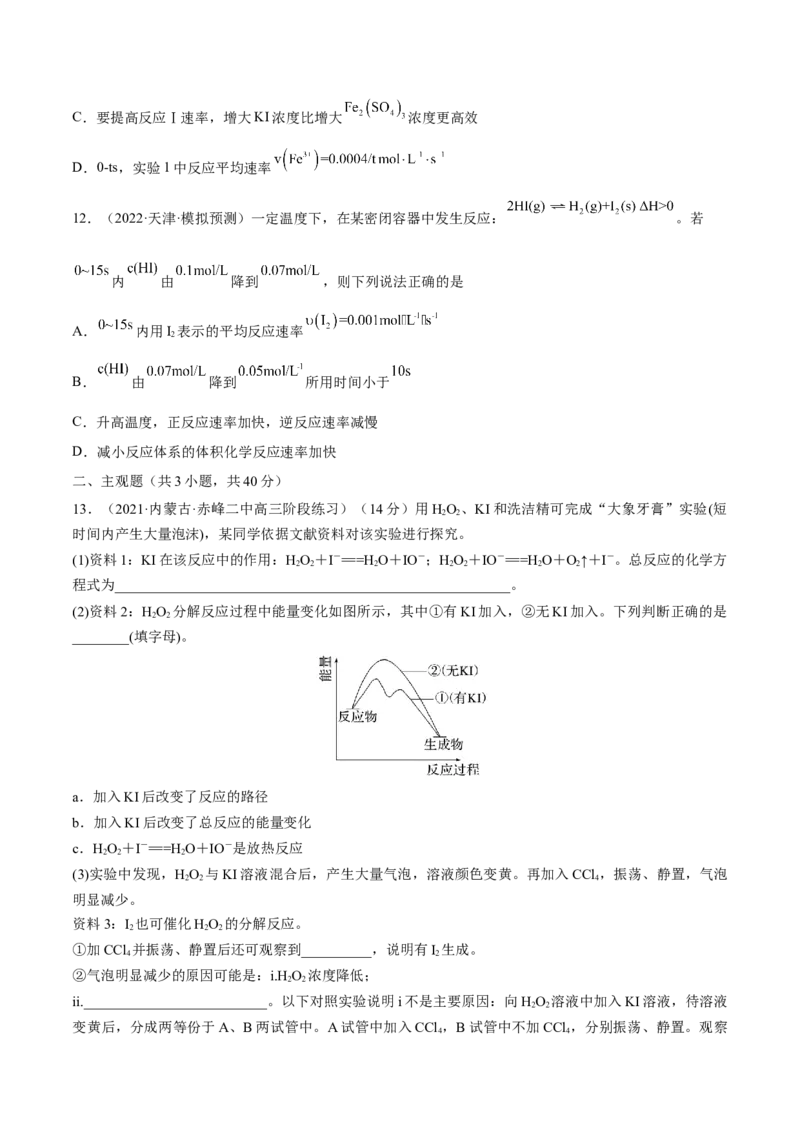
11.(2022·浙江·温州中学模拟预测)已知:反应Ⅰ ;反应
Ⅱ 。为研究反应Ⅰ速率与反应物浓度的关系,设计了对比实验,将下列溶液
按表格中用量混合并开始计时,一段时间后蓝色出现,停止计时。
溶液用量
组 蓝色开始出现
别 时刻
1%淀粉
1 20mL 20mL 5mL 0mL 5mL t s
2 20mL 10mL 5mL 10mL 5mL 4t s
3 10mL 20mL 5mL 10mL 5mL 2t s
下列说法不正确的是A.根据“一段时间后蓝色出现”的现象,推知反应Ⅰ速率比反应Ⅱ慢
B.若将实验中 浓度改为 ,蓝色出现时间不受影响C.要提高反应Ⅰ速率,增大KI浓度比增大 浓度更高效
D.0-ts,实验1中反应平均速率
12.(2022·天津·模拟预测)一定温度下,在某密闭容器中发生反应: 。若
内 由 降到 ,则下列说法正确的是
A. 内用I 表示的平均反应速率
2
B. 由 降到 所用时间小于
C.升高温度,正反应速率加快,逆反应速率减慢
D.减小反应体系的体积化学反应速率加快
二、主观题(共3小题,共40分)
13.(2021·内蒙古·赤峰二中高三阶段练习)(14分)用HO 、KI和洗洁精可完成“大象牙膏”实验(短
2 2
时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
(1)资料1:KI在该反应中的作用:HO+I-===H O+IO-;HO+IO-===H O+O↑+I-。总反应的化学方
2 2 2 2 2 2 2
程式为________________________________________________________。
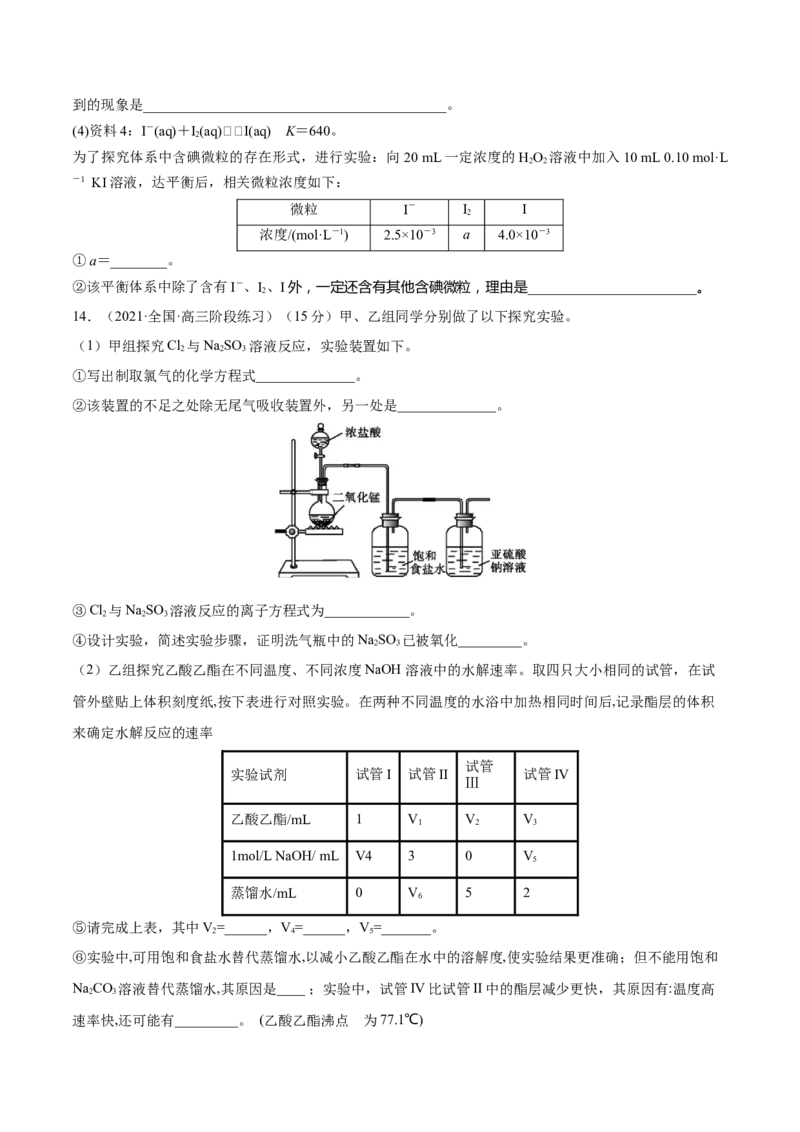
(2)资料2:HO 分解反应过程中能量变化如图所示,其中①有KI加入,②无KI加入。下列判断正确的是
2 2
________(填字母)。
a.加入KI后改变了反应的路径
b.加入KI后改变了总反应的能量变化
c.HO+I-===H O+IO-是放热反应
2 2 2
(3)实验中发现,HO 与KI溶液混合后,产生大量气泡,溶液颜色变黄。再加入CCl ,振荡、静置,气泡
2 2 4
明显减少。
资料3:I 也可催化HO 的分解反应。
2 2 2
①加CCl 并振荡、静置后还可观察到__________,说明有I 生成。
4 2
②气泡明显减少的原因可能是:i.H O 浓度降低;
2 2
ii.__________________________。以下对照实验说明i不是主要原因:向HO 溶液中加入KI溶液,待溶液
2 2
变黄后,分成两等份于A、B两试管中。A试管中加入CCl ,B试管中不加CCl ,分别振荡、静置。观察
4 4到的现象是___________________________________________。
(4)资料4:I-(aq)+I(aq)I(aq) K=640。
2
为了探究体系中含碘微粒的存在形式,进行实验:向20 mL一定浓度的HO 溶液中加入10 mL 0.10 mol·L
2 2
-1 KI溶液,达平衡后,相关微粒浓度如下:
微粒 I- I I
2
浓度/(mol·L-1) 2.5×10-3 a 4.0×10-3
①a=________。
②该平衡体系中除了含有I-、I、I外,一定还含有其他含碘微粒,理由是________________________。
2
14.(2021·全国·高三阶段练习)(15分)甲、乙组同学分别做了以下探究实验。
(1)甲组探究Cl 与NaSO 溶液反应,实验装置如下。
2 2 3
①写出制取氯气的化学方程式______________。
②该装置的不足之处除无尾气吸收装置外,另一处是______________。
③Cl 与NaSO 溶液反应的离子方程式为____________。
2 2 3
④设计实验,简述实验步骤,证明洗气瓶中的NaSO 已被氧化_________。
2 3
(2)乙组探究乙酸乙酯在不同温度、不同浓度NaOH 溶液中的水解速率。取四只大小相同的试管,在试
管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积
来确定水解反应的速率
试管
实验试剂 试管I 试管II 试管IV
Ⅲ
乙酸乙酯/mL 1 V V V
1 2 3
1mol/L NaOH/ mL V4 3 0 V
5
蒸馏水/mL 0 V 5 2
6
⑤请完成上表,其中V=______,V=______,V=_______。
2 4 5
⑥实验中,可用饱和食盐水替代蒸馏水,以减小乙酸乙酯在水中的溶解度,使实验结果更准确;但不能用饱和
NaCO 溶液替代蒸馏水,其原因是____ ;实验中,试管IV比试管II中的酯层减少更快,其原因有:温度高
2 3
速率快,还可能有_________。 (乙酸乙酯沸点 为77.1℃)15.(2021·浙江·模拟预测)(11分)科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变
成CO 和N,其反应为2NO(g)+2CO(g) N(g)+2CO (g)。
2 2 2 2
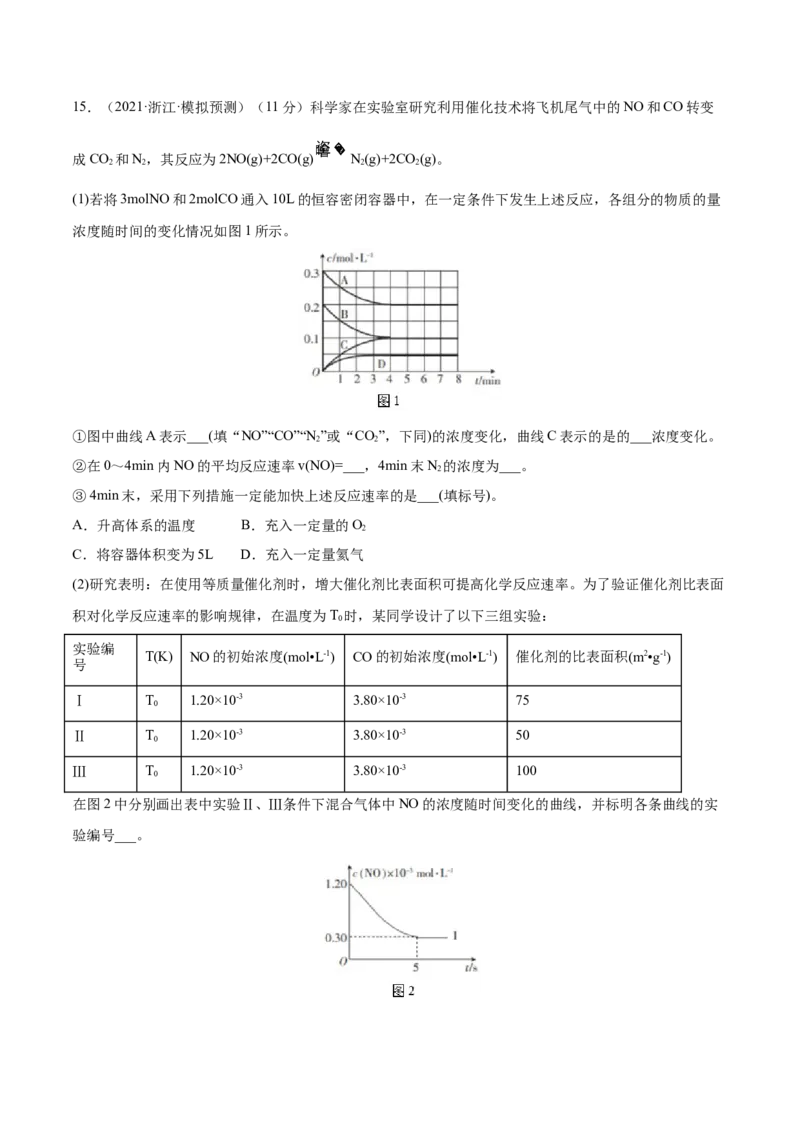
(1)若将3molNO和2molCO通入10L的恒容密闭容器中,在一定条件下发生上述反应,各组分的物质的量
浓度随时间的变化情况如图1所示。
①图中曲线A表示___(填“NO”“CO”“N ”或“CO”,下同)的浓度变化,曲线C表示的是的___浓度变化。
2 2
②在0~4min内NO的平均反应速率v(NO)=___,4min末N 的浓度为___。
2
③4min末,采用下列措施一定能加快上述反应速率的是___(填标号)。
A.升高体系的温度 B.充入一定量的O
2
C.将容器体积变为5L D.充入一定量氦气
(2)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证催化剂比表面
积对化学反应速率的影响规律,在温度为T 时,某同学设计了以下三组实验:
0
实验编
T(K) NO的初始浓度(mol•L-1) CO的初始浓度(mol•L-1) 催化剂的比表面积(m2•g-1)
号
Ⅰ T 1.20×10-3 3.80×10-3 75
0
Ⅱ T 1.20×10-3 3.80×10-3 50
0
Ⅲ T 1.20×10-3 3.80×10-3 100
0
在图2中分别画出表中实验Ⅱ、Ⅲ条件下混合气体中NO的浓度随时间变化的曲线,并标明各条曲线的实
验编号___。