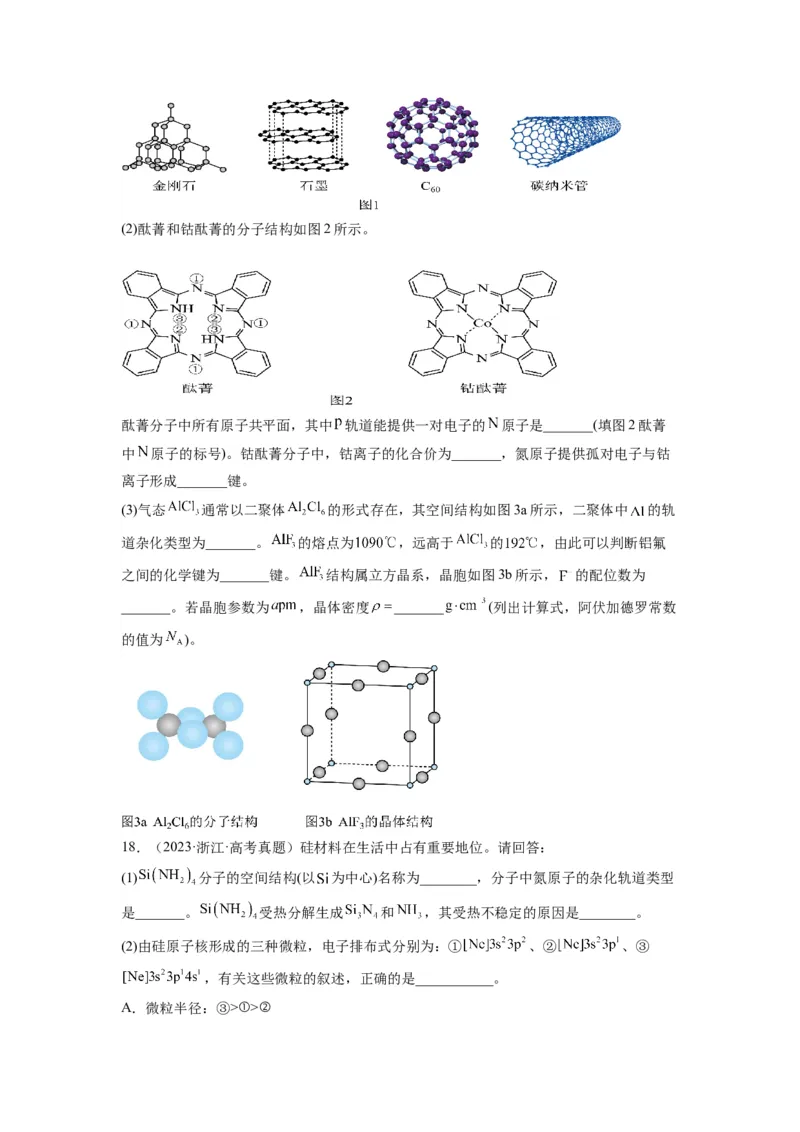
文档内容
第 21 练 物质结构与性质综合题
一、考情分析
物质结构与性质题考查主要集中在原子内部结构和电子排布规则上,将分子结构、杂
化理论与晶体类型理论结合起来,通过用主观题的形式考核学生对此理论知识掌握的程
度。从主观题的构成来看,给出一定的知识背景,然后设置成4—5个小题,每个小题考查
一个知识要点是主要的命题模式,内容主要考查基本概念,如电子排布式,轨道式,电离
能,电负性,杂化方式以及空间构型等,也可联系有机考查有机物中C原子的杂化,联系
数学几何知识考查晶体的计算等,一般利用均摊法考查晶胞中的原子个数,或者考查晶体
的化学式的书写、晶体类型的判断等,考查的抽象思维能力、逻辑思维能力;同时培养学
生的分析和推理能力。
二、高频考点及应对策略
1.核外电子排布的书写
(1)一般原子核外电子排布式的四种表示方法
表示方法 举例
电子排布式 Mn:1s22s22p63s23p63d54s2
简化电子排布式 Zn:[Ar]3d104s2
价电子排布式 Co:3d74s2
电子排布图(或轨道表示式)
O:
(2)特殊原子的核外电子排布式
①Cr的核外电子排布:因3d5为半充满状态,比较稳定,故该原子的电子排布式:
1s22s22p63s23p63d54s1。
②Cu的核外电子排布:因3d10为全充满状态,比较稳定,故该原子的电子排布式:
1s22s22p63s23p63d104s1。
2.第一电离能、电负性大小比较
(1)元素第一电离能的周期性变化规律
①同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势,稀有气体元素的
第一电离能最大,碱金属元素的第一电离能最小;同一主族,随着电子层数的增加,元素的第
一电离能逐渐减小。
②反常情况:第一电离能的变化与元素原子的核外电子排布有关。通常情况下,当原子
核外电子排布在能量相等的轨道上形成全空(p0、d0、f0)、半满(p3、d5、f7)和全满(p6、
d10、f14)结构时,原子的能量较低,该元素具有较大的第一电离能。如同周期主族元素,第
ⅡA族元素的原子最外层s能级全充满、ⅤA族元素的原子最外层p能级半充满,比较稳
定,所以其第一电离能大于同周期相邻的主族元素。
(2)电负性大小判断
①在周期表中,同周期主族元素电负性从左到右逐渐增大,同主族从上往下逐渐减小。
②特殊情况:常常应用化合价及物质类别判断电负性的大小,如O与Cl的电负性比
较:①HClO中Cl为+1价、O为-2价,可知O的电负性大于Cl;②AlO 是离子化合物、AlCl
2 3 3
是共价化合物,可知O的电负性大于Cl。
3.中心原子A的价层电子对数的速算方法
对AB 型化合物,中心原子A的价层电子对数n=,计算时一般说来,价电子数即为最
m
外层电子数,但B为卤素原子、氢原子时,提供1个价电子,若为氧原子、硫原子时,则
不提供电子。
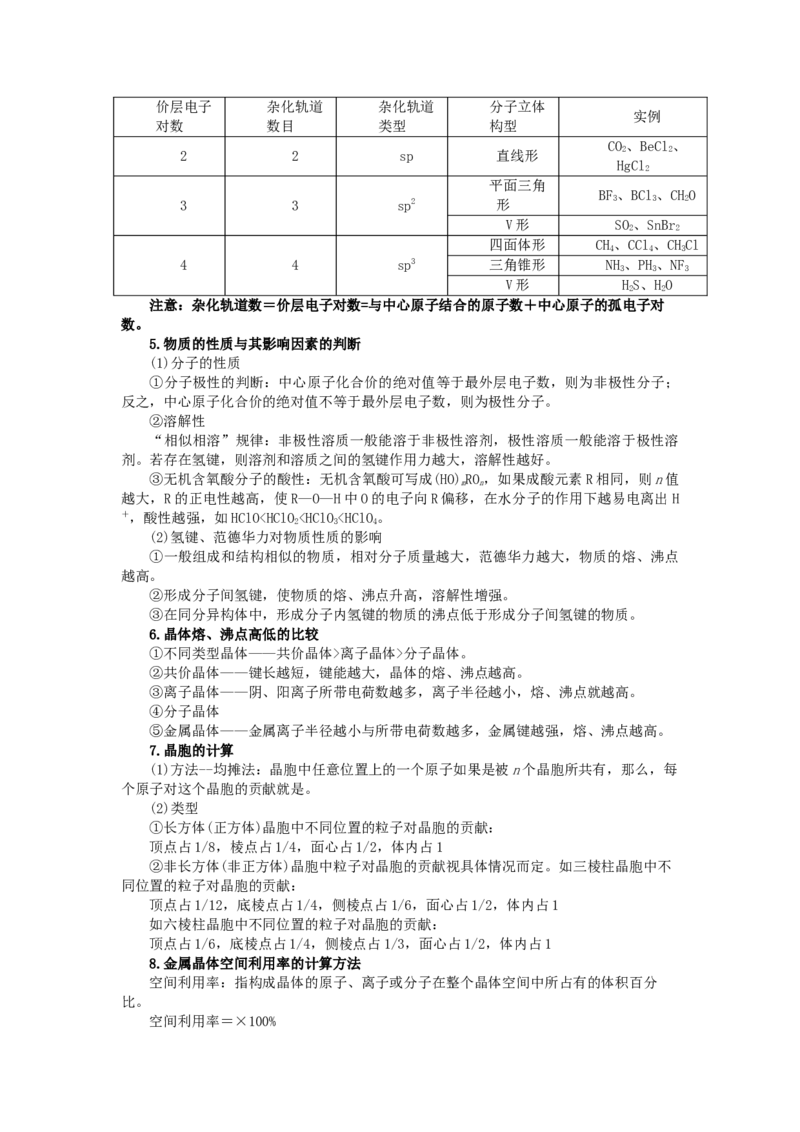
4.杂化轨道类型与分子立体构型的关系价层电子 杂化轨道 杂化轨道 分子立体
实例
对数 数目 类型 构型
CO、BeCl、
2 2 sp 直线形 2 2
HgCl
2
平面三角
BF、BCl、CHO
3 3 sp2 形 3 3 2
V形 SO、SnBr
2 2
四面体形 CH、CCl、CHCl
4 4 3
4 4 sp3 三角锥形 NH、PH、NF
3 3 3
V形 HS、HO
2 2
注意:杂化轨道数=价层电子对数=与中心原子结合的原子数+中心原子的孤电子对
数。
5.物质的性质与其影响因素的判断
(1)分子的性质
①分子极性的判断:中心原子化合价的绝对值等于最外层电子数,则为非极性分子;
反之,中心原子化合价的绝对值不等于最外层电子数,则为极性分子。
②溶解性
“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶
剂。若存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越好。
③无机含氧酸分子的酸性:无机含氧酸可写成(HO)RO ,如果成酸元素R相同,则n值
m n
越大,R的正电性越高,使R—O—H中O的电子向R偏移,在水分子的作用下越易电离出H
+,酸性越强,如HClO离子晶体>分子晶体。
②共价晶体——键长越短,键能越大,晶体的熔、沸点越高。
③离子晶体——阴、阳离子所带电荷数越多,离子半径越小,熔、沸点就越高。
④分子晶体
⑤金属晶体——金属离子半径越小与所带电荷数越多,金属键越强,熔、沸点越高。
7.晶胞的计算
(1)方法--均摊法:晶胞中任意位置上的一个原子如果是被n个晶胞所共有,那么,每
个原子对这个晶胞的贡献就是。
(2)类型
①长方体(正方体)晶胞中不同位置的粒子对晶胞的贡献:
顶点占1/8,棱点占1/4,面心占1/2,体内占1
②非长方体(非正方体)晶胞中粒子对晶胞的贡献视具体情况而定。如三棱柱晶胞中不
同位置的粒子对晶胞的贡献:
顶点占1/12,底棱点占1/4,侧棱点占1/6,面心占1/2,体内占1
如六棱柱晶胞中不同位置的粒子对晶胞的贡献:
顶点占1/6,底棱点占1/4,侧棱点占1/3,面心占1/2,体内占1
8.金属晶体空间利用率的计算方法
空间利用率:指构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分
比。
空间利用率=×100%9.计算晶体密度的方法:密度=质量/体积
1.(2023·全国·模拟预测)铁、镍都是磁性金属,在新型电池领域应用广泛。回答下列问
题:
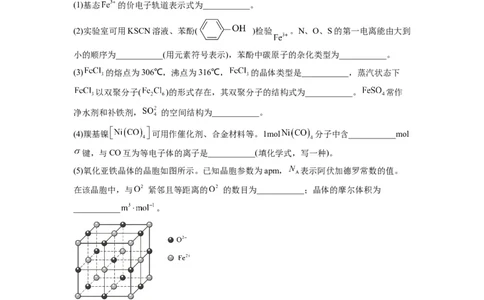
(1)基态 的价电子轨道表示式为___________。
(2)实验室可用KSCN溶液、苯酚( )检验 。N、O、S的第一电离能由大到
小的顺序为___________(用元素符号表示),苯酚中碳原子的杂化类型为___________。
(3) 的熔点为306℃,沸点为316℃, 的晶体类型是___________,蒸汽状态下
以双聚分子( )的形式存在,其双聚分子的结构式为___________。 常作
净水剂和补铁剂, 的空间结构为___________。
(4)羰基镍 可用作催化剂、合金材料等。1mol 分子中含___________mol
键,与CO互为等电子体的离子是___________(填化学式,写一种)。
(5)氧化亚铁晶体的晶胞如图所示。已知晶胞参数为apm, 表示阿伏加德罗常数的值。
在该晶胞中,与 紧邻且等距离的 的数目为___________;晶体的摩尔体积为
___________ 。
2.(2023·山东聊城·统考二模)金属及其化合物在化工、医药、材料等领域有着广泛的应
用。请回答下列问题:
(1)与Fe最外层电子数相同且同周期的过渡元素有___________种。
(2)次磷酸的正盐KH PO 中P的___________杂化轨道与O的___________轨道形成 键。
2 2
(3)Zn、Fe、Cu等过渡金属的原子或离子易通过配位键形成配合物或配离子。
① 和 中所有原子均共面,其中氮原子较易形成配位键的是___________。②配位原子提供孤电子对的能力与元素的电负性大小有关,元素电负性越大,其原子越不
容易提供孤电子对。则对于配合物Fe(SCN) ,配体SCN-中提供孤电子对的原子是
3
___________(填元素符号)。
③将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列
物质中,属于顺磁性物质的是___________。
A.[Cu(NH )]C1 B.[Cu(NH )]SO
3 2 3 4 4
C.[Zn(NH )]SO D.[Cr(H O) Cl]Cl
3 4 4 2 5 2
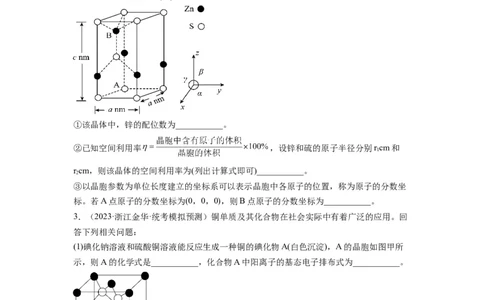
(4)硫化锌(ZnS)晶体属于六方晶系,Zn原子位于4个S原子形成的正四面体空隙中。晶胞
参数如图所示α=120°,β=γ=90°。
①该晶体中,锌的配位数为___________。
②已知空间利用率 ,设锌和硫的原子半径分别rcm和
1
rcm,则该晶体的空间利用率为(列出计算式即可)___________。
2
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐
标。若A点原子的分数坐标为(0,0,0),则B点原子的分数坐标为___________。
3.(2023·浙江金华·统考模拟预测)铜单质及其化合物在社会实际中有着广泛的应用。回
答下列相关问题:
(1)碘化钠溶液和硫酸铜溶液能反应生成一种铜的碘化物A(白色沉淀),A的晶胞如图甲所
示,则A的化学式是___________,化合物A中阳离子的基态电子排布式为___________。
(2)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝
色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的 沉淀,
该物质中的 通过___________键与中心离子 结合, 离子的空间结构为___________,N、O元素第一电离能大小关系为___________,原因是___________。
(3)晶体铜的晶胞结构如图乙表示,原子之间相对位置关系的平面图如图丙所示,铜原子半
径为127.8pm, 表示阿佛加德罗常数的值,晶体铜的密度为___________ (列出计
算式即可)。
4.(2023·浙江金华·模拟预测)物质的组成与结构决定物质的性质与变化。请回答:
(1)有如下反应: (氯化苯重氮盐),NO 的空间
结构名称为______,产物中两个氮原子直接相连,其中与碳原子直接相连的N原子的杂化
轨道类型是_____。
(2)MgCl 的熔点比BeCl 高的原因是______。
2 2
(3)下列叙述正确的是______。
A.电离一个电子所需最低能量:Mg+(g)<Al+(g)
B.键角大小:HO+<HO
3 2
C.沸点:邻羟基苯甲酸>对羟基苯甲酸
D.pK:CFCOOH<CHCOOH
a 3 3
(4)单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。该物质的晶体类型
是_____,该化合物的化学式为______。
5.(2023·北京房山·统考二模)短周期元素B、C、N等元素可以形成多种物质,呈现出
不同的性质,请回答以下问题:
(1)B、C、N三种元素中第一电离能最大的是___________。
(2)硅、金刚石和碳化硅晶体的熔点从高到低依次是___________。
(3) 的结构与 类似、但是性质差异较大。
① 的空间结构为___________形。N原子的轨道杂化类型为___________。
② 具有碱性(可与 结合)而 不显碱性,原因是___________。
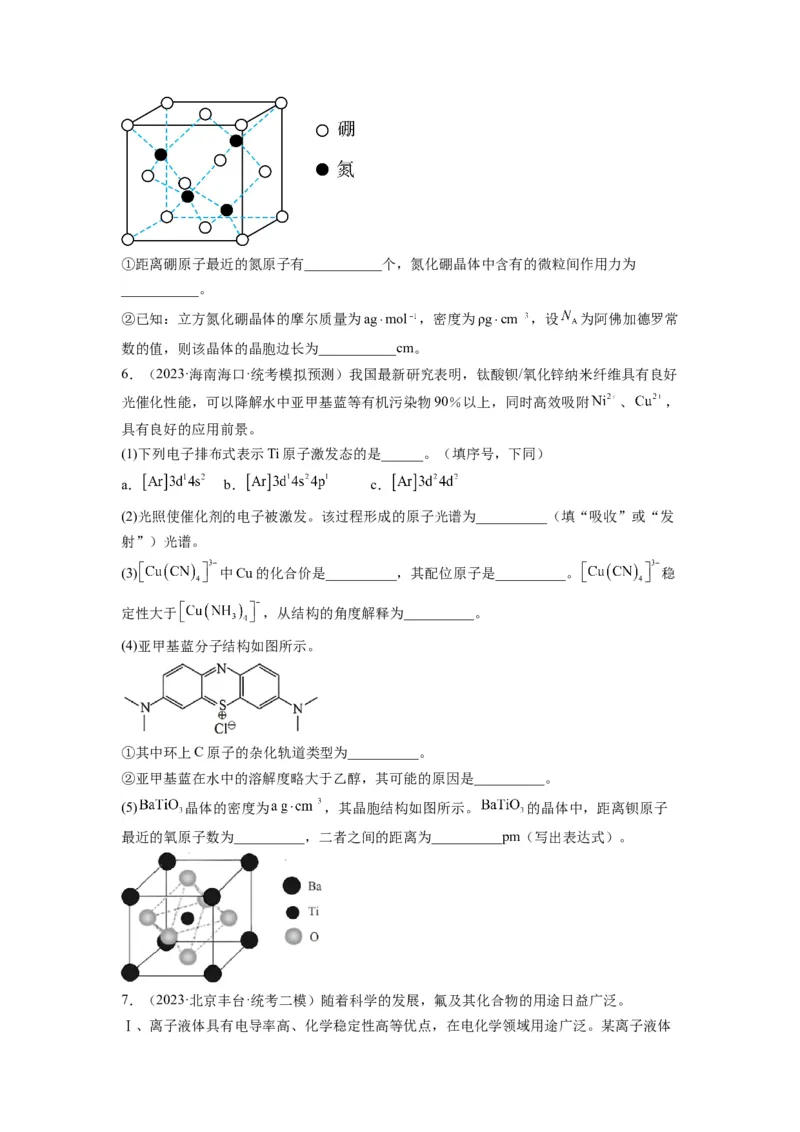
(4)立方氮化硼晶体结构与金刚石相似,其晶胞如图所示。①距离硼原子最近的氮原子有___________个,氮化硼晶体中含有的微粒间作用力为
___________。
②已知:立方氮化硼晶体的摩尔质量为ag⋅mol ,密度为ρg⋅cm ,设 为阿佛加德罗常
数的值,则该晶体的晶胞边长为___________cm。
6.(2023·海南海口·统考模拟预测)我国最新研究表明,钛酸钡/氧化锌纳米纤维具有良好
光催化性能,可以降解水中亚甲基蓝等有机污染物90%以上,同时高效吸附 、 ,
具有良好的应用前景。
(1)下列电子排布式表示Ti原子激发态的是______。(填序号,下同)
a. b. c.
(2)光照使催化剂的电子被激发。该过程形成的原子光谱为__________(填“吸收”或“发
射”)光谱。
(3) 中Cu的化合价是__________,其配位原子是__________。 稳
定性大于 ,从结构的角度解释为__________。
(4)亚甲基蓝分子结构如图所示。
①其中环上C原子的杂化轨道类型为__________。
②亚甲基蓝在水中的溶解度略大于乙醇,其可能的原因是__________。
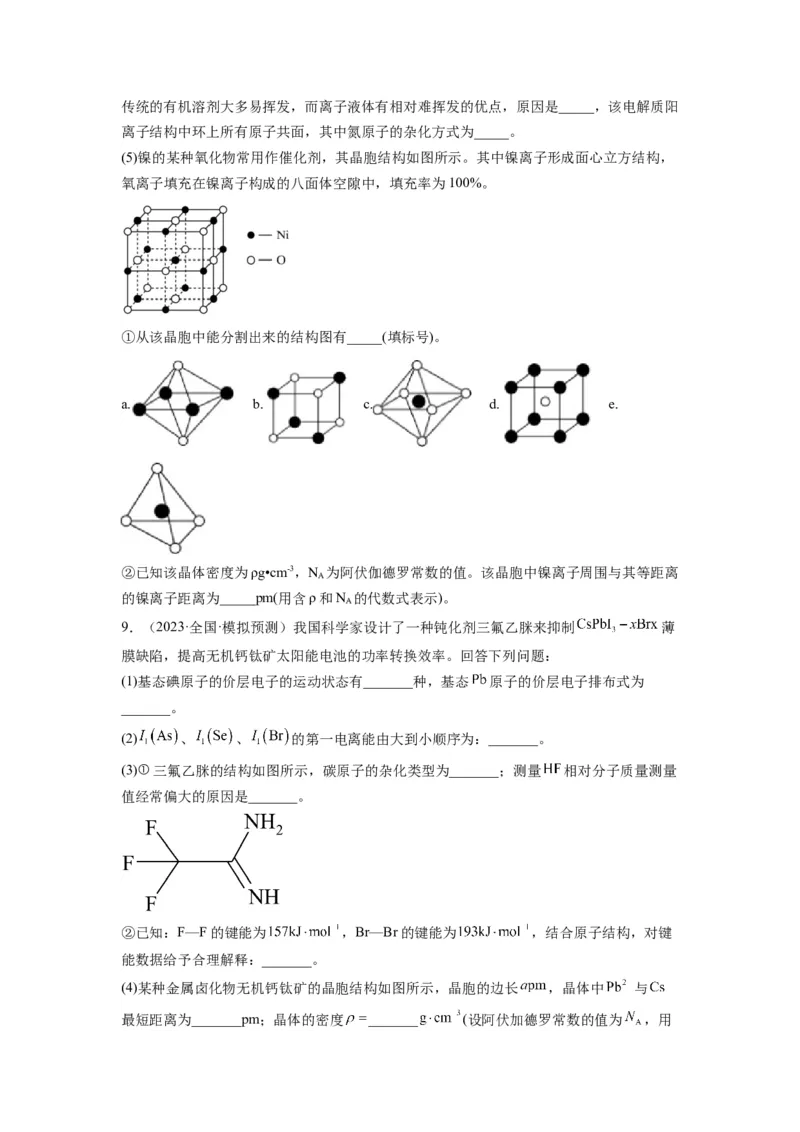
(5) 晶体的密度为 ,其晶胞结构如图所示。 的晶体中,距离钡原子
最近的氧原子数为__________,二者之间的距离为__________pm(写出表达式)。
7.(2023·北京丰台·统考二模)随着科学的发展,氟及其化合物的用途日益广泛。
Ⅰ、离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如下图。
1−乙基−3−甲基咪唑四氟硼酸盐( )
(1)写出基态铜原子的价电子排布式___________。
(2) 是制备此离子液体的原料。
①微粒中 键角: ___________ (填“>”、“<”或“=”)。
② 可以与 反应生成 的原因是___________。
(3)以 和 的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,
阳极材料为___________,电解质溶液中 向___________极移动(填“阴”或“阳”)。
Ⅱ、 等氟化物可以做光导纤维材料,一定条件下,某 的晶体结构如下图。
(4)与 距离最近且相等的 有___________个。
(5) 表示阿伏伽德罗常数的值。 晶胞为正方体,边长为 ,则晶体的摩尔体积
___________ 。( )
8.(2023·广西玉林·统考模拟预测)中科院大连化物所化学研究团队在化学链合成NH 研
3
究方面取得新进展,该研究中涉及的物质有Ni-BaH/Al O、Fe-KO-Al O、Cs-Ru/
2 2 3 2 2 3
MgO等,相关研究成果发表于《自然》上。请回答下列问题:
(1)[Fe(CN) ]3-离子中σ键和π键的数目之比为_____,Ni的价电子排布式_____。
6
(2)元素的第一电离能:Mg_____Al(填“>”或“<”)。H、B、N、O的电负性由大到小
的顺序为_____。
(3)已知MgO的熔点为2852℃,CaO的熔点为2614℃,二者的晶体类型为_____,NaBH 阴
4
离子的空间构型是_____。
(4)铝离子电池能量密度高、成本低且安全性高,是有前景的下一代储能电池。铝离子电池
一般采用离子液体作为电解质,一种电解质离子的结构如图:传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是_____,该电解质阳
离子结构中环上所有原子共面,其中氮原子的杂化方式为_____。
(5)镍的某种氧化物常用作催化剂,其晶胞结构如图所示。其中镍离子形成面心立方结构,
氧离子填充在镍离子构成的八面体空隙中,填充率为100%。
①从该晶胞中能分割出来的结构图有_____(填标号)。
a. b. c. d. e.
②已知该晶体密度为ρg•cm-3,N 为阿伏伽德罗常数的值。该晶胞中镍离子周围与其等距离
A
的镍离子距离为_____pm(用含ρ和N 的代数式表示)。
A
9.(2023·全国·模拟预测)我国科学家设计了一种钝化剂三氟乙脒来抑制 薄
膜缺陷,提高无机钙钛矿太阳能电池的功率转换效率。回答下列问题:
(1)基态碘原子的价层电子的运动状态有_______种,基态 原子的价层电子排布式为
_______。
(2) 、 、 的第一电离能由大到小顺序为:_______。
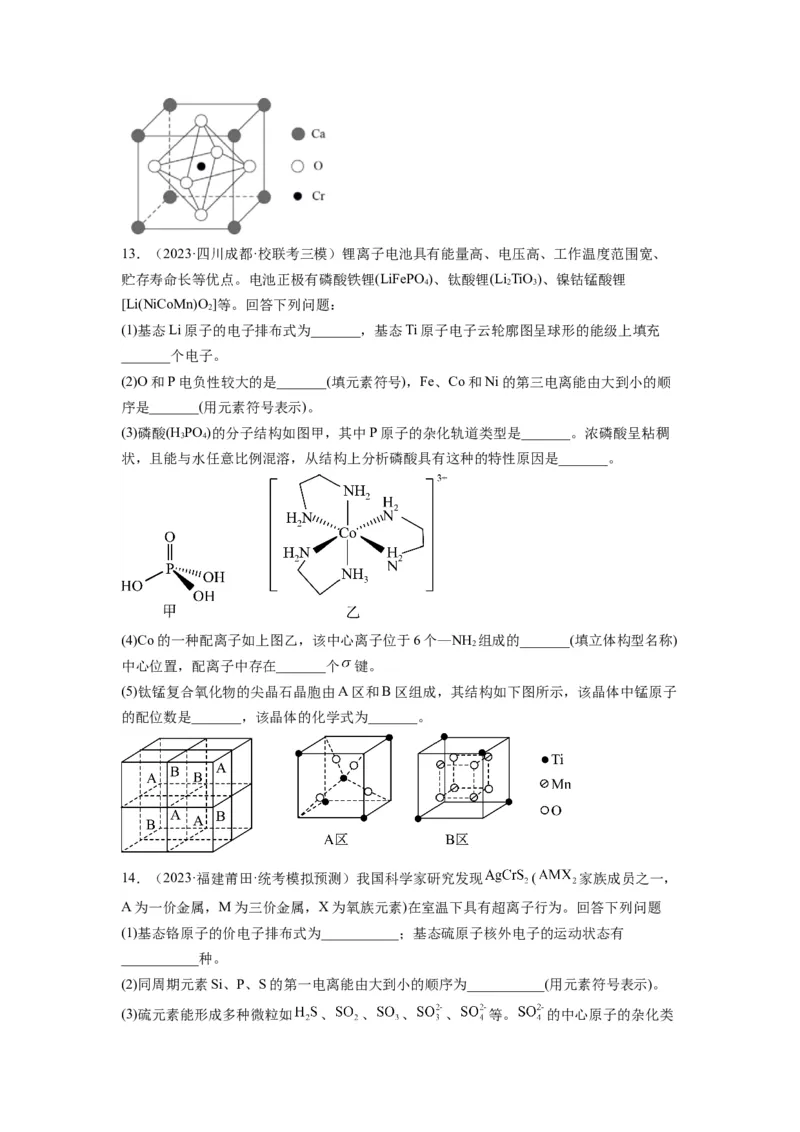
(3)①三氟乙脒的结构如图所示,碳原子的杂化类型为_______;测量 相对分子质量测量
值经常偏大的原因是_______。
②已知:F—F的键能为 ,Br—Br的键能为 ,结合原子结构,对键
能数据给予合理解释:_______。
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长 ,晶体中 与
最短距离为_______pm;晶体的密度 _______ (设阿伏加德罗常数的值为 ,用含a、 的代数式表示;可能用到相对原子质量: )
10.(2023·山东青岛·统考二模)硼、铝及其化合物在生产、生活和科研中应用广泛。回
答下列问题:
(1)基态B原子核外电子有___________种空间运动状态。
(2) 、 、 沸点由高到低的顺序为___________, 、 、 的热稳定性
由强到弱的顺序为___________。
(3) 分子中 键长远比B和F的半径之和小,原因是分子中含有与苯类似的大 大 键。
该分子中的大 键表示为___________。
(4)下列物质均与 发生配位反应,其中形成N-B键最强的是___________。
A. B. C.
(5)氮化硼( )有立方氮化硼和六方氮化硼两种结构。
①立方氮化硼晶胞如图,N与B原子的配位数之比为___________。已知N-B的键长为
anm,则该晶胞的晶胞参数为___________nm。
②六方氮化硼又称“白石墨”,结构与石墨相似,氮硼交替形成层状结构,与石墨的导电
能力不同,是优良的绝缘体,原因是___________。
11.(2023·福建龙岩·统考模拟预测)硅在地壳中含量丰富,晶体硅与硅化物等新材料在
现代工业领域作用巨大。回答下列问题:
(1)下列属于硅原子激发态的电子排布式有___________(填标号,下同),其中能量较高的是
___________。
a.1s22s22p63s23p2 b.1s22s22p63s13p3 c.1s22s22p63s13p2 d.1s22s22p63s13p24s1
(2)SiCl 可发生水解反应,机理如图1所示。
4①a与c的水溶性:a___________c(填“>”“<”或“=”),理由是___________。
②c分子中氧原子杂化方式为___________;c分子中键长从大到小顺序为___________。
(3)一种新型导电陶瓷材料硅的钨化物,其晶胞结构如图2所示,硅原子的配位数为
___________,设N 为阿伏伽德罗常数的值,则该硅的钨化物晶体的密度为
A
___________g·cm-3(列出计算式)
12.(2023·陕西榆林·统考模拟预测)我国科学家研究发现AgCrS (AMX 家族成员之一,
2 2
A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态铬原子的价电子排布式为___________ ;基态硫原子核外电子的空间运动状态有
___________种。
(2)同周期元素Si、P、S的第一电离能由大到小的顺序为___________ (用元素符号表示),
O、S为同主族元素, HO的沸点比HS高的原因是___________。
2 2
(3)硫元素能形成多种微粒如HS、SO 、SO 、 、 等。SO 的立体构型为
2 2 3 2
___________, 的中心原子的杂化类型是___________。
(4)CrO 中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为___________ (填标号)。
5
A B C
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为___________;与Cr最近的氧原子
的个数为___________;Ca和Cr的最近距离为a nm,设N 为阿伏加德罗常数的值,则该
A
晶体密度为__________(填含a、N 的表达式)g·cm-3。
A13.(2023·四川成都·校联考三模)锂离子电池具有能量高、电压高、工作温度范围宽、
贮存寿命长等优点。电池正极有磷酸铁锂(LiFePO )、钛酸锂(Li TiO)、镍钴锰酸锂
4 2 3
[Li(NiCoMn)O ]等。回答下列问题:
2
(1)基态Li原子的电子排布式为_______,基态Ti原子电子云轮廓图呈球形的能级上填充
_______个电子。
(2)O和P电负性较大的是_______(填元素符号),Fe、Co和Ni的第三电离能由大到小的顺
序是_______(用元素符号表示)。
(3)磷酸(H PO )的分子结构如图甲,其中P原子的杂化轨道类型是_______。浓磷酸呈粘稠
3 4
状,且能与水任意比例混溶,从结构上分析磷酸具有这种的特性原因是_______。
(4)Co的一种配离子如上图乙,该中心离子位于6个—NH 组成的_______(填立体构型名称)
2
中心位置,配离子中存在_______个 键。
(5)钛锰复合氧化物的尖晶石晶胞由A区和B区组成,其结构如下图所示,该晶体中锰原子
的配位数是_______,该晶体的化学式为_______。
14.(2023·福建莆田·统考模拟预测)我国科学家研究发现 ( 家族成员之一,
A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题
(1)基态铬原子的价电子排布式为___________;基态硫原子核外电子的运动状态有
___________种。
(2)同周期元素Si、P、S的第一电离能由大到小的顺序为___________(用元素符号表示)。
(3)硫元素能形成多种微粒如 、 、 、 、 等。 的中心原子的杂化类型是___________。
(4) 中 元素化合价为+6价,常温下呈蓝色,则其结构式可能为___________(填标号)。
A B C
(5)某含铬化合物立方晶胞如图所示。该晶体的化学式为___________;与Cr最近的氧原子
的个数为___________。
15.(2023·天津·统考三模)CaF 、CaC 都是工业生产的重要物质。回答下列问题:
2 2
(1)基态钙原子的电子排布式________,钙原子核外有________种能量状态的电子。
(2)CaC 与水反应生成乙炔(C H),乙炔中的σ键与π键数之比为_______。
2 2 2
(3)CaF 与浓HSO 反应生成HF,HF的沸点高于C H,原因是________。
2 2 4 2 2
(4)F 通入稀NaOH溶液中可生成OF ,OF 分子构型为___________,其中氧原子的杂化方
2 2 2
式为___________。
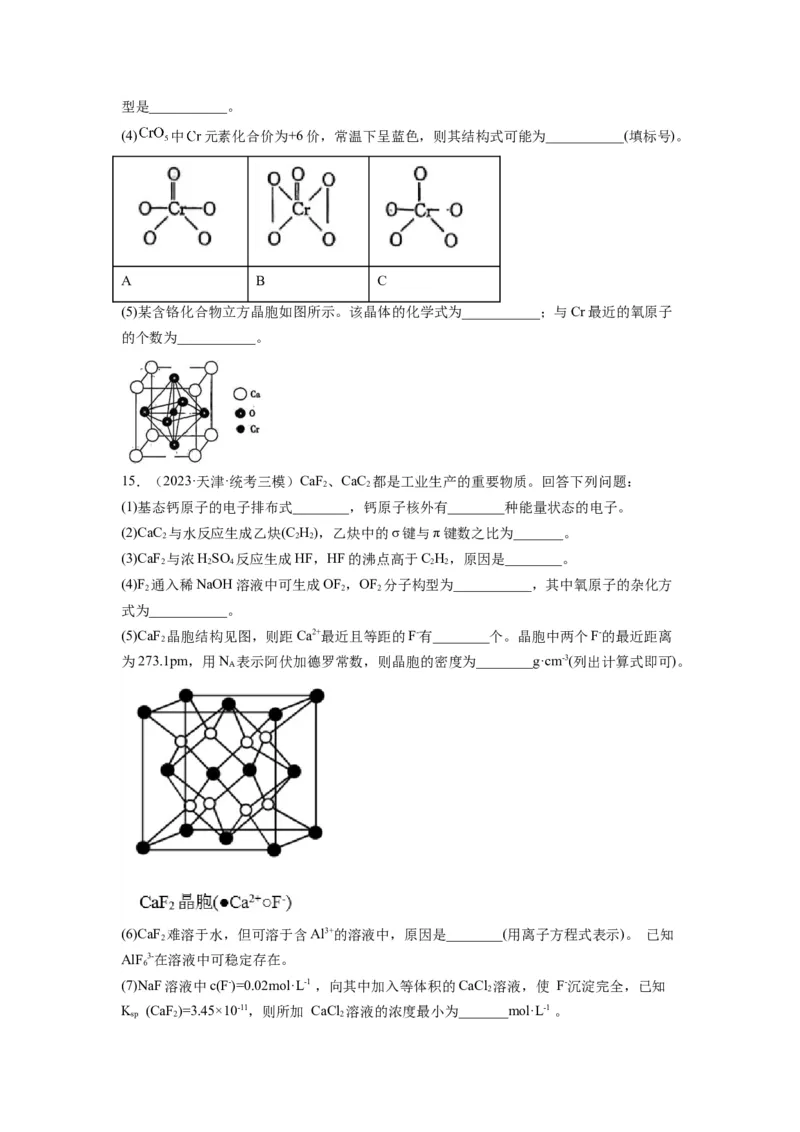
(5)CaF 晶胞结构见图,则距Ca2+最近且等距的F-有________个。晶胞中两个F-的最近距离
2
为273.1pm,用N 表示阿伏加德罗常数,则晶胞的密度为________g·cm-3(列出计算式即可)。
A
(6)CaF 难溶于水,但可溶于含Al3+的溶液中,原因是________(用离子方程式表示)。 已知
2
AlF3-在溶液中可稳定存在。
6
(7)NaF溶液中c(F-)=0.02mol·L-1 ,向其中加入等体积的CaCl 溶液,使 F-沉淀完全,已知
2
K (CaF )=3.45×10-11,则所加 CaCl 溶液的浓度最小为_______mol·L-1 。
sp 2 216.(2023·全国乙卷·统考高考真题)中国第一辆火星车“祝融号”成功登陆火星。探测
发现火星上存在大量橄榄石矿物( )。回答下列问题:
(1)基态 原子的价电子排布式为_______。橄榄石中,各元素电负性大小顺序为_______,
铁的化合价为_______。
(2)已知一些物质的熔点数据如下表:
物质 熔点/℃
800.7
与 均为第三周期元素, 熔点明显高于 ,原因是_______。分析同族元素的
氯化物 、 、 熔点变化趋势及其原因_______。 的空间结构为_______,
其中 的轨道杂化形式为_______。
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投
影图如下所示,晶胞中含有_______个 。该物质化学式为_______,B-B最近距离为
_______。
17.(2023·全国甲卷·统考高考真题)将酞菁—钴钛—三氯化铝复合嵌接在碳纳米管上,
制得一种高效催化还原二氧化碳的催化剂。回答下列问题:
(1)图1所示的几种碳单质,它们互为_______,其中属于原子晶体的是_______, 间的
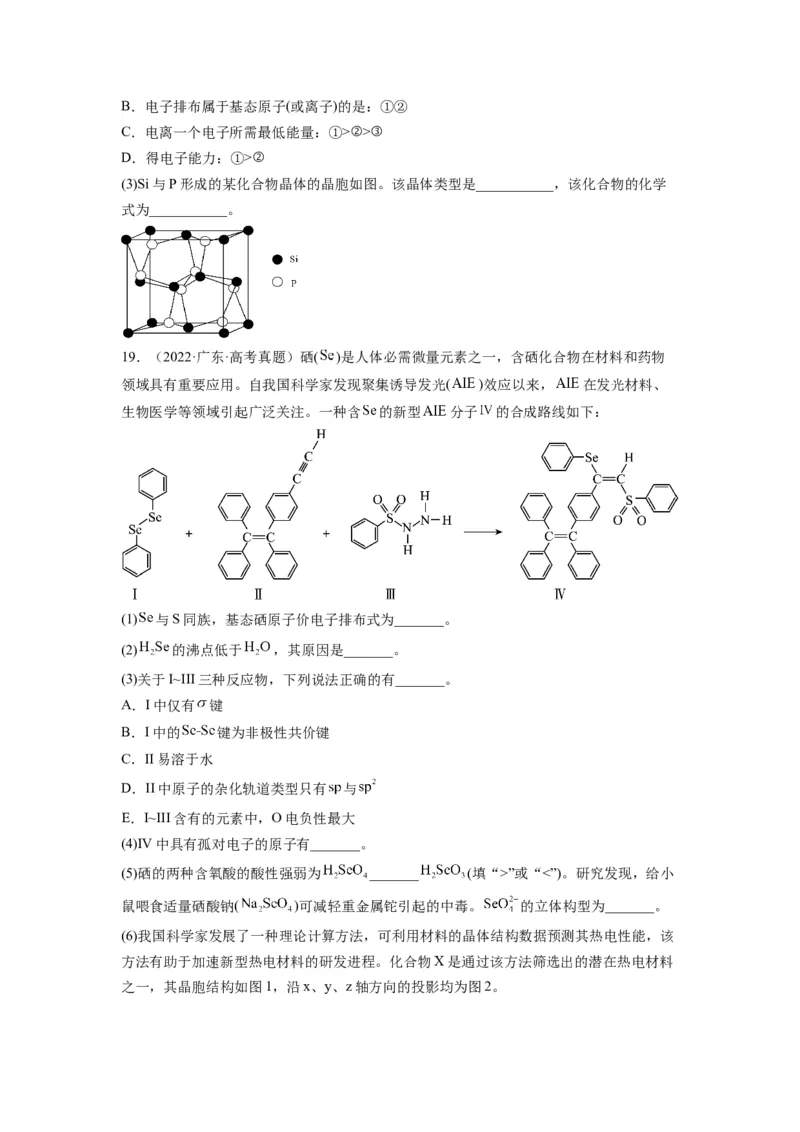
作用力是_______。(2)酞菁和钴酞菁的分子结构如图2所示。
酞菁分子中所有原子共平面,其中 轨道能提供一对电子的 原子是_______(填图2酞菁
中 原子的标号)。钴酞菁分子中,钴离子的化合价为_______,氮原子提供孤对电子与钴
离子形成_______键。
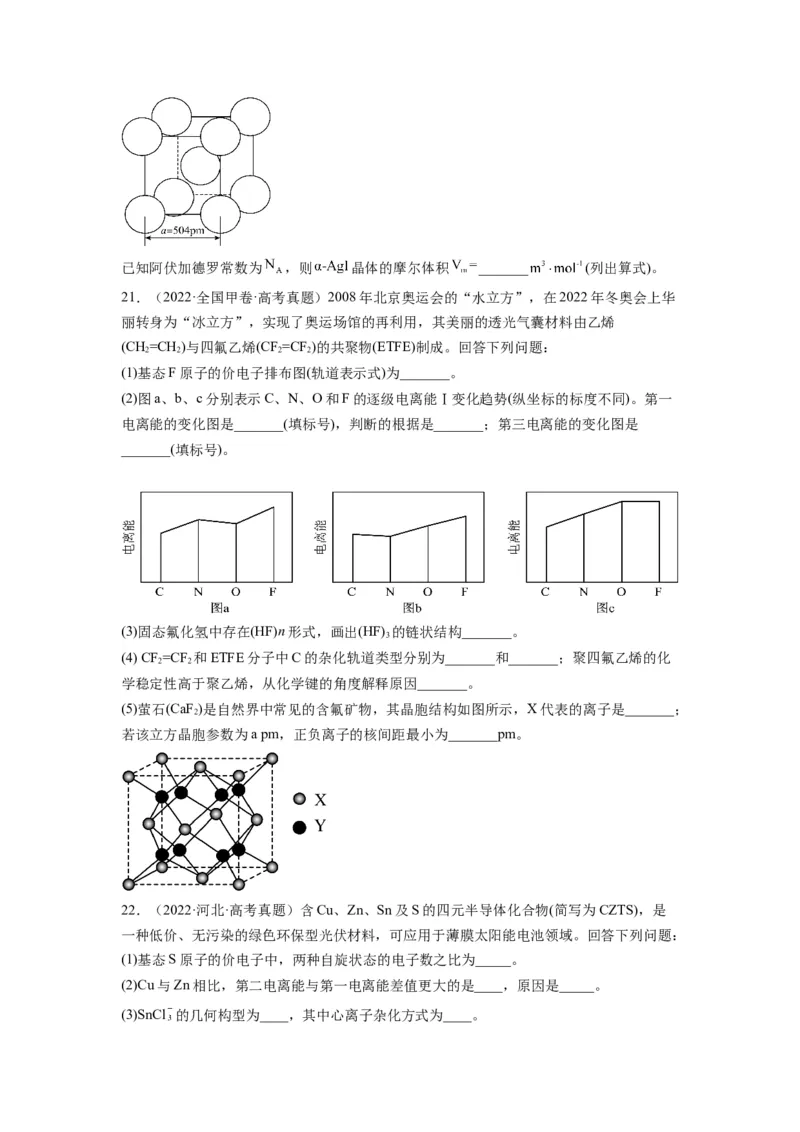
(3)气态 通常以二聚体 的形式存在,其空间结构如图3a所示,二聚体中 的轨
道杂化类型为_______。 的熔点为 ,远高于 的 ,由此可以判断铝氟
之间的化学键为_______键。 结构属立方晶系,晶胞如图3b所示, 的配位数为
_______。若晶胞参数为 ,晶体密度 _______ (列出计算式,阿伏加德罗常数
的值为 )。
18.(2023·浙江·高考真题)硅材料在生活中占有重要地位。请回答:
(1) 分子的空间结构(以 为中心)名称为________,分子中氮原子的杂化轨道类型
是_______。 受热分解生成 和 ,其受热不稳定的原因是________。
(2)由硅原子核形成的三种微粒,电子排布式分别为:① 、② 、③
,有关这些微粒的叙述,正确的是___________。
A.微粒半径:③>①>②B.电子排布属于基态原子(或离子)的是:①②
C.电离一个电子所需最低能量:①>②>③
D.得电子能力:①>②
(3)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是___________,该化合物的化学
式为___________。
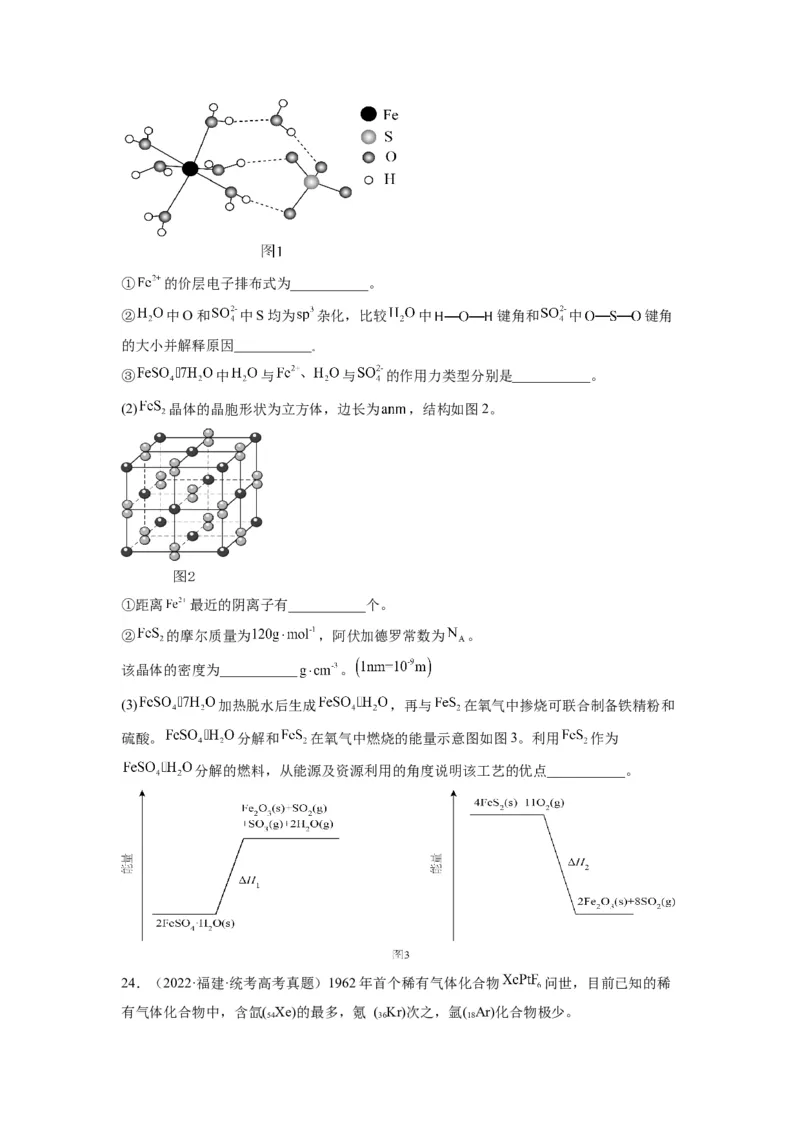
19.(2022·广东·高考真题)硒( )是人体必需微量元素之一,含硒化合物在材料和药物
领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来, 在发光材料、
生物医学等领域引起广泛关注。一种含 的新型 分子 的合成路线如下:
(1) 与S同族,基态硒原子价电子排布式为_______。
(2) 的沸点低于 ,其原因是_______。
(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有 键
B.I中的 键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为 _______ (填“>”或“<”)。研究发现,给小
鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。 的立体构型为_______。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该
方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料
之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为
_______ (列出计算式, 为阿伏加德罗常数的值)。
20.(2022·全国乙卷·统考高考真题)卤素单质及其化合物在科研和工农业生产中有着广
泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a. b. c. d.
(2)①一氯乙烯 分子中,C的一个_______杂化轨道与Cl的 轨道形成
_______键,并且Cl的 轨道与C的 轨道形成3中心4电子的大 键 。
②一氯乙烷 、一氯乙烯 、一氯乙炔 分子中, 键长的顺序是
_______,理由:(ⅰ)C的杂化轨道中s成分越多,形成的 键越强;(ⅱ)_______。
(3)卤化物 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。
解释X的熔点比Y高的原因_______。
(4) 晶体中 离子作体心立方堆积(如图所示), 主要分布在由 构成的四面体、八
面体等空隙中。在电场作用下, 不需要克服太大的阻力即可发生迁移。因此,
晶体在电池中可作为_______。已知阿伏加德罗常数为 ,则 晶体的摩尔体积 _______ (列出算式)。
21.(2022·全国甲卷·高考真题)2008年北京奥运会的“水立方”,在2022年冬奥会上华
丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯
(CH=CH )与四氟乙烯(CF=CF )的共聚物(ETFE)制成。回答下列问题:
2 2 2 2
(1)基态F原子的价电子排布图(轨道表示式)为_______。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一
电离能的变化图是_______(填标号),判断的根据是_______;第三电离能的变化图是
_______(填标号)。
(3)固态氟化氢中存在(HF)n形式,画出(HF) 的链状结构_______。
3
(4) CF =CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的化
2 2
学稳定性高于聚乙烯,从化学键的角度解释原因_______。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______;
2
若该立方晶胞参数为a pm,正负离子的核间距最小为_______pm。
22.(2022·河北·高考真题)含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是
一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_____。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是____,原因是_____。
(3)SnCl 的几何构型为____,其中心离子杂化方式为____。(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列
物质中,属于顺磁性物质的是____(填标号)。
A.[Cu(NH )]Cl B.[Cu(NH )]SO C.[Zn(NH )]SO D.Na[Zn(OH) ]
3 2 3 4 4 3 4 4 2 4
(5)如图是硫的四种含氧酸根的结构:
A. B. C.
D.
根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO 的是____(填标号),理由是
____。
(6)如图是CZTS四元半导体化合物的四方晶胞。
①该物质的化学式为_____。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,
例如图中A原子的坐标为( , , ),则B原子的坐标为_____。
23.(2022·北京·高考真题)工业中可利用生产钛白的副产物 和硫铁矿
联合制备铁精粉 和硫酸,实现能源及资源的有效利用。
(1) 结构示意图如图1。① 的价层电子排布式为___________。
② 中O和 中S均为 杂化,比较 中 键角和 中 键角
的大小并解释原因___________
。
③ 中 与 与 的作用力类型分别是___________。
(2) 晶体的晶胞形状为立方体,边长为 ,结构如图2。
①距离 最近的阴离子有___________个。
② 的摩尔质量为 ,阿伏加德罗常数为 。
该晶体的密度为___________ 。
(3) 加热脱水后生成 ,再与 在氧气中掺烧可联合制备铁精粉和
硫酸。 分解和 在氧气中燃烧的能量示意图如图3。利用 作为
分解的燃料,从能源及资源利用的角度说明该工艺的优点___________。
24.(2022·福建·统考高考真题)1962年首个稀有气体化合物 问世,目前已知的稀
有气体化合物中,含氙( Xe)的最多,氪 ( Kr)次之,氩( Ar)化合物极少。
54 36 18是 与 分子形成的加合物,其晶胞如下图所示。
回答下列问题:
(1)基态 原子的价电子排布式为_______。
(2) 原子的活泼性依序增强,原因是_______。
(3)晶体熔点: _______ (填“>”“<”或“=”),判断依据是_______。
(4) 的中心原子 的杂化轨道类型为_______。
(5) 加合物中 _______,晶体中的微粒间作用力有_____(填标号)。
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
25.(2022·重庆·统考高考真题)配位化合物X由配体L2-(如图)和具有正四面体结构的
[Zn O]6+构成。
4
(1)基态Zn2+的电子排布式为______。
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为
______形;每个L2-中采取sp2杂化的C原子数目为______个,C与O之间形成σ键的数目
为______个。
(3)X晶体内部空腔可吸附小分子,要增强X与HO的吸附作用,可在L2-上引入______。
2
(假设X晶胞形状不变)。
A.-Cl B.-OH C.-NH D.-CH
2 3
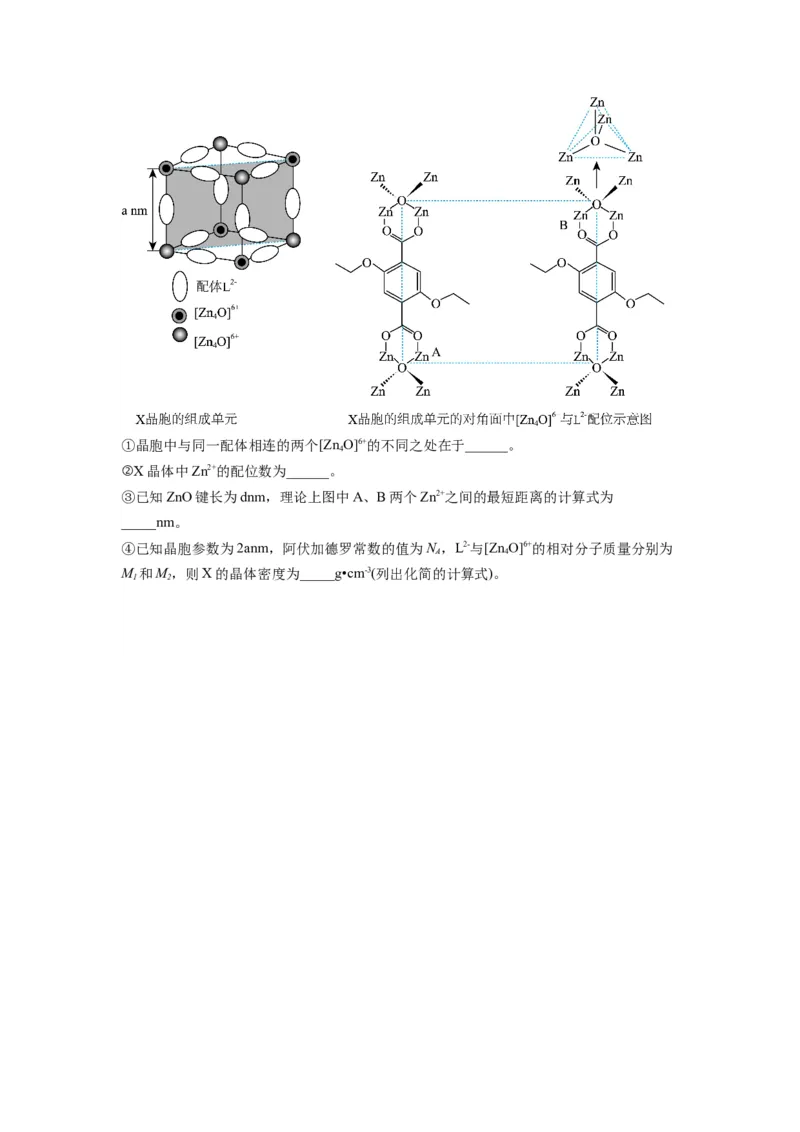
(4)X晶体具有面心立方结构,其晶胞由8个结构相似的组成单元(如图)构成。①晶胞中与同一配体相连的两个[Zn O]6+的不同之处在于______。
4
②X晶体中Zn2+的配位数为______。
③已知ZnO键长为dnm,理论上图中A、B两个Zn2+之间的最短距离的计算式为
_____nm。
④已知晶胞参数为2anm,阿伏加德罗常数的值为N ,L2-与[Zn O]6+的相对分子质量分别为
A 4
M 和M,则X的晶体密度为_____g•cm-3(列出化简的计算式)。
1 2