文档内容
第二十一讲 化学能与热能
【基础巩固】
1.(2022·济南高三月考)下列说法正确的是( )
A.焓的大小受体系的温度、压强等因素的影响
B.化学反应的反应热等于反应前后焓的变化
C.浓硫酸溶于水是放热反应
D.煤的液化有利于实现碳达峰、碳中和
【答案】 A
【解析】 等压条件下,化学反应的反应热等于反应的焓变,B错误;浓硫酸溶于水是物理变化,C错误;
煤的液化能提高煤的能量利用率,但CO 气体的排放量不变,D错误。
2
2.“太阳能燃料”国际会议于2019年10月在我国武汉举行,旨在交流和探讨太阳能光催化分解水制氢、
太阳能光催化二氧化碳转化为燃料等问题。下列说法错误的是( )
A.太阳能燃料属于一次能源
B.直接电催化CO 制取燃料时,燃料是阴极产物
2
C.光催化分解水产生的H 是理想的绿色能源
2
D.研发和利用太阳能燃料,有利于经济的可持续发展
【答案】 A
【解析】 太阳能燃料属于二次能源,故A错误;直接电催化CO 制取燃料时,C元素化合价降低,在阴
2
极反应,故B正确;光催化分解水产生H,H 燃烧放出的热量多,产物为HO,无污染,故C正确;太阳
2 2 2
能燃料可重复利用,避免对环境造成污染,故D正确。
3.(2023·太原检测)分别向1 L 0.5 mol·L-1的Ba(OH) 溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完
2
全反应时的热效应分别为ΔH、ΔH、ΔH,下列关系正确的是( )
1 2 3
A.ΔH>ΔH>ΔH B.ΔH<ΔH<ΔH
1 2 3 1 2 3
C.ΔH>ΔH=ΔH D.ΔH=ΔH<ΔH
1 2 3 1 2 3
【答案】 B
【解析】 混合时浓硫酸在被稀释的过程中放热;浓、稀硫酸在与 Ba(OH) 反应时还会形成BaSO 沉淀,
2 4
Ba2+、SO之间形成化学键的过程中也会放出热量。因放热反应的ΔH取负值,故ΔH<ΔH<ΔH。
1 2 3
4.我国学者研究了在金催化剂表面上水煤气变换的反应历程,如图所示(其中吸附在金催化剂表面上的物种
用标注)
资料整理【淘宝店铺:向阳百分百】下列说法不正确的是( )
A.催化剂能够改变反应历程
B.H O*转化为 H*和OH*时需要吸收能量
2
C.反应过程中,过渡态1比过渡态2更难达到
D.总反应方程式为CO(g)+HO(g)===CO (g)+H(g) ΔH=-0.72N eV/mol
2 2 2 A
【答案】 C
【解析】 A.由反应历程图可知,在过渡态中,催化剂能够改变反应过程中的相对能量,改变的是反应的
历程,但是最终反应物和生成物不会改变,故A正确;B.根据反应历程图可知,CO*+HO(g)+HO*的能
2 2
垒为-0.32 eV;CO*+HO(g)+ H*+OH*的能垒为1.25 eV,所以HO*转化为 H*和OH*时需要吸收能量,
2 2
故B正确;C.由反应历程图可知,反应过程中生成过渡态1比过渡态2的能垒小,所以过渡态1反应更容
易,故C错误;D.根据反应历程图可知,整个反应历程中1 mol CO(g)和2 mol H O(g)生成1 mol CO (g)和1
2 2
mol HO(g)和1 mol H (g)时,放出0.72 N eV的能量,而ΔH为每1 mol反应对应的能量变化,所以该反
2 2 A
应的总反应方程式为CO(g)+HO(g)===CO (g)+H(g) ΔH=-0.72N eV/mol,故D正确。
2 2 2 A
5.分别取40 mL 的0.50 mol·L-1盐酸与40 mL 0.55 mol·L-1氢氧化钠溶液进行中和反应反应热的测定实验。
下列说法错误的是( )
A.稍过量的氢氧化钠是确保盐酸完全反应
B.仪器A的名称是环形玻璃搅拌棒
C.在实验过程中,把温度计上的酸用水冲洗干净后再测量NaOH溶液的温度
D.用硫酸和Ba(OH) 溶液代替盐酸和氢氧化钠溶液,结果也是正确的
2
【答案】 D
资料整理【淘宝店铺:向阳百分百】【解析】 测定中和热时,为了使盐酸完全反应,需要让 NaOH稍过量,A项正确;仪器A是环形玻璃搅
拌棒,B项正确;温度计上残留的酸溶液需要清洗干净,否则会和 NaOH溶液反应,使测得NaOH溶液的
温度偏高,C项正确;用硫酸和Ba(OH) 溶液代替盐酸和氢氧化钠溶液,除了发生中和反应,还生成了
2
BaSO 沉淀(生成沉淀的过程放热),因此会影响中和热的测定,D项错误。
4
6.(2022·湖北重点中学高三质检)设N 为阿伏加德罗常数的值。已知反应;
A
①C H(g)+3O(g)===2CO (g)+2HO(g) ΔH=-a kJ·mol-1
2 4 2 2 2 1
②C H(g)+3O(g)===2CO (g)+2HO(l) ΔH=-b kJ·mol-1
2 4 2 2 2 2
其他数据如下表:
化学键 C===O O===O C—H O—H C===C
键能/(kJ·mol-1) 798 x 413 463 610
下列说法正确的是( )
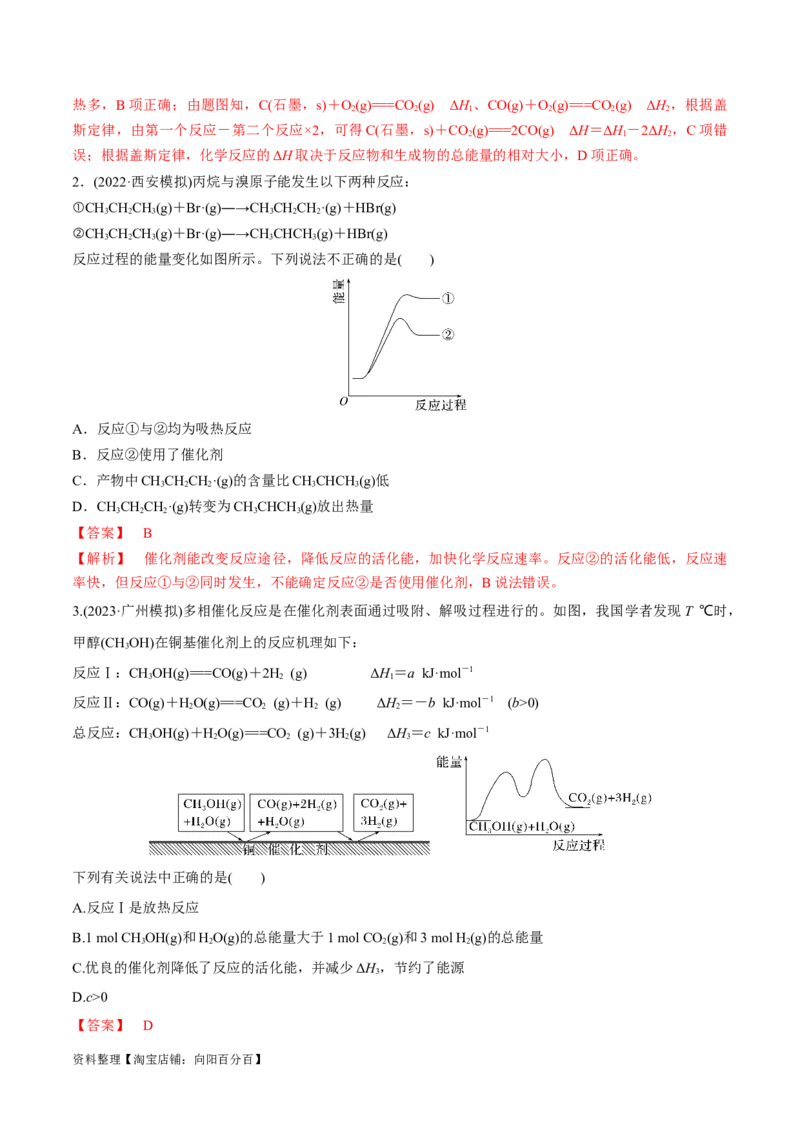
A.a0)
2 2 2 2
总反应:CHOH(g)+HO(g)===CO (g)+3H(g) ΔH=c kJ·mol-1
3 2 2 2 3
下列有关说法中正确的是( )
A.反应Ⅰ是放热反应
B.1 mol CH OH(g)和HO(g)的总能量大于1 mol CO (g)和3 mol H (g)的总能量
3 2 2 2
C.优良的催化剂降低了反应的活化能,并减少ΔH,节约了能源
3
D.c>0
【答案】 D
资料整理【淘宝店铺:向阳百分百】【解析】 根据图像可知反应Ⅰ生成物能量大于反应物能量,因此为吸热反应,故 A错误;根据图像可知
1 mol CH OH(g)和1 mol H O(g)的总能量小于1 mol CO (g)和3 mol H (g)的总能量,故B错误;
3 2 2 2
优良的催化剂降低了反应的活化能,焓变不变,焓变只能由反应物和生成物总能量决定,故C错误;1 mol
CHOH(g)和1 mol H O(g)的总能量小于1 mol CO (g)和3 mol H (g)的总能量,是吸热反应,因此
3 2 2 2
c>0,故D正确。
4.(2022·泉州质监)N 转化为NO的过程如图所示。下列说法正确的是( )
2
A.催化剂a和b可增大反应的活化能(E)
a
B.在催化剂b作用下,氮元素发生了还原反应
C.催化剂a、b不会改变反应的焓变(ΔH)
D.催化剂b可提高NH 的平衡转化率
3
【答案】 C
【解析】 由题图知,催化剂a、b能降低反应的活化能,加快化学反应速率,A项错误;在催化剂b作用
下,NH 转化为NO,氮元素由-3价升高为+2价,发生氧化反应,B项错误;化学反应的焓变与反应物
3
和生成物的总能量有关,催化剂只降低反应的活化能,不能改变反应的焓变,C项正确;催化剂不影响化
学平衡移动,不能提高NH 的平衡转化率,D项错误。
3
5.(2022·重庆育才中学模拟)甲烷分子结构具有高度对称性,且断开1 mol C—H需要吸收
440 kJ能量。无催化剂作用下,甲烷在温度达到1 200 ℃以上才可裂解。在催化剂及一定条件下,CH 可在
4
较低温度下发生裂解反应,甲烷在镍基催化剂上转化过程中的能量变化如图所示。下列说法正确的是(
)
A.催化剂使用一段时间后失活的原因可能是碳在催化剂表面沉积
B.步骤②③反应均为吸热反应
C.1 mol甲烷催化裂解成C和H 的ΔH=+1 760 kJ·mol-1
2
资料整理【淘宝店铺:向阳百分百】D.使用该催化剂,反应的焓变减小
【答案】 A
【解析】 由题中图示可知,C可吸附在催化剂的表面,则催化剂使用一段时间后失活的原因可能是碳在
催化剂表面沉积,A正确;由题中图示可知,步骤②③反应物总能量都大于生成物总能量,B错误;CH
4
存在4个C—H,断开4 mol C—H需要吸收的能量为440 kJ×4=1 760 kJ,但不是甲烷催化裂解成C和H
2
需要吸收的能量,C错误;加入催化剂,反应的路径改变,但反应的焓变不变,D错误。
6.(2021·浙江6月选考,21)相同温度和压强下,关于反应的ΔH,下列判断正确的是( )
(g)+H(g)―→ (g) ΔH
2 1
(g)+2H(g)―→ (g) ΔH
2 2
(g)+3H(g)―→ (g) ΔH
2 3
(g)+H(g)―→ (g) ΔH
2 4
A.ΔH>0,ΔH>0
1 2
B.ΔH=ΔH+ΔH
3 1 2
C.ΔH>ΔH,ΔH>ΔH
1 2 3 2
D.ΔH=ΔH+ΔH
2 3 4
【答案】 C
【解析】 环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此,ΔH <0,ΔH <0 ,A
1 2
不正确;苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊的共价键,因此,其与氢气
完全加成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生的加成反应的反应热之和,即ΔH≠ΔH +
3 1
ΔH ,B不正确;由于1 mol 1,3-环己二烯与氢气完全加成后消耗的氢气是等量环己烯的2倍,故其放出的
2
热量更多,则ΔH>ΔH ;苯与氢气发生加成反应生成1,3-环己二烯的反应为吸热反应(ΔH>0),根据盖斯定
1 2 4
律可知,苯与氢气完全加成的反应热:ΔH =ΔH +ΔH ,因此ΔH>ΔH ,ΔH =ΔH -ΔH ,C正确、D不
3 4 2 3 2 2 3 4
正确。
7.Li/Li O体系的能量循环如图所示。下列说法正确的是( )
2
A.ΔH<0
3
资料整理【淘宝店铺:向阳百分百】B.ΔH+ΔH+ΔH=ΔH
3 4 5 6
C.ΔH>ΔH
6 5
D.ΔH+ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5 6
【答案】 C
【解析】 O 的气态分子变为气态原子,需要断裂分子中的化学键,因此要吸收能量,ΔH>0,A项错误;
2 3
物质含有的能量只与物质的始态与终态有关,与反应途径无关,根据物质转化关系可知,ΔH +ΔH +ΔH
1 2 3
+ΔH+ΔH=ΔH,B、D两项错误。
4 5 6
8.(2023·全国·统考高考真题)“肼合成酶”以其中的 配合物为催化中心,可将 与 转化
为肼( ),其反应历程如下所示。
下列说法错误的是
A. 、 和 均为极性分子
B.反应涉及 、 键断裂和 键生成
C.催化中心的 被氧化为 ,后又被还原为
D.将 替换为 ,反应可得
【答案】 D
【解析】 A.NH OH,NH ,HO的电荷分布都不均匀,不对称,为极性分子,A正确;B.由反应历
2 3 2
程可知,有N-H,N-O键断裂,还有N-H键的生成,B正确;C.由反应历程可知,反应过程中,
Fe2+先失去电子发生氧化反应生成Fe3+,后面又得到电子生成Fe2+,C正确;D.由反应历程可知,反应过
程中,生成的NH NH 有两个氢来源于NH ,所以将NH OH替换为ND OD,不可能得到ND ND ,得到
2 2 3 2 2 2 2
ND NH 和HDO,D错误;故选D。
2 2
9.(2023·浙江·统考高考真题)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如
下:
资料整理【淘宝店铺:向阳百分百】反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
【答案】 C
【详解】 A.反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于反应Ⅱ放出的热量,
反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,故A正确;B.短时间里反应I得到
的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速率越快,其活化能越小,则反应
活化能:反应I<反应Ⅱ,故B正确;C.增加 浓度,平衡正向移动,但平衡时产物Ⅱ和产物I的比例
可能降低,故C错误;D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,
故D正确。综上所述,答案为C。
10.(2022·重庆·统考高考真题)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH )SO 的
4 2 4
离子键强弱,设计如图所示的循环过程,可得△H/(kJ•mol-1)为
4
A.+838 B.+686 C.+533 D.+1143
【答案】 A
【解析】① ;② ;③
资料整理【淘宝店铺:向阳百分百】;④ ;⑤
;⑥ ;则⑤+①-⑥-
②+③得④,得到 +838 kJ•mol-1 所以B、C、D错误, C正确,故选A。
,
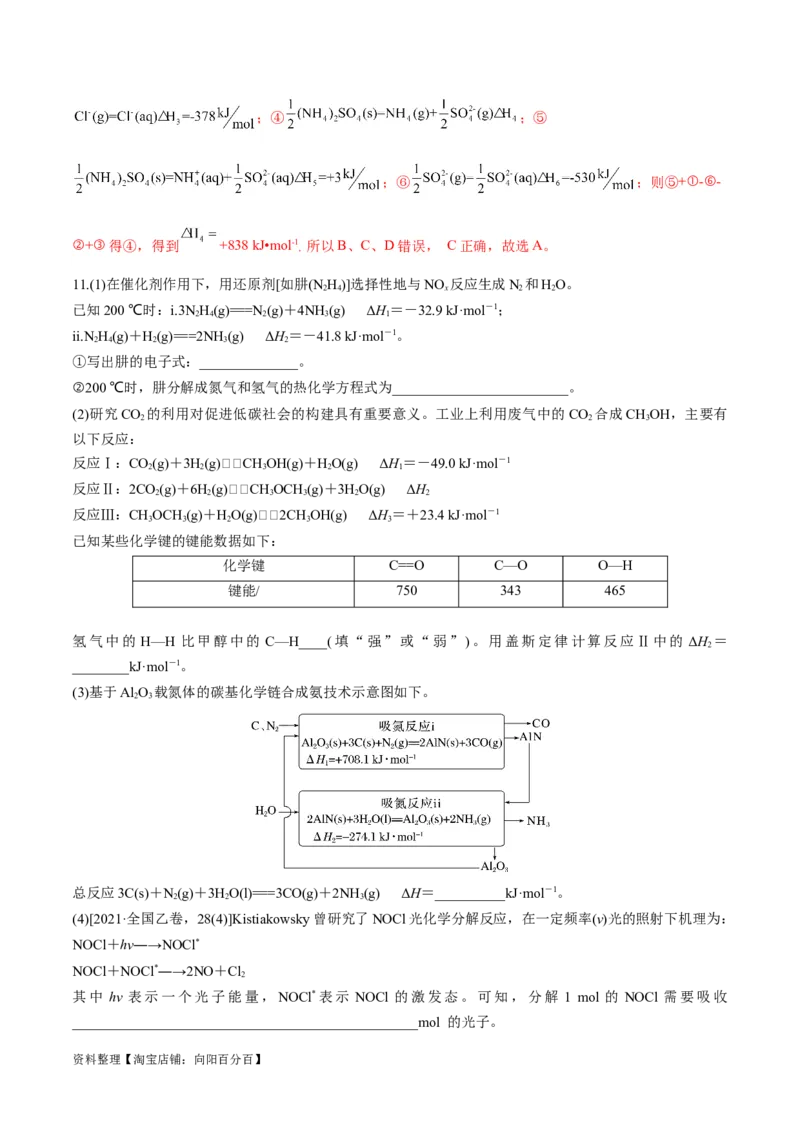
11.(1)在催化剂作用下,用还原剂[如肼(N H)]选择性地与NO 反应生成N 和HO。
2 4 x 2 2
已知200 ℃时:i.3N H(g)===N (g)+4NH (g) ΔH=-32.9 kJ·mol-1;
2 4 2 3 1
ii.NH(g)+H(g)===2NH(g) ΔH=-41.8 kJ·mol-1。
2 4 2 3 2
①写出肼的电子式:______________。
②200 ℃时,肼分解成氮气和氢气的热化学方程式为_________________________。
(2)研究CO 的利用对促进低碳社会的构建具有重要意义。工业上利用废气中的CO 合成CHOH,主要有
2 2 3
以下反应:
反应Ⅰ:CO(g)+3H(g)CH OH(g)+HO(g) ΔH=-49.0 kJ·mol-1
2 2 3 2 1
反应Ⅱ:2CO(g)+6H(g)CH OCH (g)+3HO(g) ΔH
2 2 3 3 2 2
反应Ⅲ:CHOCH (g)+HO(g)2CHOH(g) ΔH=+23.4 kJ·mol-1
3 3 2 3 3
已知某些化学键的键能数据如下:
化学键 C==O C—O O—H
键能/ 750 343 465
氢气中的 H—H 比甲醇中的 C—H____(填“强”或“弱”)。用盖斯定律计算反应Ⅱ中的 ΔH =
2
________kJ·mol-1。
(3)基于Al O 载氮体的碳基化学链合成氨技术示意图如下。
2 3
总反应3C(s)+N(g)+3HO(l)===3CO(g)+2NH (g) ΔH=__________kJ·mol-1。
2 2 3
(4)[2021·全国乙卷,28(4)]Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(ν)光的照射下机理为:
NOCl+hν―→NOCl*
NOCl+NOCl*―→2NO+Cl
2
其中 hν 表示一个光子能量,NOCl*表示 NOCl 的激发态。可知,分解 1 mol 的 NOCl 需要吸收
_________________________________________________mol 的光子。
资料整理【淘宝店铺:向阳百分百】【答案】 (1)① ②NH(g)===N (g)+2H(g) ΔH=+50.7 kJ·mol-1
2 4 2 2
(2)强 -121.4
(3)+434.0 (4)0.5
【解析】 (1)②根据盖斯定律i-2×ii得肼分解成氮气和氢气的热化学方程式:NH(g)===N (g)+2H(g)
2 4 2 2
ΔH=-32.9 kJ·mol-1-(-41.8 kJ·mol-1)×2=+50.7 kJ·mol-1。
(2)ΔH=反应物的总键能-生成物的总键能,根据反应Ⅰ,ΔH =2E +3E -(3E +E +3E ),
1 C=O H—H C—H C-O O—H
代入题表数据可得E -E =63 kJ·mol-1>0,故氢气中的H—H比甲醇中的C—H强。根据盖斯定律可
H—H C—H
知,反应Ⅱ=反应Ⅰ×2-反应Ⅲ,故ΔH=2ΔH-ΔH=
2 1 3
-121.4 kJ·mol-1。
(3)将反应ⅰ和反应ⅱ相加,即可得到总反应3C(s)+N(g)+3HO(l)===3CO(g)+2NH (g) ΔH=+708.1
2 2 3
kJ·mol-1+(-274.1 kJ·mol-1)=+434.0 kJ·mol-1
(4)Ⅰ.NOCl+hν―→NOCl*
Ⅱ.NOCl+NOCl*―→2NO+Cl
2
Ⅰ+Ⅱ得总反应为2NOCl+hν―→2NO+Cl ,因此分解2 mol NOCl需要吸收1 mol光子能量,则分解1
2
mol的NOCl需要吸收0.5 mol的光子。
12.(1)已知CHOH(l)的燃烧热 ΔH=-726.5 kJ·mol-1,CHOH(l)+O(g)===CO (g)+2H(g) ΔH=-a
3 3 2 2 2
kJ·mol-1,则a (填“>”“<”或“=”)726.5。
(2)将Cl 和HO(g)通过灼热的炭层,生成HCl和CO ,当有1 mol Cl 参与反应时释放出145.0 kJ热量,写
2 2 2 2
出该反应的热化学方程式: 。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物
质可作耐高温材料:4Al(s)+3TiO(s)+3C(s)===2AlO(s)+3TiC(s) ΔH=
2 2 3
-1 176.0 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为 。
(4)CO 与H 在某催化剂的作用下反应如图所示:
2 2
化学键
键能/ (kJ·mol-1) 436 326 803 464 414
写出该反应的热化学方程式: 。
(5)CO 催化加氢制CHOH的一种反应历程如图所示(吸附在催化剂表面的物质用*标注,如CO表示CO 吸
2 3 2
附在催化剂表面)。
资料整理【淘宝店铺:向阳百分百】该反应历程中决速步反应的化学方程式为 。
【答案】 (1)< (2)2Cl (g)+2HO(g)+C(s)===4HCl(g)+CO(g) ΔH=-290.0 kJ·mol-1 (3)98.0 kJ
2 2 2
(4)CO (g)+3H(g)===CH OH(g)+HO(g) ΔH=-46 kJ·mol-1
2 2 3 2
(5)CO (g)+2H*+2H(g)===COOH*+H*+2H(g)[或CO(g)+2H*===COOH*+H*或CO(g)+H*===COOH*]
2 2 2 2 2
【解析】 (1)所述反应未完全燃烧,生成的氢气燃烧还要放出热量,则a<726.5。
(2)当有 1 mol Cl 参与反应时释放出 145.0 kJ 热量,该反应的热化学方程式:2Cl(g)+2HO(g)+
2 2 2
C(s)===4HCl(g)+CO(g) ΔH=-145.0 kJ·mol-1×2=-290.0 kJ·mol-1。
2
(3)4Al(s)+3TiO(s)+3C(s)===2AlO(s)+3TiC(s) ΔH=-1 176.0 kJ·mol-1,每转移12 mol电子放出的热量
2 2 3
为1 176.0 kJ,则反应过程中,每转移1 mol电子放出的热量为 kJ= 98.0 kJ。
(4)由反应图示可知图形与化学键对应关系为
H—H C—O C==O O—H C—H
ΔH=反应物总键能-生成物总键能=2×803 kJ·mol-1+3×436 kJ·mol-1-3×414 kJ·mol-1-326 kJ·mol-1-
3×464 kJ·mol-1=-46 kJ·mol-1。
(5)据图可知CO(g)+2H*+2H(g)===COOH*+H*+2H(g)活化能最大,是决速步骤。
2 2 2
13.(2023·北京·统考高考真题)尿素 合成的发展体现了化学科学与技术的不断进步。
(1)十九世纪初,用氰酸银 与 在一定条件下反应制得 ,实现了由无机物到有机
物的合成。该反应的化学方程式是 。
(2)二十世纪初,工业上以 和 为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ. 和 生成 ;
ⅱ. 分解生成尿素。
资料整理【淘宝店铺:向阳百分百】结合反应过程中能量变化示意图,下列说法正确的是 (填序号)。
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.
(3)近年研究发现,电催化 和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮
废水污染问题。向一定浓度的 溶液通 至饱和,在电极上反应生成 ,电解原理如图所
示。
①电极 是电解池的 极。
②电解过程中生成尿素的电极反应式是 。
(4)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用 溶液准确滴定。
资料整理【淘宝店铺:向阳百分百】①消化液中的含氮粒子是 。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为 和 ,计算样品含氮量还需要的实验数据有
。
【答案】(1) (2)ab
(3) 阳
(4) 样品的质量、步骤Ⅲ所加入 溶液的体积和浓度
【解析】(1)根据原子守恒分析,二者反应生成尿素和氯化银,化学方程式是
。答案为 ;(2)a.反应ⅰ的活
化能是 ,反应ⅱ活化能是 , ,a项正确;b.从图中反应物和生成物能量的相对大小可看出反应
ⅰ放热,反应ⅱ吸热,b项正确;c.总反应的: ,c项错误;故选ab。(3)①电极b上
发生 失电子生成 的氧化反应,是电解池的阳极。②a极硝酸根离子得电子转化为尿素,再结合酸性
环境可分析出电极反应式为 。答案为阳极;
;(4)①尿素消化分解生成 和 ,由于反应中存在
浓 ,则消化液中含氮粒子为 。②除了已知数据外,还需要的是样品的质量、步骤ⅲ所加入
溶液的体积和浓度。答案为 ;样品的质量、步骤Ⅲ所加入HSO 溶液的体积和浓度。
2 4
资料整理【淘宝店铺:向阳百分百】资料整理【淘宝店铺:向阳百分百】