文档内容
第 24 讲 水的电离和溶液的 pH
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查影响水电离平衡的因素及结果判断
高频考点2 考查水电离出的c(H+)和c(OH-)及K 的应用的计算
W
高频考点3 考查混合溶液酸碱性的判断
高频考点4 考查溶液pH的计算
高频考点5 考查中和滴定仪器、指示剂的选择及滴定终点的规范描述
高频考点6 考查滴定终点的规范描述
高频考点7 考查中和滴定的数据处理及误差分析
高频考点8 考查酸碱中和滴定曲线分析
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆知识点一 水的电离与水的离子积常数
1.水的电离
(1)水是极弱的电解质
①水的电离方程式为HO+HO HO++OH-简写为HO H++OH-。
2 2 3 2
②水的电离常数表达式K=。
(2)水的电离过程吸热
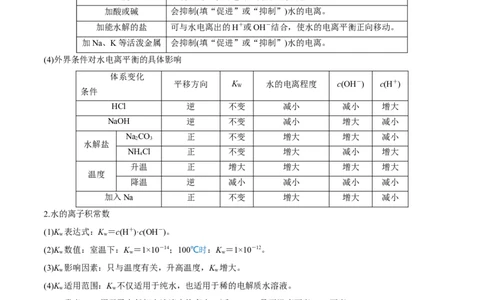
(3)影响水的电离平衡的因素
温度 温度升高,水的电离平衡向正方向移动。
加酸或碱 会抑制(填“促进”或“抑制”)水的电离。
加能水解的盐 可与水电离出的H+或OH-结合,使水的电离平衡正向移动。
加Na、K等活泼金属 会抑制(填“促进”或“抑制”)水的电离。
(4)外界条件对水电离平衡的具体影响
体系变化
平移方向 K 水的电离程度 c(OH-) c(H+)
W
条件
HCl 逆 不变 减小 减小 增大
NaOH 逆 不变 减小 增大 减小
NaCO 正 不变 增大 增大 减小
2 3
水解盐
NH Cl 正 不变 增大 减小 增大
4
升温 正 增大 增大 增大 增大
温度
降温 逆 减小 减小 减小 减小
加入Na 正 不变 增大 增大 减小
2.水的离子积常数
(1)K 表达式:K =c(H+)·c(OH-)。
w w
(2)K 数值:室温下:K =1×10-14;100℃时:K =1×10-12。
w w w
(3)K 影响因素:只与温度有关,升高温度,K 增大。
w w
(4)K 适用范围:K 不仅适用于纯水,也适用于稀的电解质水溶液。
w w
(5)K 意义:K 揭示了在任何水溶液中均存在H+和OH-,只要温度不变,K 不变。
w w w
【易错警示】(1)在不同溶液中,c(H+)、c(OH-)可能不同,但任何溶液中由水电离产生的c(H+)、c(OH-)总是相
等的。在Kw的表达式中,c(H+)、c(OH-)均表示整个溶液中H+、OH-总的物质的量浓度而不是单指由水电离
出的c(H+)、c(OH-)。
(2)水的离子积常数显示了在任何水溶液中均存在水的电离平衡,都有H+和OH-共存,只是相对含量不同而已。
(3)水的电离是吸热过程,升高温度,水的电离平衡向电离方向移动,c(H+)和c(OH-)都增大,故Kw增大,但溶液仍
呈中性;对于Kw,若未注明温度,一般认为在常温下,即25 ℃。知识点二 溶液的酸碱性和pH
1.溶液的酸碱性
溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小。
【易错提醒】溶液显酸碱性的实质是溶液中c(H+)与c(OH-)的相对大小。利用c(H+)大于、小于或等于
1×10-7 mol·L-1或pH大于、小于或等于7来判断溶液的酸碱性,利用pH判断前提条件是在常温下。
2.pH及其测量
(1)计算公式:pH=-lg c(H+)。
(2)测量方法
①pH试纸法:用镊子夹取一小块试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液点在试纸的中
央,变色后与标准比色卡对照,即可确定溶液的pH。
【易错提醒】1.使用pH试纸测溶液pH时用蒸馏水润湿相当于将待测液稀释;
2.不能用pH试纸测定“漂白性”溶液的pH;
3.使用pH试纸测溶液的pH,读数只读取整数,如pH=2;
4.pH的使用范围0~14。
②pH计测量法
(3)溶液的酸碱性与pH的关系(常温下):
3.溶液pH的计算
(1)单一溶液的pH计算
强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)=-lg (nc)。
n
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lg c(H+)=14+lg (nc)。
n
(2)混合溶液pH的计算类型
①两种强酸混合:直接求出c(H+) ,再据此求pH。c(H+) =。
混 混
②两种强碱混合:先求出c(OH-) ,再据K 求出c(H+) ,最后求pH。c(OH-) =。
混 w 混 混
③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。
c(H+) 或c(OH-) =。
混 混
【规律总结】1.稀释规律:酸、碱溶液稀释相同倍数时,强电解质溶液比弱电解质溶液的pH变化幅度大,
但不管稀释多少倍,最终都无限接近中性。
2.酸碱混合规律(1)等浓度等体积一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”。
(2)25 ℃时,等体积pH之和等于14的一强一弱酸碱混合溶液——“谁弱谁过量,谁弱显谁性”。
(3)强酸、强碱等体积混合(25 ℃时)
①pH之和等于14呈中性;
②pH之和小于14呈酸性;
③pH之和大于14呈碱性。
知识点三 酸碱中和滴定
1.实验原理
(1)用已知浓度的酸(或碱)滴定未知浓度的碱(或酸),根据中和反应的等量关系来测定酸(或碱)的浓度。
(2)利用酸碱指示剂明显的颜色变化,表示反应已完全,指示滴定终点。
(3)酸碱中和滴定的关键:
①准确测定标准液和待测液的体积;
②准确判断滴定终点。
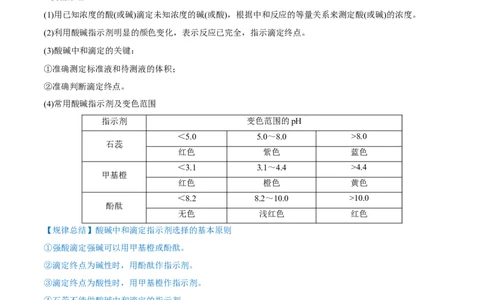
(4)常用酸碱指示剂及变色范围
指示剂 变色范围的pH
<5.0 5.0~8.0 >8.0
石蕊
红色 紫色 蓝色
<3.1 3.1~4.4 >4.4
甲基橙
红色 橙色 黄色
<8.2 8.2~10.0 >10.0
酚酞
无色 浅红色 红色
【规律总结】酸碱中和滴定指示剂选择的基本原则
①强酸滴定强碱可以用甲基橙或酚酞。
②滴定终点为碱性时,用酚酞作指示剂。
③滴定终点为酸性时,用甲基橙作指示剂。
④石蕊不能做酸碱中和滴定的指示剂。
2.实验用品
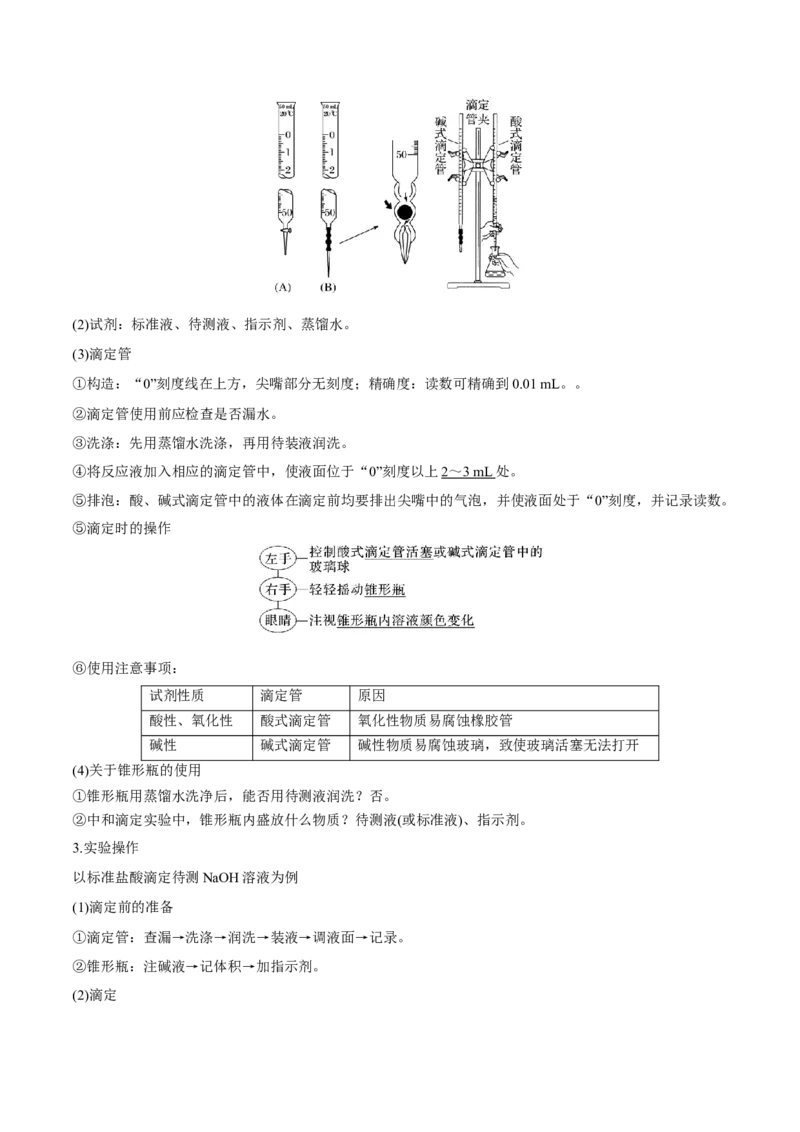
(1)仪器
图(A)是酸式滴定管、图(B)是碱式滴定管、滴定管夹、铁架台、锥形瓶。(2)试剂:标准液、待测液、指示剂、蒸馏水。
(3)滴定管
①构造:“0”刻度线在上方,尖嘴部分无刻度;精确度:读数可精确到0.01 mL。。
②滴定管使用前应检查是否漏水。
③洗涤:先用蒸馏水洗涤,再用待装液润洗。
④将反应液加入相应的滴定管中,使液面位于“0”刻度以上 2 ~ 3 mL 处。
⑤排泡:酸、碱式滴定管中的液体在滴定前均要排出尖嘴中的气泡,并使液面处于“0”刻度,并记录读数。
⑤滴定时的操作
⑥使用注意事项:
试剂性质 滴定管 原因
酸性、氧化性 酸式滴定管 氧化性物质易腐蚀橡胶管
碱性 碱式滴定管 碱性物质易腐蚀玻璃,致使玻璃活塞无法打开
(4)关于锥形瓶的使用
①锥形瓶用蒸馏水洗净后,能否用待测液润洗?否。
②中和滴定实验中,锥形瓶内盛放什么物质?待测液(或标准液)、指示剂。
3.实验操作
以标准盐酸滴定待测NaOH溶液为例
(1)滴定前的准备
①滴定管:查漏→洗涤→润洗→装液→调液面→记录。
②锥形瓶:注碱液→记体积→加指示剂。
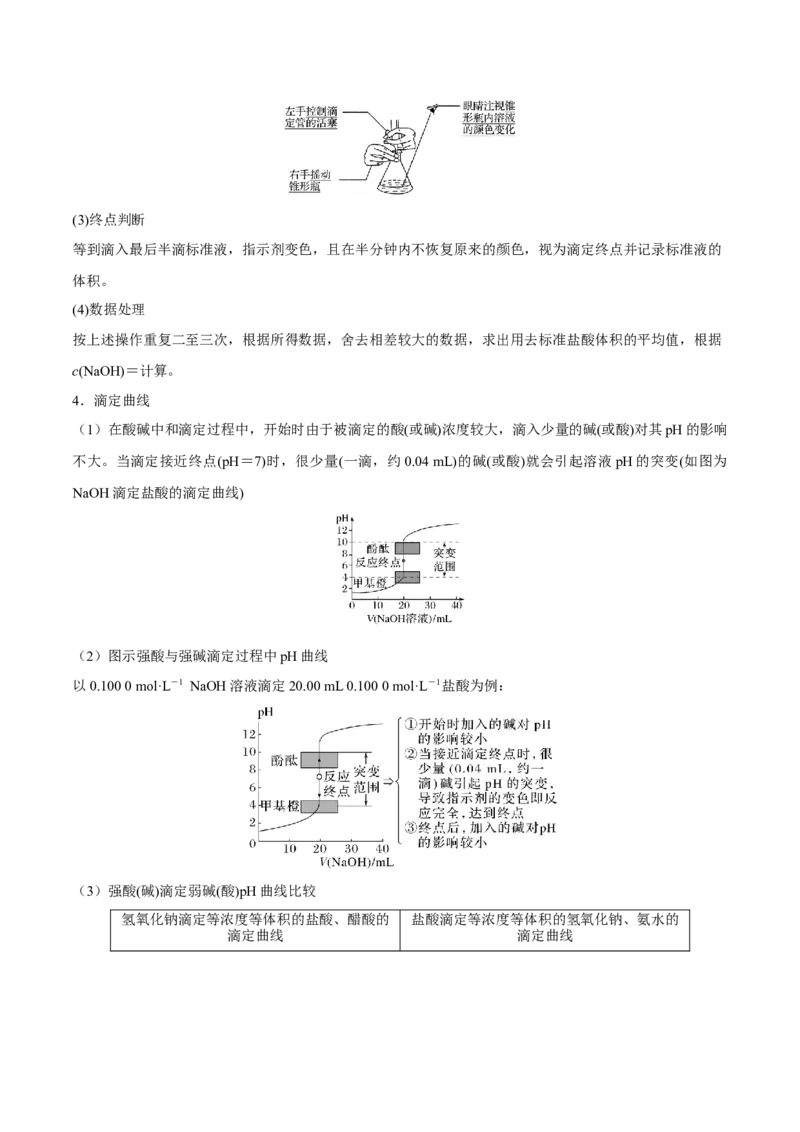
(2)滴定(3)终点判断
等到滴入最后半滴标准液,指示剂变色,且在半分钟内不恢复原来的颜色,视为滴定终点并记录标准液的
体积。
(4)数据处理
按上述操作重复二至三次,根据所得数据,舍去相差较大的数据,求出用去标准盐酸体积的平均值,根据
c(NaOH)=计算。
4.滴定曲线
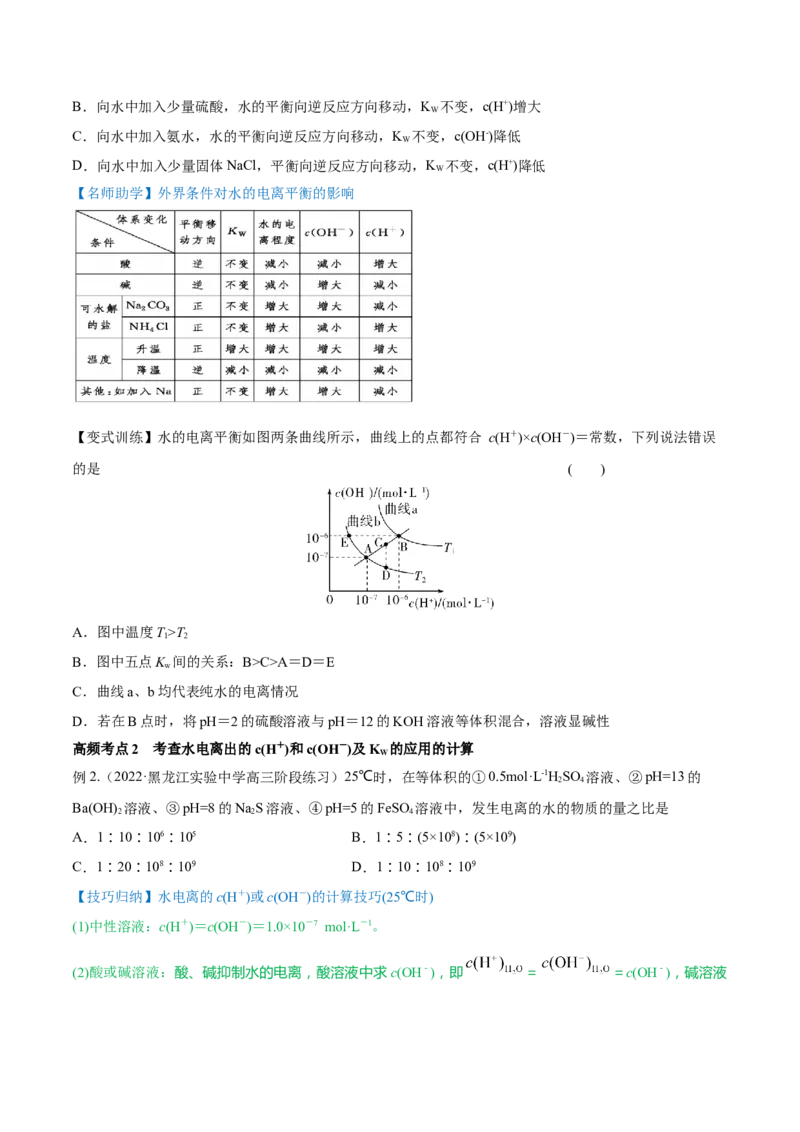
(1)在酸碱中和滴定过程中,开始时由于被滴定的酸(或碱)浓度较大,滴入少量的碱(或酸)对其pH的影响
不大。当滴定接近终点(pH=7)时,很少量(一滴,约0.04 mL)的碱(或酸)就会引起溶液pH的突变(如图为
NaOH滴定盐酸的滴定曲线)
(2)图示强酸与强碱滴定过程中pH曲线
以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例:
(3)强酸(碱)滴定弱碱(酸)pH曲线比较
氢氧化钠滴定等浓度等体积的盐酸、醋酸的 盐酸滴定等浓度等体积的氢氧化钠、氨水的
滴定曲线 滴定曲线曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强
碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与弱酸
反应(强酸与弱碱反应)
5.误差分析
(1)误差分析的方法
依据原理c(标准)·V(标准)=c(待测)·V(待测),得c(待测)=,因为c(标准)与V(待测)已确定,所以只要
分析出不正确操作引起V(标准)的变化,即分析出结果。
(2)常见误差分析
以标准酸溶液滴定未知浓度的碱(酚酞作指示剂)为例,常见的因操作不正确而引起的误差有:
步骤 操作 V(标准) c(待测)
酸式滴定管未用标准溶液润洗 变大 偏高
碱式滴定管未用待测溶液润洗 变小 偏低
洗涤
锥形瓶用待测溶液润洗 变大 偏高
锥形瓶洗净后还留有蒸馏水 不变 无影响
取液 放出碱液的滴定管开始有气泡,放出液体后气泡消失 变小 偏低
步骤 操作 V(标准) c(待测)
酸式滴定管未用标准溶液润洗 变大 偏高
碱式滴定管未用待测溶液润洗 变小 偏低
洗涤
锥形瓶用待测溶液润洗 变大 偏高
锥形瓶洗净后还留有蒸馏水 不变 无影响
取液 放出碱液的滴定管开始有气泡,放出液体后气泡消失 变小 偏低
【特别提醒】1.中和滴定终点是指示剂颜色发生突变的点,但不一定是酸碱恰好中和的点。通常有一定误差(允许误差)。
2.滴定停止后,必须等待1~2分钟,待附着在滴定管内壁的溶液流下后,再进行读数。
知识点四 氧化还原滴定和沉淀滴定
(一)氧化还原滴定原理及应用
1.原理
以氧化剂(或还原剂)为滴定剂,直接滴定一些具有还原性(或氧化性)的物质。
2.试剂
(1)常见的用于滴定的氧化剂有KMnO 、KCr O 等;
4 2 2 7
(2)常见的用于滴定的还原剂有亚铁盐、草酸、维生素C等。
(3)指示剂:氧化还原滴定所用指示剂可归纳为三类:
①氧化还原指示剂;
②专用指示剂,如在碘量法滴定中,可溶性淀粉溶液遇碘变蓝;
③自身指示剂,如高锰酸钾标准溶液滴定草酸时,滴定终点为溶液由无色变为浅红色。
3.实例
(1)酸性KMnO 溶液滴定HC O 溶液
4 2 2 4
原理 2MnO+6H++5HC O===10CO ↑+2Mn2++8HO
2 2 4 2 2
指示剂 酸性KMnO 溶液本身呈紫色,不用另外选择指示剂
4
当滴入最后一滴酸性KMnO 溶液后,溶液由无色变浅红色,且
终点判断 4
半分钟内不褪色,说明到达滴定终点
(2)Na SO 溶液滴定碘液
2 2 3
原理 2NaSO+I===Na SO+2NaI
2 2 3 2 2 4 6
指示剂 用淀粉溶液作指示剂
当滴入最后一滴NaSO 溶液后,溶液的蓝色褪去,且半分钟
终点判断 2 2 3
内不恢复原色,说明到达滴定终点
(二)沉淀滴定原理及应用
沉淀滴定法是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的
含义 反应很多,但符合条件的却很少,实际上应用最多的是银量法,即利
用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度
沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应
的生成物的溶解度要比滴定剂与指示剂反应的生成物的溶解度小,否
原理
则不能用这种指示剂。如用AgNO 溶液滴定溶液中的Cl-的含量时常
3
以CrO为指示剂,这是因为AgCl比Ag CrO 更难溶
2 4
第三部分:典型例题剖析
高频考点1 考查影响水电离平衡的因素及结果判断
例1.关于水的电离,下列叙述中,正确的是
A.升高温度,水的平衡向正反应方向移动,K 增大,c(H+)不变
WB.向水中加入少量硫酸,水的平衡向逆反应方向移动,K 不变,c(H+)增大
W
C.向水中加入氨水,水的平衡向逆反应方向移动,K 不变,c(OH-)降低
W
D.向水中加入少量固体NaCl,平衡向逆反应方向移动,K 不变,c(H+)降低
W
【名师助学】外界条件对水的电离平衡的影响
【变式训练】水的电离平衡如图两条曲线所示,曲线上的点都符合 c(H+)×c(OH-)=常数,下列说法错误
的是 ( )
A.图中温度T>T
1 2
B.图中五点K 间的关系:B>C>A=D=E
w
C.曲线a、b均代表纯水的电离情况
D.若在B点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合,溶液显碱性
高频考点2 考查水电离出的c(H+)和c(OH-)及K 的应用的计算
W
例2.(2022·黑龙江实验中学高三阶段练习)25℃时,在等体积的①0.5mol·L-1HSO 溶液、②pH=13的
2 4
Ba(OH) 溶液、③pH=8的NaS溶液、④pH=5的FeSO 溶液中,发生电离的水的物质的量之比是
2 2 4
A.1∶10∶106∶105 B.1∶5∶(5×108)∶(5×109)
C.1∶20∶108∶109 D.1∶10∶108∶109
【技巧归纳】水电离的c(H+)或c(OH-)的计算技巧(25℃时)
(1)中性溶液:c(H+)=c(OH-)=1.0×10-7 mol·L-1。
(2)酸或碱溶液:酸、碱抑制水的电离,酸溶液中求c(OH-),即 = =c(OH-),碱溶液中求c(H+),即 = =c(H+),计算出溶液中的c(H+)和c(OH-),数值小的为水电离的
c(H+)或c(OH-)数值。
(3)可水解的盐溶液:水解的盐促进水的电离,故 等于显性离子的浓度,计算出溶液中的c(H+)和
c(OH-),数值大的为水电离的c(H+)或c(OH-)数值。
(3)酸式盐溶液
酸式根以电离为主: = =c(OH-)。
酸式根以水解为主: = =c(OH-)。
【变式训练】(2021·北京丰台·一模)常温下,下列说法不正确的是
A.pH均为5的稀盐酸和NH Cl溶液,由水电离的H+浓度之比为1:104
4
B.向水中加入少量NaHSO 固体,c(H+)增大,K 不变
4 w
C.等物质的量浓度的HCOONa和NaF溶液,前者pH较大,则可发生反应:HCOOH+NaF=HF+HCOONa
D.等物质的量浓度等体积的CHCOOH和CHCOONa溶液混合后pH约为4.7,则混合液中
3 3
c(CHCOO-)>c(Na-)>c(H+)>c(OH-)
3
高频考点3 考查混合溶液酸碱性的判断
例3.(2022·上海黄浦·二模)下列溶液一定呈中性的是
A. 的溶液 B.等物质的量的强酸和强碱反应得到的溶液
C.c(H+)=c(OH—)的溶液 D.紫色石蕊试液不变色的溶液
【方法归纳】混合溶液酸碱性的判断方法
(1)等浓度等体积一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”
中和反应 反应后所得溶液的酸碱性
强酸与强碱 中性
强酸与弱碱 酸性
弱酸与强碱 碱性
(2)室温下,已知酸和碱pH之和的溶液等体积混合
①两强混合:
a.若pH之和等于14,则混合后溶液显中性,pH=7。
b.若pH之和大于14,则混合后溶液显碱性,pH>7。
c.若pH之和小于14,则混合后溶液显酸性,pH<7。
②一强一弱混合——“谁弱显谁性”。
pH之和等于14时,一元强酸和一元弱碱等体积混合呈碱性;一元弱酸和一元强碱等体积混合呈酸性。
【变式训练】已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1
W
的一元碱BOH等体积混合,可判定该溶液呈中性的依据是A.a=b
B.混合溶液的PH=7
C.混合溶液中,c(H+)= mol.L-1
D.混合溶液中c(H+)+c(B+)=c(OH-)+C(A-)
高频考点4 考查溶液pH的计算
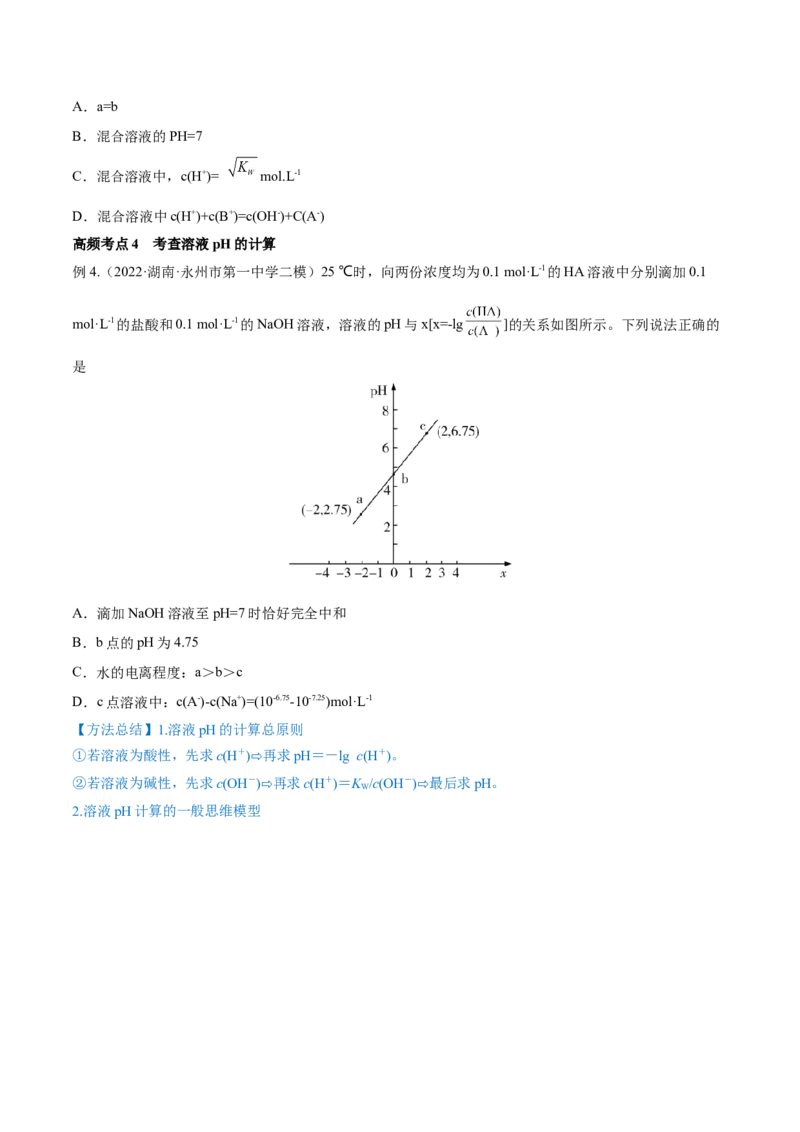
例4.(2022·湖南·永州市第一中学二模)25 ℃时,向两份浓度均为0.1 mol·L-1的HA溶液中分别滴加0.1
mol·L-1的盐酸和0.1 mol·L-1的NaOH溶液,溶液的pH与x[x=-lg ]的关系如图所示。下列说法正确的
是
A.滴加NaOH溶液至pH=7时恰好完全中和
B.b点的pH为4.75
C.水的电离程度:a>b>c
D.c点溶液中:c(A-)-c(Na+)=(10-6.75-10-7.25)mol·L-1
【方法总结】1.溶液pH的计算总原则
①若溶液为酸性,先求c(H+) 再求pH=-lg c(H+)。
②若溶液为碱性,先求c(OH- ⇨) 再求c(H+)=K
W
/c(OH-) 最后求pH。
2.溶液pH计算的一般思维模型
⇨ ⇨【变式训练】(2022·上海徐汇·二模)室温时,将浓度和体积分别为 的 溶液和 的
溶液混合,下列关于混合溶液的叙述正确的是
A.若 ,则一定是
B.若 ,则
C.当 时,若 ,则一定是
D.当 时,
高频考点5 考查中和滴定仪器及指示剂的选择
例5.(2022·上海黄浦·二模)用已知浓度的 溶液测定浓硫酸试剂中 含量的主要操作中,不需
要用到的仪器为
A. B. C. D.
【变式训练】实验室现有3种酸碱指示剂。其pH变色范围如下
甲基橙:3.1~4.4 石蕊:`5.0~8.0 酚酞:8.2~10.0
用0.1000 mol/L NaOH溶液滴定未知浓度的CHCOOH溶液,反应恰好完全时。下列叙述正确的是
3A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈酸性,可选用甲基橙作指示剂
D.溶液星碱性,只能选用酚酞作指示剂
【规律总结】指示剂选择的基本原则:变色要灵敏,变色范围要小,使变色范围尽量与滴定终点溶液的酸
碱性一致。
(1)不能用石蕊作指示剂。
(2)滴定终点为碱性时,用酚酞作指示剂,例如用NaOH溶液滴定醋酸。
(3)滴定终点为酸性时,用甲基橙作指示剂,例如用盐酸滴定氨水。
(4)强酸滴定强碱一般用甲基橙,但用酚酞也可以。
(5)并不是所有的滴定都须使用指示剂,如用标准的NaSO 溶液滴定KMnO 溶液时,KMnO 颜色恰好褪去
2 3 4 4
时即为滴定终点。
高频考点6 考查滴定终点的规范描述
例6.(1)用amol·L-1的HCl滴定未知浓度的NaOH溶液,用酚酞做指示剂,达到滴定终点的现象是___。
若用甲基橙做指示剂,滴定终点现象是___。
(2)用标准碘溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,应选用___做指示剂,达到滴定终点
2 2
的现象是__。
(3)用标准酸性KMnO 溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,是否需要选用指示剂
4 2 2
___(填“是”或“否”),达到滴定终点的现象是___。
【名师归纳】1.滴定终点的判断答题模板:当滴入最后一滴××××××标准溶液后,溶液变成××××××色,且
半分钟内不恢复原来的颜色。
2.解答此类题目注意三个关键点:
(1)最后一滴:必须说明是滴入“最后半滴”溶液。
(2)颜色变化:必须说明滴入“最后半滴”溶液后溶液的颜色变化。
(3)半分钟:必须说明溶液颜色变化后“半分钟内不恢复原来的颜色”。
【变式训练】(2022·全国·高三专题练习)已知:I+2 = +2I-,某学习小组用“间接碘量法”测定
2
含有CuCl HO的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入
2. 2
过量KI固体,充分反应,生成白色沉淀。用0.1000mol/LNa SO 标准溶液20.00mL。可选用_______作滴
2 2 3
定指示剂,滴定终点的现象是_______。
高频考点7 考查中和滴定的数据处理及误差分析
例7.氧化还原滴定实验是用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之。现用0.1000 mol·L-1
KMnO 酸性溶液滴定未知浓度的无色HC O 溶液,完成下列问题:
4 2 2 4(1)配制100mL0.1000mol/L的KMnO 溶液所需要的玻璃仪器有量筒、烧杯、胶头滴管、玻璃棒、
4
___________。
(2)该滴定实验应选用如下图所示的滴定管___________(填“A”或“B”)盛放高锰酸钾溶液,原因是
_________________________ 。
(3)写出酸性高锰酸钾与草酸反应的离子方程式___________。
(4)滴定终点的现象为___________。
(5)某学生按照滴定步骤进行了3次实验,分别记录有关数据如表:
0.1000 mol·L-1KMnO 的体积/mL
4
待测HC O 溶液
滴定次数 2 2 4
的体积/mL
滴定前刻度 滴定后刻度 溶液体积/mL
第一次 20.00 0.00 20.11 20.11
第二次 20.00 1.56 23.30 21.74
第三次 20.00 0.30 20.19 19.89
依据上表数据计算该HC O 溶液的物质的量浓度为___________ mol·L-1(保留4位有效数字)。
2 2 4
(6)下列操作和叙述错误的是___________。
a.滴定过程中,眼睛应一直注视滴定管的刻度值变化,直至滴定终点
b.酸碱中和滴定中可以任意选用酚酞、石蕊、甲基橙等常用指示剂
c.左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶
d.滴定时,控制滴加速率:先快后慢
【易错提醒】要注意某个数值与其他数据相差较大时,可以舍去,否则计算结果错误。
【变式训练】为测定某醋酸溶液浓度,量取20.00mL待测醋酸溶液于锥形瓶中,用0.1000mol·L-1NaOH溶
液滴定。以下实验操作导致测定浓度偏高的操作有几个
①酸式滴定管用蒸馏水洗涤后加入醋酸溶液
②锥形瓶用待测液润洗后加入20.00mL醋酸溶液
③选酚酞做指示剂④当滴入最后半滴NaOH溶液时,溶液由无色变为浅红色,即为滴定终点
⑤滴定管(装标准溶液)滴定前尖嘴处有气泡,滴定后无气泡,所测得待测液的浓度
⑥中和滴定达终点时俯视滴定管内液面读数
A.1个 B.2个 C.3个 D.4个
高频考点8 考查酸碱中和滴定曲线分析
例8.(2022·青海·海东市第一中学一模)常温下,用0.1 mol·L-1的NaOH溶液滴定20.00 mL 0.1 mol·L-1
CHCOOH溶液所得滴定曲线如图。下列说法正确的是
3
A.点①所示溶液中:c(CHCOO-)>c(H+)>c(CH COOH)
3 3
B.点②所示溶液中:c(CHCOO-)+c(OH-)=c(CH COOH)+c(H+)
3 3
C.点③所示溶液中:c(Na+)=c(CH COOH)+c(CH COO-)
3 3
D.点④所示溶液中:c(Na+)>c(CH COO-)>c(OH-)>c(H+)
3
【名师归纳】酸碱中和滴定曲线图是以所滴入的酸或碱溶液的体积为横坐标、以中和反应后溶液的pH为
纵坐标体现中和滴定过程的曲线图。
(1)强酸与强碱互相滴定的曲线图,前半部分与后半部分形状变化不大,但中间突跃大(即酸或碱溶液一
滴之差,溶液pH变化大,出现突变)。分析强酸与强碱互相滴定时的离子浓度大小,只要关注水的电离平
衡即可,没有其它平衡影响。
(2)强酸滴定弱碱或强碱滴定弱酸的曲线图,突跃小,较平缓;强酸滴定弱碱的起点低(因弱碱pH相对
较小),前半部分形状有差异;强碱滴弱酸的起点高(因弱酸pH相对较大),前半部分形状有差异。分析强
碱滴定弱酸或强酸滴定弱碱时的离子浓度大小,不仅要考虑生成盐的水解平衡,而且还要考虑过量弱酸或
弱碱的电离平衡与水的电离平衡。
【变式训练】(2022·四川达州·一模)用0.1000mol/L的NaOH溶液滴定20. 00mLcmol/L二元酸HA溶液,
2
滴定曲线如图所示,下列叙述正确的是A.HA-的电离常数的数量级是10-5
B.a点:c(HA-)> c(Na+)>c (H+)>c(A2-)>c (OH-)
C.b点:c (H+)=c(A2-)+c (OH-)
D.c点:c(Na+)