文档内容
第 36 讲 原子结构与性质
目录
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查核外电子排布的表示方法
高频考点2 考查原子结构与元素周期表、元素性质的关系
高频考点3 考查电离能、电负性的应用
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 原子核外电子排布原理
1.能层、能级与原子轨道
(1)能层(n)
在多电子原子中,核外电子的能量是不同的,按照电子的能量差异将其分成不同能层。通常用K、L、M、
N……表示,能量依次升高。
(2)能级
同一能层里电子的能量也可能不同,又将其分成不同的能级,通常用s、p、d、f等表示,同一能层里,各
能级的能量按s、p、d、f的顺序依次升高,即:E(s)<E(p)<E(d)<E(f)。(3)原子轨道
电子云轮廓图给出了电子在核外经常出现的区域。这种电子云轮廓图称为原子轨道。
原子轨道 轨道形状 轨道个数
s 球形 1
p 哑铃形 3
【特别提醒】第一能层(K),只有s能级;第二能层(L),有s、p两种能级,p能级上有三个原子轨道p、
x
p、p,它们具有相同的能量;第三能层(M),有s、p、d三种能级。
y z
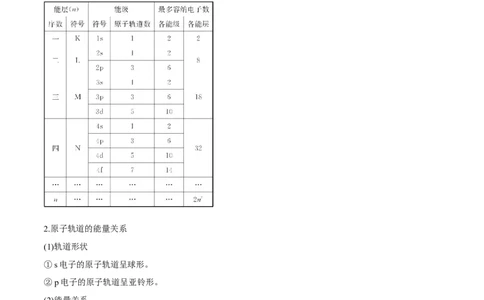
(4)能层、能级与原子轨道之间的关系
2.原子轨道的能量关系
(1)轨道形状
①s电子的原子轨道呈球形。
②p电子的原子轨道呈亚铃形。
(2)能量关系
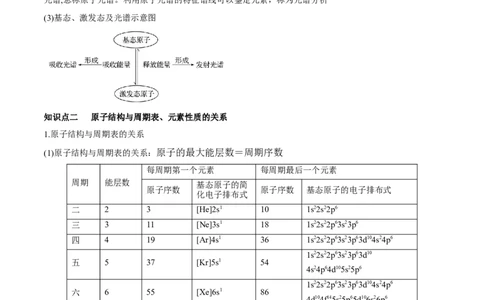
①相同能层上原子轨道能量的高低:ns③>②>① B.原子半径:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
【特别提醒】第二、三、四周期中,第ⅡA族、第ⅤA族元素的第一电离能比相邻元素都大。元素电负性
与元素非金属性的变化规律一致。
【变式训练】(2022·江苏镇江·高三开学考试)白云土是一种硅酸盐,用氢氟酸处理白云土生成一种水溶
性很低的物质 。下列说法正确的是
A.电负性大小: B.半径大小:
C.电离能大小: D.碱性强弱:
高频考点3 考查电离能、电负性的应用
例3.(2022·全国·高三专题练习)已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表数据
判断下列说法中错误的是
元
I I I I
素 1 2 3 4
690
X 500 4600 9500
0
270
Y 580 1800 11600
0
A.元素X的常见化合价是+1价 B.元素X与氯形成化合物时,化学式可能是XCl
C.元素Y是第IIIA族元素 D.若元素Y处于第三周期,它可与冷水剧烈反应
【名师点睛】1.电离能常见的四个应用
(1)判断元素金属性的强弱
电离能越小,金属越容易失去电子,金属性越强;反之越弱。
(2)判断元素的化合价
如果某元素的I I,则该元素的常见化合价为+n,如钠元素I I,所以钠元素的化合价为+1。
n+1 n 2 1
(3)判断核外电子的≫分层排布情况 ≫
多电子原子中,元素的各级电离能逐渐增大,当电离能的变化出现突跃时,电子层数就可能发生变化。
(4)反映元素原子的核外电子排布特点同周期元素原子的最外层电子排布是全空、半充满和全充满状态时,第一电离能就会反常得大,如第ⅡA
族、ⅤA族元素。
2.电负性常见的四个应用
(1)确定元素类型(电负性>1.8,为非金属元素;电负性<1.8,为金属元素)。
(2)确定化学键类型(一般两成键元素电负性差值>1.7,为离子键;两成键元素电负性差值<1.7,为共价键)。
(3)判断元素价态正、负(化合物中电负性大的元素呈现负价,电负性小的元素呈现正价)。
(4)判断元素金属性和非金属性强弱(表征原子得电子能力强弱)。
【变式训练】(2022·全国·高三专题练习)已知X、Y元素同周期,且电负性X>Y,下列说法错误的是
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能Y一定小于X
C.最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性
D.气态氢化物的稳定性:HY小于H X
n m