文档内容
第 36 讲 原子结构与性质
第一部分:高考真题感悟
1.(2022·江苏·高考真题)工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的
是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
【答案】A
【解析】A.核外电子数相同时,核电荷数越大半径越小,故半径大小为 ,故A正确;
B.同周期元素核电荷数越大电负性越大,故 ,故B错误;C.同周期从左往右第一电离能呈增
大趋势,同主族从上往下第一电离能呈减小趋势,故电离能大小为 ,故C错误;D.元素金
属性越强,其最高价氧化物对应水化物的碱性越强,故碱性强弱为 ,故D错误;故选A。
2.(2022·海南·高考真题)钠和钾是两种常见金属,下列说法正确的是
A.钠元素的第一电离能大于钾 B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠 D.钠元素与钾元素的原子序数相差18
【答案】A
【解析】A.同一主族元素的第一电离能从上到下依次减小,金属性越强的元素,其第一电离能越小,因
此,钠元素的第一电离能大于钾,A说法正确;B.基态钾原子价层电子为4s1,其轨道表示式为 ,B说
法不正确;C.钾和钠均能与水发生置换反应,因此,钾不能置换出 NaC1溶液中的钠,C说法不正确;
D.钠元素与钾元素的原子序数分别为11和19,两者相差8,D说法不正确;综上所述,本题选A。
3.(2022·辽宁·高考真题)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是
A.X能与多种元素形成共价键 B.简单氢化物沸点:
C.第一电离能: D.电负性:
【答案】B
【解析】短周期元素X、Y、Z、W、Q原子序数依次增大,W简单离子在同周期离子中半径最小,说明W
为第三周期元素Al。短周期元素的基态原子中有两个单电子,可分类讨论:①为第二周期元素时,最外层
电子排布为2s22p2或2s22p4,即C或O;②为第三周期元素时,最外层电子排布为3s23p2或3s23p4,即Si或
S。Q与Z同主族,结合原子序数大小关系可知,则X、Z、Q分别为C、O和S,则Y为N。A.X为C,
能与多种元素(H、O、N、P、S等)形成共价键,A正确;B.Z和Q形成的简单氢化物为HO和HS,由
2 2
于HO分子间能形成氢键,故HO沸点高于HS,B错误;C.Y为N,Z为O,N的最外层p轨道电子为
2 2 2
半充满结构,比较稳定,故其第一电离能比O大,C正确;D.W为Al,Z为O,O的电负性更大,D正
确;故选B。
4.(2021·湖北·高考真题)金属Na溶解于液氨中形成氨合钠离子和氨合电子,向该溶液中加入穴醚类配
体L,得到首个含碱金属阴离子的金黄色化合物[NaL]+Na-。下列说法错误的是
A.Na-的半径比F-的大 B.Na-的还原性比Na的强
C.Na-的第一电离能比H-的大 D.该事实说明Na也可表现出非金属性
【答案】C
【解析】A. 核外有3个电子层、 核外有2个电子层,故 的半径比 的大,A项正确;B.
的半径比Na的大, 中原子核对最外层电子的引力小,易失电子,故 的还原性比Na的强,B项正
确;C. 的1s上有2个电子,为全充满稳定结构,不易失去电子,故 的第一电离能比 的小,C项
错误;D.该事实说明Na可以形成 ,得电子表现出非金属性,D项正确。故选C。
5.(2020·浙江·高考真题)下列说法正确的是
A.同一原子中,在离核较远的区域运动的电子能量较高
B.原子核外电子排布,先排满K层再排L层,先排满M层再排N层
C.同一周期中,随着核电荷数的增加,元素的原子半径逐渐增大
D.同一周期中,Ⅱ A与Ⅲ A族元素原子的核电荷数都相差1【答案】A
【解析】A.电子能量越低,挣脱原子核束缚的能力弱,在距离原子核近的区域运动;电子能量高,挣脱
原子核束缚的能力强,在距离原子核远的区域运动,故A正确;B.M能层中d能级的能量高于N能层中
s能级能量,填充完4s能级后才能填充3d能级,故B错误;C.同一周期中,主族元素随着核电荷数的增
加,元素的原子半径逐渐减小,故C错误;D.第四周期中,Ⅱ A与Ⅲ A族元素原子的核电荷数相差
11,故D错误;故选:A。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·上海宝山·一模)下列原子的最外层电子轨道表示式正确的是
A.铍原子:
B.碳原子:
C.氮原子:
D.铝原子:
【答案】C
【解析】A.铍原子最外层含有2个电子,均属于2s轨道,其外层电子轨道表示式为 ,故A错误;
B.碳原子最外层含有4个电子,其最外层电子轨道表示式为 ,故B错误;C.氮原子最
外层2s轨道含有2个电子,2p轨道含有3个电子,其最外层电子轨道表示式为 ,故C正确;D.Al的核电荷数为13,其最外层电子排布式为3s23p1,则Al原子的最外层电子轨道表示式为
,故D错误;故选:C。
2.(2022·辽宁·一模)下列化学用语表述错误的是
A.NaH的电子式为
B. 表示的一定不是基态原子
C.乙炔的结构简式为CHCH
D.基态C原子价电子排布图为
【答案】C
【解析】A.NaH为离子化合物,电子式为 ,A正确;B. 中2p轨道的电子可能处
于激发态,故表示的一定不是基态原子,B正确;C.乙炔含有官能团碳碳三键,其结构简式为CH≡CH,
C错误;D.碳原子核外电子排布:1s22s22p2 基态C原子价电子排布图为 ,D正确;
,
故选C。
3.(2022·北京房山·一模)下列关于元素或物质性质的比较中,不正确的是
A.稳定性:HF>HCl>HBr>HI B.第一电离能:C>N>O>F
C.酸性: D.电负性:CHCl>HBr>HI,A正确;B.同一周期随着原子序数变大,第一电离能
变大,但是N的2p轨道为半充满稳定状态,第一电离能大于同周期相邻元素,故第一电离能大小:F
>N>O> C,B错误;C.同周期从左到右,金属性减弱,非金属性变强,最高价氧化物对应水化物的酸性
逐渐变强,碱性减弱;同主族元素从上到下,最高价氧化物对应水化物的酸性减弱;酸性:,C正确;D.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;
电负性:Cr(Z)>r(Y)>r(X)
B.X氧化物的水化物是一定是强酸
C.Y的第一电离能比同周期相邻元素小
D.W的简单气态氢化物的稳定性比Y的强
【答案】C
【解析】X原子2p轨道上有3个电子,该元素为N;Z是元素周期表中电负性最大的元素,该元素为F,
W与Y同主族,且X、Y、Z、W的原子序数依次增大,故Y为O,W为S,综上可知X、Y、Z、W分别
为N、O、F、S。A.同周期自左而右原子半径减小,同主族元素半径从上到下依次增大,故原子半径
r(S)> r(N)> r(O)> r(F),A项错误;B.X为N,氮的氧化物的水化物不一定是强酸,如亚硝酸,B项错误;
C.N元素的第一电离能大于同周期相邻元素,主族元素同周期从左向右第一电离能呈增大趋势,则O的
第一电离能小于N和F,C项正确;D.Y为O,W为S,非金属性O > S,故Y的简单气态氢化物的热稳
定性比W的强,D项错误;答案选C。
6.(2022·江苏江苏·三模)前4周期主族元素X、Y、Z、W的原子序数依次增大。X与Z同主族,且基态
X原子中p能级和s能级上的电子数相同。Y、Z同周期,Y位于IIIA族,W最外层有2个电子。下列说法
正确的是
A.原子半径:r(X)Y>Z
B.基态原子未成对电子数:X>Y>Z
C.原子半径:X>Y>Z
D.简单气态氢化物稳定性:Z>Y>X
【答案】A
【解析】主族元素同周期随着原子序数的增大第一电离能呈增大趋势,但第IIA族、第VA族元素第一电
离能大于相邻元素,则第一电离能最大的元素是N,基态Z原子的第一电离能的大小在本周期元素中排第
二位,则Z为F元素,X、Y、Z紧邻元素,X为N元素,Y为O元素;根据分析可知,X为N,Y为O,
Z为F元素,A.主族元素同周期从左向右电负性逐渐增大,则电负性:Z(F)>Y(O)>X(N),故A错误;
B.N、O、F基态原子未成对电子数分别为3、2、1,即基态原子未成对电子数:X>Y>Z,故B正确;
C.主族元素同周期从左向右原子半径逐渐减小,则原子半径:X(N)>Y(O)>Z(F),故C正确;D.非金属
性越强,简单气态氢化物稳定性越强,非金属性:F>O>N,则简单气态氢化物稳定性:Z>Y>X,故D正
确;故选:A。
8.(2022·湖北·宜昌市夷陵中学模拟预测)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电
荷数,Y为元素的有关性质)。下列比较的性质与图像不对应的是A B C D
第三周期元素的最高正 ⅠA族元素单质 同一短周期元素的基态原 、 、 、 四种
化合价 熔点 子第一电离能 离子的离子半径
【答案】D
【解析】A.第三周期从 到 价电子数由1到7,其最高正价由 到 ,而 化学性质一般稳定,难
形成化合物, 在单质中计为0价,A不合题意;B.ⅠA族质子数最小为氢,其单质为分子晶体,沸点
最低,而从 到铷属于金属晶体,它们离子半径逐渐减小,阳离子与自由电子之间金属键键能减小,熔,
点逐渐降低,B不合题意;C.同一周前自左至右元素基态原子第一电离能增大趋势,但第ⅡA、ⅤA族
反常,C不合题意;D. 四种离子核外电子排布相同,其离子半径逐渐减小,D图像
与性质不对应,D符合题意;故答案为:D。
9.(2022·山东省实验中学模拟预测)含有N 、N 的材料Pb(N )、NAsF 可以用于炸药。下列说法正确
3 2 5 6
的是
A.Pb属于d区元素
B.基态As原子的d轨道与p轨道上的电子数之比为3:2
C.N 的空间构型为直线形
D.基态F原子中,核外电子的空间运动状态有9种
【答案】C
【解析】A.铅元素的原子序数为82,价电子排布式为6s26p2,处于元素周期表的p区,故A错误;B.砷
元素的原子序数为33,电子排布式为1s22s22p63s23p63d104s24p3,则原子的d轨道与p轨道上的电子数之比为
10:15=2:3,故B错误;C.等电子体具有相同的空间构型,N 离子与二氧化碳分子的原子个数都为3、
价电子数都为16,互为等电子体,二氧化碳的空间构型为直线形,则N 离子的空间构型为直线形,故C
正确;D.核外电子的空间运动状态与原子轨道的数目相同,氟元素的原子序数为9,电子排布式为
1s22s22p5,氟原子的原子轨道数目为5,则核外电子的空间运动状态有5种,故D错误;故选C。10.(2022·海南·一模)下列化学用语或图示表达正确的是
A.N 的结构式:N≡N B.基态Fe3+的电子排布式:[Ar]3d64s0
2
C.CO 的空间填充模型: D.基态氯原子的价电子排布式:1s22s22p63s23p5
2
【答案】A
【解析】A. 氮气分子内存在氮氮三键,则N 的结构式:N≡N,A正确;
2
B. Fe的原子序数为26,基态Fe的电子排布式:[Ar]3d64s2,基态Fe3+的电子排布式:[Ar]3d5,B错误;
C.空间填充模型为 的分子构型为V形,CO 分子中,孤电子对数 、价电子对数
2
,CO 分子的空间构型为直线形、不是V形,C错误;D. 基态氯原子的电子排布式:
2
1s22s22p63s23p5,价电子排布式: 3s23p5,D错误;答案选A。
11.(2022·全国·模拟预测)有机化合物M的结构简式如右图所示,其组成元素X、Y、Z、W、Q为原子
序数依次增大的短周期元素。只有Y、Z、W为同周期相邻元素,Z的原子序数与Q的最外层电子数相同。
下列说法正确的是
A.简单氢化物的沸点由高到低顺序为
B.含氧酸的酸性强弱顺序为
C.元素第一电离能由小到大的顺序为
D.元素X、Z、W形成的离子化合物中含有正四面体结构
【答案】D
【解析】Z的原子序数与Q的最外层电子数相同,说明Z为第二周期,Q为第三周期元素,依据有机物结
构简式可知,元素Y形成四个键,应为C元素,则Z、W依次为N、O元素,Q则为Cl元素,X为H元素。
A.W、Q的简单氢化物依次为 、HCl,其沸点由高到低顺序为 ,A错误;B.Q、Y、Z对应最高价含氧酸分别为 、 、 ,满足酸性强弱顺序为 ,但含氧酸则不正确,如
HClO酸性弱于 ,B错误;C.N元素2p轨道半充满,较为稳定,元素第一电离能最大,即顺序应
为 ,C错误;D.元素X、Z、W形成的离子化合物 中含有的 为正四面体结构离子,
D正确。故选D。
12.(2021·上海嘉定·一模)下列各组原子中,彼此化学性质一定相似的是
A.最外层都只有一个电子的X、Y原子
B.原子核外L层上有8个电子的X原子与M层上有8个电子的Y原子
C.2p轨道上有3个未成对电子的X原子与3p轨道上有3个未成对电子的Y原子
D.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
【答案】C
【解析】A.最外层只有一个电子可能是H原子、碱金属元素原子或者ⅠB族元素原子,H原子、碱金属
元素原子性质有相似的地方,都具有还原性,但与ⅠB族元素原子性质不同,故A错误;B.原子核外L
层上有8个电子的X原子,没有指明有没有M层,M层上有8个电子的Y原子,没有指明有没有N层,
无法判断它们是什么原子,无法判断它们的化学性质是否相似,故B错误;C.2p轨道上有3个未成对电
子的X原子为N原子,3p轨道上有3个未成对电子的Y原子为P原子,N和P位于同一主族,最外层电子
数相同,性质相似,故C正确;D.原子核外电子排布式为1s2的X原子为He原子,原子核外电子排布式
为1s22s2的Y原子为Be,二者性质不同,故D错误;故答案为C。
二、主观题(共4小题,共40分)
13.(2021·天津市红桥区教师发展中心高三期末)(10分)根据已学知识,回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是____,占据该能层电子的电子云轮廓图形状为____。
(2)写出3p轨道上有2个未成对电子的元素的符号____或____。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的
名称是____。
(4)已知铁是26号元素,写出Fe的价层电子排布式____;在元素周期表中,该元素在____(填“s”“p”“d”“f”
或“ds”)区。
(5)写出与N同主族的As的基态原子的核外电子排布式____。
(6)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为____。
(7)写出Fe2+的核外电子排布式:____。(8)Zn2+的核外电子排布式为____。
【答案】(除标注外,每空1分)(1)L 球形和哑铃形
(2)Si(0.5分) S(0.5分)
(3)硒
(4)3d64s2 d
(5)1s22s22p63s23p63d104s24p3或[Ar]3d104s24p3
(6)N>O>B
(7)1s22s22p63s23p63d6
(8)1s22s22p63s23p63d10
【解析】(1)N原子核外有7个电子,基态N原子核外电子排布式为1s2 2s2 2p3,核外电子占据的最高能层
的符号是L,s轨道电子云为球形、p轨道电子云为哑铃形,占据该能层电子的电子云轮廓图形状为球形和
哑铃形。
(2)根据泡利原理和洪特规则,3p轨道上有2个未成对电子的情况分两种情况,一种情况是3p轨道上只有2
个电子,则该元素是Si,一种情况是3p轨道上有4个电子,则该元素是S,故答案为Si和S。
(3)该元素原子的外围电子排布式为4s24p4,则该元素的核电子排布式是[Ar]3d104s24p4,该元素的名称是硒。
(4)铁是26号元素,Fe的价层电子排布式为3d64s2;在元素周期表中,Fe是Ⅷ族元素,该元素在d区。
(5)As是33号元素,其元素的核电子排布式是1s22s22p63s23p63d104s24p3或[Ar]3d104s24p3。
(6)同周期元素从左到右,第一电离能有增大趋势,但N原子2p轨道半充满,故N原子第一电离能大于同
周期相邻元素, 则B、N和O的第一电离能由大到小的顺序为N > O > B。
(7)铁是26号元素,Fe的核外电子排布式为1s22s22p63s23p63d64s2,则其Fe2+的核外电子排布式为
1s22s22p63s23p63d6。
(8)锌是30号元素,Zn的核外电子排布式为1s22s22p63s23p63d104s2,则其Zn2+的核外电子排布式为
1s22s22p63s23p63d10。
14.(2022·全国·高三专题练习)(10分)下表是元素周期表的一部分,表中所列的字母分别代表一种化
学元素。试回答下列问题:
(1)元素p为26号元素,请写出其基态原子电子排布式:___________。
(2)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_________________。
(3)o、p两元素的部分电离能数据如表:元素
o p
电离能/kJ·mol-1
I 717 759
1
I 1 509 1 561
2
I 3 248 2 957
3
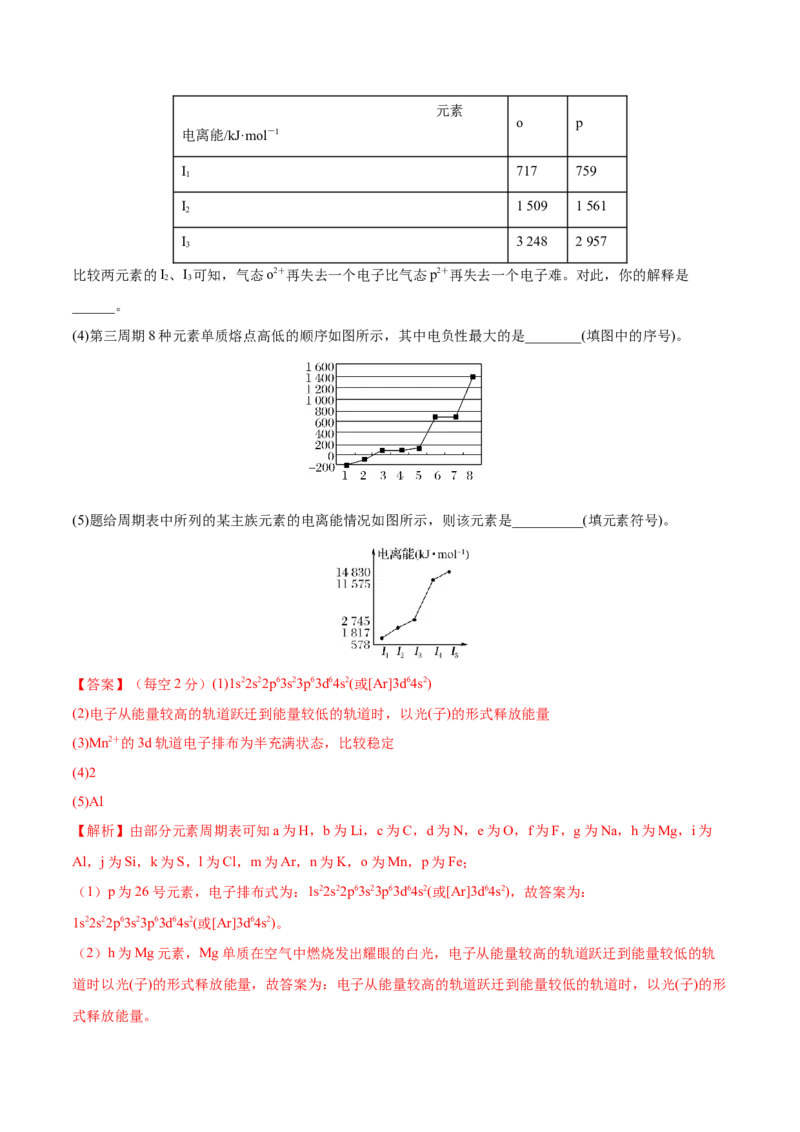
比较两元素的I、I 可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是
2 3
______。
(4)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是________(填图中的序号)。
(5)题给周期表中所列的某主族元素的电离能情况如图所示,则该元素是__________(填元素符号)。
【答案】(每空2分)(1)1s22s22p63s23p63d64s2(或[Ar]3d64s2)
(2)电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量
(3)Mn2+的3d轨道电子排布为半充满状态,比较稳定
(4)2
(5)Al
【解析】由部分元素周期表可知a为H,b为Li,c为C,d为N,e为O,f为F,g为Na,h为Mg,i为
Al,j为Si,k为S,l为Cl,m为Ar,n为K,o为Mn,p为Fe;
(1)p为26号元素,电子排布式为:1s22s22p63s23p63d64s2(或[Ar]3d64s2),故答案为:
1s22s22p63s23p63d64s2(或[Ar]3d64s2)。
(2)h为Mg元素,Mg单质在空气中燃烧发出耀眼的白光,电子从能量较高的轨道跃迁到能量较低的轨
道时以光(子)的形式释放能量,故答案为:电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形
式释放能量。(3)o元素为Mn,其基态原子电子排布式为1s22s22p63s23p63d54s2,Mn2+的基态电子排布式为
1s22s22p63s23p63d5,其3d能级为半充满状态,相对比较稳定,当其失去第3个电子时比较困难,而Fe2+的
基态电子排布式为1s22s22p63s23p63d6,其3d能级再失去一个电子即为半充满状态,故其失去第3个电子比
较容易,故答案为:Mn2+的3d轨道电子排布为半充满状态,比较稳定。
(4)第三周期8种元素分别为钠、镁、铝、硅、磷、硫、氯、氩,其单质中钠、镁、铝形成金属晶体,熔
点依次升高;硅形成原子晶体;磷、硫、氯、氩形成分子晶体,且常温下磷、硫为固体,氯气、氩为气体,
8种元素熔点最低的为氩,其次为氯,其中电负性最大的为氯,故答案为:2。
(5)由图可知,该元素的电离能I 远大于I,故为第ⅢA族元素,应为Al,故答案为:Al。
4 3
15.(2021·辽宁·沈阳市第十中学高三阶段练习)(10分)X、Y、Z、W为元素周期表前四周期元素,原
子序数依次增大,X核外有6种不同运动状态的电子;Y原子基态时2p原子轨道上有3个未成对电子;Z
有多种氧化物,其中一种红棕色氧化物可作颜料;W位于第四周期,其原子最外层只有一个电子,且内层
都处于全满状态。
回答下列问题:
(1)X在元素周期表中的位置___________;
(2)元素X的第一电离能与氢元素比较X___________H(氢)(填“大于”或“小于”下同),元素的电负性
X___________Y。最简单气态氢化物的沸点X___________Y;
(3)Z的基态原子核外有___________种不同空间运动状态的电子,Z有两种常见的离子,较稳定的是
___________检验溶液中存在该离子的实验方法___________。与Z元素处于同周期同族且原子序数比Z大
2的元素Q,写出Q元素+3价阳离子的核外电子排布式___________。
(4)W位于元素周期表的___________区。
【答案】(除标注外,每空1分)(1)第二周期第IVA族
(2)①小于 ②小于 ③小于
(3)①26种 ② ③取少量待测液于洁净的试管中,滴加硫氰化钾,若溶液变血红色,则存在 (2
分) ④
(4)ds区
【解析】周期表前四周期的元素X、Y、Z、W,原子序数依次增大,原子核外有6种不同运动状态的电子,
X为C元素;Y原子基态时2p原子轨道上有3个未成对的电子,Y为N元素;Z有多种氧化物,其中一种
红棕色氧化物可作涂料,该物质为Fe O,Z为Fe元素;W位于第四周期,其原子最外层只有1个电子,
2 3
且内层都处于全充满状态1s22s2p63s23p63d104s1,即为Cu元素;所以前四周期的元素X、Y、Z、W分别为:C、N、Fe、Cu。
(1)根据分析,X为C,位于第二周期IVA族,故答案为:第二周期IVA族;
(2)①H的电子排布式为1s1,1s轨道半满,比较稳定,因此第一电离能C<H,故答案为:小于;
②同周期元素从左到右电负性依次增强,因此电负性C<N,故答案为:小于;
③NH 分子间有氢键,熔沸点较高,因此沸点CH<NH ,故答案为:小于;
3 4 3
(3)①Z为Fe元素,核外电子排布式为1s22s2p63s23p63d64s2,每个电子空间运动状态都不相同,因此共有26
种不同空间运动状态的电子;
②Fe2+的核外电子排布式为1s22s2p63s23p63d6,Fe3+的核外电子排布式为1s22s2p63s23p63d5,Fe3+的3d轨道半
满,因此Fe3+较稳定;
③Fe3+遇SCN-生成血红色的Fe(SCN) ,可用SCN-检验,取少量待测液于洁净的试管中,滴加KSCN,若溶
3
液变血红色,则存在Fe3+;
④与Z元素处于同周期同族且原子序数比Z大2的元素为Ni,Ni3+的核外电子排布式为1s22s22p63s23p63d7;
(4)Cu位于元素周期表的ds区;
16.(2021·全国·高三课时练习)(10分)现有五种元素,其中A、B、C为短周期主族元素,D、E为第
四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等
B元素原子的核外p电子数比s电子数少1
C元素的第一至第四电离能如下:
I = 738 kJ·mol-1 I= 1451 kJ·mol-1 I = 7733 kJ·mol-1 I = 10540 kJ·mol-1
1 2 3 4
D是前四周期中电负性最小的元素
E在周期表的第七列
(1)B元素基态原子中能量最高的电子的电子云在空间有_______个伸展方向,原子轨道呈_______形。
(2)E位于第_______族、_______区,该元素原子的核外电子排布式为_______。
(3)某同学根据上述信息,推断C基态原子的电子排布图为 , 该同学所画的电子排布
图违背了_______。
(4)已知BA 为离子化合物,写出其电子式:_______。
5
(5)检验D元素的方法是_______,请用原子结构的知识解释产生此现象的原因:_______。
【答案】(除标注外,每空1分)(1)3 哑铃
(2)Ⅶ B d 1s2 2s2 2p63s2 3p63d54s2 (或[Ar]3d54s2)
(3)泡利不相容原理(4)
(5)焰色反应 当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。电子从
较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量(2分)
【解析】A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大,其中A元素的
核外电子数和电子层数相等,则A为H元素;B元素原子的核外p电子数比s电子数少1,则其原子核外
电子排布式为1s22s22p3,故B为N元素;C元素第三电离能剧增,则C元素原子最外层有2个电子,原子
序数大于氮,故C为Mg;D是前四周期中电负性最小的元素,则D为K元素;E在周期表的第七列,则E
为Mn。
(1)B元素为N元素,基态N原子的核外电子排布式为1s22s22p3,能量最高的电子为2p能级电子,其电子
云在空间有3个伸展方向,原子轨道呈哑铃形,故答案为:3;哑铃;
(2)E为Mn元素,Mn位于第四周期第七列,即处于周期表中第四周期第VII B族,属于d区元素,基态
Mn原子的核外电子排布式为1s22s22p63s23p63d54s2 (或[Ar]3d54s2),故答案为:ⅦB;d;
1s22s22p63s23p63d54s2 (或[Ar]3d54s2);
(3)由图可知,该同学所画的电子排布图3s轨道2个电子自旋方向相同,因此该同学所画的电子排布图违背
了泡利不相容原理,故答案为:泡利不相容原理;
(4)NH 为离子化合物,由 与H-构成,其电子式为 ,故答案为:
5
;
(5)D元素为K元素,检验钾元素的方法是焰色反应,产生此现象的原因是:基态原子的电子吸收能量后,
电子会跃迁到较高能级,变为激发态原子,电子从较高能量的激发态跃迁到较低能级或基态时,以光的形
式释放能量,故答案为:焰色反应;当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态
原子,电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量。