第 3 讲 化学平衡常数
课 程 标 准 知 识 建 构
1.能书写平衡常数表达式,能进行平衡常数、转化率
的简单计算。
2.能利用平衡常数和浓度商的关系判断化学反应是
否达到平衡及平衡移动的方向。
3.了解浓度商和化学平衡常数的相对大小与反应方
向间的联系。
4.知道化学反应是有方向的,知道化学反应的方向
与反应的焓变和熵变有关。
一、化学平衡常数
1.概念
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应
物浓度幂之积的比值是一个常数,用符号K 表示。
2.数学表达式
(1)一般形式:对于反应mA(g)+nB(g)pC(g)+qD(g),K=(固体和纯液体的
浓度视为常数,通常不计入平衡常数表达式中)。
(2)实例
如:①C(s)+H O(g)CO(g)+H (g)的平衡常数表达式K=。
2 2
②Fe3+(aq)+3H O(l)Fe(OH) (s)+3H+(aq)的平衡常数表达式K=。
2 3
(3)化学平衡常数与化学方程式的关系
化学平衡常数是指某一具体反应的平衡常数。若反应方向改变,则平衡常数
改变。若化学方程式中各物质的化学计量数等倍扩大或缩小,尽管是同一反应,
平衡常数也会改变。如:
化学方程式 平衡常数 关系式
N (g)+
2
K = K =
1 2
3H (g)2NH (g)
2 3
(或K1)
N (g)+H (g)NH (g) K =
2 2 3 2
K =
3
2NH 3 (g)N 2 (g)+ K 3 =3H (g)
2
3.意义
平衡常数表示可逆反应正向进行的程度,K值越大,反应进行的程度越大。
4.影响因素
K只受温度影响,与反应物或生成物的浓度变化无关。
5.应用
(1)判断可逆反应进行的程度。通常K>105可认为反应彻底,K<10-5认为反应
不能发生。
(2)判断反应是否达到平衡或反应进行的方向。
对于化学反应aA(g)+bB(g)cC(g)+dD(g)的任意状态,浓度商:Q=。
(3)判断可逆反应的热效应
升高温度
降低温度
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)平衡常数能体现可逆反应进行的程度( )
(2)平衡常数大的可逆反应的平衡体系中,生成物的浓度一定大( )
(3)平衡常数表达式中应含有参加反应的所有物质( )
(4)增大反应物的浓度,平衡正向移动,化学平衡常数增大( )
(5)对于某一可逆反应,升高温度则化学平衡常数一定变大( )
(6)平衡常数发生变化,化学平衡必定发生移动( )
(7)反应A(g)+3B(g)2C(g)达到平衡后,温度不变,增大压强,平衡正向移
动,平衡常数增大( )
答案 (1)√ (2)× (3)× (4)× (5)× (6)√ (7)×
二、转化率
1.概念
转化率是指反应进行到一定程度时某一反应物转化的百分率。平衡转化率是
可逆反应达到平衡状态时某反应物的转化百分率。
2.数学表达式
对于反应mA(g)+nB(g)pC(g)+qD(g),A(g)的平衡转化率可表示为:
α(A)= × 100%c (A)代表A的初始浓度,c (A)代表A的平衡浓度。
0 平
3.“三段式”法应用于化学平衡的计算
(1)一个模式——“三段式”
如mA(g)+nB(g)pC(g)+qD(g),令A、B起始物质的量浓度分别为a mol·L
-1、b mol·L-1,达到平衡后消耗A的物质的量浓度为mx mol·L-1。
则K=,α(A)=×100%。
(2)明确三个量的关系
①三个量:即起始量、变化量、平衡量。
②对于同一反应物,起始量-变化量=平衡量。
③对于同一生成物,起始量+变化量=平衡量。
④各转化量之比等于各反应物的化学计量数之比。
(3)掌握四个公式
①恒容条件下反应物的转化率=×100%=×100%。
②生成物的产率:实际产量(指生成物)占理论产量的百分数。一般来讲,转化
率越高,原料利用率越高,产率越高。
产率=×100%。
③平衡时混合物组分的百分含量=×100%。
④某气体组分的体积分数=×100%。
【诊断2】 在一定温度下,向容积为2 L的恒容密闭容器中充入2 mol M和一
定量的N,发生反应M(g)+N(g)E(g);当反应进行到4 min时达到平衡,测得
M的浓度为0.2 mol·L-1。下列说法正确的是( )
A.4 min时,M的转化率为80%
B.0~4 min,用M表示的平均反应速率为0.8 mol·L-1·min-1
C.2 min时,M的物质的量浓度为0.6 mol·L-1
D.4 min后,向容器中充入惰性气体,M的物质的量减小
答案 A
解析 根据题意列出三段式:
M(g)+N(g)E(g)
起始(mol·L-1) 1 0
转化(mol·L-1) 0.8 0.8
平衡(mol·L-1) 0.2 0.84 min时,M的转化率为×100%=80%,故A正确;0~4 min,用M表示的平
均反应速率为=0.2 mol·L-1·min-1,故B错误;若反应速率不变,2 min时M的转
化浓度为 0.2 mol·L-1·min-1×2 min=0.4 mol·L-1,M 的物质的量浓度为 0.6
mol·L-1,但在反应过程中,正反应速率逐渐减小,前2 min的反应速率比后2 min
反应速率快,因此M的物质的量浓度小于0.6 mol·L-1,故C错误;恒容条件下,
向容器中充入惰性气体,平衡不移动,M的物质的量不变,故D错误。
三、化学反应进行的方
1.自发过程
(1)含义
在一定条件下,不需要借助外力作用就能自动进行的过程。
(2)特点
①体系趋向于从高能状态转变为低能状态(体系对外部做功或释放热量)
②在密闭条件下,体系有从有序自发地转变为无序的倾向性(无序体系更加
稳定)。
2.化学反应方向
(1)判据
(2)一般规律
①ΔH<0,ΔS>0的反应任何温度下都能自发进行;
②ΔH>0,ΔS<0的反应任何温度下都不能自发进行;③ΔH和ΔS的作用相反,且相差不大时,温度对反应的方向起决定性作用。当
ΔH<0,ΔS<0时,低温下反应能自发进行;当ΔH>0,ΔS>0时,高温下反应能自
发进行。
【诊断3】 判断下列说法是否正确,正确的打√,错误的打×。
(1)放热过程有自发进行的倾向性,但并不一定能自发进行,吸热过程没有自
发进行的倾向性,但在一定条件下也可自发进行( )
(2)CaCO (s)===CaO(s)+CO (g)室温下不能自发进行,说明该反应的ΔH<0(
3 2
)
(3)某化学反应的ΔH=-122 kJ·mol-1,ΔS=-431 J·mol-1·K-1,则此反应仅
在低温下自发进行( )
(4)-10 ℃的水结成冰,可用熵变的判据来解释反应的自发性( )
(5)判断过程的自发性能确定过程能否一定发生和过程发生的速率( )
(6)在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方
向( )
答案 (1)√ (2)× (3)√ (4)× (5)× (6)×
考点一 化学平衡常数的意义和应用
【典例1】 甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用
CO或CO 来生产燃料甲醇。已知制备甲醇的有关化学反应以及在不同温度下的
2
化学反应平衡常数如下表所示:
温度/℃
化学反应 平衡常数
500 800
①2H (g)+CO(g)CH OH(g) K 2.5 0.15
2 3 1
②H (g)+CO (g)H O(g)+CO(g) K 1.0 2.50
2 2 2 2
③3H (g)+CO (g)CH OH(g)+H O(g) K
2 2 3 2 3
(1)据反应①与②可推导出K 、K 与K 之间的关系,则K =________(用K 、
1 2 3 3 1
K 表示)。
2
(2)反应③的ΔH________(填“>”或“<”)0。
(3)500 ℃时测得反应③在某时刻H (g)、CO (g)、CH OH(g)、H O(g)的浓度
2 2 3 2
(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v ________(填“>”“=”或
正
“<”)v 。
逆
答案 (1)K ·K (2)< (3)>
1 2解析 (1)K =,
1
K =,
2
K =,
3
K =K ·K 。
3 1 2
(2)根据K =K ·K 500 ℃、800 ℃时,反应③的平衡常数分别为2.5、0.375;升
3 1 2,
温,K减小,正反应为放热反应,所以ΔH<0。
(3)500 ℃时,K =2.5
3
Q==≈0.88<K
3
故反应正向进行,v >v 。
正 逆
【对点练1】 (平衡常数与方程式的关系)(2020·西安市铁一中学质检)O 是一
3
种很好的消毒剂,具有高效、洁净、方便、经济等优点。O 可溶于水,在水中易分
3
解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生的反应如
下:
反应① O O +[O] ΔH>0 平衡常数为K ;
3 2 1
反应② [O]+O 2O ΔH<0 平衡常数为K ;
3 2 2
总反应:2O 3O ΔH<0 平衡常数为K。
3 2
下列叙述正确的是( )
A.降低温度,总反应K减小
B.K=K +K
1 2
C.适当升温,可提高消毒效率
D.压强增大,K 减小
2
答案 C
解析 降温,总反应平衡向右移动,K增大,A项错误;K =、K =、K==
1 2
K ·K ,B项错误;升高温度,反应①平衡向右移动,c([O])增大,可提高消毒效率,
1 2
C项正确;对于给定的反应,平衡常数只与温度有关,D项错误。
【对点练2】 (平衡常数及影响因素)在25 ℃时,密闭容器中X、Y、Z三种气
体的初始浓度和平衡浓度如下表:
物质 X Y Z
初始浓度/mol·L-1 0.1 0.2 0
平衡浓度/mol·L-1 0.05 0.05 0.1
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%B.反应可表示为X(g)+3Y(g)2Z(g),其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
答案 C
解析 反应达到平衡时,X的转化率为
×100%=50%,故A正确;根据反应速率之比等于浓度变化量之比等于化学
计量数之比可知,Δc(X)∶Δc(Y)∶Δc(Z)=0.05∶0.15∶0.1=1∶3∶2,则反应的
化学方程式为X(g)+3Y(g)2Z(g),K===1 600,故B正确;增大压强平衡向
生成Z的方向移动,但温度不变,平衡常数不变,故C错误;平衡常数只受温度的
影响,温度改变时,化学平衡常数一定变化,故D正确。
【对点练3】 (平衡常数的应用)(2020·四川省成都模拟)在300 mL的密闭容器
中,放入镍粉并充入一定量的 CO 气体,一定条件下发生反应:Ni(s)+
4CO(g)Ni(CO) (g),已知该反应平衡常数与温度的关系如下表:
4
温度/ ℃ 25 80 230
平衡常数 5×104 2 1.9×10-5
下列说法不正确的是( )
A.上述生成Ni(CO) (g)的反应为放热反应
4
B.25 ℃时反应Ni(CO) (g)Ni(s)+4CO(g)的平衡常数为2×10-5
4
C.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO) 的平衡浓度为2 mol·L
4
-1
D.80 ℃时,测得某时刻,Ni(CO) 、CO 浓度均为 0.5 mol·L-1,则此时
4
v(正)>v(逆)
答案 D
解析 随着温度的升高,平衡常数逐渐减小,说明升高温度,平衡向逆反应方
向移动,因此正反应是放热反应,A项正确;逆反应的平衡常数是正反应的倒数,
B正确;选项C中,根据80 ℃时平衡常数的表达式可知,Ni(CO) 的平衡浓度为2
4
mol·L-1,C正确;如果80 ℃时,测得某时刻,Ni(CO) 、CO浓度均为0.5 mol·L-1,
4
则此时Q==8>K=2,反应向逆反应方向进行,则此时v(正)
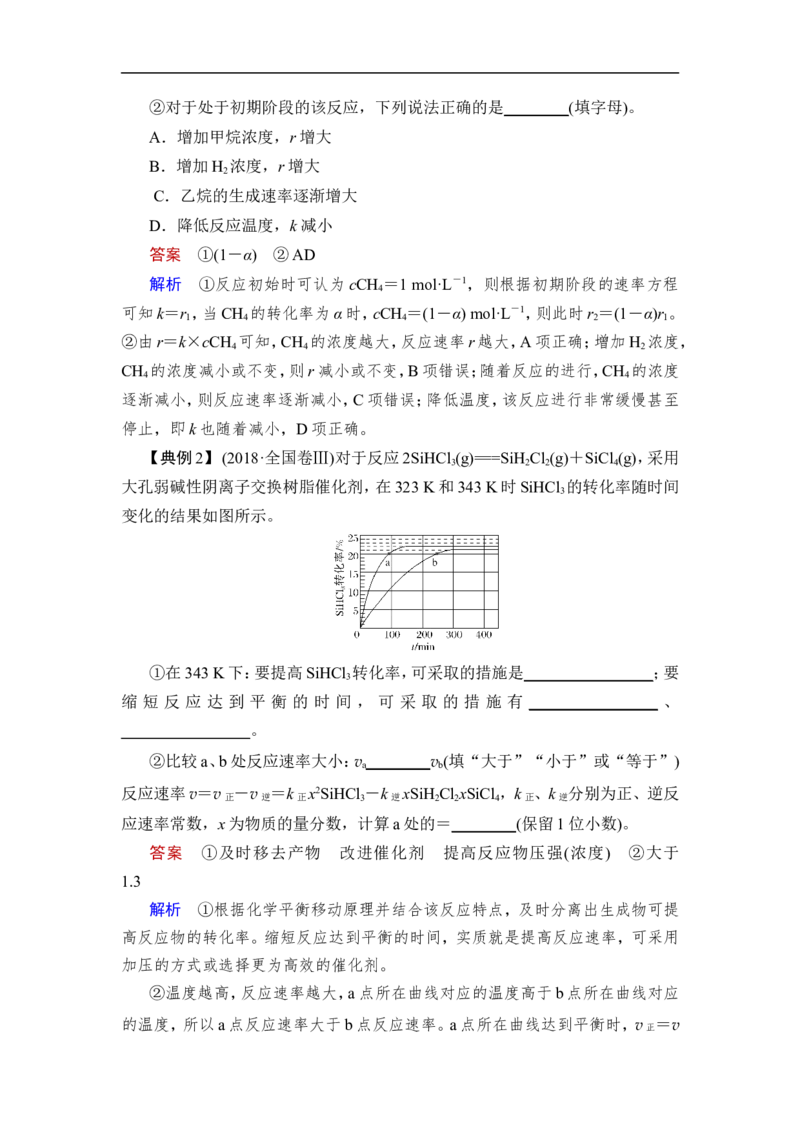
v(Z)
C.若Z点处于化学平衡,则210 ℃时反应的平衡常数K= mol/L
D.190 ℃时,0~150 min之间的MTP的平均反应速率为 mol/(L·min)
答案 C
解析 A项,因起始浓度相同,X、Y两点转化率相同,所以MTP的浓度也相等,
正确;B项,Z点转化率高,此时TOME浓度只有0.02a mol/L,所以瞬时速率
v(X)>v(Z),正确;C项,若Z点为平衡点,此时c(TOME)=0.02a mol/L,c(MTP)=
0.98a mol/L,但因移出甲醇,甲醇浓度不为0.98a mol/L,错误;D项,0~150 min
时间内,Δc(MTP)=0.67a mol/L,正确。
2.(2021·1月江苏省新高考适应性考试,13)在二氧化碳加氢制甲烷的反应体系中,
主要发生反应的热化学方程式为
反应Ⅰ: CO (g)+4H (g)CH (g)+2H O(g)
2 2 4 2
ΔH=-164.7 kJ·mol-1
反应 Ⅱ:CO (g)+H (g)CO(g)+ H O(g)
2 2 2
ΔH=41.2 kJ·mol-1
反应Ⅲ:2CO(g)+2H (g)CO (g)+ CH (g)
2 2 4
ΔH=-247.1 kJ·mol-1
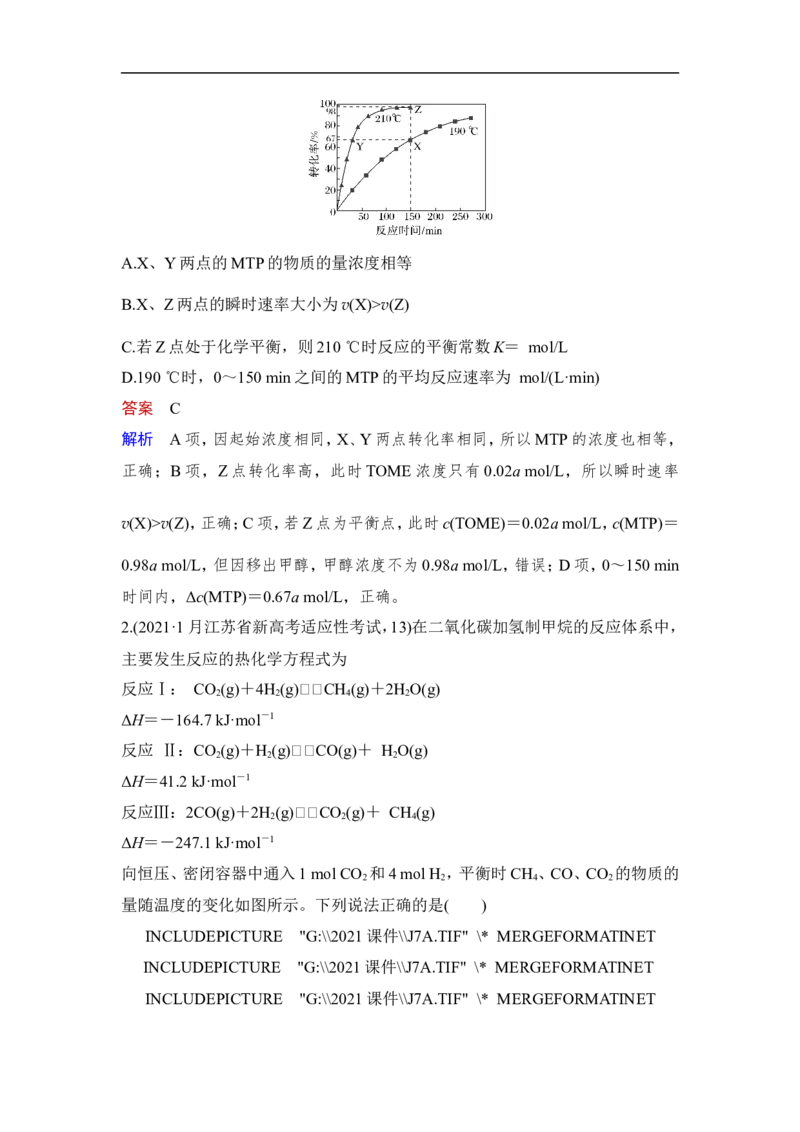
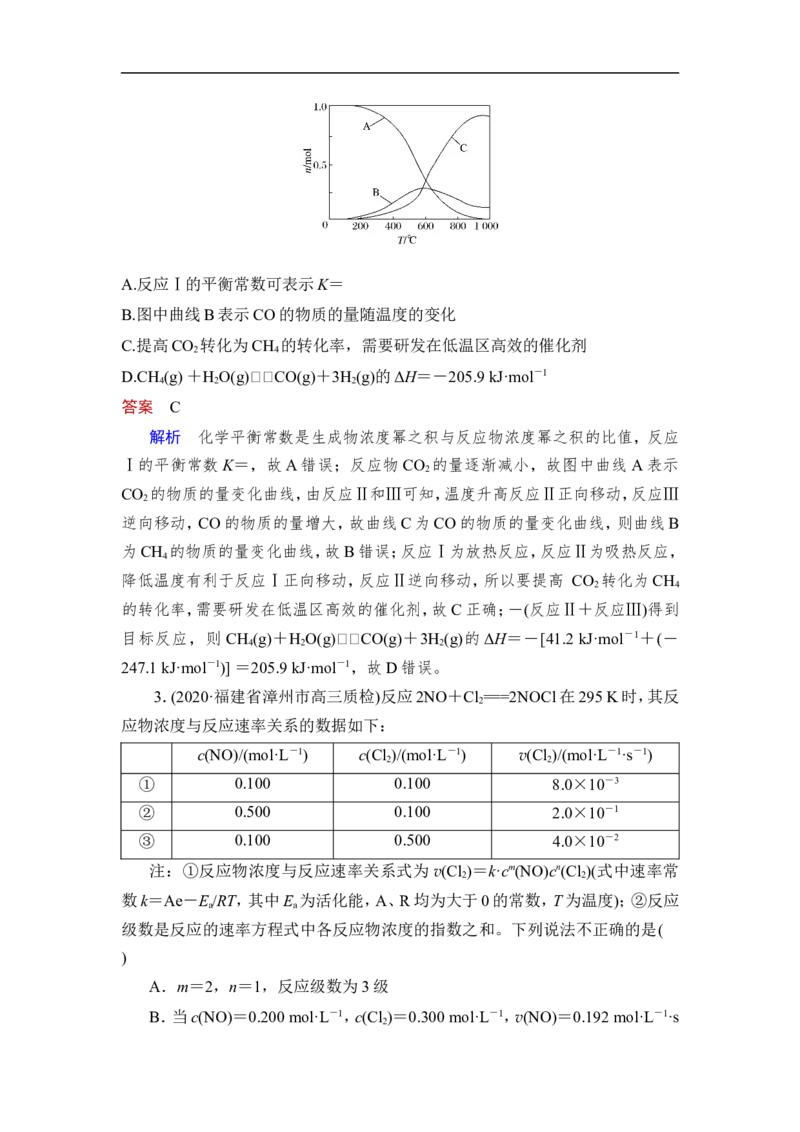
向恒压、密闭容器中通入1 mol CO 和4 mol H ,平衡时CH 、CO、CO 的物质的
2 2 4 2
量随温度的变化如图所示。下列说法正确的是( )
INCLUDEPICTURE "G:\\2021课件\\J7A.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\J7A.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\J7A.TIF" \* MERGEFORMATINETA.反应Ⅰ的平衡常数可表示K=
B.图中曲线B表示CO的物质的量随温度的变化
C.提高CO 转化为CH 的转化率,需要研发在低温区高效的催化剂
2 4
D.CH (g) +H O(g)CO(g)+3H (g)的ΔH=-205.9 kJ·mol-1
4 2 2
答案 C
解析 化学平衡常数是生成物浓度幂之积与反应物浓度幂之积的比值,反应
Ⅰ的平衡常数K=,故A错误;反应物CO 的量逐渐减小,故图中曲线 A表示
2
CO 的物质的量变化曲线,由反应Ⅱ和Ⅲ可知,温度升高反应Ⅱ正向移动,反应Ⅲ
2
逆向移动,CO的物质的量增大,故曲线C为CO的物质的量变化曲线,则曲线B
为CH 的物质的量变化曲线,故B错误;反应Ⅰ为放热反应,反应Ⅱ为吸热反应,
4
降低温度有利于反应Ⅰ正向移动,反应Ⅱ逆向移动,所以要提高 CO 转化为CH
2 4
的转化率,需要研发在低温区高效的催化剂,故C正确;-(反应Ⅱ+反应Ⅲ)得到
目标反应,则 CH (g)+H O(g)CO(g)+3H (g)的ΔH=-[41.2 kJ·mol-1+(-
4 2 2
247.1 kJ·mol-1)] =205.9 kJ·mol-1,故D错误。
3.(2020·福建省漳州市高三质检)反应2NO+Cl ===2NOCl在295 K时,其反
2
应物浓度与反应速率关系的数据如下:
c(NO)/(mol·L-1) c(Cl )/(mol·L-1) v(Cl )/(mol·L-1·s-1)
2 2
① 0.100 0.100 8.0×10-3
② 0.500 0.100 2.0×10-1
③ 0.100 0.500 4.0×10-2
注:①反应物浓度与反应速率关系式为 v(Cl )=k·cm(NO)cn(Cl )(式中速率常
2 2
数k=Ae-E /RT,其中E 为活化能,A、R均为大于0的常数,T为温度);②反应
a a
级数是反应的速率方程式中各反应物浓度的指数之和。下列说法不正确的是(
)
A.m=2,n=1,反应级数为3级
B.当c(NO)=0.200 mol·L-1,c(Cl )=0.300 mol·L-1,v(NO)=0.192 mol·L-1·s
2-1
C.加入催化剂可以改变反应途径,也可以增大速率常数k,而加快反应速率
D.升高温度,可以增大反应的活化能E ,从而使速率常数k增大
a
答案 D
解析 由表中①③数据可知=()n,n=1,由①②组数据可知=()m,m=2,由①
数据可知k==8.0;据数据分析知m=2,n=1,反应级数为3级,A正确;当
c(NO) = 0.200 mol·L - 1 , c(Cl ) = 0.300 mol·L - 1 时 , v(NO) = 2v(Cl ) =
2 2
2×8.0×0.2002×0.300 mol·L-1·s-1=0.192 mol·L-1·s-1,B正确;催化剂可降低反
应的活化能,增大速率常数,增大反应速率,C正确;升高温度,活化能不变,D错
误。
4.T 温度时,在容积为 2 L 的恒容密闭容器中发生反应 2NO(g)+
1
O (g)2NO (g) ΔH<0,实验测得:v =v (NO)=2v (O )=k
2 2 正 消耗 消耗 2 正
c2(NO)·c(O ),v =v (NO )=k c2(NO )、k 、k 为速率常数,受温度影响。容
2 逆 消耗 2 逆 2 正 逆
器中各反应物和生成物的物质的量随时间变化如图所示:
(1)下列说法能表明该反应已经达到平衡状态的是________________(填标号)。
A.混合气体的密度不变
B.混合气体的颜色不变
C.k 、k 不变
正 逆
D.2v (O )=v (NO )
正 2 逆 2
(2)化学平衡常数K与速率常数k 、k 的数学关系式为K=________。
正 逆
答案 (1)BD (2)
解析 (1)由于气体质量和容器体积保持不变,故混合气体密度始终保持恒定
不能由此判断是否达到平衡状态,A错误;混合气体的颜色不变,即NO 的量保
2
持不变,可以说明反应达到平衡状态,B正确;k 、k 只与温度有关,与是否达到
正 逆
平衡状态无关,C错误;当2v (O )=v (NO )时,正、逆反应速率相等,可以说明
正 2 逆 2
反应达到平衡状态,D正确。(2)达到化学平衡状态时v =v ,即k c2(NO)·c(O )
正 逆 正 2
=k c2(NO ),则平衡常数K==。
逆 25 . (1) 已 知 反 应 2NO(g) + O (g)2NO (g) 的 正 反 应 速 率 v( 正 ) =
2 2
k·cm(NO)·cn(O ),其中k为速率常数,可通过下列实验数据计算k 、m、n。
2 1
起始浓度/(mol·L-1)
组别
NO O
2
1 0.02 0.012 5 7.98×10-3
2 0.02 0.025 0 15.96×10-3
3 0.04 0.012 5 31.92×10-3
则k=________,m=________,n=________。
(2)已知反应2NO(g)+O (g)2NO (g)的历程可表示为
2 2
第一步:NO+NON O 快速平衡
2 2
第二步:N O +O ――→2NO 慢反应
2 2 2 2
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中,v(正)=
k ·c2(NO),v(逆)=k ·c(N O )。下列叙述正确的是________(填字母)
1 -1 2 2
A.第一步反应的平衡常数K=
B.v(第一步的正反应)<v(第二步的反应)
C.第二步的活化能比第一步的活化能高
D.第二步中N O 与O 的碰撞100%有效
2 2 2
答案 (1)1 596 L2·mol-2·s-1 2 1 (2)AC
解析 (1)由组1和2可知,NO浓度不变时,氧气的浓度增大1倍,正反应速
率增大1倍,故n=1;由组1和3可知,氧气的浓度不变时,NO的浓度增大1倍,
正反应速率变为原来的 4 倍,故 m=2;将 m=2 和 n=1 代入第 1 组数据:
7.98×10-3 mol·L-1·s-1=k×(0.02 mol·L-1)2×0.012 5 mol·L-1,解得 k=1 596
L2·mol-2·s-1。(2)第一步反应的平衡常数 K=,达到平衡时v(正)=v(逆),则有
k ·c2(NO)=k ·c(N O ),得=,K==,A正确;v(第一步的正反应)是快反应,v(第
1 -1 2 2
二步的反应)是慢反应,则有v(第一步的正反应)>v(第二步的反应),B错误;第二
步的反应慢,活化能高,第二步的活化能比第一步的活化能高,C正确;第二步是
慢反应,说明N O 与O 的有效碰撞的几率较小,不可能达到100%,D错误。
2 2 2
6.(2020·课标全国Ⅰ节选)研究表明,SO 催化氧化的反应速率方程为:v=
2
k(-1)0.8(1-nα′),式中:k为反应速率常数,随温度t升高而增大;α为SO 平衡
2
转化率,α′为某时刻SO 转化率,n为常数。在α′=0.90时,将一系列温度下的
2
k、α值代入上述速率方程,得到v~t曲线,如图所示。曲线上v最大值所对应温度称为该α′下反应的最适宜温度t 。tt 后,v逐渐下降,原因是______________________________。
m
答案 升高温度,k增大使v逐渐提高,但α降低使v逐渐下降。tt 后,k增大对v的提高小于α引起的降低
m
解析 升高温度,反应速率常数k增大,反应速率v提高,但α降低使反应速
率逐渐下降。tt 后,k增大对v的
m m
提高小于α引起的降低。
7.(2020·山东模考)探索氮氧化合物反应的特征及机理,对处理该类化合物
的污染问题具有重要意义。回答下列问题:
(1)工业上利用Na CO 溶液吸收NO、NO 混合气制备NaNO ,该反应可实现
2 3 2 2
NO和NO 的完全转化,反应的化学方程式为_________________________。
2
(2)NO 可发生二聚反应生成N O ,化学方程式为2NO (g)N O (g),
2 2 4 2 2 4
上述反应达到平衡后,升高温度可使体系颜色加深,则该反应的ΔH________0(填
“>”或“<”)。
已知该反应的正反应速率方程为v =k ·c2(NO ),逆反应速率方程为v =k
正 正 2 逆
·c(N O ),其中k 、k 分别为正、逆反应的速率常数。则下图(lg k表示速率常数
逆 2 4 正 逆
的对数;表示温度的倒数)所示①、②、③、④四条斜线中,能表示lg k 随变化关
正
系的是斜线________,能表示lg k 随变化关系的是斜线________。
逆
(3)图中A、B、C、D点的纵坐标分别为a+1.5、a+0.5、a-0.5、a-1.5,则温度
T 时化学平衡常数K=________mol-1·L。已知温度T 时,某时刻恒容密闭容器中
1 1
NO 、N O 浓度均为0.2 mol·L-1,此时v ________v (填“>”或“<”);上述
2 2 4 正 逆
反应达到平衡后,继续通入一定量的NO ,则NO 的平衡转化率将________,NO
2 2 2
的平衡浓度将________(填“增大”、“减小”或“不变”)。答案 (1)NO+NO +Na CO ===2NaNO +CO
2 2 3 2 2
(2)< ③ ④ (3)10 > 增大 增大
解析 (1)Na CO 溶液和NO、NO 反应生成NaNO ,根据原子守恒,化合价升
2 3 2 2
降守恒可得化学方程式为:NO+NO +Na CO ===2NaNO +CO 。(2)升高温度体
2 2 3 2 2
系颜色加深,平衡逆向移动,则正反应为放热反应,ΔH<0;化学反应速率和温度
成正比,随着温度降低,增大,正逆反应速率减小,则lg k 和lg k 均减小,由于
正 逆
温度降低平衡正向移动,v >v ,则降低相同温度时lg k 减小更快,则③表示
正 逆 逆
lg k 随变化关系的斜线,④表示lg k 随变化关系的斜线。(3)化学平衡常数K=
正 逆
=×=×=mol-1·L=10 mol-1·L;NO 、N O 浓度均为0.2 mol·L-1。则浓度商Q=
2 2 4
mol-1·L=5 mol-1·L<K,则平衡正向移动,v >v ;反应达到平衡后,继续通入
正 逆
一定量的NO ,恒容密闭容器中,等效于达到平衡后增大压强,平衡正向移动;根
2
据勒夏特列原理,达到平衡时浓度比起始时大。
1.(2020·北京卷)一定温度下,反应I (g)+H (g)2HI(g)在密闭容器中达到
2 2
平衡时,测得c(I )=0.11 mmol·L-1,c(HI)=0.78 mmol·L-1。相同温度下,按下列4
2
组初始浓度进行实验,反应逆向进行的是(注:1 mmol·L-1=10-3 mol·L-1)( )
A B C D
c(I )/mmol·L-1 1.00 0.22 0.44 0.11
2
c(H )/mmol·L-1 1.00 0.22 0.44 0.44
2
c(HI)/mmol·L-1 1.00 1.56 4.00 1.56
答案 C
解析 题目中缺少c(H ),不能计算K,则不能通过Q与K的关系判断平衡的
2
移动方向,但可比较4个选项中Q的大小关系,Q越大,则可能逆向移动。
Q(A)==1,
Q(B)==50.28,
Q(C)==82.64,
Q(D)==50.28,
Q(C)的值最大,答案为C。
2.(2020·海南卷)NO与CO是燃油汽车尾气中的两种有害气体,常温常压下
它们之间的反应:
CO(g)+NO(g)===CO (g)+N (g)
2 2
ΔH=-374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确的是( )
A.K很大,NO与CO在排入大气之前就已反应完全
B.增大压强,平衡将向右移动,K>2.5×1060
C.升高温度,既增大反应速率又增大K
D.选用适宜催化剂可达到尾气排放标准
答案 D
解析 平衡常数很大,表示该反应所能进行的程度大,由于NO与CO反应速
率较小,在排入大气之前没有反应完全,故A错误;平衡常数只与温度有关,增大
压强,K不变,故B错误;CO(g)+NO(g)===CO (g)+N (g)正反应放热,升高温度,
2 2
速率加快,平衡逆向移动,K减小,故C错误;选用适宜催化剂可加快反应速率,
使尾气得到净化,达到尾气排放标准,故D正确。
3.(2020·全国卷Ⅰ节选)硫酸是一种重要的基本化工产品。接触法制硫酸生产
中的关键工序是SO 的催化氧化:
2
SO (g)+O (g)SO (g) ΔH=-98 kJ·mol-1。
2 2 3
回答下列问题:
将组成(物质的量分数)为2m% SO (g)、m% O (g)和q% N (g)的气体通入反应
2 2 2
器,在温度t、压强p条件下进行反应。平衡时,若SO 转化率为α,则SO 压强为
2 3
____________,平衡常数K =________(以分压表示,分压=总压×物质的量分
p
数)。
答案 p
解析 设通入的SO 、O 和N 共100 mol,利用三段式法进行计算:
2 2 2
平衡时气体的总物质的量为(3m+q-mα) mol,则 p(SO )=p×(2m-
2
2mα)/(3m+q-mα),p(O )=p×(m-mα)/(3m+q-mα),p(SO )=p×2mα/(3m+q
2 3
-mα),因3m+q=100,K =,代入计算得K =。
p p
4.(2020·全国卷Ⅲ节选)二氧化碳催化加氢合成乙烯是综合利用CO 的热点
2
研究领域。回答下列问题:
CO 催化加氢生成乙烯和水的反应中理论计算表明,原料初始组成
2
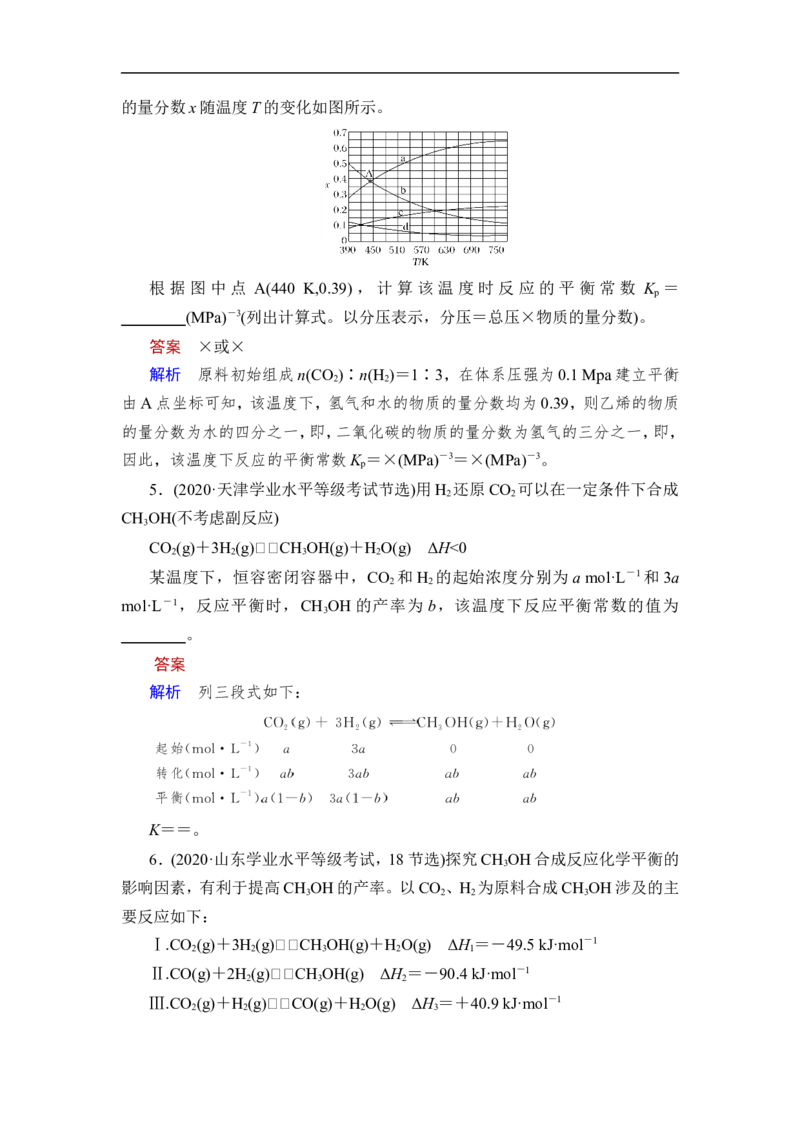
n(CO )∶n(H )=1∶3,在体系压强为0.1 MPa,反应达到平衡时,四种组分的物质
2 2的量分数x随温度T的变化如图所示。
根 据 图 中 点 A(440 K,0.39) , 计 算 该 温 度 时 反 应 的 平 衡 常 数 K =
p
________(MPa)-3(列出计算式。以分压表示,分压=总压×物质的量分数)。
答案 ×或×
解析 原料初始组成n(CO )∶n(H )=1∶3,在体系压强为0.1 Mpa建立平衡
2 2
由A点坐标可知,该温度下,氢气和水的物质的量分数均为0.39,则乙烯的物质
的量分数为水的四分之一,即,二氧化碳的物质的量分数为氢气的三分之一,即,
因此,该温度下反应的平衡常数K =×(MPa)-3=×(MPa)-3。
p
5.(2020·天津学业水平等级考试节选)用H 还原CO 可以在一定条件下合成
2 2
CH OH(不考虑副反应)
3
CO (g)+3H (g)CH OH(g)+H O(g) ΔH<0
2 2 3 2
某温度下,恒容密闭容器中,CO 和H 的起始浓度分别为a mol·L-1和3a
2 2
mol·L-1,反应平衡时,CH OH 的产率为 b,该温度下反应平衡常数的值为
3
________。
答案
解析 列三段式如下:
K==。
6.(2020·山东学业水平等级考试,18节选)探究CH OH合成反应化学平衡的
3
影响因素,有利于提高CH OH的产率。以CO 、H 为原料合成CH OH涉及的主
3 2 2 3
要反应如下:
Ⅰ.CO (g)+3H (g)CH OH(g)+H O(g) ΔH =-49.5 kJ·mol-1
2 2 3 2 1
Ⅱ.CO(g)+2H (g)CH OH(g) ΔH =-90.4 kJ·mol-1
2 3 2
Ⅲ.CO (g)+H (g)CO(g)+H O(g) ΔH =+40.9 kJ·mol-1
2 2 2 3一定条件下,向容积为V L的恒容密闭容器中通入1 mol CO 和3 mol H 发生
2 2
上述反应,达到平衡时,容器中CH OH(g)为a mol,CO为b mol,此时H O(g)的浓
3 2
度为________ mol·L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为
________。
答案
解析 由题述三个反应可知,根据碳元素守恒,剩余CO 为(1-a-b) mol,则
2
反应消耗CO 为[1-(1-a-b)] mol=(a+b) mol,根据反应Ⅰ和Ⅲ中物质对应关
2
系可知,反应Ⅰ中CO (g)~H O(g),反应Ⅲ中也有CO (g)~H O(g),故生成H O
2 2 2 2 2
为(a+b) mol,即H O(g)的浓度为 mol·L-1。平衡时CH OH(g)、CO(g)、H O(g)的
2 3 2
浓度分别为 mol·L-1、 mol·L-1、 mol·L-1,则从开始至平衡,消耗CO (g)的浓度
2
为(+) mol·L-1= mol·L-1,达到平衡时n(CH OH)=a mol,根据H原子守恒,起
3
始时通入3 mol H ,平衡时CH OH和H O中所含H原子的物质的量为4a mol+
2 3 2
2(a+b) mol=(6a+2b) mol,平衡时n(H )=3 mol- mol=(3-3a-b) mol,即平
2
衡时CO (g)、H (g)的浓度分别为 mol·L-1、 mol·L-1,则反应Ⅲ的平衡常数为=
2 2
=。
7.(2021·1月湖南普高校招生适应性考试,17)氨基甲酸铵(H NCOONH )为尿素生
2 4
产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
己知:Ⅰ.N (g)+3H (g)2NH (g) ΔH =-92.4 kJ·mol-1
2 2 3 1
Ⅱ.C(s)+O (g)CO (g) ΔH =-393.8 kJ·mol-1
2 2 2
Ⅲ.N (g)+3H (g)+C(s)+O (g)H NCOONH (s) ΔH =-645.7 kJ·mol-1
2 2 2 2 4 3
回答下列问题:
(1) 写 出 H NCOONH 分 解 生 成 NH 与 CO 气 体 的 热 化 学 方 程 式 :
2 4 3 2
___________________________________________________________。
(2)恒容条件下,实验测得数据如下表所示:
T/K 293 298 303 308 313
p/kPa 8.60 11.40 16.24 20.86 30.66
①恒温恒容时,下列能够说明该反应已达到化学平衡状态的是__________(填字
母)。
A.容器内总压强不再改变
B.2v (NH )=v (CO )
正 3 逆 2
C.c2(NH )·c(CO )的值不再改变
3 2D.NH 的体积分数不再改变
3
②某温度下,该反应达到平衡时容器内总压强为p,写出该反应的压强平衡常数
的计算式K =________(用平衡分压代替平衡浓度,分压=总压×物质的量分数)
p
③随着温度升高,K 逐渐__________(填“增大”“减小”或“不变”),其主要
p
原因是________________。
④某温度下,达到平衡后,欲增加NH 的平衡浓度,可采取的措施有________(填
3
字母)。
A.加H NCOONH
2 4
B.加催化剂
C.减小体积增大压强
D.移走CO
2
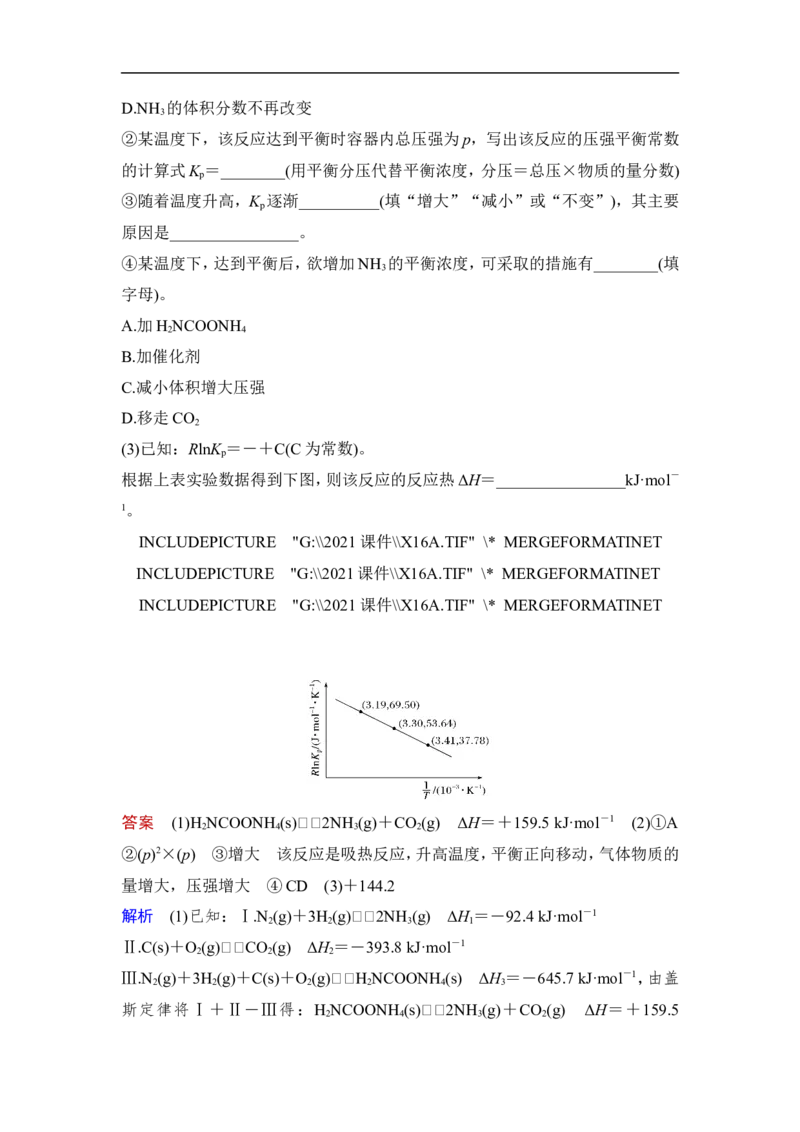
(3)已知:RlnK =-+C(C为常数)。
p
根据上表实验数据得到下图,则该反应的反应热ΔH=________________kJ·mol-
1。
INCLUDEPICTURE "G:\\2021课件\\X16A.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\X16A.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\X16A.TIF" \* MERGEFORMATINET
答案 (1)H NCOONH (s)2NH (g)+CO (g) ΔH=+159.5 kJ·mol-1 (2)①A
2 4 3 2
②(p)2×(p) ③增大 该反应是吸热反应,升高温度,平衡正向移动,气体物质的
量增大,压强增大 ④CD (3)+144.2
解析 (1)已知:Ⅰ.N (g)+3H (g)2NH (g) ΔH =-92.4 kJ·mol-1
2 2 3 1
Ⅱ.C(s)+O (g)CO (g) ΔH =-393.8 kJ·mol-1
2 2 2
Ⅲ.N (g)+3H (g)+C(s)+O (g)H NCOONH (s) ΔH =-645.7 kJ·mol-1,由盖
2 2 2 2 4 3
斯定律将Ⅰ+Ⅱ-Ⅲ得:H NCOONH (s)2NH (g)+CO (g) ΔH=+159.5
2 4 3 2kJ·mol-1。(2)①容器内总压强不再改变,说明气体的体积不再发生变化,说明可
逆反应处于平衡状态,故A正确;2v (NH )=v (CO ),不符合反应速率之比等
正 3 逆 2
于化学计量数之比,故B错误;c2(NH )·c(CO )是化学平衡常数,温度不变,平衡
3 2
常数的值不变,不能说明处于平衡状态,故C错误;反应体系中只有氨气和二氧
化碳是气体,物质的量之比等于化学计量数之比,则NH 的体积分数不再改变,
3
不能作为达到平衡状态判断的依据,故D错误。③随着温度升高,K 逐渐增大,主
p
要原因是该反应是吸热反应,升高温度,平衡正向移动,气体物质的量增大,压强
增大。④加H NCOONH ,平衡不移动,氨气的浓度不变,故A错误;加催化剂,平
2 4
衡不移动,氨气的浓度不变,故B错误;减小体积增大压强,氨气的浓度增大,故
C正确;移走CO ,平衡正向移动,氨气的浓度增大,故D正确。(3)图像上的点代
2
入RlnK =-+C得:69.50=-ΔH×3.19×10-3+C和53.64=-ΔH×3.30×10-3
p
+C,联立求解得,ΔH≈+144.2 kJ·mol-1。
一、选择题(每小题只有一个选项符合题意)
1.在一定温度下,反应N (g)+3H (g)2NH (g)的反应热和化学平衡常数分
2 2 3
别为ΔH和K,则相同温度时反应 4NH (g)2N (g)+6H (g)的反应热和化学平
3 2 2
衡常数为( )
A.2ΔH和2K B.-2ΔH和K2
C.-2ΔH和K-2 D.2ΔH和-2K
答案 C
解析 根据热化学方程式的意义,4NH (g)2N (g)+6H (g)的反应热为-
3 2 2
2ΔH,再根据平衡常数的表达式,得出其平衡常数为K-2,C项正确。
2.可逆反应:2SO (g)+O (g)2SO (g)达到平衡状态时,保持恒温恒容向容
2 2 3
器中加入一定量的O ,下列说法正确的是(K为平衡常数,Q为浓度商)( )
2
A.Q变小,K不变,O 转化率减小
2
B.Q不变,K变大,SO 转化率减小
2
C.Q不变,K变大,O 转化率增大
2
D.Q增大,K不变,SO 转化率增大
2
答案 A
解析 当可逆反应2SO (g)+O (g)2SO (g)达到平衡状态时,保持恒温恒
2 2 3容向容器中加入一定量的O ,O 的浓度增大,浓度商Q变小,平衡向右移动,氧
2 2
气转化率减小,平衡常数只受温度影响,温度不变平衡常数不变,故A正确。
3.放热反应CO(g)+H O(g)CO (g)+H (g)在温度t 时达到平衡,c (CO)=
2 2 2 1 1
c (H O)=1.0 mol·L-1,其平衡常数为K 。升高反应体系的温度至t 时,反应物的
1 2 1 2
平衡浓度分别为c (CO)和c (H O),平衡常数为K ,则( )
2 2 2 2
A.K 和K 的单位均为mol·L-1
2 1
B.K >K
2 1
C.c (CO)=c (H O)
2 2 2
D.c (CO)>c (CO)
1 2
答案 C
解析 升高温度,平衡向逆反应方向移动,平衡常数之间的关系为K <K ,
2 1
K 、K 的单位均为1,c (CO)<c (CO),故C项正确。
1 2 1 2
4.反应物和生成物均为气态的平衡体系,平衡常数表达式为K=,有关该平
衡体系说法不正确的是( )
A.升高温度,该反应平衡常数K一定发生改变
B.增大压强,W的质量分数减小
C.该反应的化学方程式为3Z(g)+2W(g)X(g)+2Y(g)
D.增大X气体浓度平衡向正反应方向移动
答案 D
解析 A项,升高温度,化学平衡向吸热的方向移动,因此化学平衡常数一定
发生变化,故A正确;B项,根据化学平衡常数表达式可知,反应物W、Z计量数
之和为3+2=5;生成物X、Y计量数之和为1+2=3,因此增大压强时,化学平衡
向正反应方向移动,因此W质量分数减小,故B正确;C项,由化学平衡常数表达
式知,该反应的化学方程式为3Z(g)+2W(g)X(g)+2Y(g),故C正确;D项,X
为生成物,增大X浓度,化学平衡向逆反应方向移动,故D错误。
5.某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反
应:3A(g)+2B(g)4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6 mol
C,则下列有关说法正确的是( )
A.该反应的化学平衡常数表达式是K=
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加B,平衡向右移动,B的平衡转化率增大答案 B
解析 A项,纯固体物质不能在平衡常数表达式中出现;B项,生成1.6 mol
的C则反应掉0.8 mol的B,则B的转化率为×100%=40%,B正确;C项,化学
平衡常数只与温度有关;D项,B的平衡转化率减小。
6.(2020·天津重点中学联考)一定温度下,在一个容积为1 L的密闭容器中,
充入1 mol H (g)和1 mol I (g),发生反应H (g)+I (g)2HI(g),经充分反应达到
2 2 2 2
平衡后,生成的HI(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭
容器中充入1 mol HI(g)发生反应HI(g)H (g)+I (g),则下列判断正确的是(
2 2
)
A.后一反应的平衡常数为1
B.后一反应的平衡常数为0.5
C.后一反应达到平衡时,H 的平衡浓度为0.25 mol·L-1
2
D.后一反应达到平衡时,HI(g)的平衡浓度为0.5 mol·L-1
答案 B
解析
平衡常数K ===4,而反应HI(g)H (g)+I (g)的平衡常数K ===0.5,
1 2 2 2
A项错误,B项正确;设反应HI(g)H (g)+I (g)达平衡时c(H )=x mol·L-1,则
2 2 2
平衡时c(I )=x mol·L-1,c(HI)=(0.5-2x) mol·L-1,K ==0.5,解得x=0.125,故
2 2
平衡时c(HI)=0.25 mol·L-1,C、D项错误。
7.(2020·山东模考)反应Ⅰ、Ⅱ、Ⅲ均会在工业生产硝酸过程中发生,其中反
应Ⅰ、Ⅱ发生在氧化炉中,反应Ⅲ发生在氧化塔中,不同温度下各反应的化学平
衡常数如下表所示。
化学平衡常数
温度(K) 反应Ⅰ:4NH + 反应Ⅱ:4NH + 反应Ⅲ:2NO+
3 3
5O ===4NO+6H O 3O ===2N +6H O O ===2NO
2 2 2 2 2 2 2
500 1.1×1026 7.0×1034 1.3×102
700 2.1×1019 2.6×1025 1.0
下列说法正确的是( )A.使用选择性催化反应Ⅰ的催化剂可增大氧化炉中NO的含量
B.通过改变氧化炉的温度可促进反应Ⅰ而抑制反应Ⅱ
C.通过改变氧化炉的压强可促进反应Ⅰ而抑制反应Ⅱ
D.氧化炉出气在进入氧化塔前应进一步提高温度
答案 A
解析 使用选择性催化反应Ⅰ的催化剂可促进反应Ⅰ的发生,增大氧化炉中
NO的含量,故A正确;升高温度,反应Ⅰ和反应Ⅱ的化学平衡常数均减小,则正
反应均为放热反应,无法通过改变氧化炉的温度达到促进反应Ⅰ而抑制反应Ⅱ的
效果,故B错误;反应Ⅰ和反应Ⅱ的正反应均为气体分子数增大的反应,无法通
过改变氧化炉的压强达到促进反应Ⅰ而抑制反应Ⅱ的效果,故C错误;反应Ⅰ、
Ⅱ、Ⅲ正反应均为放热反应,所以氧化炉出气在进入氧化塔前应降低温度,故D
错误。
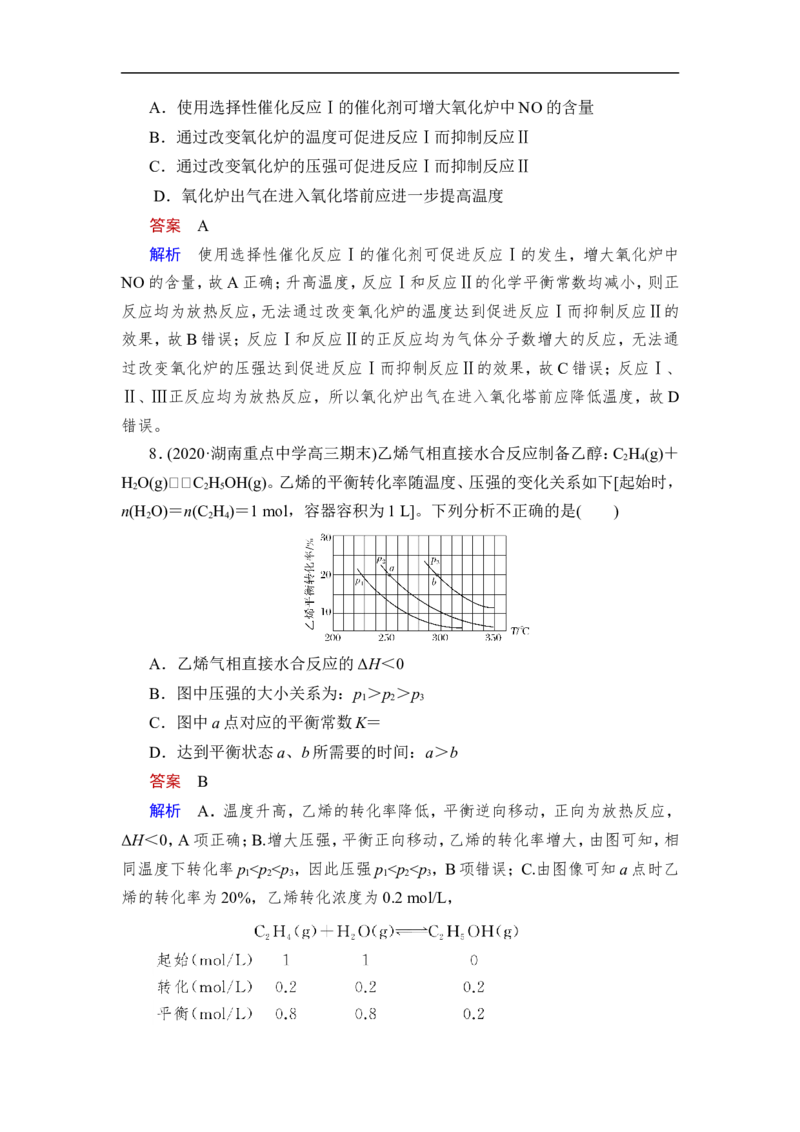
8.(2020·湖南重点中学高三期末)乙烯气相直接水合反应制备乙醇:C H (g)+
2 4
H O(g)C H OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下[起始时,
2 2 5
n(H O)=n(C H )=1 mol,容器容积为1 L]。下列分析不正确的是( )
2 2 4
A.乙烯气相直接水合反应的ΔH<0
B.图中压强的大小关系为:p >p >p
1 2 3
C.图中a点对应的平衡常数K=
D.达到平衡状态a、b所需要的时间:a>b
答案 B
解析 A.温度升高,乙烯的转化率降低,平衡逆向移动,正向为放热反应,
ΔH<0,A项正确;B.增大压强,平衡正向移动,乙烯的转化率增大,由图可知,相
同温度下转化率p a,所需要的时间a>b,D项正确。
9.在一个容积为2 L的密闭容器中,加入0.8 mol的A 气体和0.6 mol B 气体
2 2
一定条件下发生如下反应:A (g)+B (g)2AB(g) ΔH<0,反应中各物质的浓度
2 2
随时间的变化情况如图所示,下列说法不正确的是( )
A.图中a点的值为0.15
B.该反应的平衡常数K=0.03
C.温度升高,平衡常数K值减小
D.平衡时A 的转化率为62.5%
2
答案 B
解析 当 AB 的浓度改变 0.5 mol·L-1 时,由化学方程式 A (g)+
2
B (g)2AB(g)知,A 的浓度改变0.25 mol·L-1,所以a=(0.4-0.25) mol·L-1=
2 2
0.15 mol·L-1,即图中a点的值为0.15,故A正确;当AB的浓度改变0.5 mol·L-1
时,B 的浓度改变0.25 mol·L-1,所以平衡时B 的浓度为(0.3-0.25) mol·L-1=
2 2
0.05 mol·L-1,K===,故B错误;已知反应为放热反应,温度升高,平衡左移,平
衡常数K值减小,故C正确;当AB的浓度改变0.5 mol·L-1时,A 的浓度改变
2
0.25 mol·L-1,已知A 的初始量为0.4 mol·L-1,所以平衡时A 的转化率为×100%
2 2
=62.5%,故D正确。
10.N O 是一种新型硝化剂,一定温度下发生反应2N O (g)4NO (g)+
2 5 2 5 2
O (g) ΔH>0,T 温度下的部分实验数据为:
2 1
t/s 0 500 1 000 1 500
c(N O )/(mol·L-1) 5.00 3.52 2.50 2.50
2 5
下列说法不正确的是( )
A.500 s内,N O 的分解速率为2.96×10-3 mol·L-1·s-1
2 5
B.T 温度下的平衡常数为K =125,1 000 s时N O 的转化率为50%
1 1 2 5
C.其他条件不变时,T 温度下反应到 1 000 s 时测得 N O (g)浓度为 2.98
2 2 5
mol·L-1,则有T >T
1 2
D.T 温度下的平衡常数为K ,T 温度下的平衡常数为K ,若T >T ,则有
1 1 2 2 1 2K K ②2
A B C
解析 (1)①=2,又n(CO)+n(H )=3 mol,
2
则n(H )=2 mol,n(CO)=1 mol,
2
0~5 min内转化的n(CO)=0.6 mol,则有
v(H )=0.6 mol·L-1÷5 min=0.12 mol·L-1·min-1,
2
K=>,所以平衡正向移动,H 的转化率将增大。②反应物按方程式中各物质
2的化学计量数比投料时产物的体积分数最大,否则都会使产物的体积分数减小,
故应选F点。(2)①平衡常数只与温度有关,CO与H 反应生成CH OH的反应为
2 3
放热反应,升高温度,平衡常数减小,K K 。②达到平衡状态A时,容器的容积为10 L,状态A
A B C
与B的平衡常数相同,状态A时CO的转化率是0.5,则平衡时CO的物质的量是
10 mol×(1-0.5)=5 mol,浓度是0.5 mol·L-1,c(H )=1 mol·L-1,生成甲醇的物质
2
的量是5 mol,浓度是0.5 mol·L-1,所以平衡常数K =1;设状态B时容器的容积
A
是V L,状态B时CO的转化率是0.8,则平衡时,CO的物质的量浓度为 mol·L-
1,氢气的物质的量浓度是 mol·L-1,生成甲醇的物质的量浓度是 mol·L-1,K =
B
=1,解得V=2。
14.(2020·山东模考)聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催
化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:CH COOCH (l)
3 3
+C H OH(l)=====CH COOC H (l)+CH OH(l)
6 13 3 6 13 3
已 知 v = k ·x(CH COOCH )·x(C H OH) , v = k
正 正 3 3 6 13 逆
·x(CH COOC H )·x(CH OH),其中v ,v 为正、逆反应速率,k ,k 为速率常
逆 3 6 13 3 正 逆 正 逆
数,x为各组分的物质的量分数。
(1)反应开始时,己醇和乙酸甲酯按物质的量之比1∶1投料,测得348 K、343
K、338 K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。
该醇解反应的ΔH________0(填“>”或“<”)。348 K时,以物质的量分数
表示的化学平衡常数K =________(保留2位有效数字)。在曲线①、②、③中,k
x 正
-k 值最大的曲线是________;A、B、C、D四点中,v 最大的是________,v 最
逆 正 逆
大的是________。
(2)343 K时,己醇和乙酸甲酯按物质的量之比1∶1、1∶2和2∶1进行初始投
料。则达到平衡后,初始投料比________时,乙酸甲酯转化率最大;与按1∶2投
料相比,按2∶1投料时化学平衡常数K ________(填增大、减小、不变)。
x
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的
是________。a.参与了醇解反应,但并不改变反应历程
b.使k 和k 增大相同的倍数
正 逆
c.降低了醇解反应的活化能
d.提高乙酸甲酯的平衡转化率
答案 (1)> 3.2 ① A C (2)2∶1 不变 (3)bc
解析 (1)根据图像,①的速率最快,说明①对应的是最高温度348 K,温度升
高,平衡时转化率增大,说明正反应是吸热的,所以ΔH>0。348 K时,设初始投
入反应物各1 mol,则有:
平衡常数K ===3.2。
x
k 、k 是温度的函数,根据平衡移动的规律,k 受温度影响更大,因此温度
正 逆 正
升高,k 增大的程度大于k ,因此,k -k 值最大的曲线是①;根据v =k
正 逆 正 逆 正
·x(CH COOCH )·x(C H OH),v =k ·x(CH COOC H )·x(CH OH),A 点
正 3 3 6 13 逆 逆 3 6 13 3
x(CH COOCH )·x(C H OH)大,温度高,因此 A 点 v 最大,C 点 x(CH COO
3 3 6 13 正 3
C H )·x(CH OH)大且温度高,因此C点v 最大;(2)增大己醇的投入量,可以增大
6 13 3 逆
乙酸甲酯转化率,因此,2∶1时乙酸甲酯转化率最大,化学平衡常数K 只与温度
x
有关,因此K 不变;(3)a、催化剂参与了醇解反应,改变了反应历程,a错误;b、催
x
化剂不影响化学平衡,说明催化剂使k 和k 增大相同倍数,b正确;c、催化剂能
正 逆
够降低反应的活化能,c正确;d、催化剂不改变化学平衡,d错误;故选bc。