文档内容
1.中华优秀传统文化涉及很多化学知识。下列有关说法不正确的是( )
A.“火树银花合,星桥铁锁开”中的“火树银花”涉及金属元素的焰色
B.古剑沈卢“以剂钢为刃,柔铁为茎干,不尔则多断折”中的“剂钢”是铁的合金
C.“以曾青涂铁,铁赤色如铜”中的“曾青”是铜盐
D.《天工开物》中有“至于矾现五金色之形,硫为群石之将,皆变化于烈火”,其中的
“矾”指的是金属硫化物
2.(2022·武汉模拟)旅游景点售卖的仿银饰品大多是白铜(铜镍合金)。下列说法正确的是(
)
A.硬度比铜的大
B.熔点比铜的高
C.容易被腐蚀
D.通过外观颜色即可区分它和白银
3.(2022·南通高三期末)下列铜及其化合物性质与用途具有对应关系的是( )
A.铜单质具有延展性,可用作传输电流
B.Cu O的熔、沸点较高,可用作催化反应
2
C.Cu(OH) 具有氧化性,可用作检验醛基
2
D.CuSO 能使蛋白质变性,可用于饮用水消毒
4
4.(2022·辽宁铁岭高三模拟)下列古诗或古文中的描述与化学方程式对应关系不正确的是(
)
A.丹砂烧之成水银:HgS=====Hg+S
B.爆竹声中一岁除:S+2KNO+3C=====KS+3CO↑+N↑
3 2 2 2
C.炉火照天地,红星乱紫烟:Cu CO+2H=====Cu+CO+3HO
22 3 2 2 2
D.曾青得铁则化为铜:CuSO +Fe===FeSO +Cu
4 4
5.我国古代“药金”的冶炼方法是将炉甘石(ZnCO)和赤铜矿(Cu O)与木炭按一定的比例混
3 2
合后加热至800 ℃,即可炼出闪烁似金子般光泽的“药金”。下列叙述正确的是( )
A.“药金”实质上是铜锌合金
B.冶炼炉中炉甘石直接被木炭还原为锌
C.用王水可区别黄金和“药金”
D.用火焰灼烧不能区别黄金和“药金”
6.人类最早冶金的历史年代曲线图如图所示(-1000表示公元前1000年)。下列说法正确的是( )
A.金属越活泼,冶炼的年代一定越晚
B.冶炼金属的历史:电解氯化物比电解氧化物早
C.自然界中铜元素以游离态形式存在,故铜的冶炼年代最早
D.金属氧化物(如Al O、Cu O)也属于金属材料
2 3 2
7.(2023·西安质检)金属的冶炼与生产、生活及国防军事等领域均密切相关。下列有关金属
冶炼的原理错误的是( )
A.用电解法制取金属钠:2NaCl(熔融)=====2Na+Cl↑
2
B.用Na、Mg等活泼金属为还原剂冶炼Ti:2Mg+TiCl (熔融)=====Ti+2MgCl
4 2
C.用Al作还原剂冶炼金属V:3VO+10Al=====6V+5Al O
2 5 2 3
D.用H 作还原剂冶炼金属Ag:Ag O+H=====2Ag+HO
2 2 2 2
8.向CuSO 溶液中加入HO 溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶
4 2 2
液变为红色浑浊(Cu O),继续加入HO 溶液,红色浑浊又变为蓝色溶液,这个反应可以反
2 2 2
复多次。下列关于上述过程的说法不正确的是( )
A.Cu2+将HO 还原为O
2 2 2
B.HO 既表现氧化性又表现还原性
2 2
C.Cu2+是HO 分解反应的催化剂
2 2
D.发生了反应:Cu O+HO+4H+===2Cu2++3HO
2 2 2 2
9.氧化还原反应广泛应用于金属的冶炼,下列说法不正确的是( )
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.湿法炼铜的反应中,铜元素发生还原反应
C.用磁铁矿炼铁的反应中,1 mol Fe O 被CO还原成Fe,转移9 mol电子
3 4
D.铝热法还原铁的反应中,放出的热量能使铁熔化
10.实验室用含有少量氧化铁杂质的废铜粉制取无水硫酸铜的实验步骤如图:
下列有关说法正确的是( )
A.溶解废铜粉“过量酸”是指稀硝酸
B.气体A是Cl,将亚铁离子氧化为铁离子
2C.生成沉淀D的离子方程式可以为3CuO+2Fe3++3HO===2Fe(OH) +3Cu2+
2 3
D.从滤液中得到无水硫酸铜的方法是冷却结晶
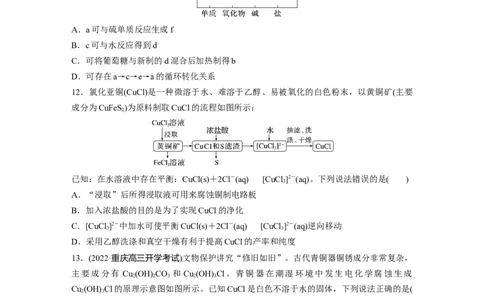
11.(2022·深圳市光明区高级中学高三模拟)部分含铜物质的分类与相应化合价关系如图所示。
下列推断不合理的是( )
A.a可与硫单质反应生成f
B.c可与水反应得到d
C.可将葡萄糖与新制的d混合后加热制得b
D.可存在a→c→e→a的循环转化关系
12.氯化亚铜(CuCl)是一种微溶于水、难溶于乙醇、易被氧化的白色粉末,以黄铜矿(主要
成分为CuFeS)为原料制取CuCl的流程如图所示:
2
已知:在水溶液中存在平衡:CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)。下列说法错误的是( )
3
A.“浸取”后所得浸取液可用来腐蚀铜制电路板
B.加入浓盐酸的目的是为了实现CuCl的净化
C.[CuCl ]2-中加水可使平衡CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)逆向移动
3 3
D.采用乙醇洗涤和真空干燥有利于提高CuCl的产率和纯度
13.(2022·重庆高三开学考试)文物保护讲究“修旧如旧”。古代青铜器铜锈成分非常复杂,
主要成分有 Cu (OH) CO 和 Cu (OH) Cl。青铜器在潮湿环境中发生电化学腐蚀生成
2 2 3 2 3
Cu (OH) Cl的原理示意图如图所示。已知CuCl是白色不溶于水的固体,下列说法正确的是(
2 3
)
A.疏松的Cu (OH) Cl属于无害锈
2 3
B.过程Ⅰ中负极的电极反应式为Cu-e-===Cu+C.若生成2.145 g Cu (OH) Cl理论上消耗标准状况下氧气的体积为0.224 L
2 3
D.用HNO 溶液除青铜器上的铜锈,可实现“修旧如旧”,保护文物的艺术价值
3
14.化学学习活动小组学习了铁、铜化合物知识后,查阅资料,积极思考,提出了一系列问
题,请予以解答:
(1)氯化亚铜(CuCl)是重要的化工原料,工业上常通过下列反应制备CuCl:
2CuSO +NaSO +2NaCl+NaCO===2CuCl↓+3NaSO +CO↑
4 2 3 2 3 2 4 2
查阅资料可得,CuCl可以溶解在FeCl 溶液中,请写出该反应的离子方程式: ____
3
________________________________________________________________________。
(2)已知:Cu O在酸性溶液中发生歧化反应:Cu O+2H+===Cu2++Cu+HO。现将一定量
2 2 2
混合物(Fe O 、Cu O、CuCl、Fe)溶解于过量稀盐酸中,反应完全后,得到W(包括溶液和少
2 3 2
量剩余固体),此时溶液中一定含有的阳离子是______________(用离子符号表示,下同)。
(3)继续往W中通入足量的氯气,不断搅拌,充分反应,溶液中哪些离子的物质的量一定有
明显变化?________________。
(4)不通入气体,改向 W中加入过量铁粉,过滤,调节 pH约为7,加入淀粉-KI溶液和
HO ,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的
2 2
离 子 方 程 式 是
________________________________________________________________________
________________________________________________________________________。
15.辉铜矿的主要成分为Cu S,此外还含有少量SiO 、Fe O 等杂质,软锰矿主要含有
2 2 2 3
MnO ,以及少量SiO 、Fe O 等杂质。研究人员开发综合利用这两种资源,用同槽酸浸湿法
2 2 2 3
冶炼工艺,制备硫酸锰晶体和碱式碳酸铜。主要工艺流程如下:
已知:①MnO 有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
2
②[Cu(NH )]SO 在常温下稳定,在热水溶液中会分解生成NH ;
3 4 4 3
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
Fe3+:1.5~3.2;Mn2+:8.3~9.8;Cu2+:4.4~6.4;
④MnSO ·H O溶于1份冷水、0.6份沸水,不溶于乙醇。
4 2
(1)实验室配制250 mL 4.8 mol·L-1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还
需要________________________________________________________________________。
(2)酸浸时,为了提高浸取率可采取的措施有__________________________________
________________________________________________________________________(任写一
点)。(3)酸浸时,得到浸出液中主要含有 CuSO 、MnSO 等。写出该反应的化学方程式:
4 4
________________________________________________________________________
________________________________________________________________________。
(4)调节浸出液pH=4的作用是____________________________________________
________________________________________________________________________。
(5)本工艺流程中可循环使用的物质是________(写化学式)。
(6)获得的MnSO ·H O晶体需要进一步洗涤、干燥,洗涤时应用________洗涤。
4 2
(7)测定MnSO ·H O样品的纯度:准确称取样品14.00 g,加蒸馏水配成100 mL溶液,取出
4 2
25.00 mL用标准的BaCl 溶液测定,完全反应后得到了 4.66 g沉淀,则此样品的纯度为
2
______(保留四位有效数字)。