文档内容
第 17 讲 铝、镁及其化合物
[复习目标] 1.了解镁、铝及其重要化合物的存在、性质和用途。2.掌握工业提取铝、镁的
一般方法。
考点一 铝及其化合物
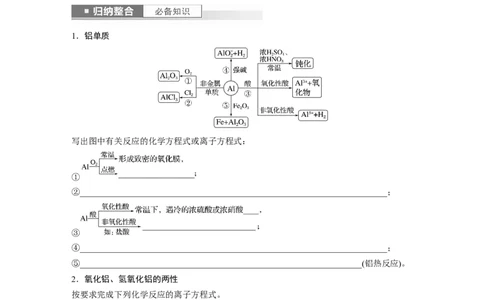
1.铝单质
写出图中有关反应的化学方程式或离子方程式:
①
②________________________________________________________________________;
③
④________________________________________________________________________;
⑤__________________________________________________________________(铝热反应)。
2.氧化铝、氢氧化铝的两性
按要求完成下列化学反应的离子方程式。
(1)氧化铝分别溶于盐酸、NaOH溶液:_________________________________________
________________________________________________________________________ 、
________________________________________________________________________。
(2)氢氧化铝分别溶于盐酸、NaOH溶液:______________________________________
________________________________________________________________________、
________________________________________________________________________。
3.Al(OH) 的制备
3
写出下列反应的离子方程式。(1)Al3+与氨水反应(不用强碱):
________________________________________________________________________。
(2)向含AlO的溶液中通入过量的CO:
2
________________________________________________________________________。
(3)Al3+与AlO发生相互促进的水解反应:
________________________________________________________________________。
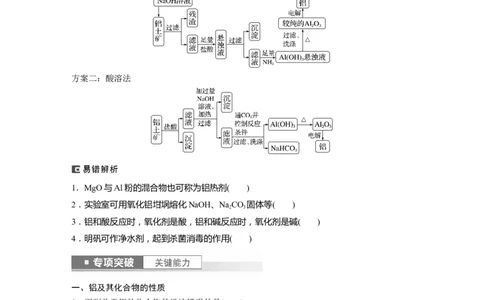
4.工业炼铝的流程
方案一:碱溶法
方案二:酸溶法
1.MgO与Al粉的混合物也可称为铝热剂( )
2.实验室可用氧化铝坩埚熔化NaOH、NaCO 固体等( )
2 3
3.铝和酸反应时,氧化剂是酸,铝和碱反应时,氧化剂是碱( )
4.明矾可作净水剂,起到杀菌消毒的作用( )
一、铝及其化合物的性质
1.下列关于铝的化合物的说法错误的是( )
A.氧化铝俗名为刚玉,是高温耐火材料
B.KAl(SO )·12H O溶于水可形成Al(OH) 胶体,可以净水
4 2 2 3
C.Al3+和AlO两种离子不能大量共存于同一溶液中
D.将AlCl 溶液滴入浓氨水中的离子方程式:Al3++4NH ·H O===AlO+4NH+2HO
3 3 2 2
2.称取两份铝粉,第一份加入足量氢氧化钠溶液,第二份加入足量盐酸,若要放出等量的
气体,两份铝粉的质量之比为( )
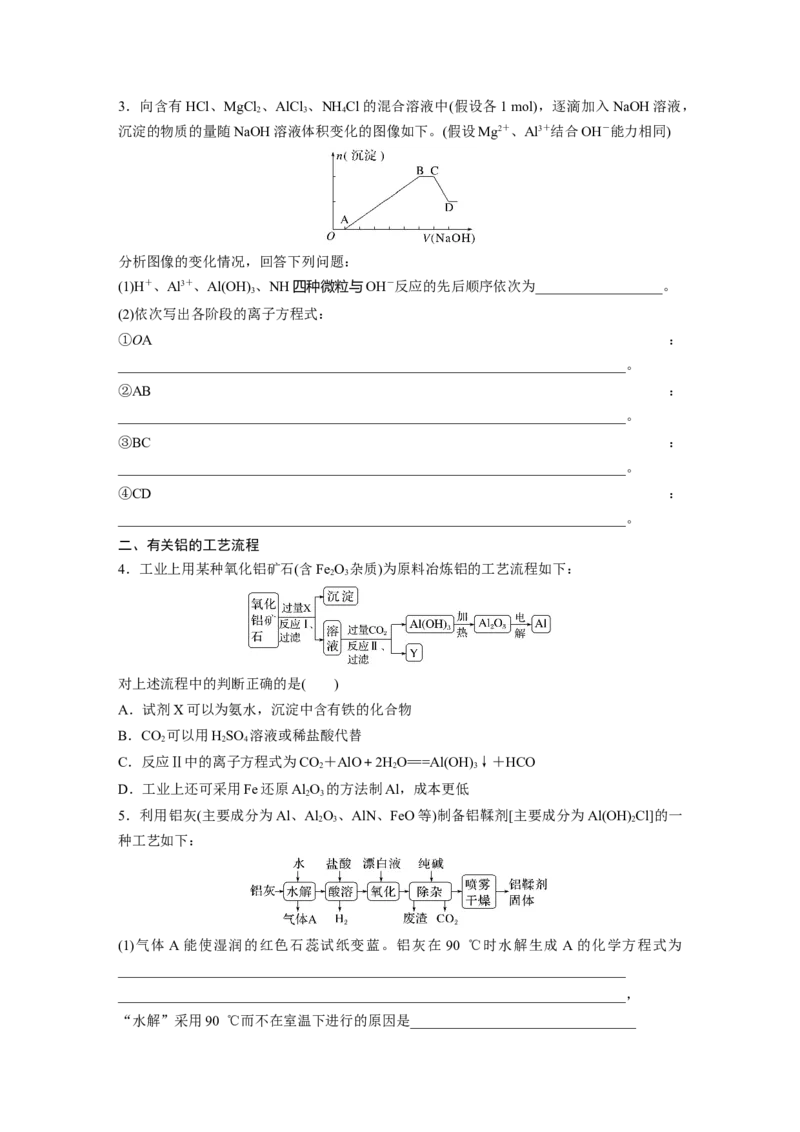
A.1∶3 B.3∶1 C.1∶1 D.4∶33.向含有HCl、MgCl 、AlCl 、NH Cl的混合溶液中(假设各1 mol),逐滴加入NaOH溶液,
2 3 4
沉淀的物质的量随NaOH溶液体积变化的图像如下。(假设Mg2+、Al3+结合OH-能力相同)
分析图像的变化情况,回答下列问题:
(1)H+、Al3+、Al(OH) 、NH四种微粒与OH-反应的先后顺序依次为__________________。
3
(2)依次写出各阶段的离子方程式:
①OA :
________________________________________________________________________。
②AB :
________________________________________________________________________。
③BC :
________________________________________________________________________。
④CD :
________________________________________________________________________。
二、有关铝的工艺流程
4.工业上用某种氧化铝矿石(含Fe O 杂质)为原料冶炼铝的工艺流程如下:
2 3
对上述流程中的判断正确的是( )
A.试剂X可以为氨水,沉淀中含有铁的化合物
B.CO 可以用HSO 溶液或稀盐酸代替
2 2 4
C.反应Ⅱ中的离子方程式为CO+AlO+2HO===Al(OH) ↓+HCO
2 2 3
D.工业上还可采用Fe还原Al O 的方法制Al,成本更低
2 3
5.利用铝灰(主要成分为Al、Al O 、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH) Cl]的一
2 3 2
种工艺如下:
(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在 90 ℃时水解生成 A的化学方程式为
________________________________________________________________________
________________________________________________________________________,
“水解”采用90 ℃而不在室温下进行的原因是________________________________________________________________________________________________________。
(2)“酸溶”时,Al O 发生反应的离子方程式为_________________________________
2 3
________________________________________________________________________。
(3)“氧化”时,发生反应的离子方程式为_____________________________________
________________________________________________________________________。
(4)“废渣”的成分为____________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是_______________________________________。
考点二 镁 海水提镁
1.从海水中提取镁的流程
主要化学反应为
(1)制石灰乳:________________________________________________________、
________________________________________________________________________;
(2)沉淀Mg2+:_________________________________________________________;
(3)制备MgCl :___________________________________________________________、
2
________________________________________________________________________;
(4)电解MgCl :___________________________________________________________。
2
2.镁的重要化合物
(1)氧化镁:白色粉末状固体,____溶于水,属于______________,与盐酸反应的离子方程
式为_____________________________________________________________________。
(2)氢氧化镁:白色固体,____溶于水,中强碱,与盐酸反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
特别提醒 氢氧化镁的溶解度小于碳酸镁,能发生反应 MgCO +HO=====Mg(OH) +
3 2 2
CO↑,镁元素在水垢中的存在形式是Mg(OH) 。
2 2
1.加热MgCl 溶液最终可制得MgCl 固体( )
2 2
2.工业上冶炼金属镁也可以采用电解熔融MgO的方法( )3.镁不慎着火,可以用CO 灭火( )
2
4.在Mg(HCO ) 溶液中加入足量的Ca(OH) 溶液,最终得到的沉淀是MgCO 和CaCO (
3 2 2 3 3
)
化工流程中的“镁”
1.以混有SiO 的MgCO 为原料制备氧化镁的实验流程如图:
2 3
下列说法错误的是( )
A.酸浸的离子方程式为CO+2H+===CO↑+HO
2 2
B.浸出渣的成分是SiO
2
C.母液的主要溶质是NH Cl
4
D.固体X是Mg(OH)
2
2.从海水中提取镁的工艺流程如图所示:
回答下列问题:
(1)海水通过结晶、过滤得到的固体物质主要是________。
(2)怎样使MgCl ·6H O失去结晶水得到MgCl ? _______________________________
2 2 2
(3)上述工艺流程涉及到的基本反应类型有____________________________________
________________________________________________________________________。
(4)写出电解熔融MgCl 的电极反应式。
2
________________________________________________________________________
1.正误判断,正确的打“√”,错误的打“×”。
(1)氧化铝熔点高,常用于制造耐高温材料(2022·浙江6月选考,8C)( )
(2)工业上通过电解六水合氯化镁制取金属镁(2022·浙江6月选考,9A)( )
(3)铝热反应非常剧烈,操作时要戴上石棉手套和护目镜(2022·浙江6月选考,11B)( )
(4)技术人员开发高端耐腐蚀镀铝钢板,是因为铝能形成致密氧化膜(2022·广东,6D)( )
(5)利用海水制取溴和镁单质,此过程中 Br-可被氧化,Mg2+可被还原(2022·广东,12B)()
(6)MgCl 溶液中滴加NaOH溶液至过量,现象为产生白色沉淀后沉淀消失
2
(2022·海南,6A)( )
2.(2020·江苏,3)下列有关物质的性质与用途具有对应关系的是( )
A.铝的金属活泼性强,可用于制作铝金属制品
B.氧化铝熔点高,可用作电解冶炼铝的原料
C.氢氧化铝受热分解,可用于中和过多的胃酸
D.明矾溶于水并水解形成胶体,可用于净水
3.(2020·山东,9)以菱镁矿(主要成分为MgCO ,含少量SiO 、Fe O 和Al O)为原料制备高
3 2 2 3 2 3
纯镁砂的工艺流程如下:
已知浸出时产生的废渣中有SiO、Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
4.[2016·海南,14(1)(2)(3)]KAl(SO )·12H O(明矾)是一种复盐,在造纸等方面应用广泛。实
4 2 2
验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所
示。回答下列问题:
――――――→―――――→―――→
(1)为尽量少引入杂质,试剂①应选用_____________________________________________
(填标号)。
a.HCl溶液 b.HSO 溶液
2 4
c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为_______________________________。
(3)沉淀B的化学式为________________________________________________________;
将少量明矾溶于水,溶液呈弱酸性,其原因是_________________________________
________________________________________________________________________。