文档内容
第 25 讲 氮及其氧化物 硝酸
[复习目标] 1.了解氮及其氧化物的主要性质及应用;了解氮氧化物对环境的影响。2.掌握
硝酸的性质及应用。
考点一 氮及其氧化物
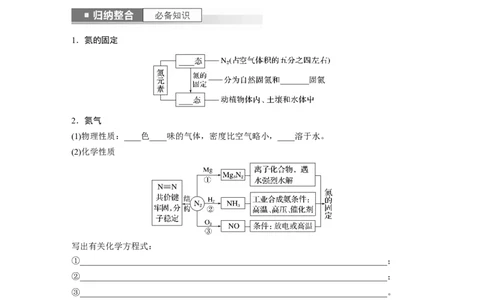
1.氮的固定
2.氮气
(1)物理性质:____色____味的气体,密度比空气略小,____溶于水。
(2)化学性质
写出有关化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
(3)下列氮气的用途叙述中,分别应用了氮气的什么性质?
①文物馆将贵重文物保存在氮气中________________________________________。
②氮气是合成氨工业的重要原料___________________________________________。
③雷电是自然界重要的固氮方式___________________________________________。
④医疗上,液氮是常见的冷冻剂____________________________________________
________________________________________________________________________。
3.氮的氧化物
(1)氮有多种价态的氧化物,氮元素从+1→+5价都有对应的氧化物,如 NO、____、
2NO、NO (或____)、NO,其中属于酸性氧化物的是NO、____。
2 3 2 2 5 2 3
(2)NO和NO 的比较
2
性质 NO NO
2
色、味、态
水溶性 易溶于水
毒性 有毒,大气污染物之一 有毒,大气污染物之一
与水反应 不反应 3NO +HO===2HNO+NO
2 2 3
与氧气反应 不反应
提醒 ①NO 与NO 存在下列平衡:2NO NO ,因此实验测得NO 的平均相对分子质
2 2 4 2 2 4 2
量总大于46。②验证某无色气体为NO的方法是向该无色气体中通入O(或空气),无色气体
2
变为红棕色。
4.氮氧化物对环境的污染及防治
(1)常见的污染类型
①光化学烟雾:NO 在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生了一种有
x
毒的烟雾。
②酸雨:NO 排入大气中后,与水反应生成HNO 和HNO,随雨雪降到地面。
x 3 2
③破坏臭氧层:NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加。
2
④NO与血红蛋白结合使人中毒。
(2)常见的NO 尾气处理方法
x
①碱液吸收法
工业尾气中的NO 常用碱液吸收处理,NO 、NO的混合气体能被足量烧碱溶液完全吸收的
x 2
条件是 n(NO )≥n(NO)。
2
②催化转化法
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N ),或NO 与CO在一定温度下
2 x
催化转化为无毒气体(N 和CO)。一般适用于汽车尾气的处理。
2 2
1.固氮反应一定属于氧化还原反应( )
2.N 与O 在放电条件下直接化合成NO ( )
2 2 2
3.可用NO 与水反应制取硝酸,故NO 是酸性氧化物( )
2 2
4.利用AgNO、CCl 和蒸馏水均可鉴别NO 和溴蒸气( )
3 4 2
5.NO 通入FeSO 溶液中始终无明显现象( )
2 4
一、氮气、NO和NO 的性质
21.氮是生命活动不可缺少的重要元素。下列叙述错误的是( )
A.液氮可用于医学和高科技领域,制造低温环境
B.点燃的镁条在氮气中不反应
C.氮气是工业合成氨的原料之一
D.氮的固定是将大气中的氮气转化成氮的化合物
2.下列有关氮的氧化物的说法正确的是( )
A.NO和NO 混合气体的尾气可以用水吸收
2
B.4.6 g NO 和NO 混合气体中含有的氧原子数目小于0.2N
2 2 4 A
C.用湿润的淀粉KI试纸鉴别Br (g)和NO
2 2
D.除去NO中混有少量NO 气体时,可以用水洗涤后再干燥
2
二、氮的氧化物与O、HO反应定量关系应用
2 2
3.将盛有12 mL NO 和O 的混合气体的量筒倒立于水槽中,充分反应后,还剩余 2 mL无
2 2
色气体。
(1)若剩余的气体是________,则NO 、O 的体积分别是______________。
2 2
(2)若剩余的气体是________,则NO 、O 的体积分别是______________。
2 2
三、废气中氮氧化物的治理
4.(1)汽车尾气中的CO、NO 在适宜温度下采用催化转化法处理,使它们相互反应生成参
x
与大气循环的无毒气体。写出NO被CO还原的化学方程式:
________________________________________________________________________。
(2)用氨可将氮氧化物转化为无毒气体。如4NH +6NO=====5N +6HO,写出氨气转化NO
3 2 2 2
的化学方程式: __________________________________________________________,
该反应中氧化产物与还原产物的质量之比为_________________________________。
(3)工业尾气中氮的氧化物常采用碱液吸收法处理。
①NO 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为 1∶1,写出该反应的化学方
2
程式:________________________________________________________________________
________________________________________________________________________。
②NO与NO 按物质的量之比1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐
2
的化学式是________________。
考点二 硝酸
1.物理性质
硝酸是____色、____挥发、____________气味的液体。
2.化学性质(1)不稳定性
反应:________________________________________________________________________。
(2)强氧化性
硝酸无论浓、稀都具有强氧化性,而且浓度越大,氧化性越强。
①与金属反应
稀硝酸与铜反应的化学方程式: ____________________________________________
________________________________________________________________________;
浓硝酸与铜反应的化学方程式: ____________________________________________
________________________________________________________________________。
②与非金属反应
浓硝酸与C反应的化学方程式: ____________________________________________
________________________________________________________________________。
③与还原性化合物反应
硝酸可氧化HS、SO 、NaSO 、HI、Fe2+等还原性物质。
2 2 2 3
稀硝酸与FeSO 溶液反应的离子方程式: ____________________________________
4
________________________________________________________________________。
(3)与有机物反应
①硝化反应(与反应): ____________________________________________________;
②显色反应:含有苯环的蛋白质遇到浓硝酸加热后变____色。
1.常温下,铁、铝在浓硝酸中的钝化为化学变化( )
2.可用稀HNO 与FeS固体反应制取HS( )
3 2
3.铜、碳分别与浓HNO 反应,都体现了浓硝酸的强氧化性和酸性( )
3
4.在酸性条件下,NO与I-、Fe2+、SO等离子均不能大量共存( )
5.Cu在KNO 溶液和稀HSO 中均不溶解,但能溶解在其混合液中( )
3 2 4
6.试管内壁上的银镜可用稀HNO 除去,也可用氨水除去( )
3
7.浓HNO 和氯水均用棕色试剂瓶保存,其原理相同( )
3
8.浓HNO 溅到皮肤上,皮肤会变黄( )
3一、金属与硝酸反应的定性分析
1.用动态观点理解Cu与浓HNO 的反应
3
向一定量的浓硝酸中加入过量的铜片。
(1)反应开始阶段产生________________色气体,化学方程式为__________________。
(2)反应进行一段时间后又产生无色气体,此时的化学方程式为__________________。
(3)待反应停止后,再加入少量的稀硫酸,这时 Cu 片上又有气泡产生,原因是
________________________________________________________________________
________________________________________________________________________。
二、金属与硝酸反应的定量计算
2.将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO 混合气体
2
在标准状况下的体积为11.2 L。请回答下列问题:
(1)NO的体积为____ L,NO 的体积为______ L。
2
(2)参加反应的HNO 的物质的量是__________________________________________。
3
(3)待产生的气体全部释放后,向溶液中加入V mL a mol·L-1的NaOH溶液,恰好使溶液中
的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为______________________ mol·L-1。
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO ,至少需要30%的双氧
3
水________ g。
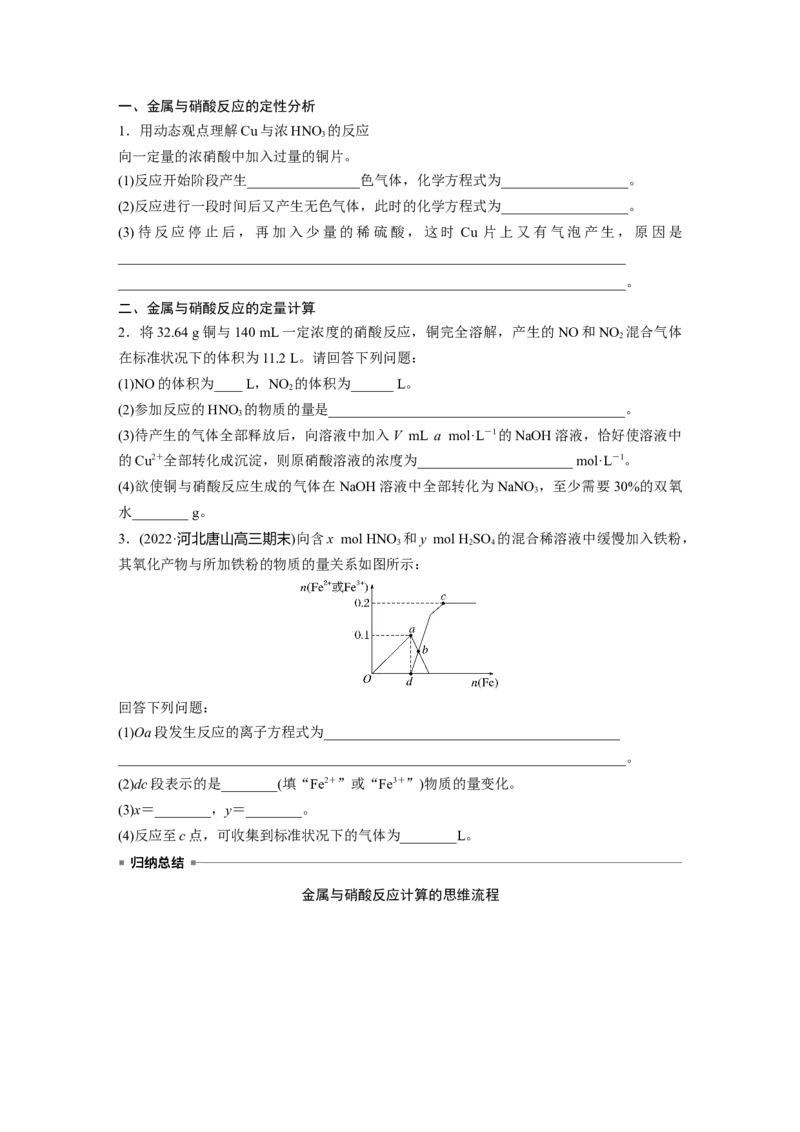
3.(2022·河北唐山高三期末)向含x mol HNO 和y mol HSO 的混合稀溶液中缓慢加入铁粉,
3 2 4
其氧化产物与所加铁粉的物质的量关系如图所示:
回答下列问题:
(1)Oa段发生反应的离子方程式为__________________________________________
________________________________________________________________________。
(2)dc段表示的是________(填“Fe2+”或“Fe3+”)物质的量变化。
(3)x=________,y=________。
(4)反应至c点,可收集到标准状况下的气体为________L。
金属与硝酸反应计算的思维流程1.正误判断,正确的打“√”,错误的打“×”。
(1)浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
(2021·河北,10D)( )
(2)向浓HNO 中插入红热的炭,产生红棕色气体,证明炭可与浓HNO 反应生成NO
3 3 2
(2021·山东,5C)( )
2.(2022·江苏,8)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将N 转化为NH
2 3
B.侯氏制碱法以HO、NH 、CO、NaCl为原料制备NaHCO 和NH Cl
2 3 2 3 4
C.工业上通过NH 催化氧化等反应过程生产HNO
3 3
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
3.(2022·北京,12)某MOFs的多孔材料刚好可将NO“固定”,实现了NO 与NO 分离
2 4 2 2 4
并制备HNO,如图所示:
3
已知:2NO (g)NO(g) ΔH<0
2 2 4
下列说法不正确的是( )
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O+2HO===4HNO
3 2 4 2 2 3
D.每制备0.4 mol HNO ,转移电子数约为6.02×1022
3
4.(2017·北京,12)下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸产生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO,由此说明木炭一定与浓硝酸发生了反应
2