文档内容
第 5 讲 氧化还原反应
【学科核心素养】
证据推理与模型认知:建立氧化还原反应的观点,掌握氧化还原反应的规律,结合常见的氧化还原反
应理解有关规律;通过分析、推理等方法认识氧化还原反应的特征和实质,建立氧化还原反应计算和配平
的思维模型。
科学探究与创新意识:认识科学探究是进行科学解释和发现。创造和应用的科学实践活动;能从氧化
还原反应的角度,设计探究方案,进行实验探究,加深对物质氧化性、还原性的理解。
【核心素养发展目标】
1.从化合价变化和电子转移的角度认识并判断氧化还原反应。能从宏观和微观相结合的角度理解氧化
还原反应与四种基本反应类型的关系。
2.认识元素在物质中可以具有不同价态,可通过氧化还原反应实现含有不同价态同种元素的物质的相
互转化。
3.能从化学反应中元素化合价的变化认识氧化剂和还原剂、氧化产物和还原产物等概念,熟知常见的
氧化剂和还原剂,理清相关概念间的关系。促进“变化观念”化学核心素养的发展。
4.认识物质的氧化性、还原性,学会分析预测物质具有的氧化性或还原性,建立判断物质氧化性、还
原性强弱的“思维模型”。
【知识点解读】
知识点一 氧化还原反应的相关概念
一、氧化还原反应
1.氧化还原反应的本质和特征
2.氧化还原反应的相关概念及其关系例如,反应MnO +4HCl(浓)=====MnCl +Cl↑+2HO中,氧化剂是MnO ,还原剂是HCl,氧化产
2 2 2 2 2
物是Cl。生成1 mol Cl 时转移电子数目为2N ,被氧化的HCl的物质的量是2_mol,盐酸表现的性质是酸
2 2 A
性和还原性。
【特别提醒】元素由化合态变为游离态时,该元素不一定被还原。如:Cu2+→Cu时,铜元素被还原,
Cl-→Cl 时,氯元素被氧化。
2
3.氧化还原反应中电子转移的表示方法
(1)双线桥法
①表示方法
写出Cu与稀硝酸反应的化学方程式并用双线桥标出电子转移的方向和数目:
。
②注意事项
a.箭头指向反应前后有元素化合价变化的同种元素的原子,且需注明“得到”或“失去”。
b.箭头的方向不代表电子转移的方向,仅表示电子转移前后的变化。
c.失去电子的总数等于得到电子的总数。
(2)单线桥法
①表示方法
写出Cu与稀硝酸反应的化学方程式并用单线桥标出电子转移的方向和数目:。
②注意事项
a.箭头从失电子元素的原子指向得电子元素的原子。
b.不标“得到”或“失去”,只标明电子转移的总数。
c.线桥只出现在反应物中。
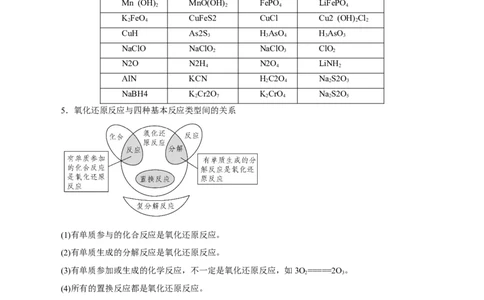
4.一些特殊物质中元素的化合价
Mn (OH) MnO(OH) FePO LiFePO
2 2 4 4
KFeO CuFeS2 CuCl Cu2 (OH) Cl
2 4 2 2
CuH As2S HAsO HAsO
3 3 4 3 3
NaClO NaClO NaClO ClO
2 3 2
N2O N2H N2O LiNH
4 4 2
AlN KCN HC2O NaS2O
2 4 2 3
NaBH4 KCr2O KCrO NaS2O
2 7 2 4 2 5
5.氧化还原反应与四种基本反应类型间的关系
(1)有单质参与的化合反应是氧化还原反应。
(2)有单质生成的分解反应是氧化还原反应。
(3)有单质参加或生成的化学反应,不一定是氧化还原反应,如3O=====2O。
2 3
(4)所有的置换反应都是氧化还原反应。
(5)所有的复分解反应都不是氧化还原反应。
二、氧化剂与还原剂
1.常见氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:【特别提醒】
(1)O、O 在水溶液中的还原产物,其中酸性条件下是HO,中性、碱性条件下是OH-;而当还原
2 3 2
产物为固态时是O2-或O。
(2)浓硝酸的还原产物是NO ,稀HNO 的还原产物是NO。
2 3
2.常见还原剂
常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、非金属单质及其氢
化物等。如:
3.既可作氧化剂,又可作还原剂的物质或粒子
具有中间价态的物质或粒子既具有氧化性,又具有还原性,当遇到强还原剂反应时,作氧化剂,表现
氧化性;当遇到强氧化剂反应时,作还原剂,表现还原性。常考物质或粒子归纳如下:
【特别提醒】同一种氧化剂(或还原剂)所对应的还原产物(或氧化产物)不是一成不变的,而是决定于还
原剂(或氧化剂)的性质、反应条件、反应物的浓度、反应介质的酸碱性等多种因素。如KMnO 在酸性溶液
4
中的还原产物一般是Mn2+;在中性或碱性溶液中的还原产物一般是锰的较高价态的化合物,如MnO 、
2
KMnO 等。
2 4
【名师归纳】氧化还原反应概念的“五个误区”
误区一:某元素由化合态变为游离态时,该元素不一定被还原,也不一定被氧化。因为元素处于化合
态时,其化合价可能为正,也可能为负。若元素由负价变为0价,则其被氧化,若元素由正价变为0价,
则其被还原。
误区二:在氧化还原反应中,非金属单质不一定只作氧化剂,大部分非金属单质往往既具有氧化性又
具有还原性,只是以氧化性为主。如在反应Cl+HO HCl+HClO中,Cl 既表现氧化性又表现还原性。
2 2 2
误区三:物质的氧化性或还原性的强弱取决于元素原子得失电子的难易程度,与得失电子数目的多少无关。
误区四:氧化还原反应中的反应物不一定都是氧化剂或还原剂,有的反应物可能既不是氧化剂也不是
还原剂。如Cl+HO HCl+HClO,HO既不是氧化剂,也不是还原剂。
2 2 2
误区五:在氧化还原反应中,一种元素被氧化,不一定有另一种元素被还原,也可能是同一元素既被
氧化又被还原。如:2NaO+2HO===4NaOH+O↑中,NaO 既是氧化剂又是还原剂,氧元素一部分化合
2 2 2 2 2 2
价升高,一部分化合价降低。
【归纳总结】
知识点二 物质氧化性、还原性强弱的判断
一、氧化性、还原性强弱的认识
1.氧化性指物质得电子的性质(或能力);还原性指物质失电子的性质(或能力)。
2.氧化性、还原性的强弱取决于物质得、失电子的难易程度,与得、失电子数目的多少无关。例如:
Na-e-===Na+,Al-3e-===Al3+,根据金属活动性顺序可知,Na比Al活泼,更易失去电子,所以Na比
Al的还原性强。
3.从元素的价态考虑:最高价态——只有氧化性,如 HSO 、KMnO 等;最低价态——只有还原性,
2 4 4
如金属单质、Cl-、S2-等;中间价态——既有氧化性,又有还原性,如Fe2+、S、Cl 等。
2
二、氧化性、还原性强弱的比较方法
物质氧化性(得电子的能力)、还原性(失电子的能力)的强弱取决于物质得失电子的难易,与得失电子的
数目无关,但也与外界因素(如反应条件、反应物浓度、酸碱性等)有关,具体判断方法如下:
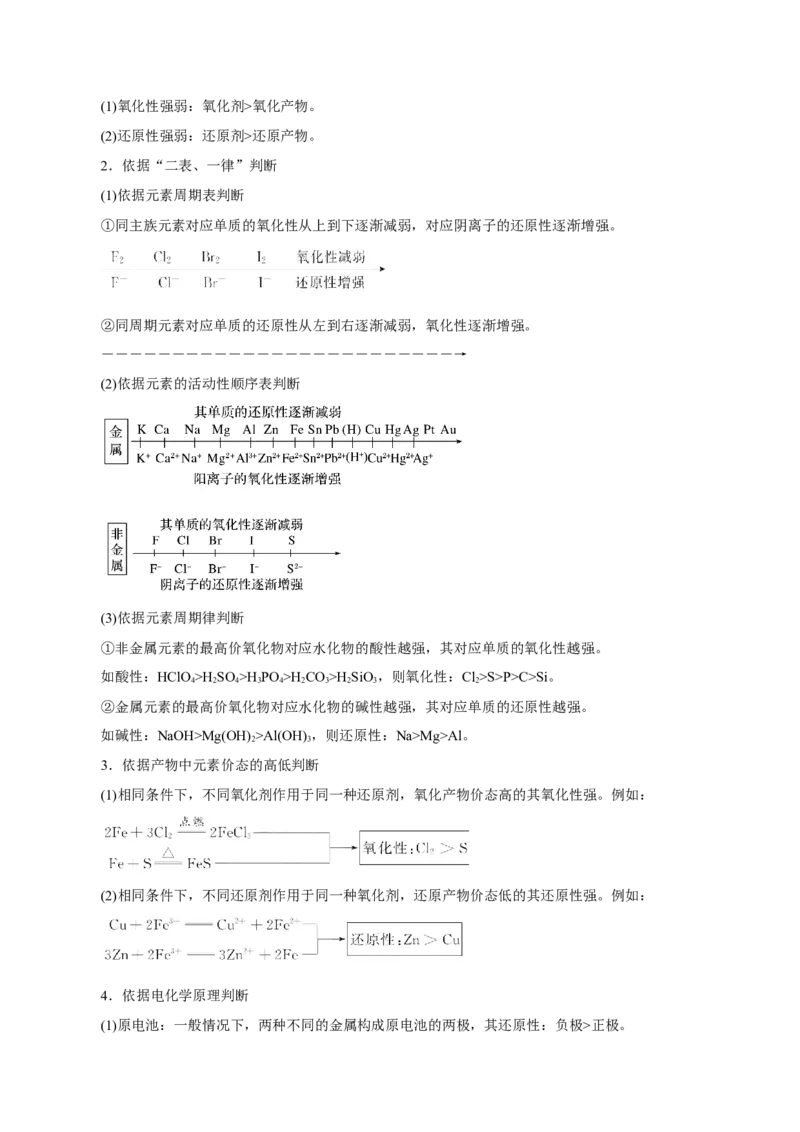
1.依据氧化还原反应原理来判断(1)氧化性强弱:氧化剂>氧化产物。
(2)还原性强弱:还原剂>还原产物。
2.依据“二表、一律”判断
(1)依据元素周期表判断
①同主族元素对应单质的氧化性从上到下逐渐减弱,对应阴离子的还原性逐渐增强。
②同周期元素对应单质的还原性从左到右逐渐减弱,氧化性逐渐增强。
―――――――――――――――――――――――――→
(2)依据元素的活动性顺序表判断
(3)依据元素周期律判断
①非金属元素的最高价氧化物对应水化物的酸性越强,其对应单质的氧化性越强。
如酸性:HClO>H SO >H PO >H CO>H SiO,则氧化性:Cl>S>P>C>Si。
4 2 4 3 4 2 3 2 3 2
②金属元素的最高价氧化物对应水化物的碱性越强,其对应单质的还原性越强。
如碱性:NaOH>Mg(OH) >Al(OH) ,则还原性:Na>Mg>Al。
2 3
3.依据产物中元素价态的高低判断
(1)相同条件下,不同氧化剂作用于同一种还原剂,氧化产物价态高的其氧化性强。例如:
(2)相同条件下,不同还原剂作用于同一种氧化剂,还原产物价态低的其还原性强。例如:
4.依据电化学原理判断
(1)原电池:一般情况下,两种不同的金属构成原电池的两极,其还原性:负极>正极。(2)电解池:用惰性电极电解混合溶液时,在阴极先放电的阳离子的氧化性较强,在阳极先放电的阴离
子的还原性较强。
5.依据影响因素判断
(1)浓度:同一种物质,浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO >稀HSO ,浓HNO>
2 4 2 4 3
稀HNO;还原性:浓HCl>稀HCl。
3
(2)温度:同一种物质,温度越高其氧化性越强。如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强。
(3)酸碱性:同一种物质,所处环境酸(碱)性越强其氧化(还原)性越强。如氧化性:KMnO (酸
4
性)>KMnO (中性)>KMnO (碱性)。
4 4
6.依据反应条件判断
同一种物质,浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO >稀
浓度 2 4
HSO ,浓HNO>稀HNO;还原性:浓HCl>稀HCl
2 4 3 3
同一种物质,温度越高其氧化性越强。如热的浓硫酸的氧化性比冷的浓硫酸的
温度
氧化性强
知识点三 氧化还原反应的规律及其应用
一、价态规律
1.升降规律
氧化还原反应中,化合价有升必有降,升降总值相等。
2.价态归中规律
含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价―→
中间价”,而不会出现交叉现象。简记为“两相靠,不相交”。
例如:不同价态硫之间可以发生的氧化还原反应是下图中的①②③④。
【特别提醒】不会出现⑤中HS转化为SO ,而HSO 转化为S的情况。
2 2 2 4
3.歧化反应规律
“中间价―→高价+低价”。具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应。
例如:Cl+2NaOH===NaCl+NaClO+HO。
2 2
二、强弱规律
1.根据氧化性和还原性规律判断
同一个反应中,氧化剂的氧化性强(填“强”或“弱”)于氧化产物的氧化性,还原剂的还原性强于还
原产物的还原性。如反应2FeCl +2KI===2FeCl +I+2KCl中,氧化性:Fe3+>I ;还原性:I->Fe2+。
3 2 2 22.根据金属活动性或非金属活动性顺序判断
K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag,由左至右,单质的还原性逐渐减弱;K
+、Ca2+、Na+、Mg2+、Al3+、Zn2+、Fe2+、Sn2+、Pb2+、(H+)、Cu2+、Hg2+、Ag+,由左至右,阳离子的
氧化性逐渐增强;F 、Cl 、Br 、I 、S,由左至右,单质的氧化性逐渐减弱;F-、Cl-、Br-、I-、S2-,由
2 2 2 2
左至右,阴离子的还原性逐渐增强。
3.根据产物中元素价态的高低判断
如2Fe+3Cl=====2FeCl ,Fe+S=====FeS,则氧化性:Cl>(填“>”或“<”)S。
2 3 2
三、先后规律
同一体系中,当有多个氧化还原反应发生时,反应的先后顺序遵循强者优先的规律。例如:向含相同
物质的量浓度的S2-、I-、Br-溶液中,缓慢通入氯气,还原性强的离子优先发生反应,先后顺序为 S2-、I
-、Br-;向含等物质的量浓度的Fe3+、Cu2+、H+、Ag+溶液中,缓慢加入足量的镁粉,氧化性强的离子优
先发生反应,先后顺序为Ag+、Fe3+、Cu2+、H+。
四、守恒规律
氧化还原反应中,氧化剂得电子总数等于还原剂失电子总数。
知识点四 氧化还原反应方程式的书写与配平
1.氧化还原方程式配平的基本原则
2.氧化还原方程式配平的一般步骤
以上方法步骤以Cu与稀HNO 反应的方程式配平为例说明如下:
3
(1)标变价
Cu+HNO(稀)——Cu (NO )+NO+HO
3 3 2 2
(2)列变化Cu+HNO(稀)——Cu (NO )+NO+HO
3 3 2 2
(3)求总数
Cu+HNO(稀)——Cu (NO )+NO+HO
3 3 2 2
(4)定系数
3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
(5)查守恒,其他原子在配平时相等,最后利用O原子守恒来进行验证。
【方法技巧】配平的基本方法
(1)全变从左边配:氧化剂、还原剂中某元素化合价是全变的,一般从左边反应物着手配平。
(2)自变从右边配:自身氧化还原反应(包括分解、歧化)一般从右边着手配平。
(3)缺项配平法:先将得失电子数配平,再观察两边电荷。若反应物这边缺正电荷,一般加H+,生成
物一边加水;若反应物这边缺负电荷,一般加OH-,生成物一边加水,然后进行两边电荷数配平。
(4)当方程式中有多个缺项时,应根据化合价的变化找准氧化剂、还原剂、氧化产物、还原产物。
(5)整体配平:指某一氧化还原反应中,有三种元素的化合价发生了变化,但其中一种反应物中同时有
两种元素化合价升高或降低,这时要进行整体配平。
知识点五 电子守恒思想在氧化还原反应计算中的应用
1.对于氧化还原反应的计算,要根据氧化还原反应的实质——反应中氧化剂得到的电子总数与还原
剂失去的电子总数相等,即得失电子守恒。利用守恒思想,可以抛开繁琐的反应过程,可不写化学方程式,
不追究中间反应过程,只要把物质分为始态和终态,从得电子与失电子两个方面进行整体思维,便可迅速
获得正确结果。
2.守恒法解题的思维流程
(1)找出氧化剂、还原剂及相应的还原产物和氧化产物。
(2)找准一个原子或离子得失电子数(注意化学式中粒子的个数)。
(3)根据题中物质的物质的量和得失电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值(高价-低价)=n(还原剂)×变价原子个数×化合价变化值(高价
-低价)。
3.氧化还原反应计算的常用方法——得失电子守恒法
得失电子守恒是指在发生氧化还原反应时,氧化剂得到的电子总数一定等于还原剂失去的电子总数。
得失电子守恒法常用于氧化还原反应中氧化剂、还原剂、氧化产物、还原产物的有关计算及电解过程中电
极产物的有关计算等。
(1)应用电子守恒解题的一般步骤——“一、二、三”。
①“一找各物质”:找出氧化剂、还原剂及相应的还原产物和氧化产物。②“二定得失数”:确定一个原子或离子得失电子数(注意化学式中原子的个数)。
③“三列关系式”:根据题中物质的物质的量和电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原子个数×化合价变化值。
(2)多步连续进行的氧化还原反应的有关计算:对于多步连续进行的氧化还原反应,只要中间各步反应
过程中电子没有损耗,可直接找出起始物和最终产物,删去中间产物,建立二者之间的电子守恒关系,快
速求解。应用以上方法解答有关氧化还原反应的计算题时,可化难为易,化繁为简。
【典例剖析】
高频考点一 氧化还原反应的判断
例1.(2020·山东卷)下列叙述不涉及氧化还原反应的是( )
A. 谷物发酵酿造食醋 B. 小苏打用作食品膨松剂
C. 含氯消毒剂用于环境消毒 D. 大气中NO 参与酸雨形成
2
【举一反三】(2019·北京卷)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
【变式探究】 (2018·北京卷)下列实验中的颜色变化,与氧化还原反应无关的是( )
选项 A B C D
NaOH溶液滴 石蕊溶液滴入 NaS溶液滴入 热铜丝插入稀
实验 2
入FeSO 溶液中 氯水中 AgCl浊液中 硝酸中
4
产生白色沉淀,随 溶液变红,随 沉淀由白色逐 产生无色气体,随
现象
后变为红褐色 后迅速褪色 渐变为黑色 后变为红棕色
高频考点二 氧化还原反应中综合判断
例2.(2021·浙江选考)关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A. NH 中H元素被氧化
3
B. NO 在反应过程中失去电子
2
C. 还原剂与氧化剂的物质的量之比为3:4
D. 氧化产物与还原产物的质量之比为4:3
【变式探究】NaSO 是重要的化工原料,用途很广,其还原性较强,在溶液中易被Cl 氧化成SO
2 2 3 2
,常用作脱氯剂,主要用于治疗氰化物中毒.工业上可利用反应NaCO+2Na S+4SO=3Na SO+CO 制取
2 3 2 2 2 2 3 2NaSO,下列说法正确的是
2 2 3
A.每吸收4molSO ,放出22.4LCO
2 2
B.每生成1molNa SO,转移N 个电子
2 2 3 A
C.氧化产物与还原产物的质量之比为2:1
D.还原性强弱:S2->SO >Cl-
2
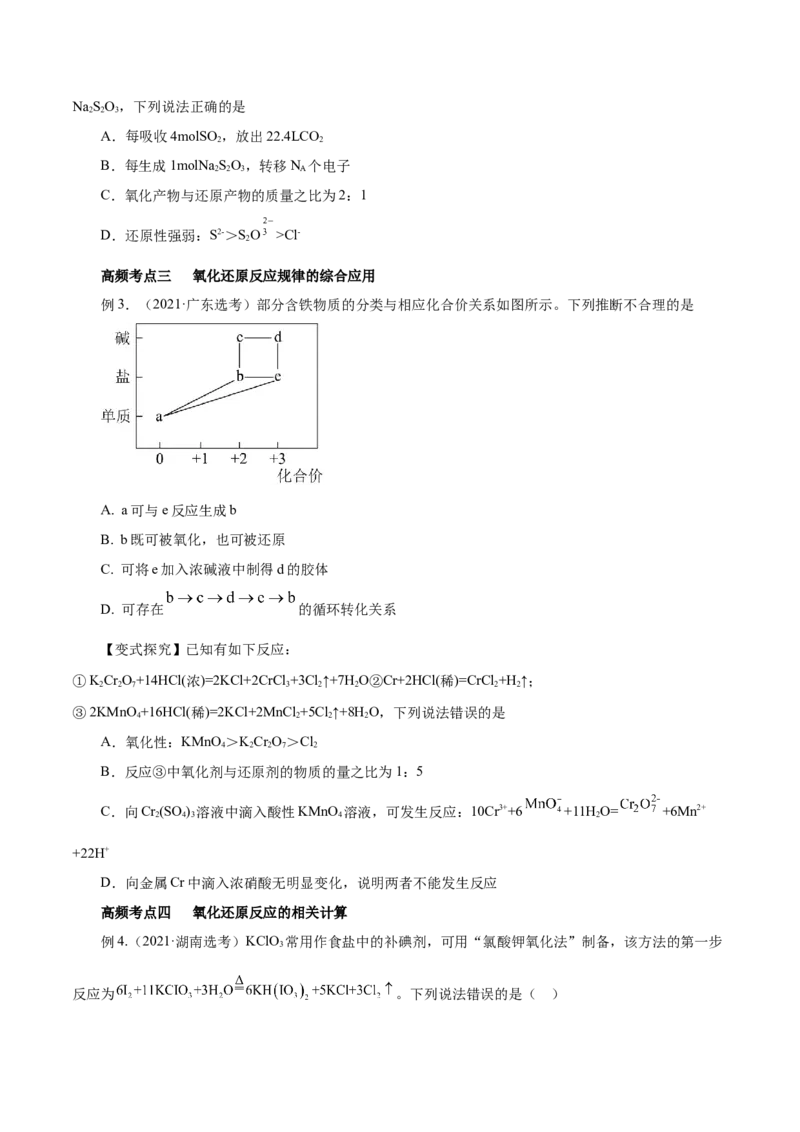
高频考点三 氧化还原反应规律的综合应用
例3.(2021·广东选考)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A. a可与e反应生成b
B. b既可被氧化,也可被还原
C. 可将e加入浓碱液中制得d的胶体
D. 可存在 的循环转化关系
【变式探究】已知有如下反应:
①KCr O+14HCl(浓)=2KCl+2CrCl +3Cl↑+7H O②Cr+2HCl(稀)=CrCl +H ↑;
2 2 7 3 2 2 2 2
③2KMnO +16HCl(稀)=2KCl+2MnCl +5Cl↑+8H O,下列说法错误的是
4 2 2 2
A.氧化性:KMnO >KCr O>Cl
4 2 2 7 2
B.反应③中氧化剂与还原剂的物质的量之比为1:5
C.向Cr (SO ) 溶液中滴入酸性KMnO 溶液,可发生反应:10Cr3++6 +11H O= +6Mn2+
2 4 3 4 2
+22H+
D.向金属Cr中滴入浓硝酸无明显变化,说明两者不能发生反应
高频考点四 氧化还原反应的相关计算
例4.(2021·湖南选考)KClO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步
3
反应为 。下列说法错误的是( )A. 产生22.4L(标准状况) Cl 时,反应中转移10 mol e-
2
B. 反应中氧化剂和还原剂的物质的量之比为11:6
C. 可用石灰乳吸收反应产生的 Cl 制备漂白粉
2
D. 可用酸化的淀粉碘化钾溶液检验食盐中IO -的存在
3
【变式探究】(2020·浙江卷)反应 中,氧化产物与还
原产物的物质的量之比是( )
A. 1:2 B. 1:1 C. 2:1 D. 4:1
【举一反三】(2019·浙江选考)反应8NH +3Cl N+6NH Cl,被氧化的NH 与被还原的Cl 的物
3 2 2 4 3 2
质的量之比为( )
A.2∶3 B.8∶3 C.6∶3 D.3∶2