文档内容
训练(二十二) 非金属化合物的制备及性质探究
1.(2021·广西钦州一中检测)金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广
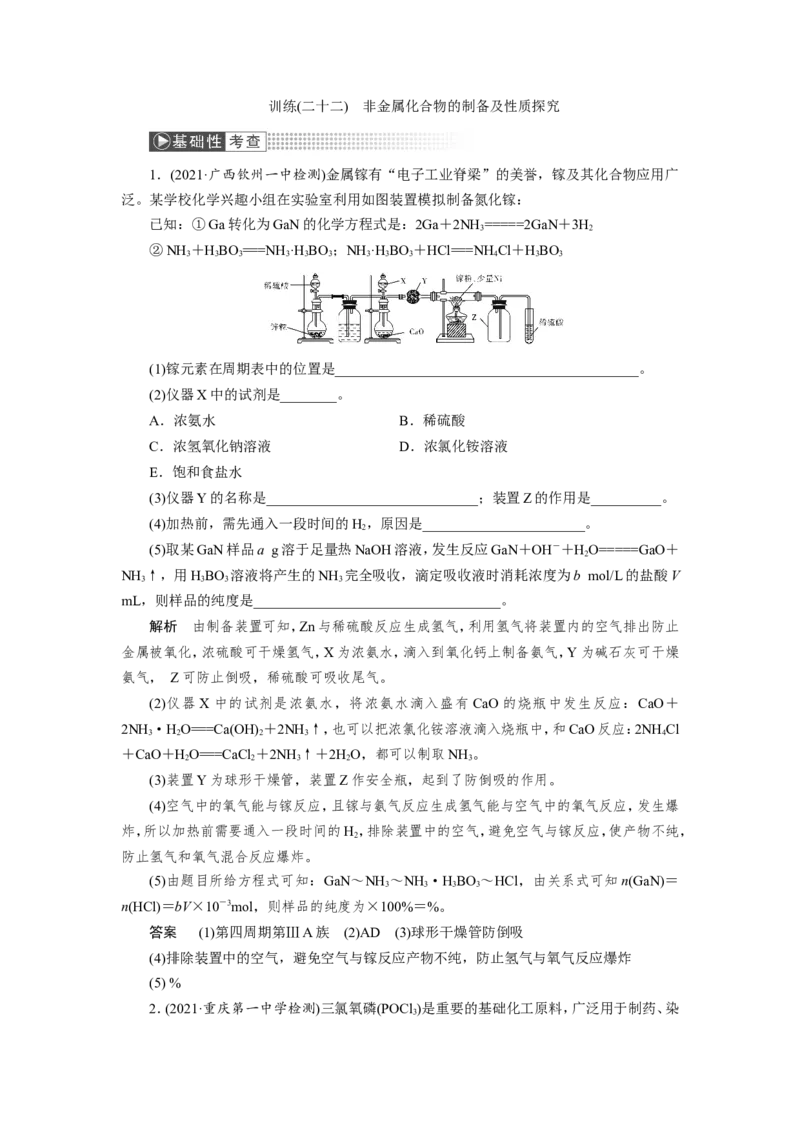
泛。某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
已知:①Ga转化为GaN的化学方程式是:2Ga+2NH =====2GaN+3H
3 2
②NH +HBO===NH·H BO;NH ·H BO+HCl===NHCl+HBO
3 3 3 3 3 3 3 3 3 4 3 3
(1)镓元素在周期表中的位置是___________________________________________。
(2)仪器X中的试剂是________。
A.浓氨水 B.稀硫酸
C.浓氢氧化钠溶液 D.浓氯化铵溶液
E.饱和食盐水
(3)仪器Y的名称是______________________________;装置Z的作用是__________。
(4)加热前,需先通入一段时间的H,原因是_______________________。
2
(5)取某GaN样品a g溶于足量热NaOH溶液,发生反应GaN+OH-+HO=====GaO+
2
NH ↑,用HBO 溶液将产生的NH 完全吸收,滴定吸收液时消耗浓度为b mol/L的盐酸V
3 3 3 3
mL,则样品的纯度是___________________________________。
解析 由制备装置可知,Zn与稀硫酸反应生成氢气,利用氢气将装置内的空气排出防止
金属被氧化,浓硫酸可干燥氢气,X为浓氨水,滴入到氧化钙上制备氨气,Y为碱石灰可干燥
氨气, Z可防止倒吸,稀硫酸可吸收尾气。
(2)仪器X中的试剂是浓氨水,将浓氨水滴入盛有 CaO的烧瓶中发生反应:CaO+
2NH ·HO===Ca(OH) +2NH ↑,也可以把浓氯化铵溶液滴入烧瓶中,和CaO反应:2NH Cl
3 2 2 3 4
+CaO+HO===CaCl +2NH ↑+2HO,都可以制取NH 。
2 2 3 2 3
(3)装置Y为球形干燥管,装置Z作安全瓶,起到了防倒吸的作用。
(4)空气中的氧气能与镓反应,且镓与氨气反应生成氢气能与空气中的氧气反应,发生爆
炸,所以加热前需要通入一段时间的H,排除装置中的空气,避免空气与镓反应,使产物不纯,
2
防止氢气和氧气混合反应爆炸。
(5)由题目所给方程式可知:GaN~NH ~NH ·HBO ~HCl,由关系式可知n(GaN)=
3 3 3 3
n(HCl)=bV×10-3mol,则样品的纯度为×100%=%。
答案 (1)第四周期第ⅢA族 (2)AD (3)球形干燥管防倒吸
(4)排除装置中的空气,避免空气与镓反应产物不纯,防止氢气与氧气反应爆炸
(5) %
2.(2021·重庆第一中学检测)三氯氧磷(POCl )是重要的基础化工原料,广泛用于制药、染
3化、塑胶助剂等行业。某兴趣小组模拟PCl 直接氧化法制备POCl ,实验装置设计如下:
3 3
有关物质的部分性质如下表:
熔点/℃ 沸点/℃ 其他
PCl -112 75.5 遇水生成HPO 和HCl,遇O 生成POCl
3 3 3 2 3
遇水生成HPO 和HCl;
3 4
POCl 2 105.3
3
能溶于PCl
3
回答下列问题:
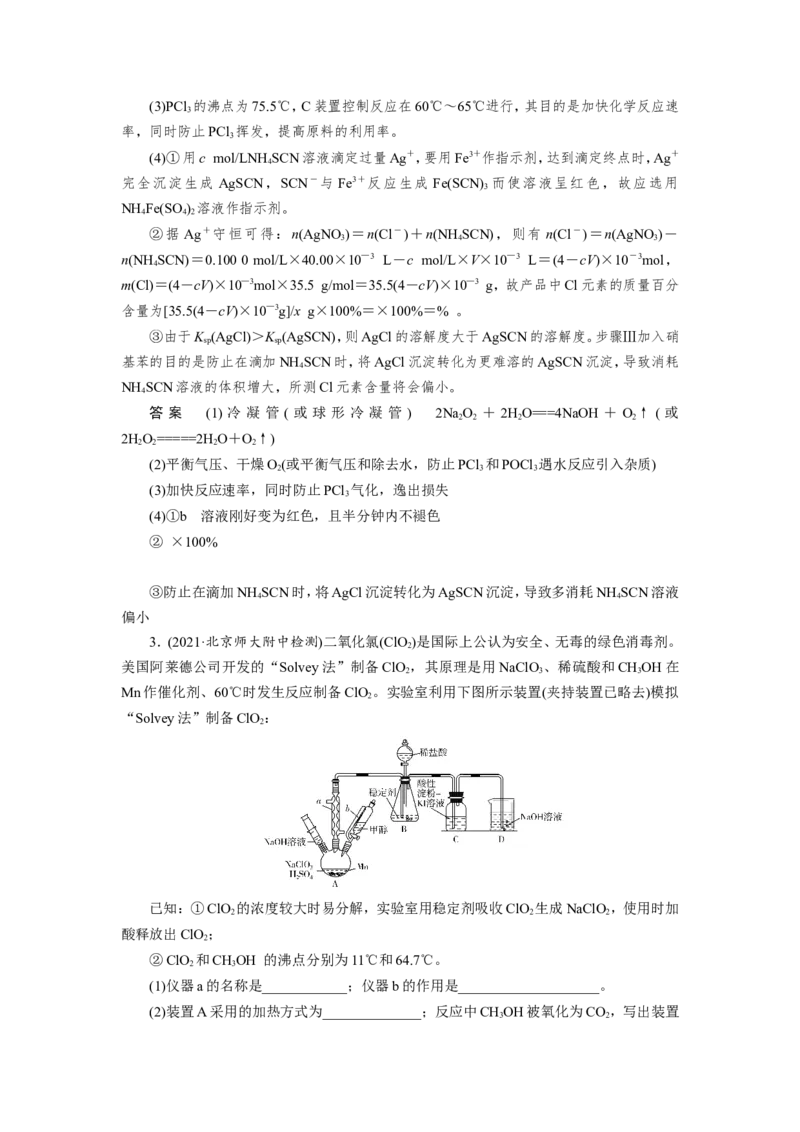
(1) 仪 器 a 的 名 称 是 __________ , 装 置 A 中 发 生 反 应 的 化 学 方 程 式 为
________________________________________________________________________。
(2)B装置的作用除观察O 的流速之外,还有____________________________。
2
(3)C装置控制反应在60℃~65℃进行,其主要目的是_______。
(4)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取x g产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.100 0 mol/L的AgNO 溶液 40.00 mL,使 Cl-完全沉淀。
3
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用c mol/L NH SCN溶液滴定过量Ag+至终点,记下所用体积V mL。
4
已知:K (AgCl)=3.2×10-10,K (AgSCN)=2×10-12
sp sp
① 滴 定 选 用 的 指 示 剂 是 __________( 填 标 号 ) , 滴 定 终 点 的 现 象 为
________________________________。
a.FeCl B.NH Fe(SO )
2 4 4 2
c.淀粉 D.甲基橙
②Cl元素的质量百分含量为(列出算式)________________________________。
③步骤Ⅲ加入硝基苯的目的是_____________________________________________,
如无此操作,所测Cl元素含量将会__________(填“偏大”“偏小”或“不变”)。
解析 (1)仪器a 的名称是球形冷凝管(或冷凝管)。该实验模拟PCl 直接氧化法制备
3
POCl ,PCl 遇O 生成POCl ,装置C三颈烧瓶中盛有PCl ,缺少氧化剂O,故装置A用于制
3 3 2 3 3 2
取O,考虑装置特点,可利用HO 催化分解,或NaO 与水反应,结合守恒规律写出化学方
2 2 2 2 2
程式。
(2)PCl 遇水生成HPO 和HCl,装置A中制得O 中混有HO(g),要通过装置B除去
3 3 3 2 2
HO(g),显然B中盛有浓硫酸。B装置中长颈漏斗下端插入浓硫酸中,上端与大气相通,起到
2
平衡气压的作用,故B装置的作用除观察O 的流速之外,还有干燥气体、平衡气压的作用。
2(3)PCl 的沸点为75.5℃,C装置控制反应在60℃~65℃进行,其目的是加快化学反应速
3
率,同时防止PCl 挥发,提高原料的利用率。
3
(4)①用c mol/LNH SCN溶液滴定过量Ag+,要用Fe3+作指示剂,达到滴定终点时,Ag+
4
完全沉淀生成 AgSCN,SCN-与 Fe3+反应生成 Fe(SCN) 而使溶液呈红色,故应选用
3
NH Fe(SO ) 溶液作指示剂。
4 4 2
②据 Ag+守恒可得:n(AgNO)=n(Cl-)+n(NH SCN),则有 n(Cl-)=n(AgNO)-
3 4 3
n(NH SCN)=0.100 0 mol/L×40.00×10—3 L-c mol/L×V×10—3 L=(4-cV)×10-3mol,
4
m(Cl)=(4-cV)×10—3mol×35.5 g/mol=35.5(4-cV)×10—3 g,故产品中Cl元素的质量百分
含量为[35.5(4-cV)×10—3g]/x g×100%=×100%=% 。
③由于K (AgCl)>K (AgSCN),则AgCl的溶解度大于AgSCN的溶解度。步骤Ⅲ加入硝
sp sp
基苯的目的是防止在滴加NH SCN时,将AgCl沉淀转化为更难溶的AgSCN沉淀,导致消耗
4
NH SCN溶液的体积增大,所测Cl元素含量将会偏小。
4
答 案 (1) 冷 凝 管 ( 或 球 形 冷 凝 管 ) 2NaO + 2HO===4NaOH + O↑ ( 或
2 2 2 2
2HO=====2HO+O↑)
2 2 2 2
(2)平衡气压、干燥O(或平衡气压和除去水,防止PCl 和POCl 遇水反应引入杂质)
2 3 3
(3)加快反应速率,同时防止PCl 气化,逸出损失
3
(4)①b 溶液刚好变为红色,且半分钟内不褪色
② ×100%
③防止在滴加NH SCN时,将AgCl沉淀转化为AgSCN沉淀,导致多消耗NH SCN溶液
4 4
偏小
3.(2021·北京师大附中检测)二氧化氯(ClO )是国际上公认为安全、无毒的绿色消毒剂。
2
美国阿莱德公司开发的“Solvey法”制备ClO ,其原理是用NaClO 、稀硫酸和CHOH在
2 3 3
Mn作催化剂、60℃时发生反应制备ClO 。实验室利用下图所示装置(夹持装置已略去)模拟
2
“Solvey法”制备ClO :
2
已知:①ClO 的浓度较大时易分解,实验室用稳定剂吸收ClO 生成NaClO,使用时加
2 2 2
酸释放出ClO ;
2
②ClO 和CHOH 的沸点分别为11℃和64.7℃。
2 3
(1)仪器a的名称是____________;仪器b的作用是____________________。
(2)装置A采用的加热方式为______________;反应中CHOH被氧化为CO,写出装置
3 2A中制备ClO 的化学方程式:______________________________________________,该方法
2
的优点是_______________________________________。
(3)稳定剂吸收ClO 后,滴加稀盐酸释放ClO ,反应的离子方程式为_________________。
2 2
(4)(双选)下列有关说法正确的是________(填序号)。
A.注射器中NaOH溶液的作用是停止反应,并吸收多余的ClO
2
B.装置C中溶液变成蓝色,证明装置A中反应有Cl 生成
2
C.装置D的作用主要是吸收尾气,防止污染环境
(5)ClO 对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-的
2
浓度为 a mg·L-1,现用ClO 将CN-氧化,只生成两种气体,该反应的离子方程式为
2
________________________________________________________________________;
处理100 m3这种污水,理论上至少需要ClO 的体积(标准状况下)为________(用含a的
2
代数式表示)。
解析 (1)仪器a的名称是球形冷凝管。仪器b是恒压滴液漏斗,其作用是平衡压强,有
利于甲醇顺利流下,并防止甲醇挥发。(2)装置A中制取ClO 在60℃下进行反应,故采用的加
2
热方式为水浴加热。NaClO、稀硫酸和CHOH在Mn作催化剂、60℃时发生反应制备ClO ,
3 3 2
反应中CHOH被氧化为CO,还生成NaHSO、HO,结合得失电子守恒和原子守恒写出化学
3 2 4 2
方程式。(3)稳定剂吸收ClO 生成NaClO,滴加稀盐酸释放ClO ,结合得失电子守恒和原子
2 2 2
守恒及电荷守恒写出离子方程式:5ClO+4H+===4ClO ↑+Cl-+2HO。(4)注射器中NaOH
2 2
溶液的作用是消耗装置A中稀硫酸,使反应停止,并吸收多余的ClO ,A正确;Cl 和ClO 都
2 2 2
具有氧化性,都能将KI氧化生成I 而使溶液变蓝色,故装置C中溶液变成蓝色,不能证明装
2
置A中反应有Cl 生成,B错误;Cl 有毒性,装置D中NaOH溶液的作用是吸收ClO 和Cl 尾
2 2 2 2
气,防止污染环境,C正确。(5)用ClO 处理含CN-的污水,将CN-氧化只生成两种无毒气体,
2
结合元素守恒推知,这两种气体为N 和CO,结合守恒规律写出离子方程式:2ClO +2CN-
2 2 2
===N +2CO+2Cl-。工厂污水中含CN-的浓度为a mg·L-1,100 m3这种污水中含有CN-
2 2
的质量为a mg·L-1×100×1 000 L=105a mg=100a g,n(CN-)=(100a g)/(26 g·mol-1)=
mol,结合反应可知,n(ClO )=n(CN-)= mol,在标准状况下的体积为 mol×22.4 L·mol-1=
2
L。
答案 (1)球形冷凝管 平衡压强,有利于甲醇顺利流下,并防止甲醇挥发 (2)水浴加
热 6NaClO+CHOH+6HSO =====6ClO ↑+CO↑+5HO+6NaHSO 反应产生CO,
3 3 2 4 2 2 2 4 2
可稀释ClO ,防止其浓度过大发生分解 (3)5ClO+4H+===4ClO ↑+Cl-+2HO (4)AC
2 2 2
(5)2ClO+2CN-===N +2CO+2Cl- L
2 2 2
4.(2020·山东潍坊模拟)肼(N H,无色液体)是一种用途广泛的化工原料。实验室中先制
2 4
备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。已知:Cl(g)+2NaOH(aq)===NaClO(aq)+NaCl(aq)+HO(g) ΔH<0。当温度超过40℃时,
2 2
Cl 与NaOH溶液反应生成NaClO。回答下列问题:
2 3
(1)仪器a的名称是____________,装置B的作用是____________________________。
(2)为控制 D 装置中的反应温度,除用冷水浴外,还需采取的实验操作是
________________________________。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭K。此时
1
装置C的作用是________________________。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开K,通入
2
NH ,使其与NaClO溶液反应制取肼。理论上通入三颈烧瓶的Cl 和NH 的最佳物质的量之
3 2 3
比为________。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性
__________________________________(说明操作、现象和结论)。
①淀粉KI溶液 ②稀硫酸(酚酞) ③NaHCO ④AgCl
3
解析 (1)仪器a为圆底烧瓶;装置A中生成Cl,气体中含有HCl,故B的作用为除去
2
Cl 中的HCl;
2
(2)由题干已知信息可知,过量的Cl 会与NaOH发生副反应,导致原料的浪费以及
2
NaClO浓度降低,故需控制Cl 的量,可采取的实验操作为:控制浓盐酸的滴加速度或控制加
2
热温度;
(3)关闭分液漏斗活塞、移去酒精灯时,圆底烧瓶中反应未立即停止,还会继续产生少量
氯气,因K 关闭,A、B装置为封闭体系,故C的作用为储存氯气;
1
(4)氯气通入D中发生反应:2NaOH+Cl===NaCl+NaClO+HO;通入NH 后,D中发
2 2 3
生反应:NaClO+2NH ===N H+NaCl+HO,由两个方程式中NaClO与Cl、NH 的关系可
3 2 4 2 2 2 4
知,通入三颈烧瓶的Cl 和NH 的最佳物质的量之比为1∶2;
2 3
(5)若要验证肼的还原性,则需要选择氧化剂,AgCl中Ag+具有氧化性,故可选用AgCl,
其实验操作及现象和结论为:取少量AgCl于试管中,加入肼溶液,固体逐渐变黑,并有气泡
产生,说明肼有还原性。
答案 (1)圆底烧瓶 除去Cl 中的HCl (2)控制浓盐酸的滴加速度或控制加热温度
2
(3)储存氯气 (4)1∶2
(5)取少量AgCl于试管中,加入肼溶液,固体逐渐变黑,并有气泡产生,说明肼有还原性
5.(2021·山东日照检测)某化学兴趣小组探究NO和NaO 的反应,设计了如下图所示实
2 2
验装置,其中E为实验前压瘪的气囊。
[查阅资料] 除浅黄色的AgNO 难溶于水外,其余亚硝酸盐均易溶于水。
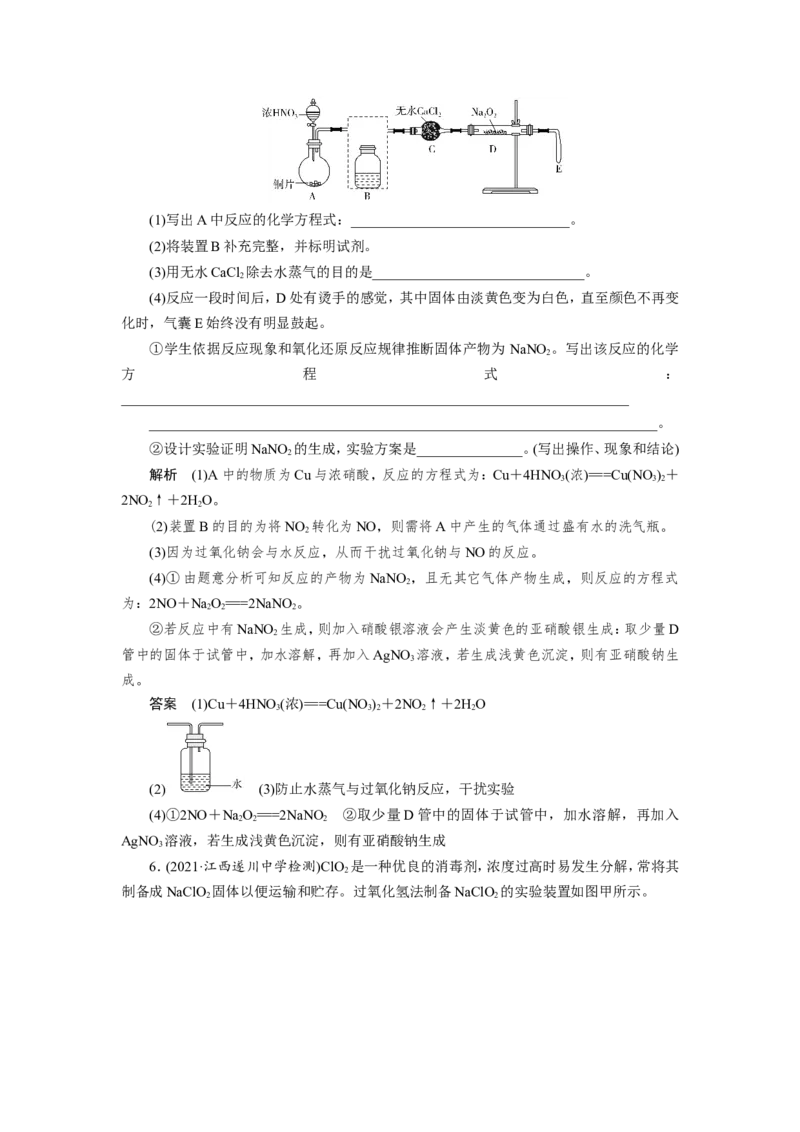
2(1)写出A中反应的化学方程式:_______________________________。
(2)将装置B补充完整,并标明试剂。
(3)用无水CaCl 除去水蒸气的目的是______________________________。
2
(4)反应一段时间后,D处有烫手的感觉,其中固体由淡黄色变为白色,直至颜色不再变
化时,气囊E始终没有明显鼓起。
①学生依据反应现象和氧化还原反应规律推断固体产物为 NaNO 。写出该反应的化学
2
方 程 式 :
________________________________________________________________________
________________________________________________________________________。
②设计实验证明NaNO 的生成,实验方案是_______________。(写出操作、现象和结论)
2
解析 (1)A中的物质为Cu与浓硝酸,反应的方程式为:Cu+4HNO(浓)===Cu(NO)+
3 3 2
2NO ↑+2HO。
2 2
(2)装置B的目的为将NO 转化为NO,则需将A中产生的气体通过盛有水的洗气瓶。
2
(3)因为过氧化钠会与水反应,从而干扰过氧化钠与NO的反应。
(4)①由题意分析可知反应的产物为NaNO ,且无其它气体产物生成,则反应的方程式
2
为:2NO+NaO===2NaNO 。
2 2 2
②若反应中有NaNO 生成,则加入硝酸银溶液会产生淡黄色的亚硝酸银生成:取少量D
2
管中的固体于试管中,加水溶解,再加入AgNO 溶液,若生成浅黄色沉淀,则有亚硝酸钠生
3
成。
答案 (1)Cu+4HNO(浓)===Cu(NO)+2NO ↑+2HO
3 3 2 2 2
(2) (3)防止水蒸气与过氧化钠反应,干扰实验
(4)①2NO+NaO===2NaNO ②取少量D管中的固体于试管中,加水溶解,再加入
2 2 2
AgNO 溶液,若生成浅黄色沉淀,则有亚硝酸钠生成
3
6.(2021·江西遂川中学检测)ClO 是一种优良的消毒剂,浓度过高时易发生分解,常将其
2
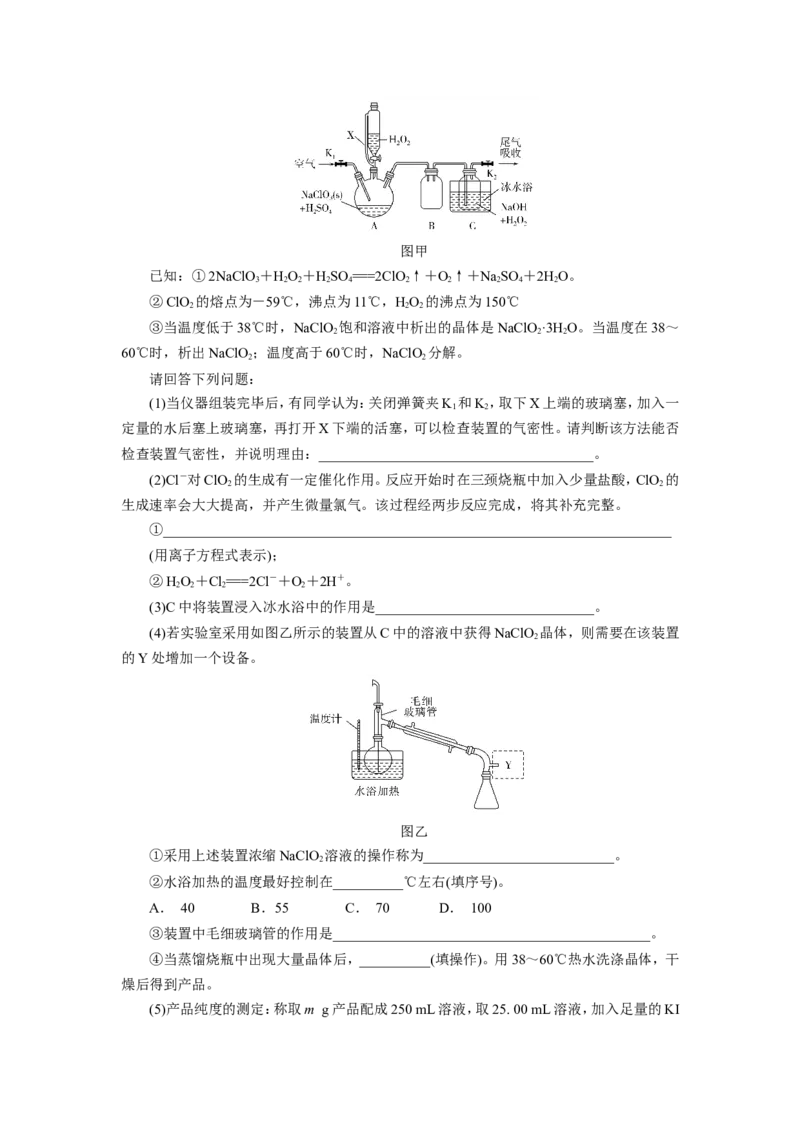
制备成NaClO 固体以便运输和贮存。过氧化氢法制备NaClO 的实验装置如图甲所示。
2 2图甲
已知:①2NaClO+HO+HSO ===2ClO ↑+O↑+NaSO +2HO。
3 2 2 2 4 2 2 2 4 2
②ClO 的熔点为-59℃,沸点为11℃,HO 的沸点为150℃
2 2 2
③当温度低于38℃时,NaClO 饱和溶液中析出的晶体是NaClO·3H O。当温度在38~
2 2 2
60℃时,析出NaClO;温度高于60℃时,NaClO 分解。
2 2
请回答下列问题:
(1)当仪器组装完毕后,有同学认为:关闭弹簧夹K 和K,取下X上端的玻璃塞,加入一
1 2
定量的水后塞上玻璃塞,再打开X下端的活塞,可以检查装置的气密性。请判断该方法能否
检查装置气密性,并说明理由:_______________________________________。
(2)Cl-对ClO 的生成有一定催化作用。反应开始时在三颈烧瓶中加入少量盐酸,ClO 的
2 2
生成速率会大大提高,并产生微量氯气。该过程经两步反应完成,将其补充完整。
①________________________________________________________________________
(用离子方程式表示);
②HO+Cl===2Cl-+O+2H+。
2 2 2 2
(3)C中将装置浸入冰水浴中的作用是_______________________________。
(4)若实验室采用如图乙所示的装置从C中的溶液中获得NaClO 晶体,则需要在该装置
2
的Y处增加一个设备。
图乙
①采用上述装置浓缩NaClO 溶液的操作称为___________________________。
2
②水浴加热的温度最好控制在__________℃左右(填序号)。
A. 40 B.55 C. 70 D. 100
③装置中毛细玻璃管的作用是_____________________________________________。
④当蒸馏烧瓶中出现大量晶体后,__________(填操作)。用38~60℃热水洗涤晶体,干
燥后得到产品。
(5)产品纯度的测定:称取m g产品配成250 mL溶液,取25. 00 mL溶液,加入足量的KI和稀 HSO ,充分反应后加入指示剂,用 c mol·L—1NaSO 标准溶液滴定至终点(I +
2 4 2 2 3 2
2SO===2I-+SO),平均消耗标准溶液的体积为V mL,则产品中NaClO 的质量分数是
2 4 2
________%。
解析 (1)装置A中恒压滴液漏斗的作用是保持容器的压强平衡,使液体顺利流下,不管
装置是否漏气,恒压滴液漏斗中的水都能滴入三颈漏斗中,故该方法不能检测装置的气密性。
(2)Cl-对ClO 的生成有一定催化作用,反应开始时在三颈烧瓶中加入少量盐酸,ClO 的
2 2
生成速率会大大提高,发生反应:2ClO+2Cl-+4H+===Cl↑+2ClO ↑+2HO,HO +
2 2 2 2 2
Cl===2Cl-+O+2H+。
2 2
(3)温度升高,ClO 的溶解度减小,HO、NaClO 易发生分解,故C中将装置浸入冰水浴
2 2 2 2
中的作用是增大ClO 的溶解度使其充分反应,并防止温度过高使HO、NaClO 分解。
2 2 2 2
(4)①Y处应接真空泵,其作用是减小系统的压强,降低液体的沸点,防止液体受热分解,
故浓缩NaClO 溶液的操作是减压蒸馏。
2
②当温度低于38℃时,NaClO 饱和溶液中析出的晶体是NaClO·3HO。当温度在38~
2 2 2
60℃时,析出NaClO;温度高于60℃时,NaClO 分解,故为了加快蒸馏速率,并防止NaClO
2 2 2
受热分解,应使温度低于60℃,且接近60℃,故应选择B项。
④为减小晶体的溶解,当蒸馏烧瓶中出现大量晶体后,要趁热过滤,并用38~60℃热水
洗涤晶体,干燥后得到产品。
(5)NaClO 溶解液中加入足量KI和稀HSO 充分反应,I—被NaClO 氧化生成I,再用标
2 2 4 2 2
准NaSO 标准溶液滴定至终点,存在关系:NaClO ~2I ~4NaSO ,则有n(NaClO)=
2 2 3 2 2 2 2 3 2
1/4n(Na SO)=1/4×c mol·L-1×V×10-3L×250/25.00=2.5cV×10-3 mol,m(NaClO)=
2 2 3 2
2.5cV×10-3 mol×90.5 g/mol=2.5cV×90.5×10-3g,故产品中 NaClO 的质量分数是
2
(2.5cV×90.5×10—3g)/m g×100%=%。
答案 (1)不能,恒压滴液漏斗的支管能够平衡气压,不管装置是否漏气,恒压滴液漏斗
中的水都能滴入三颈烧瓶中,所以该方法不能检查装置的气密性
(2)2ClO+2Cl-+4H+===Cl↑+2ClO ↑+2HO
2 2 2
(3)增大ClO 的溶解度使其充分反应,并防止温度过高使HO、NaClO 分解
2 2 2 2
(4)①减压蒸馏 ②B ③产生气化中心,防止溶液暴沸 ④趁热过滤 (5)