文档内容
第 44 讲 化学反应速率及影响因素
[复习目标] 1.了解化学反应速率的概念及表示方法,能提取信息计算化学反应速率。2.掌
握影响化学反应速率的因素,并能用有关理论解释。
考点一 化学反应速率及表示方法
1.化学反应速率
(1)
(2)各物质的化学反应速率之比=__________之比。
如mA(g)+nB(g)pC(g)+qD(g),v ∶v ∶v ∶v =____________。
A B C D
(3)注意事项
①化学反应速率一般指平均速率而不是某一时刻的瞬时速率,且无论用反应物还是用生成物
表示均取正值。
②同一化学反应,相同条件下用不同物质表示的反应速率,其数值可能不同,但表示的意义
相同。
③固体或纯液体的浓度视为常数,不能用固体或纯液体的浓度变化计算化学反应速率。
2.应用“三段式”计算化学反应速率
列起始量、转化量、某时刻量,再根据定义式或比例关系计算。
对于反应mA(g)+nB(g)pC(g),起始时A的浓度为a mol·L-1,B的浓度为b mol·L-1,C
的浓度为c mol·L-1,反应进行至t s时,A消耗了x mol·L-1,则化学反应速率的计算如下:
1mA(g)+nB(g)pC(g)
起始浓度/mol·L-1 a b c
转化浓度/mol·L-1 x ______ ______
(t s时浓度/mol·L-1 a-x ______ ______
1
则v(A)=________________,v(B)=________________,v(C)=________________。
1.对于任何化学反应来说,反应速率越大,反应现象越明显( )
2.由v=计算平均反应速率,用反应物表示为正值,用生成物表示为负值( )
3.化学反应速率为0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1( )
4.同一化学反应,相同条件下用不同物质表示的反应速率,数值越大,表示化学反应速率
越快( )
一、化学反应速率的概念及基本计算
1.一定温度下反应:4A(s)+3B(g)2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1,
对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol·L-1·min-1
B.分别用B、C、D表示反应速率,其比值是1∶2∶3
C.在2 min末的反应速率,用B表示为0.3 mol·L-1·min-1
D.在这2 min内用B和C表示的瞬时速率的值都是逐渐减小的
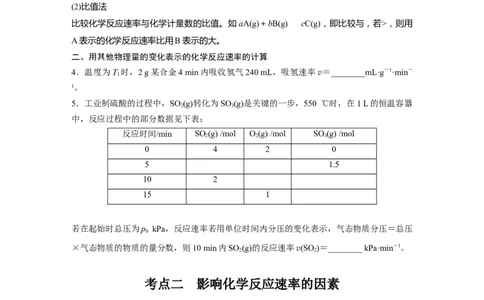
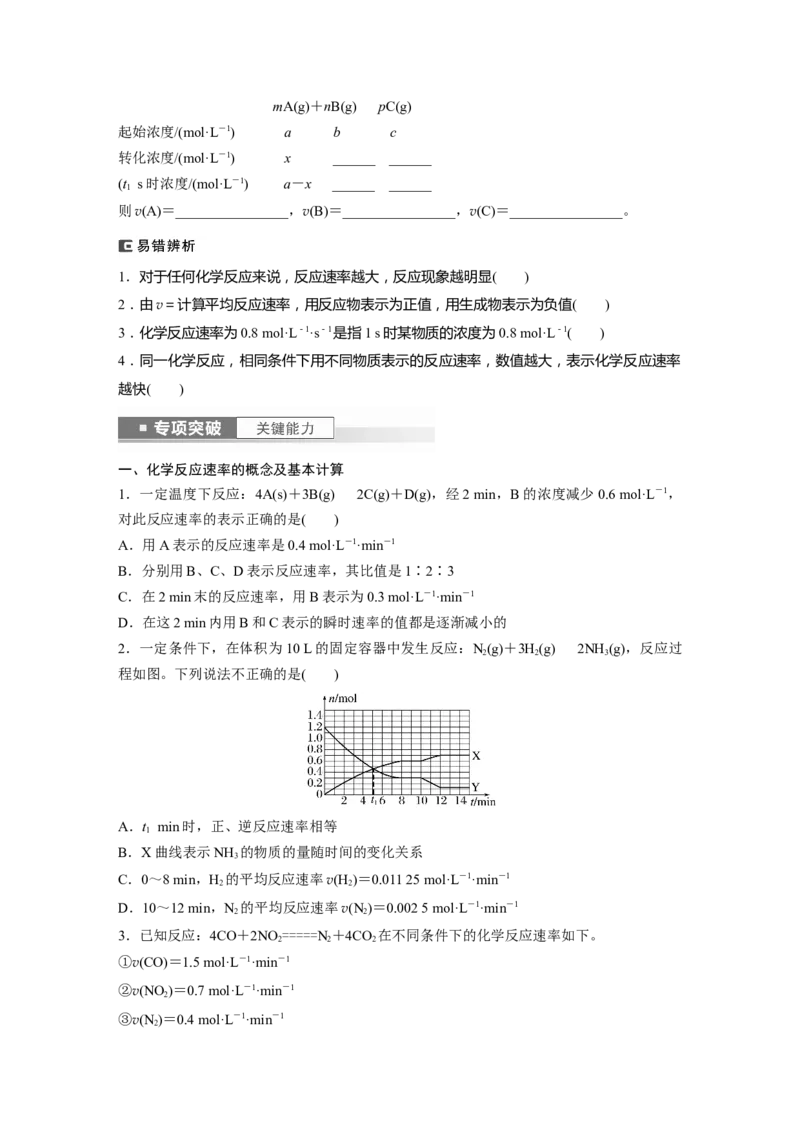
2.一定条件下,在体积为10 L的固定容器中发生反应:N(g)+3H(g)2NH (g),反应过
2 2 3
程如图。下列说法不正确的是( )
A.t min时,正、逆反应速率相等
1
B.X曲线表示NH 的物质的量随时间的变化关系
3
C.0~8 min,H 的平均反应速率v(H )=0.011 25 mol·L-1·min-1
2 2
D.10~12 min,N 的平均反应速率v(N )=0.002 5 mol·L-1·min-1
2 2
3.已知反应:4CO+2NO =====N+4CO 在不同条件下的化学反应速率如下。
2 2 2
①v(CO)=1.5 mol·L-1·min-1
②v(NO )=0.7 mol·L-1·min-1
2
③v(N )=0.4 mol·L-1·min-1
2④v(CO)=1.1 mol·L-1·min-1
2
⑤v(NO )=0.01 mol·L-1·s-1
2
请比较上述5种情况反应的快慢:__________________________________________(由大到
小的顺序)。
化学反应速率大小的比较方法
(1)归一法
按照化学计量数关系换算为同一物质、同一单位表示,再比较数值大小。
(2)比值法
比较化学反应速率与化学计量数的比值。如 aA(g)+bB(g)cC(g),即比较与,若>,则用
A表示的化学反应速率比用B表示的大。
二、用其他物理量的变化表示的化学反应速率的计算
4.温度为T 时,2 g某合金4 min内吸收氢气240 mL,吸氢速率v=________mL·g-1·min-
1
1。
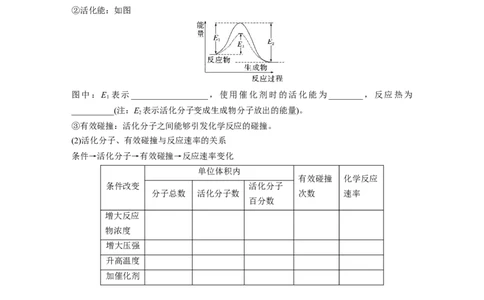
5.工业制硫酸的过程中,SO (g)转化为SO (g)是关键的一步,550 ℃时,在1 L的恒温容器
2 3
中,反应过程中的部分数据见下表:
反应时间/min SO (g) /mol O(g) /mol SO (g) /mol
2 2 3
0 4 2 0
5 1.5
10 2
15 1
若在起始时总压为p kPa,反应速率若用单位时间内分压的变化表示,气态物质分压=总压
0
×气态物质的物质的量分数,则10 min内SO (g)的反应速率v(SO )=________ kPa·min-1。
2 2
考点二 影响化学反应速率的因素
1.内因
反应物__________是主要因素。如相同条件下 Mg、Al与稀盐酸反应的速率大小关系为
Mg____Al。
2.外因3.理论解释——有效碰撞理论
(1)活化分子、活化能、有效碰撞
①活化分子:能够发生有效碰撞的分子(必须具有足够的能量)。
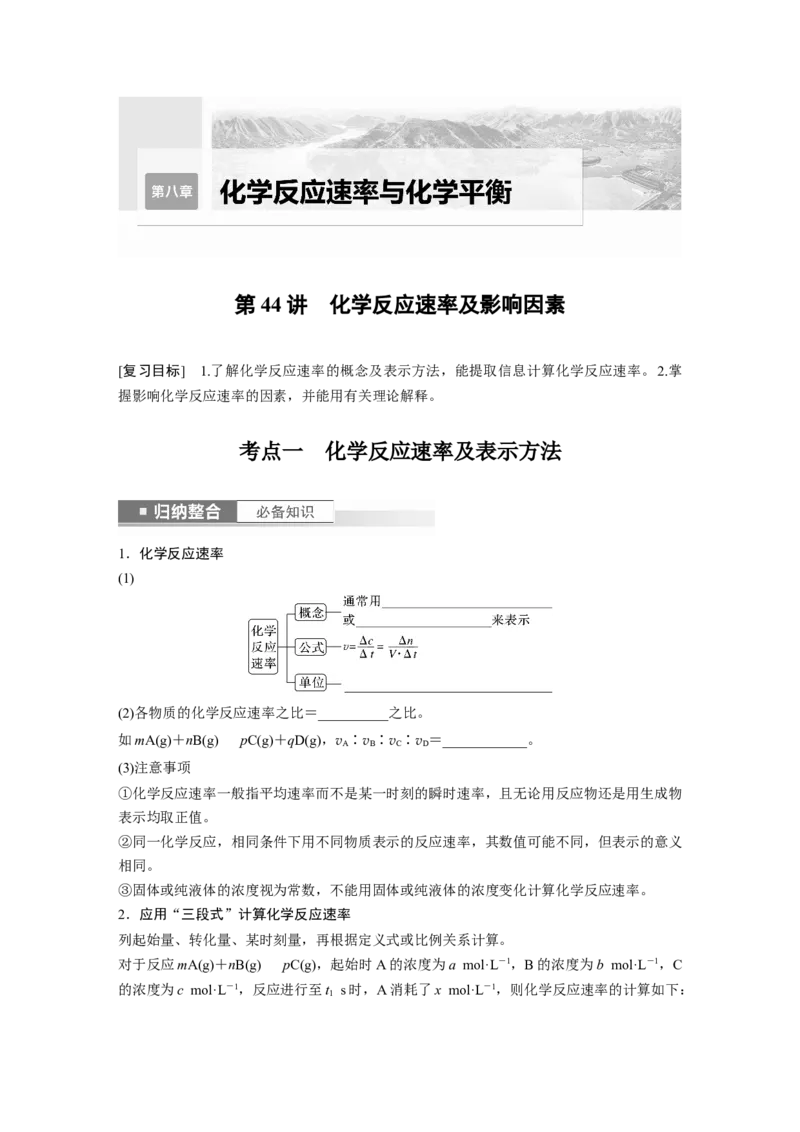
②活化能:如图
图中:E 表示__________________,使用催化剂时的活化能为________,反应热为
1
__________(注:E 表示活化分子变成生成物分子放出的能量)。
2
③有效碰撞:活化分子之间能够引发化学反应的碰撞。
(2)活化分子、有效碰撞与反应速率的关系
条件→活化分子→有效碰撞→反应速率变化
单位体积内
有效碰撞 化学反应
条件改变 活化分子
分子总数 活化分子数 次数 速率
百分数
增大反应
物浓度
增大压强
升高温度
加催化剂
1.催化剂参与化学反应,改变了活化能,但反应前后物理和化学性质保持不变( )
2.升温时吸热反应速率增大,放热反应速率减小( )
3.一定量的锌与过量的稀硫酸反应制取氢气,滴入少量硫酸铜与醋酸钠均能够提高反应速
率( )
4.增大反应物的浓度,能够增大活化分子的百分数,所以反应速率增大( )
5.100 mL 2 mol·L-1盐酸与锌片反应,加入适量的氯化钠溶液,反应速率不变( )一、影响化学反应速率的因素
1.下列措施可以增大化学反应速率的是__________(填序号)。
①Al在氧气中燃烧生成Al O,将Al片改成Al粉
2 3
②Fe与稀硫酸反应制取H 时,改用98%浓硫酸
2
③HSO 与BaCl 溶液反应时,增大压强
2 4 2
④2SO +O2SO ΔH<0,升高温度
2 2 3
⑤Na与水反应时,增大水的用量
⑥2HO===2HO+O↑反应中,加入少量MnO
2 2 2 2 2
⑦H 与Cl 混合后光照
2 2
2.一定温度下,反应N(g)+O(g)2NO(g)在密闭容器中进行,回答下列措施对化学反应
2 2
速率的影响(填“增大”“减小”或“不变”)。
(1)缩小体积使压强增大:__________,原因是_______________________________________。
(2)恒容充入N:__________。
2
(3)恒容充入He:__________,原因是______________________________________________
______________________________________________________________________________。
(4)恒压充入He:__________。
惰性气体对反应速率的影响
在恒温恒容条件下 通入惰性气体,总压增大,反应物浓度不变,反应速率不变
恒温恒压条件下 通入惰性气体,总体积增大,反应物浓度减小,反应速率减小
二、用控制变量法探究影响化学反应速率的因素
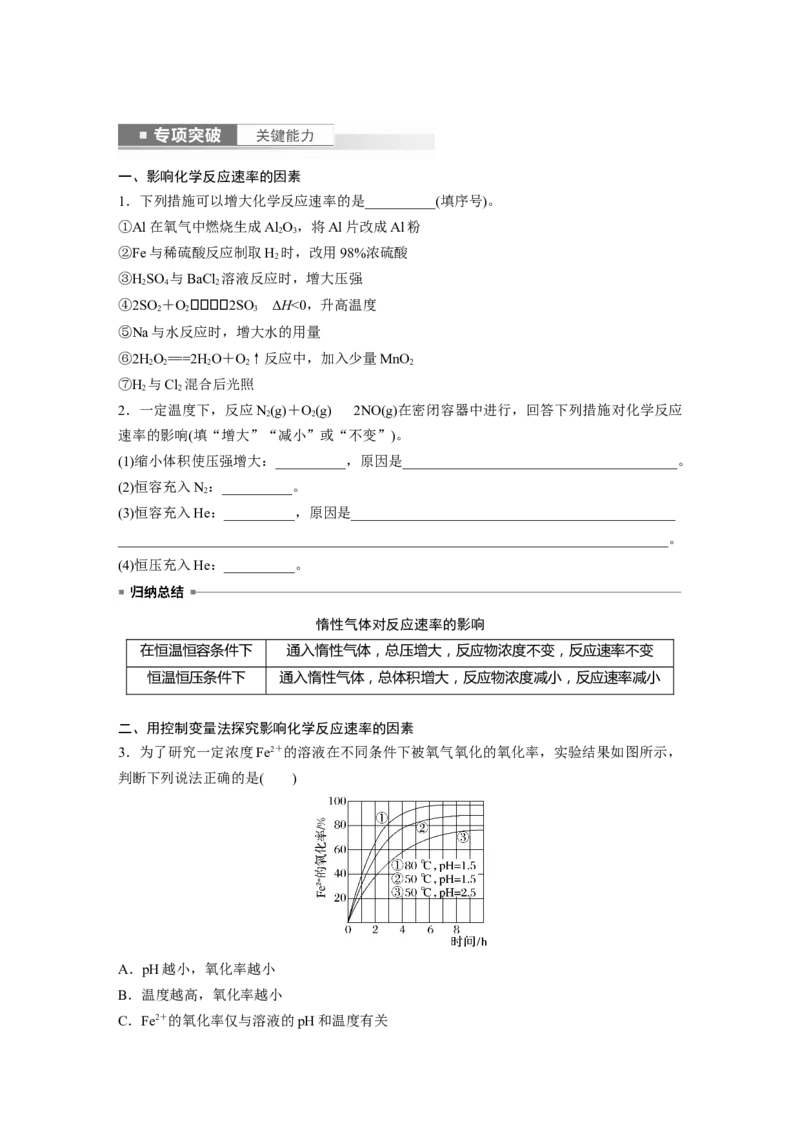
3.为了研究一定浓度Fe2+的溶液在不同条件下被氧气氧化的氧化率,实验结果如图所示,
判断下列说法正确的是( )
A.pH越小,氧化率越小
B.温度越高,氧化率越小
C.Fe2+的氧化率仅与溶液的pH和温度有关D.实验说明降低pH、升高温度有利于提高Fe2+的氧化率
4.已知:2KMnO +5HC O +3HSO ===2MnSO +KSO +10CO↑+8HO。某化学小组
4 2 2 4 2 4 4 2 4 2 2
欲探究HC O 溶液和酸性KMnO 溶液反应过程中浓度、温度对化学反应速率的影响,进行
2 2 4 4
了如下实验(忽略溶液体积变化):
0.01 mol·L-1酸性
编 0.1 mol·L-1 HC O 溶 反应温 反应时
2 2 4
KMnO 溶液体积/m 水的体积/mL
4
号 液体积/mL 度/℃ 间/min
L
Ⅰ 2 2 0 20 2.1
Ⅱ V 2 1 20 5.5
1
Ⅲ V 2 0 50 0.5
2
下列说法不正确的是( )
A.V=1,V=2
1 2
B.设计实验Ⅰ、Ⅲ的目的是探究温度对反应速率的影响
C.实验计时是从溶液混合开始,溶液呈紫红色时结束
D.实验Ⅲ中用酸性KMnO 溶液的浓度变化表示的反应速率v(KMnO)=0.01 mol·L-1·min-1
4 4
5.可逆反应2SO (g)+O(g)2SO (g)是工业上制取HSO 的重要反应。
2 2 3 2 4
(1)在恒压条件下,该反应分组实验的有关条件如下表:
起始 起始
反应条件 温度 容器容积 其他条件
n(SO ) n(O )
2 2
Ⅰ 组 500 ℃ 1 L 1 mol 2 mol 无
Ⅱ 组 500 ℃ 1 L 1 mol 2 mol
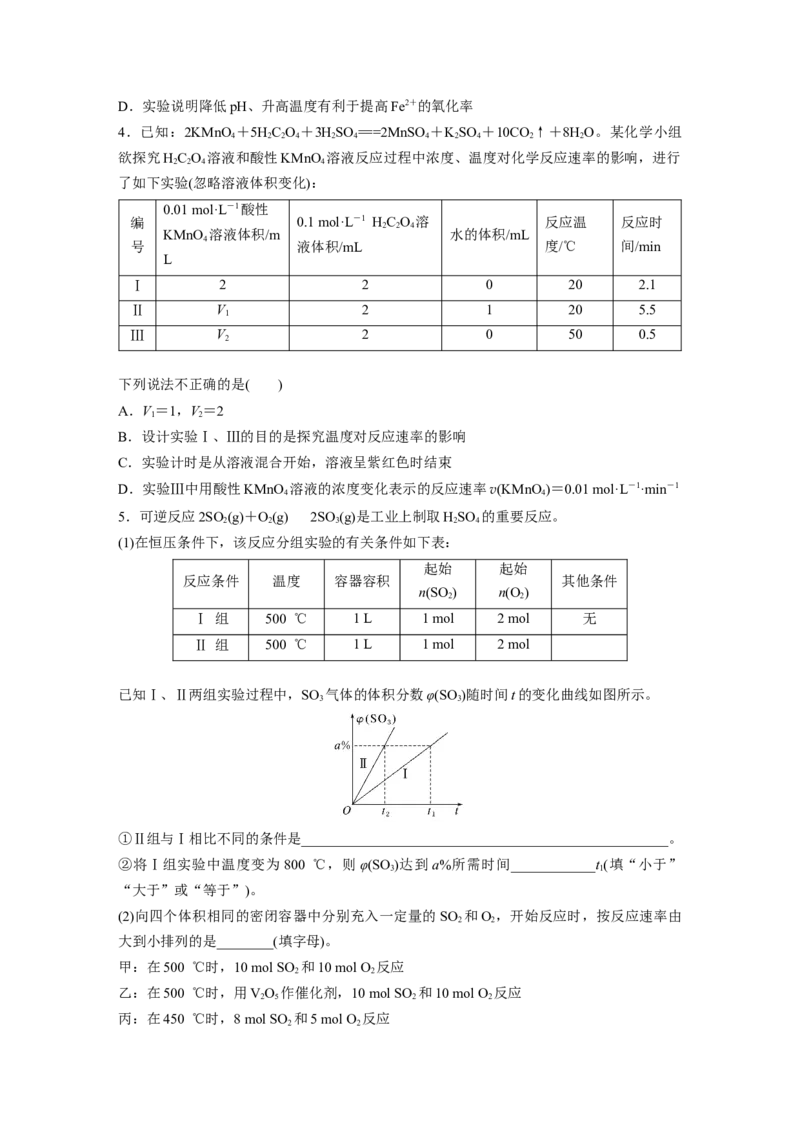
已知Ⅰ、Ⅱ两组实验过程中,SO 气体的体积分数φ(SO )随时间t的变化曲线如图所示。
3 3
①Ⅱ组与Ⅰ相比不同的条件是____________________________________________________。
②将Ⅰ组实验中温度变为800 ℃,则φ(SO )达到a%所需时间____________t(填“小于”
3 1
“大于”或“等于”)。
(2)向四个体积相同的密闭容器中分别充入一定量的SO 和O ,开始反应时,按反应速率由
2 2
大到小排列的是________(填字母)。
甲:在500 ℃时,10 mol SO 和10 mol O 反应
2 2
乙:在500 ℃时,用VO 作催化剂,10 mol SO 和10 mol O 反应
2 5 2 2
丙:在450 ℃时,8 mol SO 和5 mol O 反应
2 2丁:在500 ℃时,8 mol SO 和5 mol O 反应
2 2
A.甲、乙、丙、丁 B.乙、甲、丙、丁
C.乙、甲、丁、丙 D.丁、丙、乙、甲
关于“控制变量法”题目的解题策略
1.(2022·浙江6月选考,20)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
2NH (g)N(g)+3H(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,
3 2 2
如下表所示,下列说法不正确的是( )
时间/min
编号 cNH /10-3 mol·L-1 0 20 40 60 80
3
表面积/cm2
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①,0~20 min,v(N )=1.00×10-5 mol·L-1·min-1
2
B.实验②,60 min时处于平衡状态,x≠0.40C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
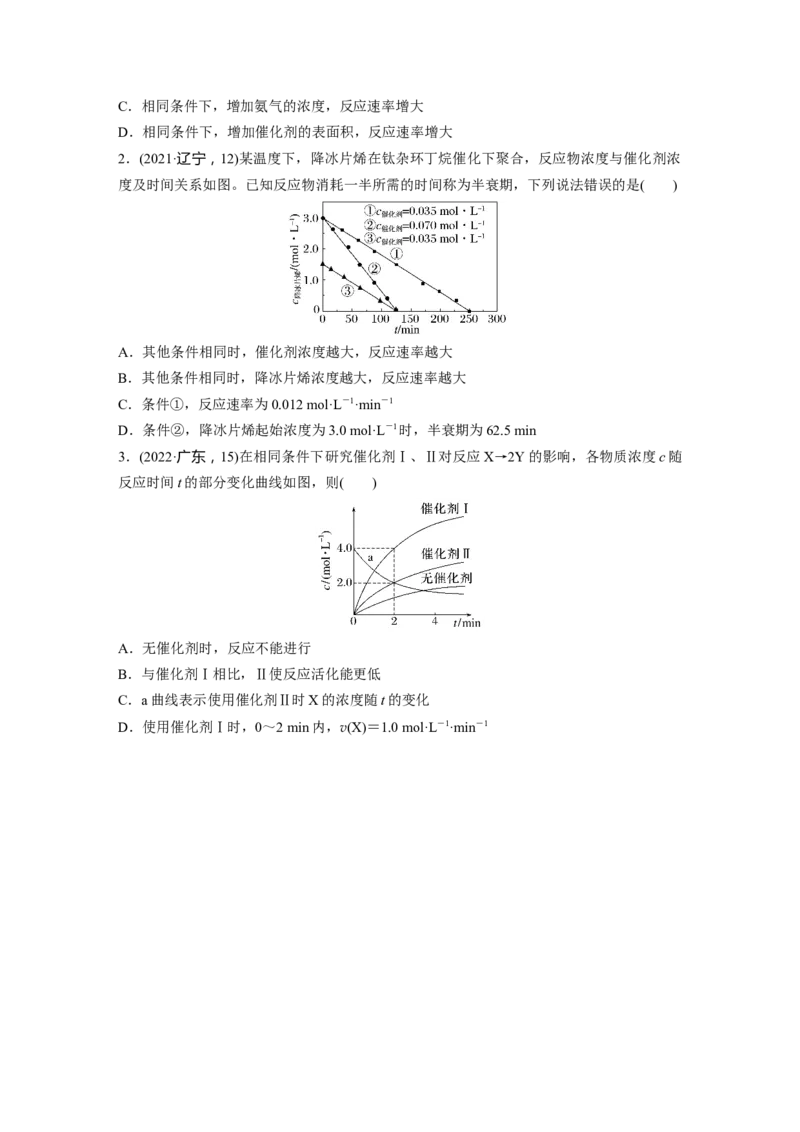
2.(2021·辽宁,12)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓
度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
3.(2022·广东,15)在相同条件下研究催化剂Ⅰ、Ⅱ对反应X→2Y的影响,各物质浓度c随
反应时间t的部分变化曲线如图,则( )
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,0~2 min内,v(X)=1.0 mol·L-1·min-1