文档内容
第 45 讲 化学反应速率与反应历程
[复习目标] 1.了解基元反应、过渡态理论,了解速率方程和速率常数。2.掌握多因素对化
学反应速率影响的分析方法。
考点一 基元反应 过渡态理论
1.基元反应
大多数化学反应都是分几步完成的,其中的____________都称为基元反应。
2.对于基元反应aA+bB===gG+hH,其速率方程可写为v=k·ca(A)·cb(B)(其中k称为速率
常数,恒温下,k不因反应物浓度的改变而变化),这种关系可以表述为基元反应的化学反应
速率与反应物浓度以其化学计量数为指数的幂的乘积成正比。有时称其为质量作用定律。
3.许多化学反应,尽管其反应方程式很简单,却不是基元反应,而是经由两个或多个步骤
完成的复杂反应。例如H(g)+I(g)===2HI(g),它的反应历程有如下两步基元反应:
2 2
①II+I(快)
2
②H+2I===2HI(慢)
2
其中慢反应为整个反应的决速步骤。
4.过渡态理论
如图所示是两步完成的化学反应,分析并回答下列问题。
(1)该反应的反应物为______,中间体为____,生成物为____。
(2)由A、B生成C的反应为____(填“吸”或“放”,下同)热反应,由C生成D的反应为
____热反应,总反应为____热反应。
(3)第一步为____(填“快”或“慢”,下同)反应,第二步为____反应,决定总反应快慢的是
第____步反应。一、反应机理——快反应与慢反应
1.甲烷与氯气在光照条件下存在如下反应历程(“·”表示电子):
①Cl――→2Cl·(慢反应)
2
②CH+Cl·―→·CH+HCl(快反应)
4 3
③·CH+Cl―→CHCl+Cl·(快反应)
3 2 3
④·CH+Cl·―→CHCl(快反应)
3 3
已知在一个分步反应中,较慢的一步反应控制总反应的速率。下列说法不正确的是( )
A.上述过程的总反应方程式为CH+Cl――→CHCl+HCl
4 2 3
B.光照的主要作用是促进反应①的进行从而使总反应速率加快
C.反应②~④都是由微粒通过碰撞而发生的反应
D.反应①是释放能量的反应
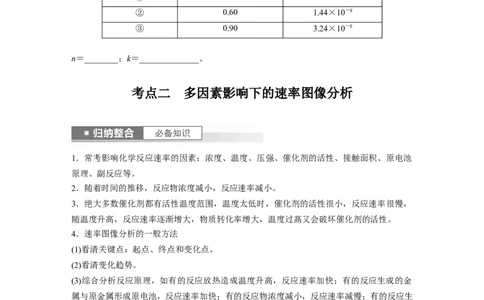
2.如图是CH 与Zr形成过渡金属化合物的过程。下列说法正确的是( )
4
A.加入合适的催化剂待反应完成时可增大过渡金属化合物的产率
B.Zr+CH―→CH—Zr…H的活化能为99.20 kJ·mol-1
4 3
C.整个反应的快慢由状态1前 →CH—Zr…H的反应快慢决定
3
D.Zr+CH―→CH—Zr…H ΔH=-39.54 kJ·mol-1
4 3
二、速率常数与速率方程
3.工业上利用 CH(混有 CO 和 H)与水蒸气在一定条件下制取 H ,原理为 CH(g)+
4 2 2 4
H
2
O(g)CO(g)+3H
2
(g),该反应的逆反应速率表达式为v逆 =k·c(CO)·c3(H
2
),k为速率常数,
在某温度下测得实验数据如表所示:
CO浓度/ (mol·L-1) H 浓度/(mol·L-1) 逆反应速率/(mol·L-1·min-1)
2
0.1 c 8.0
1c c 16.0
2 1
c 0.15 6.75
2
由上述数据可得该温度下,c=________,该反应的逆反应速率常数k=________ L3·
2
mol-3·min-1。
4.300 ℃时,2NO(g)+Cl
2
(g)2ClNO(g)的正反应速率表达式为v正 =k·cn(ClNO),测得正
反应速率和浓度的关系如下表:
序号 c(ClNO)/(mol·L-1) v正 /(mol·L-1·s-1)
① 0.30 3.60×10-9
② 0.60 1.44×10-8
③ 0.90 3.24×10-8
n=________;k=______________。
考点二 多因素影响下的速率图像分析
1.常考影响化学反应速率的因素:浓度、温度、压强、催化剂的活性、接触面积、原电池
原理、副反应等。
2.随着时间的推移,反应物浓度减小,反应速率减小。
3.绝大多数催化剂都有活性温度范围,温度太低时,催化剂的活性很小,反应速率很慢,
随温度升高,反应速率逐渐增大,物质转化率增大,温度过高又会破坏催化剂的活性。
4.速率图像分析的一般方法
(1)看清关键点:起点、终点和变化点。
(2)看清变化趋势。
(3)综合分析反应原理,如有的反应放热造成温度升高,反应速率加快;有的反应生成的金
属与原金属形成原电池,反应速率加快;有的反应物浓度减小,反应速率减慢;有的反应生
成物中有催化剂,反应速率加快;有的反应温度过高,造成催化剂失去活性,反应速率减慢
等。
一、温度与浓度的双重影响
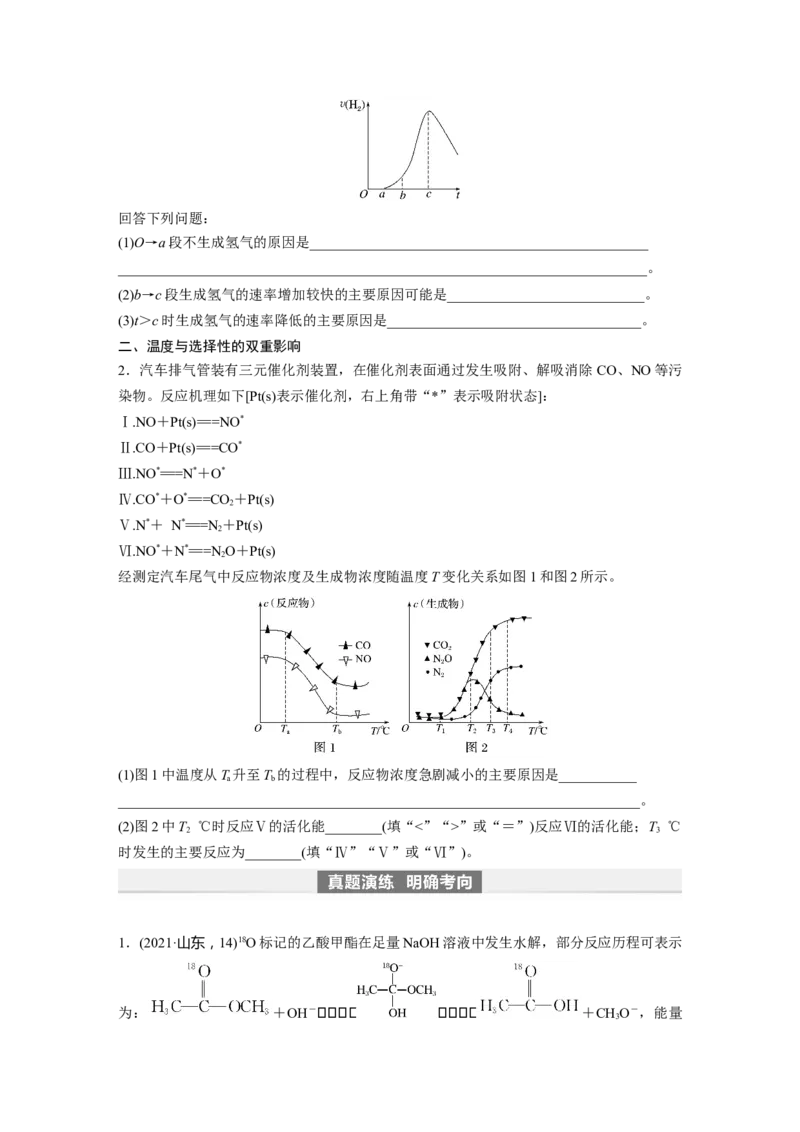
1.把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1盐酸的烧杯中,该铝片与盐酸反
应生成氢气的速率v与反应时间t可用如图的坐标曲线来表示。回答下列问题:
(1)O→a段不生成氢气的原因是________________________________________________
___________________________________________________________________________。
(2)b→c段生成氢气的速率增加较快的主要原因可能是____________________________。
(3)t>c时生成氢气的速率降低的主要原因是____________________________________。
二、温度与选择性的双重影响
2.汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除 CO、NO等污
染物。反应机理如下[Pt(s)表示催化剂,右上角带“*”表示吸附状态]:
Ⅰ.NO+Pt(s)===NO*
Ⅱ.CO+Pt(s)===CO*
Ⅲ.NO*===N*+O*
Ⅳ.CO*+O*===CO+Pt(s)
2
Ⅴ.N*+ N*===N+Pt(s)
2
Ⅵ.NO*+N*===NO+Pt(s)
2
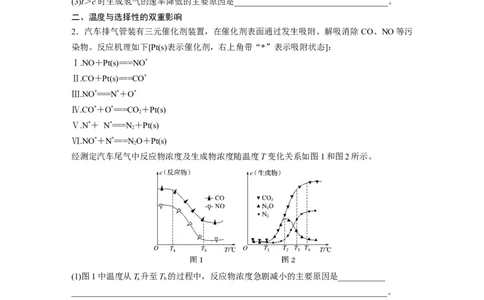
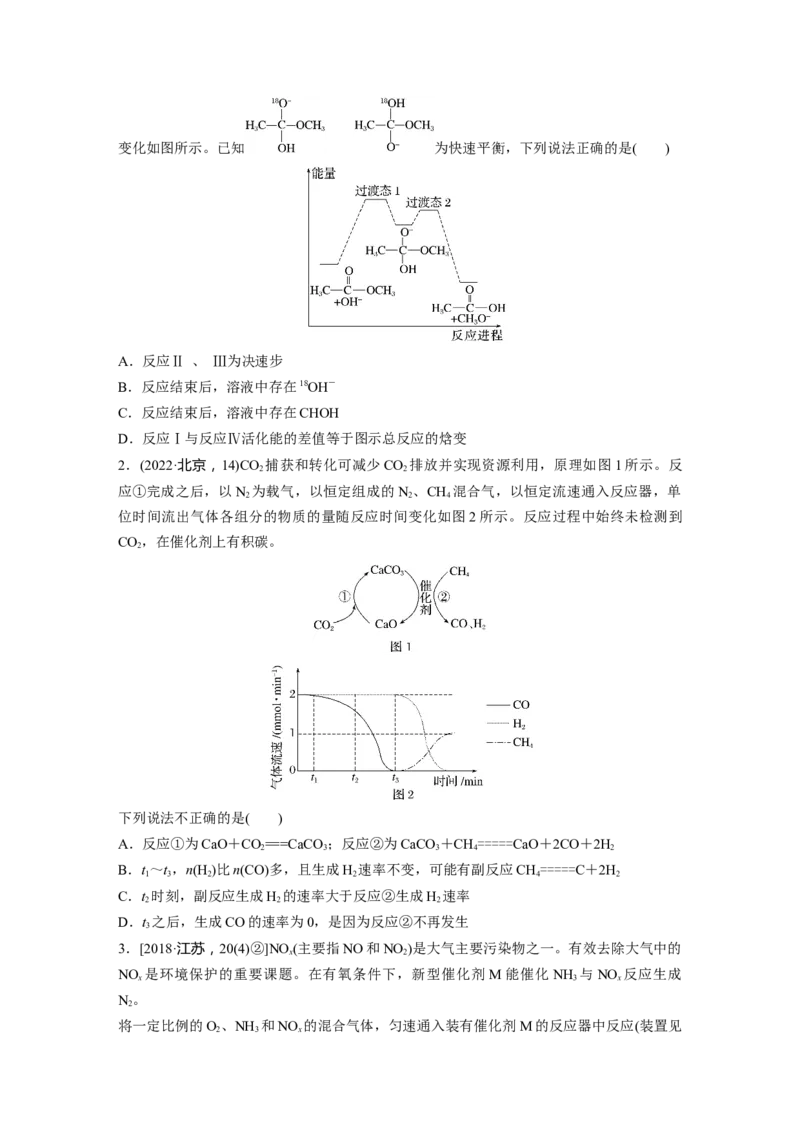
经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图1和图2所示。
(1)图1中温度从T升至T 的过程中,反应物浓度急剧减小的主要原因是___________
a b
__________________________________________________________________________。
(2)图2中T ℃时反应Ⅴ的活化能________(填“<”“>”或“=”)反应Ⅵ的活化能;T ℃
2 3
时发生的主要反应为________(填“Ⅳ”“Ⅴ”或“Ⅵ”)。
1.(2021·山东,14)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示
为: +OH- +CHO-,能量
3变化如图所示。已知 为快速平衡,下列说法正确的是( )
A.反应Ⅱ 、 Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CHOH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
2.(2022·北京,14)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反
2 2
应①完成之后,以N 为载气,以恒定组成的N 、CH 混合气,以恒定流速通入反应器,单
2 2 4
位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
CO,在催化剂上有积碳。
2
下列说法不正确的是( )
A.反应①为CaO+CO===CaCO ;反应②为CaCO +CH=====CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH=====C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3
3.[2018·江苏,20(4)②]NO(主要指NO和NO )是大气主要污染物之一。有效去除大气中的
x 2
NO 是环境保护的重要课题。在有氧条件下,新型催化剂 M能催化NH 与NO 反应生成
x 3 x
N。
2
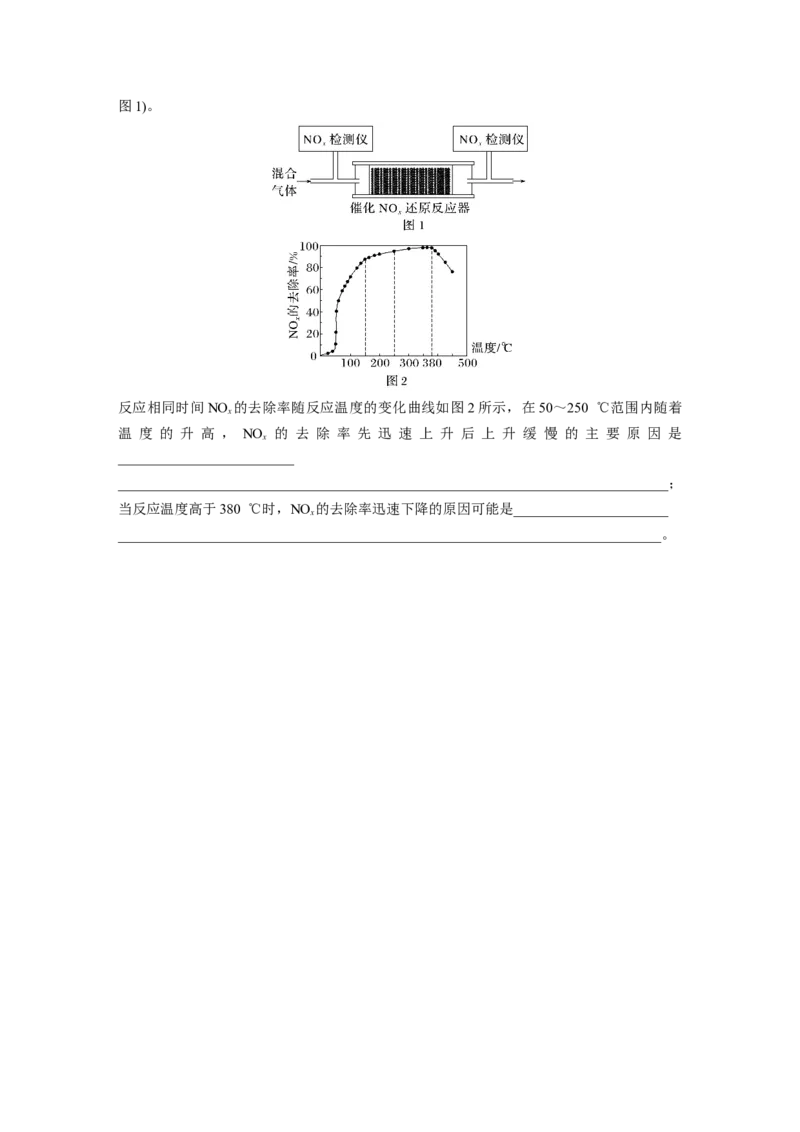
将一定比例的O 、NH 和NO 的混合气体,匀速通入装有催化剂M的反应器中反应(装置见
2 3 x图1)。
反应相同时间NO 的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范围内随着
x
温 度 的 升 高 , NO 的 去 除 率 先 迅 速 上 升 后 上 升 缓 慢 的 主 要 原 因 是
x
_________________________
______________________________________________________________________________;
当反应温度高于380 ℃时,NO 的去除率迅速下降的原因可能是______________________
x
_____________________________________________________________________________。