文档内容
1.(2022·陕西咸阳模拟)水是生命之源,也是生活中最常见的溶剂。下列有关水的说法正确
的是( )
A.水是弱电解质,其电离方程式为2HO===HO++OH-
2 3
B.水分子之间存在氢键,因此水比HS更稳定
2
C.常温下,由水电离出c(H+)=1×10-12 mol·L-1的溶液可能呈碱性
D.水和金属单质或非金属单质反应时一定是水中的氢元素被还原生成氢气
2.(2022·山西省应县一中模拟)25 ℃时,有关水的电离,下列叙述正确的是( )
A.向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,K 不变
w
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+)降低
3
D.将水加热,K 增大,c(H+)不变
w
3.25 ℃时,在等体积的①pH=0的HSO 溶液、②0.05 mol·L-1的Ba(OH) 溶液、③pH
2 4 2
=10的NaS溶液、④pH=5的NH NO 溶液中,发生电离的水的物质的量之比是( )
2 4 3
A.1∶10∶1010∶109 B.1∶5∶(5×109)∶(5×108)
C.1∶20∶1010∶109 D.1∶10∶104∶109
4.常温下,下列叙述不正确的是( )
A.c(H+)>c(OH-)的溶液一定显酸性
B.pH=3的弱酸溶液与pH=11的强碱溶液等体积混合后溶液呈酸性
C.pH=5的硫酸溶液稀释到原来的500倍,稀释后c(SO)与c(H+)之比约为1∶10
D.中和10 mL 0.1 mol·L-1醋酸溶液与100 mL 0.01 mol·L-1醋酸溶液所需NaOH的物质的
量不同
5.已知液氨的性质与水相似。T ℃时,NH +NH NH+NH,NH 的平衡浓度为
3 3
1×10-15 mol·L-1,则下列说法正确的是( )
A.在此温度下液氨的离子积为1×10-17
B.在液氨中放入金属钠,可生成NaNH
2
C.恒温下,在液氨中加入NH Cl,可使液氨的离子积减小
4
D.降温,可使液氨电离平衡逆向移动,且c(NH)<c(NH)
6.下列事实中,能说明MOH是弱碱的是( )
A.0.1 mol·L-1 MOH溶液可以使酚酞溶液变红
B.常温下,0.1 mol·L-1 MOH溶液中c(OH-)<0.1 mol·L-1
C.MOH溶液的导电能力比NaOH溶液弱
D.等体积的0.1 mol·L-1 MOH溶液与0.1 mol·L-1盐酸恰好完全反应7.下列叙述正确的是( )
A.95 ℃纯水的pH<7,说明加热可导致水呈酸性
B.室温下,pH=3的醋酸溶液,稀释10倍后pH=4
C.室温下,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
D.0.2 mol·L-1的盐酸与等体积水混合后pH=1
8.已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸HA与
w
b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
9.25 ℃时,体积为V、pH=a的某一元强酸溶液与体积为V 、pH=b的某一元强碱溶液
a b
均匀混合后,溶液的pH=7,已知b=6a,V<V,下列有关a的说法正确的是( )
a b
A.a可能等于1 B.a一定大于2
C.a一定小于2 D.a一定等于2
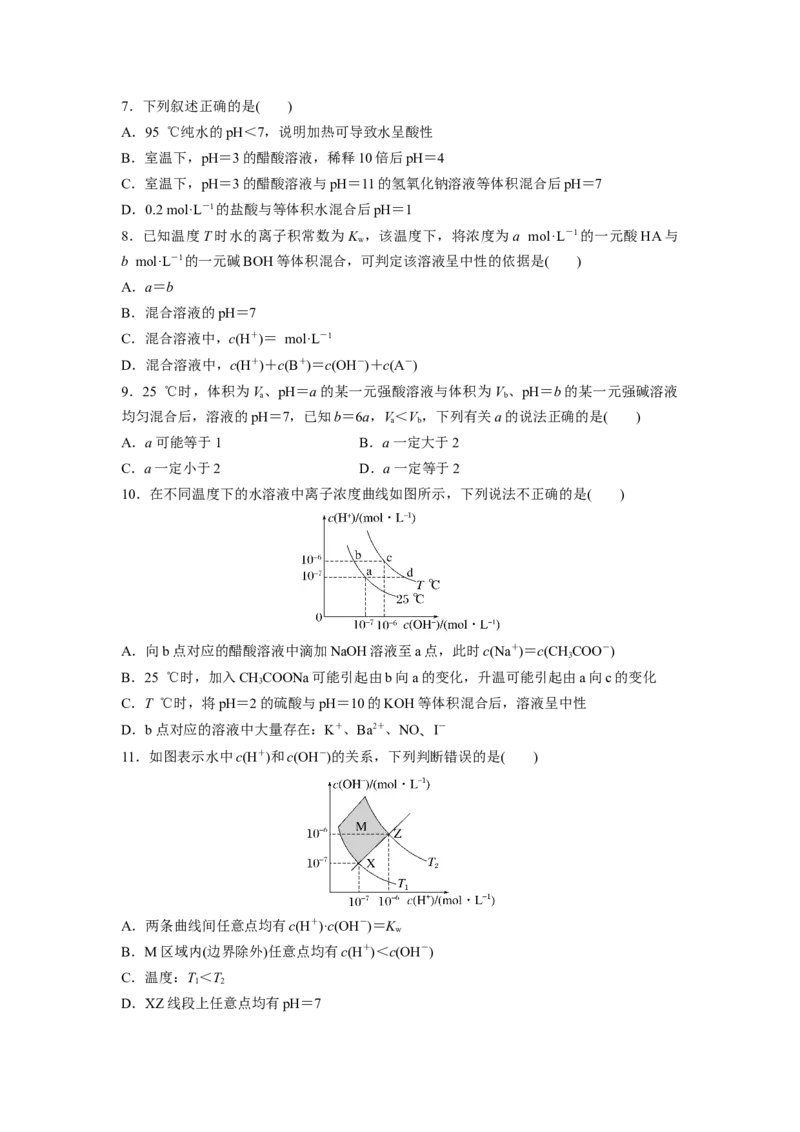
10.在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是( )
A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CHCOO-)
3
B.25 ℃时,加入CHCOONa可能引起由b向a的变化,升温可能引起由a向c的变化
3
C.T ℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液呈中性
D.b点对应的溶液中大量存在:K+、Ba2+、NO、I-
11.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A.两条曲线间任意点均有c(H+)·c(OH-)=K
w
B.M区域内(边界除外)任意点均有c(H+)<c(OH-)
C.温度:T<T
1 2
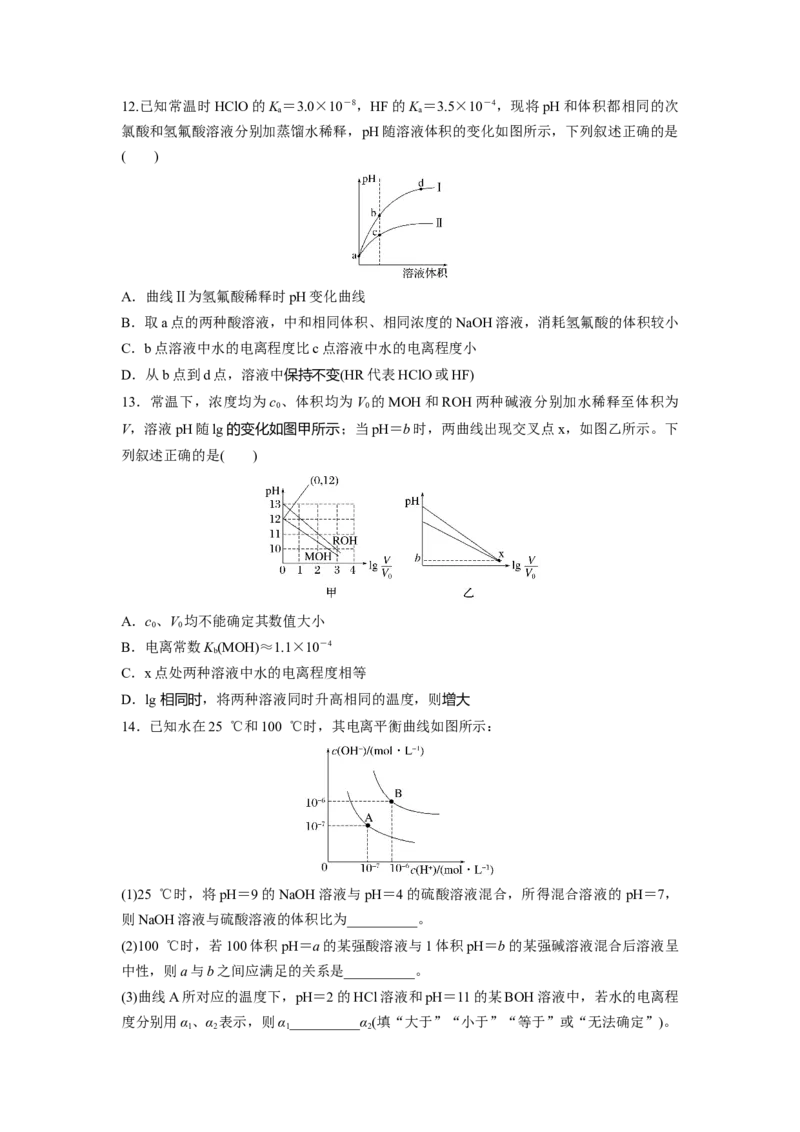
D.XZ线段上任意点均有pH=712.已知常温时HClO的K=3.0×10-8,HF的K=3.5×10-4,现将pH和体积都相同的次
a a
氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是
( )
A.曲线Ⅱ为氢氟酸稀释时pH变化曲线
B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小
C.b点溶液中水的电离程度比c点溶液中水的电离程度小
D.从b点到d点,溶液中保持不变(HR代表HClO或HF)
13.常温下,浓度均为c 、体积均为V 的MOH和ROH两种碱液分别加水稀释至体积为
0 0
V,溶液pH随lg 的变化如图甲所示;当pH=b时,两曲线出现交叉点x,如图乙所示。下
列叙述正确的是( )
A.c、V 均不能确定其数值大小
0 0
B.电离常数K (MOH)≈1.1×10-4
b
C.x点处两种溶液中水的电离程度相等
D.lg 相同时,将两种溶液同时升高相同的温度,则增大
14.已知水在25 ℃和100 ℃时,其电离平衡曲线如图所示:
(1)25 ℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,
则NaOH溶液与硫酸溶液的体积比为__________。
(2)100 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈
中性,则a与b之间应满足的关系是__________。
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程
度分别用α、α 表示,则α__________α(填“大于”“小于”“等于”或“无法确定”)。
1 2 1 2(4)曲线B对应的温度下,将0.02 mol·L-1 Ba(OH) 溶液与等物质的量浓度的NaHSO 溶液
2 4
等体积混合后,混合溶液的pH=________。