文档内容
第 51 讲 弱电解质的电离平衡
[复习目标] 1.理解弱电解质在水溶液中的电离平衡。2.理解电离常数的含义,掌握电离常
数的应用并能进行相关计算。
考点一 弱电解质的电离平衡及影响因素
1.电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速
率相等时,电离过程达到了平衡。
平衡建立过程如图所示:
2.电离平衡的特征
3.外因对电离平衡的影响
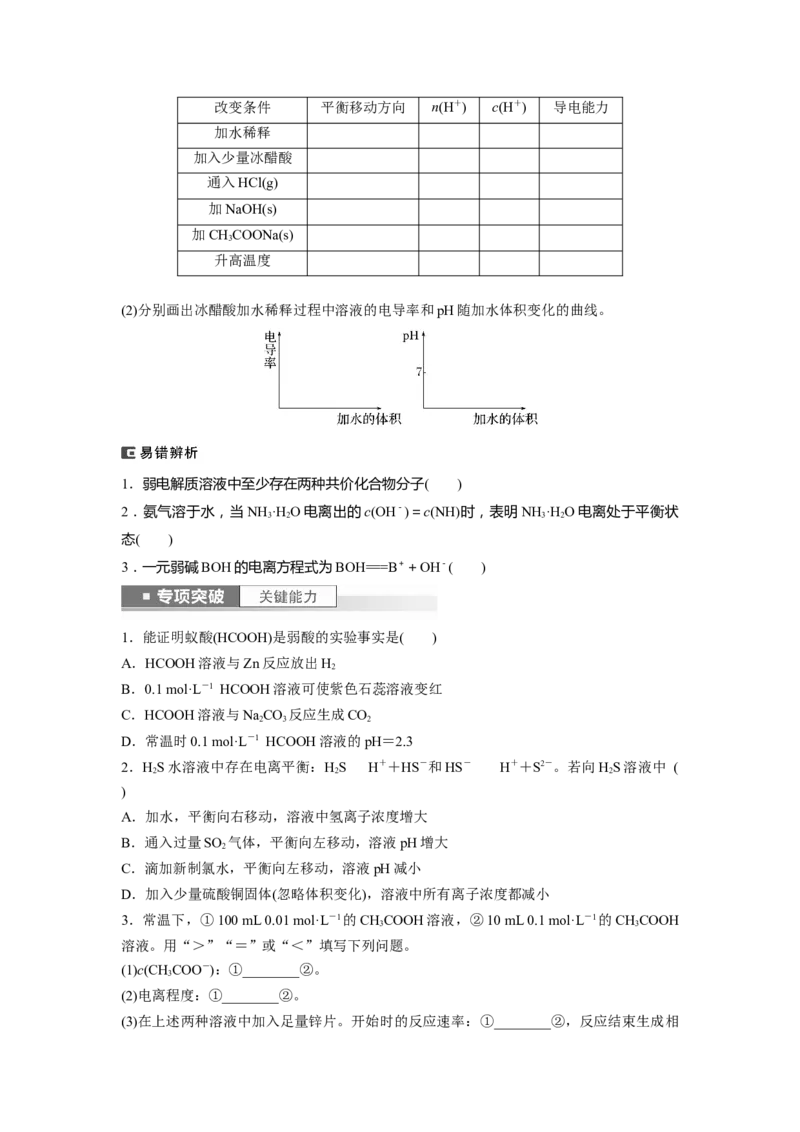
(1)以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOH(aq)CHCOO-(aq)+
3 3 3
H+(aq) ΔH>0的影响。改变条件 平衡移动方向 n(H+) c(H+) 导电能力
加水稀释
加入少量冰醋酸
通入HCl(g)
加NaOH(s)
加CHCOONa(s)
3
升高温度
(2)分别画出冰醋酸加水稀释过程中溶液的电导率和pH随加水体积变化的曲线。
1.弱电解质溶液中至少存在两种共价化合物分子( )
2.氨气溶于水,当NH ·H O电离出的c(OH-)=c(NH)时,表明NH ·H O电离处于平衡状
3 2 3 2
态( )
3.一元弱碱BOH的电离方程式为BOH===B++OH-( )
1.能证明蚁酸(HCOOH)是弱酸的实验事实是( )
A.HCOOH溶液与Zn反应放出H
2
B.0.1 mol·L-1 HCOOH溶液可使紫色石蕊溶液变红
C.HCOOH溶液与NaCO 反应生成CO
2 3 2
D.常温时0.1 mol·L-1 HCOOH溶液的pH=2.3
2.HS水溶液中存在电离平衡:HSH++HS-和HS-H++S2-。若向HS溶液中 (
2 2 2
)
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO 气体,平衡向左移动,溶液pH增大
2
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
3.常温下,①100 mL 0.01 mol·L-1的CHCOOH溶液,②10 mL 0.1 mol·L-1的CHCOOH
3 3
溶液。用“>”“=”或“<”填写下列问题。
(1)c(CHCOO-):①________②。
3
(2)电离程度:①________②。
(3)在上述两种溶液中加入足量锌片。开始时的反应速率:①________②,反应结束生成相同状况下H 的体积:①________②。
2
(4)与同浓度的NaOH溶液完全反应消耗NaOH溶液的体积:①________②。
考点二 电离平衡常数及应用
1.概念
在一定条件下,弱电解质达到电离平衡时,溶液中电离所生成的各种离子浓度(幂次方)的
乘积与溶液中未电离的分子浓度的比值是一个常数,这个常数叫做电离平衡常数,简称电
离常数,用K(弱酸用K,弱碱用K )表示。
a b
2.表达式
一元弱酸HA 一元弱碱BOH
电离方程式 HAH++A- BOHB++OH-
电离常数表达式 K= K =
a b
3.特点
(1)电离平衡常数与温度有关,与浓度无关,升高温度,K增大。
(2)电离平衡常数反映弱电解质的相对强弱,K越大,表示弱电解质越易电离,酸性或碱性
越强。
(3)多元弱酸的各步电离常数的大小关系是K >K >K ……,当K ≫K 时,计算多元弱酸
a1 a2 a3 a1 a2
中的c(H+)或比较多元弱酸酸性的相对强弱时,通常只考虑第一步电离。
4.电离度
(1)概念
在一定条件下的弱电解质达到电离平衡时,已经电离的电解质分子数占原电解质分子总数
的百分比。
(2)表示方法
α=×100%,也可表示为α=×100%。
(3)影响因素
①相同温度下,同一弱电解质,浓度越大,其电离度(α)越____。
②相同浓度下,同一弱电解质,温度越高,其电离度(α)越____。
1.同一弱电解质,浓度不同其电离常数一定不同( )
2.弱电解质的电离平衡右移,电离常数一定增大( )
3.某一弱电解质,电离度越大,电离常数就越大( )4.常温下,依据K (H CO)>K (H PO ),可知碳酸的酸性比磷酸强( )
a1 2 3 a2 3 3
一、利用电离常数判断弱电解质(酸碱性)的相对强弱
1.部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HS HCO HClO
2 2 3
电离平衡 K =1.1×10-7 K =4.5×10-7
a1 a1
K=1.77×10-4 K=4.0×10-8
a a
常数(25℃) K =1.3×10-13 K =4.7×10-11
a2 a2
按要求回答下列问题:
(1)HCOOH、HS、HCO、HClO的酸性由强到弱的顺序为_____________________。
2 2 3
(2)相同浓度的HCOO-、HS-、S2-、HCO、CO、ClO-结合H+的能力由强到弱的顺序为
________________________________________________________________________。
(3)运用上述电离常数及物质的特性判断下列化学方程式不正确的是________(填序号)。
①次氯酸与NaHCO 溶液的反应:HClO+HCO===ClO-+HO+CO↑
3 2 2
②少量CO 通入NaClO溶液中:CO+HO+2ClO-===CO+2HClO
2 2 2
③少量CO 通入NaClO溶液中:CO+HO+ClO-===HCO+HClO
2 2 2
④硫化氢通入NaClO溶液中:HS+ClO-===HS-+HClO
2
⑤碳酸钠滴入足量甲酸溶液中:2HCOOH+CO===2HCOO-+CO↑+HO
2 2
二、判断微粒浓度比值的大小
2.常温下,将0.1 mol·L-1的CHCOOH溶液加水稀释,请填写下列表达式中的数据变化
3
情况(填“变大”“变小”或“不变”)。
(1)________;
(2)________;
(3)________;
(4)________;
(5)________。
判断溶液中微粒浓度比值的三种方法
(1)将浓度之比转化为物质的量之比进行比较,这样分析起来可以忽略溶液体积的变化,只
需分析微粒数目的变化即可。
(2)“假设法”,如上述问题(3),假设无限稀释,c(CHCOO-)趋近于0,c(H+)趋于10-
3
7mol·L-1,故比值变小。
(3)“凑常数”,解题时将某些粒子的浓度比值乘以或除以某种粒子的浓度,转化为一个常
数与某种粒子浓度的乘积或相除的关系。1.(2020·北京,11)室温下,对于1 L 0.1 mol·L-1醋酸溶液。下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为6.02×1022
3
B.加入少量CHCOONa固体后,溶液的pH降低
3
C.滴加NaOH溶液过程中,n(CHCOO-)与n(CHCOOH)之和始终为0.1 mol
3 3
D.与NaCO 溶液反应的离子方程式为CO+2H+===HO+CO↑
2 3 2 2
2.(2022·全国乙卷,13)常温下,一元酸HA的K(HA)=1.0×10-3。在某体系中,H+与A-
a
不能穿过隔膜,未电离的HA可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度[]为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
3.[2020·天津,16(5)节选]已知 25 ℃碳酸电离常数为 K 、K ,当溶液 pH=12 时,
a1 a2
c(H CO)∶c(HCO)∶c(CO)=1∶________∶__________________________________。
2 3