文档内容
1.下列说法正确的有( )
①不溶于水的盐都是弱电解质 ②可溶于水的盐都是强电解质 ③0.5 mol·L-1一元酸溶液
中H+浓度一定为0.5 mol·L-1 ④强酸溶液中的c(H+)不一定大于弱酸溶液中的c(H+) ⑤
电解质溶液导电的原因是溶液中有自由移动的阴、阳离子 ⑥熔融的电解质都能导电
A.1个 B.2个 C.3个 D.4个
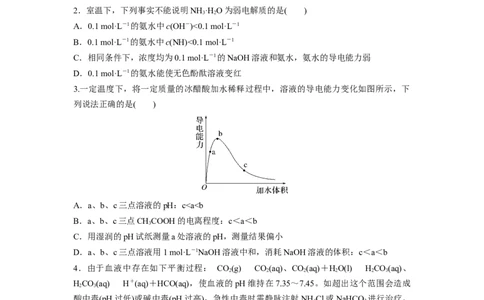
2.室温下,下列事实不能说明NH ·H O为弱电解质的是( )
3 2
A.0.1 mol·L-1的氨水中c(OH-)<0.1 mol·L-1
B.0.1 mol·L-1的氨水中c(NH)<0.1 mol·L-1
C.相同条件下,浓度均为0.1 mol·L-1的NaOH溶液和氨水,氨水的导电能力弱
D.0.1 mol·L-1的氨水能使无色酚酞溶液变红
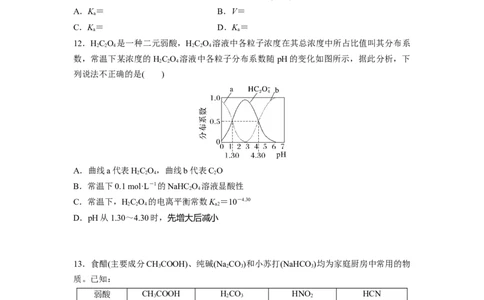
3.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下
列说法正确的是( )
A.a、b、c三点溶液的pH:c7
7.(2022·深圳模拟)硼酸(H BO)的电离方程式为HBO +HOB(OH)+H+。已知常温下,
3 3 3 3 2
K(H BO)=5.4×10-10、K(CHCOOH)=1.75×10-5。下列说法错误的是( )
a 3 3 a 3
A.HBO 为一元酸
3 3
B.0.01 mol·L-1 HBO 溶液的pH≈6
3 3
C.常温下,等浓度溶液的pH:CHCOONa>NaB(OH)
3 4
D.NaOH溶液溅到皮肤时,可用大量水冲洗,再涂上硼酸溶液
8.将浓度为0.1 mol·L-1 HF溶液加水稀释,下列各量增大的是( )
①c(H+) ②c(F-) ③c(OH-) ④K(HF) ⑤K ⑥ ⑦
a w
A.①⑥ B.②④ C.③⑦ D.④⑤
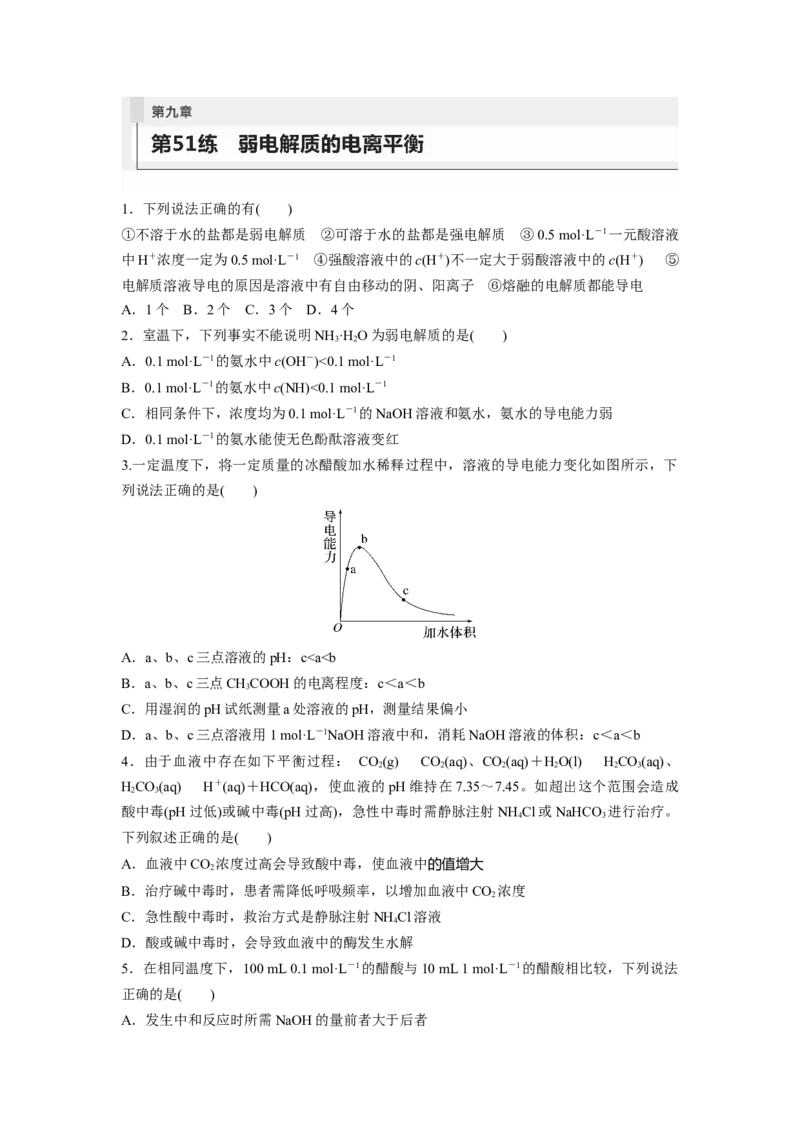
9.(2023·南京模拟)常温下,次氯酸电离平衡体系中各成分的组成分数 δ[δ(X)=,X为
HClO或ClO-]与pH的关系如图所示。下列有关说法正确的是( )
A.次氯酸的电离方程式为HClO===H++ClO-
B.曲线a、b依次表示δ(ClO-)、δ(HClO)的变化
C.次氯酸电离常数K 的数量级为10-7
a
D.向次氯酸溶液中加NaOH溶液,将减小
10.现有HX、HY和HZ三种酸,各酸及其盐之间不发生氧化还原反应,它们的电离常
2 2
数如表所示。
酸 电离常数(25 ℃)
HX K=10-9.2
a
HY K =10-6.4 K =10-10.3
2 a1 a2
HZ K =10-1.9 K =10-7.2
2 a1 a2下列说法正确的是( )
A.在水溶液中结合H+的能力:Y2-