文档内容
第 52 讲 水的电离和溶液的 pH
[复习目标] 1.了解水的电离、离子积常数(K )。2.了解溶液pH的含义及其测定方法,能进
w
行pH的简单计算。
考点一 水的电离与水的离子积常数
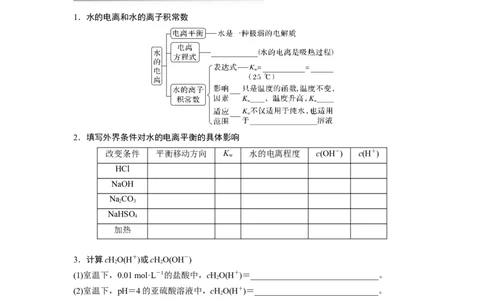
1.水的电离和水的离子积常数
2.填写外界条件对水的电离平衡的具体影响
改变条件 平衡移动方向 K 水的电离程度 c(OH-) c(H+)
w
HCl
NaOH
NaCO
2 3
NaHSO
4
加热
3.计算cHO(H+)或cHO(OH-)
2 2
(1)室温下,0.01 mol·L-1的盐酸中,cHO(H+)=______________________________。
2
(2)室温下,pH=4的亚硫酸溶液中,cHO(H+)=_____________________________。
2
(3)室温下,pH=10的KOH溶液中,cHO(OH-)=___________________________。
2
(4)室温下,pH=4的NH Cl溶液中,cHO(H+)=_____________________________。
4 2
(5)室温下,pH=10的CHCOONa溶液中,cHO(OH-)=____________。
3 2
溶液中 (H+)或 (OH-)的计算及应用(以室温为例)
(1)酸、碱抑制水的电离,酸溶液中求c(OH-),即 (H+)= (OH-)=c(OH-),碱溶液
中求c(H+),即 (OH-)= (H+)=c(H+)。(2)水解的盐促进水的电离,故 (H+)等于显性离子的浓度。
(3)酸式盐溶液
酸式酸根以电离为主: (H+)= (OH-)=c(OH-)。
酸式酸根以水解为主: (H+)= (OH-)=c(OH-)。
1.任何水溶液中均存在H+和OH-,且水电离出的c(H+)和c(OH-)相等( )
2. 将水加热,K 和c(H+) 均增大( )
w
3.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同( )
3 4
4.温度一定时,在纯水中通入少量SO ,水的电离平衡不移动,K 不变( )
2 w
1.某温度下,向c(H+)=1.0×10-6 mol·L-1的蒸馏水中加入NaHSO 晶体,保持温度不变,
4
测得溶液的c(H+)=1.0×10-2 mol·L-1。下列对该溶液的叙述不正确的是( )
A.该温度高于25 ℃
B.由水电离出来的H+的浓度为1.0×10-10 mol·L-1
C.加入NaHSO 晶体抑制水的电离
4
D.取该溶液加水稀释100倍,溶液中的c(OH-)减小
2.常温时,纯水中由水电离出的c(H+)=a mol·L-1,pH=1的盐酸中由水电离出的c(H+)
=b mol·L-1,0.1 mol·L-1的盐酸与0.1 mol·L-1的氨水等体积混合后,由水电离出的c(H+)
=c mol·L-1,则a、b、c的关系正确的是( )
A.a>b=c B.c>a>b
C.c>b>a D.b>c>a
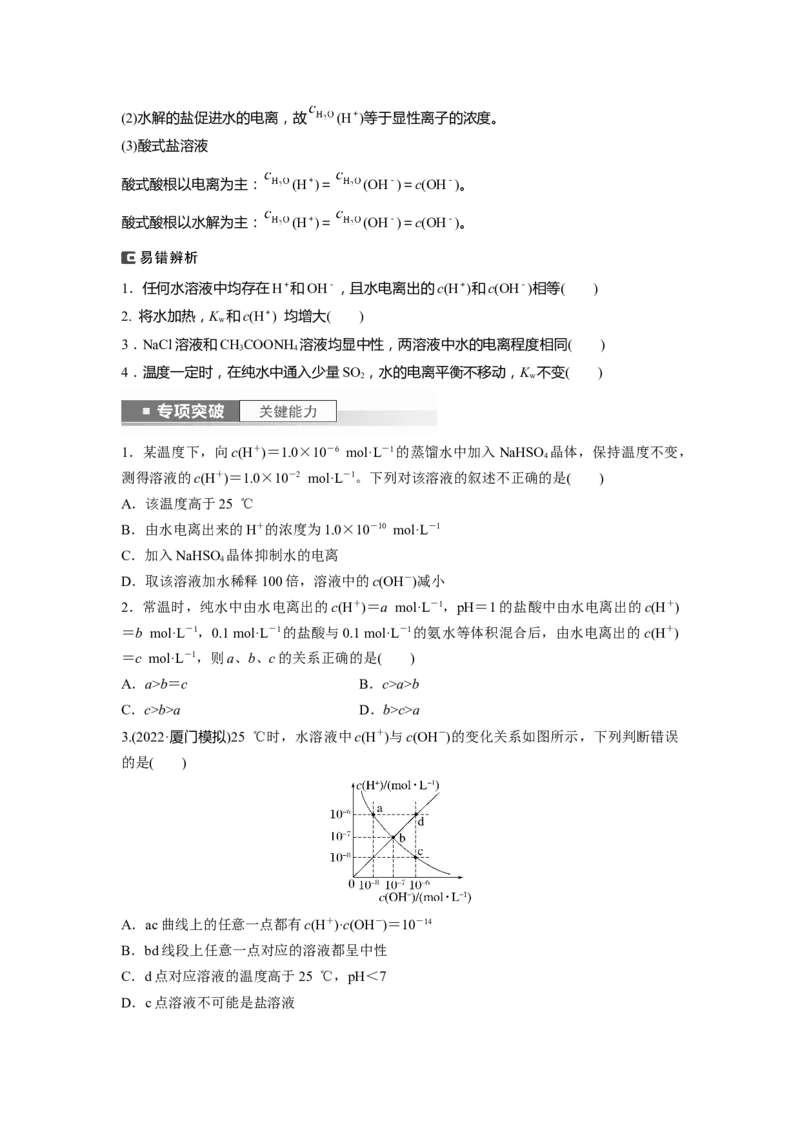
3.(2022·厦门模拟)25 ℃时,水溶液中c(H+)与c(OH-)的变化关系如图所示,下列判断错误
的是( )
A.ac曲线上的任意一点都有c(H+)·c(OH-)=10-14
B.bd线段上任意一点对应的溶液都呈中性
C.d点对应溶液的温度高于25 ℃,pH<7
D.c点溶液不可能是盐溶液4.水的电离平衡曲线如图所示,回答下列问题。
(1)图中A、B、C、D、E五点K 间的关系:__________________________。
w
(2)在水中加少量酸,可实现A点向____________点移动。
(3)ABE形成的区域中的点都呈现__________性。
(4)若在B点温度下,pH=2的硫酸溶液中,cHO(H+)=________ mol·L-1。
2
正确理解水的电离平衡曲线
(1)曲线上的任意点的K 都相同,即c(H+)·c(OH-)相同,温度相同。
w
(2)曲线外的任意点与曲线上任意点的K 不同,温度不同。
w
(3)实现曲线上点之间的转化需保持温度相同,改变酸碱性;实现曲线上点与曲线外点之间
的转化一定改变温度。
考点二 溶液的酸碱性与 pH
1.溶液的酸碱性
溶液呈酸碱性的本质:溶液的酸碱性取决于c(H+)和c(OH-)的相对大小
溶液的酸碱性 c(H+)与c(OH-)比较 常温下溶液pH
酸性溶液 c(H+)____c(OH-) ____7
中性溶液 c(H+)____c(OH-) ____7
碱性溶液 c(H+)____c(OH-) ____7
2.溶液的pH及测定方法
(1)关系:pH=________。
(2)范围:0~14。
(3)测定方法:用镊子夹取一小块试纸放在洁净的________或________上,用玻璃棒蘸取待
测液点在试纸的中央,变色后与____________对照。
(4)溶液酸碱性的另外一种表示——pOH
①pOH=________;
②常温下:pH+pOH=____。1.任何温度下,利用H+和OH-浓度的相对大小均可判断溶液的酸碱性( )
2.pH<7的溶液一定显酸性( )
3.c(H+)=的溶液一定显中性( )
4.常温下能使甲基橙显黄色的溶液一定显碱性( )
5.用pH试纸测得某氯水的pH为5( )
6.用湿润的pH试纸测定盐酸和醋酸溶液的pH,醋酸溶液的误差更大( )
一、酸碱溶液混合后酸碱性的判断
1.常温下,两种溶液混合后酸碱性的判断(在括号中填“酸性”“碱性”或“中性”)。
(1)相同浓度的HCl和NaOH溶液等体积混合( )
(2)相同浓度的CHCOOH和NaOH溶液等体积混合( )
3
(3)相同浓度的NH ·H O和HCl溶液等体积混合( )
3 2
(4)pH=2的HSO 和pH=12的NaOH溶液等体积混合( )
2 4
(5)pH=3的HCl和pH=10的NaOH溶液等体积混合( )
(6)pH=3的HCl和pH=12的NaOH溶液等体积混合( )
(7)pH=2的CHCOOH和pH=12的NaOH溶液等体积混合( )
3
(8)pH=2的HSO 和pH=12的NH ·H O等体积混合( )
2 4 3 2
酸碱溶液混合后酸碱性的判断规律
(1)等浓度等体积的一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”。
(2)室温下c (H+)=c (OH-),即pH之和等于14时,一强一弱等体积混合——“谁弱谁
酸 碱
过量,谁弱显谁性”。
(3)已知强酸和强碱的pH,等体积混合(25 ℃时):
①pH之和等于14,呈中性;
②pH之和小于14,呈酸性;
③pH之和大于14,呈碱性。
二、溶液pH的计算
2.常温下,下列关于溶液稀释的说法正确的是( )
A.pH=3的醋酸溶液稀释100倍,pH=5
B.pH=4的HSO 溶液加水稀释100倍,溶液中由水电离产生的c(H+)=1×10-6 mol·L-1
2 4
C.将1 L 0.1 mol·L-1的Ba(OH) 溶液稀释为2 L,pH=13
2
D.pH=8的NaOH溶液稀释100倍,其pH=63.计算25 ℃时下列溶液的pH。
(1)0.005 mol·L-1的HSO 溶液的pH=__________。
2 4
(2)0.001 mol·L-1的NaOH溶液的pH=____________。
(3)0.1 mol·L-1的NH ·H O溶液(NH ·H O的电离度α约为1%)的pH=________。
3 2 3 2
(4)将 pH=8 的 NaOH 溶液与 pH=10 的 NaOH 溶液等体积混合,混合溶液的 pH=
__________。
(5)0.015 mol·L-1的硫酸与 0.01 mol·L-1的 NaOH 溶液等体积混合,混合溶液的 pH=
________________________________________________________________________。
4.按要求计算下列各题(常温下,忽略溶液混合时体积的变化):
(1)25 ℃时,pH=3的硝酸和pH=12的氢氧化钡溶液按照体积比为 9∶1混合,混合溶液
的pH=________。
(2)在一定体积pH=12的Ba(OH) 溶液中,逐滴加入一定物质的量浓度的NaHSO 溶液,当
2 4
溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH) 溶液与
2
NaHSO 溶液的体积之和,则Ba(OH) 溶液与NaHSO 溶液的体积比是__________。
4 2 4
(3)将pH=a的NaOH溶液V L与pH=b的HCl溶液V L混合,若所得溶液呈中性,且a
a b
+b=13,则=__________。
混合溶液pH的计算思维模型
(1)两种强酸混合:直接求出c (H+),再据此求pHc (H+)=。
混 混
(2)两种强碱混合:先求出c (OH-),再根据K 求出c (H+),最后求pH
混 w 混
c (OH-)=。
混
(3)强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度
①若酸过量:
c (H+)=
混
②若碱过量:
c (OH-)=
混
最后根据pH=-lg c(H+),求pH。
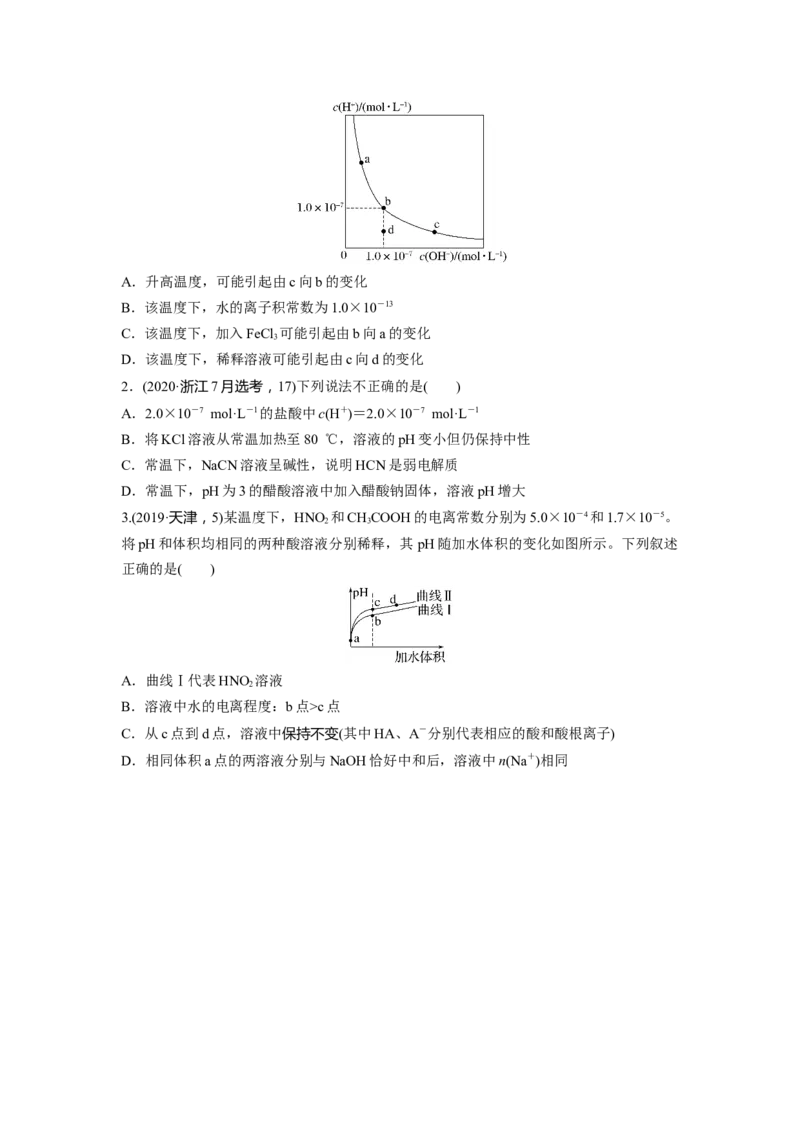
1.(2015·广东理综,11)一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法
正确的是( )A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
2.(2020·浙江7月选考,17)下列说法不正确的是( )
A.2.0×10-7 mol·L-1的盐酸中c(H+)=2.0×10-7 mol·L-1
B.将KCl溶液从常温加热至80 ℃,溶液的pH变小但仍保持中性
C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
3.(2019·天津,5)某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10-5。
2 3
将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述
正确的是( )
A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同