文档内容
第一章能力提升检测卷
完卷时间:90分钟
可能用到的相对原子质量:H 1 C 12 O16 Na 23 Al 27 P 31 S 32 Cl 35.5 K 39 Ca 40
Fe 56 Cu 64 Zn 65 As 75 Cd 112
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2021·河南郑州市·高三一模) N表示阿伏加德罗常数,下列说法正确的是
A
A. 的 溶液中含有 的数目为0.1 N
A
B.常温常压下, 和 的混合物中含有的电子数一定为N
A
C.常温常压下,31g白磷燃烧生成 时,断裂 键的数目为N
A
D. 晶体中阴、阳离子总数为0.3 N
A
【答案】B
【解析】A.铝离子为弱碱阳离子,在水溶液中部分水解,所以1L 0.1mol•L-1的AlCl 溶液中含有Al3+的
3
数目小于0.1N,故A错误;B.H18O和DO的相对分子质量均为20,常温常压下,2.0g H18O和DO的混合
A 2 2 2 2
物中含有的电子数一定为 ×10×Nmol-1=N,故B正确;C.31g白磷的物质的量为
A A
=0.25mol,而一个白磷分子中含6条P-P键,燃烧生成的 的结构为 ,燃烧后P-P键全部断
裂,0.25mol白磷中含1.5N条P-P键,因此断裂 键的数目为1.5N,故C错误;D.0.1mol NaHCO
A A 3
晶体中含有0.1mol钠离子和0.1mol碳酸氢根离子,阴、阳离子总数为0.2N,故D错误;故选B。
A
2.(2021·河北保定市·高三一模)设N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.铜与浓硝酸充分反应生成22.4L气体时转移电子数为N
A
B.4.6gNa完全与水反应,生成共价键0.1N
A
C.Al3++4OH-=[Al(OH)]-,说明1molAl(OH) 电离出H+数为N
4 3 A
D.101kPa、120℃时,7.8gCH 燃烧所得气体分子数一定为0.9N
6 6 A
【答案】D
【解析】A.生成气体所处的状态不明确,故气体的物质的量无法计算,则转移的电子数无法计算,故A错误;B.4.6gNa的物质的量为n(Na)= = =0.2mol,Na与水完全反应生成NaOH和H,即
2
2Na+2HO=2NaOH+H↑,产物NaOH中OH-存在一个共价键,H 中存在1个共价键,由于0.2molNa与水完全
2 2 2
反应生成0.2molNaOH和0.1molH,所以生成0.2N+0.1N=0.3N的共价键,故B错误;C.Al(OH) 的酸式电
2 A A A 3
离为Al(OH) H++ +HO,Al(OH) 为弱电解质,部分电离,不能完全电离,H+数目小于N,故C错
3 2 3 A
误;D.7.8gCH 的物质的量为n(CH)= = =0.1mol,120℃时HO为气体,燃烧产物为CO
6 6 6 6 2 2
或CO一种或两种及HO,根据元素守恒,碳的氧化物为0.6mol,HO为0.3mol,所得气体分子数为
2 2
0.6N+0.3N=0.9N,故D正确;答案为D。
A A A
3.(2021·浙江宁波市·高三二模)等量铝粉与等体积不同浓度 溶液(足量)反应,产生 的体
积(已换算成标准状况下)随时间变化如下表所示:
5 10 15 20
实验
Ⅰ 2016 3808 4032 4032
Ⅱ 1120 3136 3808 3920
注:实验Ⅰ为铝粉与 溶液反应;实验Ⅱ为铝粉与 溶液反应。下列
说法不正确的是
A.此反应是放热反应
B.实验Ⅰ中,至 时铝粉溶解
C. 时,生成 的速率:
D.实验Ⅱ中, 内,生成 的平均反应速率为
【答案】C
【解析】A.金属Al与NaOH溶液反应是放热反应,故A正确;B.实验Ⅰ中,至5min时2.016LH,所得H
2 2的物质的量为 =0.09mol,根据2Al+2NaOH+2HO=2NaAlO+3H↑可知溶解Al的物质的量为
2 2 2
0.6mol,故B正确;C.由实验数据可知10~15min时实验Ⅰ生成H 的总体积小于实验Ⅱ生成H 的总体积,
2 2
说明12.5min时生成H 的速率Ⅰ<Ⅱ,故C错误;D.实验Ⅱ中,15~20min时生成H 的体积为
2 2
3920mL-3808mL=112mL,则生成H 的平衡反应速率为 =22.4mL·min-1,故D正确;故答案为C。
2
4.(2020·北京高考真题)下列说法正确的是
A.同温同压下,O 和CO 的密度相同
2 2
B.质量相同的HO和DO(重水)所含的原子数相同
2 2
C.物质的量相同的CHCHOH和CHOCH 所含共价键数相同
3 2 3 3
D.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同
【答案】C
【详解】A.同温同压下,O 和CO 的体积相同时,其质量之比为32:44,则密度之比为32:44,不相同,
2 2
A说法错误;B.质量相同的HO和DO(重水)的物质的量之比为20:18,分子中均含有3个原子,则所含
2 2
的原子数之比为20:18,不相同,B说法错误;C.每个CHCHOH和CHOCH 中含共价键数均为8条,则物
3 2 3 3
质的量相同的CHCHOH和CHOCH 所含共价键数相同,C说法正确;D.室温下,pH相同的盐酸和硫酸中,
3 2 3 3
氢离子的浓度相等,硫酸能电离出2个氢离子,而盐酸只能电离出一个,故pH相同的盐酸和硫酸的物质的
量浓度不相同,D说法错误;答案为C。
5.(2021·山西临汾市·高三一模)设 为阿伏加德罗常数的值。捕获 生成甲酸的过程如图所示。
下列说法错误的是
A. 中所含的共价键数目为B.标准状况下, 中所含的质子数目为
C. 乙基所含的电子总数为
D. 的甲酸水溶液中所含的氧原子数目为
【答案】C
【解析】A. 的摩尔质量为101g/mol, 的物质的量为0.1mol,一个
分子含有21根共价键,则 中所含的共价键数目为 ,A正确;B. 标准
状况下, 的物质的量为1mol,1个 分子含有22个质子,则 中所含的质子数
目为 ,B正确;C. 乙基不带电,乙基的电子数就是C原子和O原子的电子数之和,则 乙基所
含的电子总数为 ,C错误;D. 的甲酸水溶液中含有 和 ,共含氧
原子数目为 ,D正确;故选C。
6.(2021·厦门英才学校高三月考)下列各组微粒数目一定相等的是
A.等体积的NO和 的N原子数目
B.等质量的正丁烷和异丁烷的C-H键数目
C.等物质的量浓度的KCl溶液和NaCl溶液的 离子数目
D.等质量的Cu分别与足量浓 、稀 反应生成的气体分子数目
【答案】B
【解析】A.等体积的NO和 ,状态不清楚,根据 ,其中 不确定,所以物质的量不一定相等,故A错误;B.正丁烷和异丁烷互为同分异构,质量相等,根据 ,其物质的量相等,C—H键数目相
等,故B正确;C.两物质的浓度相等,但体积未知,根据 ,无法进行计算,两物质的物质的量不
一定相等,故C错误;D.浓硝酸和稀硝酸的还原产物不相同,浓硝酸的还原产物为 ,其关系为
;稀硝酸的还原产物为 ,所以等质量的Cu与之反应产生的气体的物质的量不相
等,故D错误;故选B。
7.(2021·陕西西安市·高三一模)锌镉渣是生产立德粉(硫化锌和硫酸钡的混合物)的废渣,其主要成
分为锌、镉、锰、铁及其氧化物等,如图所示为从锌镉渣中获得金属镉的工艺流程:
已知:镉(Cd)的金属活动性介于锌、铁之间。下列说法错误的是
A.“浸取”步骤所用的1L0.1mol/L的硫酸中,氧原子的数目大于0.4N
A
B.“氧化”步骤的目的是将Fe2+氧化为Fe3+,同时将Mn2+氧化为MnO 除去
2
C.“氧化”步骤加入氧化镉的目的是调pH,除去杂质元素
D.“电解”步骤中,阴极生成11.2g金属镉时,阳极生成气体的体积为1.12L
【答案】D
【解析】锌镉渣是生产立德粉(硫化锌和硫酸钡的混合物)的废渣,其主要成分为锌、镉、锰、铁及其氧化
物等,加入稀硫酸进行酸浸浸取,金属及其氧化物与硫酸反应得到含有Zn2+、Cd2+、Mn2+、Fe2+、Fe3+的溶液,
过滤掉不溶性杂质,向滤液中加入锌单质发生置换反应,Cd2+、Mn2+、Fe2+、Fe3+全部转化为单质,过滤后的
滤液1中主要为ZnSO,海绵镉的主要成分为Zn、Mn、Fe,再向海绵镉中加入稀硫酸溶解,Zn、Mn、Fe又
4
转化为Cd2+、Mn2+、Fe2+,再加入高锰酸钾,酸性条件下将Fe2+氧化为Fe3+,Mn2+氧化为MnO,再加入氧化镉,
2
调节溶液pH值,将Fe3+转化为Fe(OH),过滤后,滤渣2的主要成分为MnO、Fe(OH),得到的滤液中主要
3 2 3
含有CdSO,最后对溶液通电电解制得金属镉。
4
A.“浸取”步骤所用的1L0.1mol/L的硫酸中硫酸的物质的量为0.1mol,硫酸溶液中含有水,也含有氧原子,则氧原子的数目大于0.4N,故A正确;B.根据分析,“氧化”步骤的目的是将Fe2+氧化为Fe3+,同时
A
将Mn2+氧化为MnO 除去,故B正确;C.根据分析,“氧化”步骤加入氧化镉的目的是调pH,将Fe3+转化为
2
Fe(OH) 除去,故C正确;D.“电解”步骤中,阴极生成11.2g金属镉,即生成0.1mol金属镉时,转移
3
0.2mol电子,阳极上电解水生成氧气和氢离子,电极反应为:2HO-4e-=O↑+4H+,生成0.05mol氧气,标
2 2
况下气体的体积为0.05mol×22.4L/mol=1.12L,题中未说明气体的状态条件,无法用标况下气体摩尔体积
计算,故D错误;答案选D。
8.(2021·福建厦门市·高三一模)Al遇到极稀的硝酸发生反应生成NHNO,其反应为
4 3
。设N为阿伏加德罗常数的值。下列说法正确的是
A
A.将0.2mol NHNO 溶于稀氨水中使溶液呈中性,溶液中 的数目小于0.2N
4 3 A
B.1L0.1mol/L Al(NO) 溶液中,阳离子的数目为0.1N
3 3 A
C.1.0g由H18O与DO组成的混合物中所含有的中子总数为0.5N
2 2 A
D.反应中每消耗2.7g金属Al,转移的电子数为3N
A
【答案】C
【解析】A.溶液中存在电荷守恒n(H+)+n( )=n(OH-)+n(NO ),溶液呈中性所以n(H+)=n(OH-),所以n(
)=n(NO )=0.2mol,即溶液中 的数目为0.2N,A错误;B.1L0.1mol/L Al(NO) 溶液中含有
A 3 3
0.1molAl(NO),溶液中存在Al3+的水解Al3++3HO Al(OH)+3H+,水解使阳离子数目增多,所以溶液中阳
3 3 2 3
离子的数目大于0.1N,B错误;C.H18O与DO的摩尔质量均为20g/mol,所以1.0g由H18O与DO组成的
A 2 2 2 2
混合物中含有0.05mol分子,一个H18O与DO分子中均含有10个中子,所以中子总数为0.5N,C正确;
2 2 A
D.该反应中Al为唯一还原剂,2.7g铝的物质的量为0.1mol,被氧化时转移0.3mol电子,D错误;综上所
述答案为C。
9.(2021·上海南汇中学高三月考)改变温度不影响
A.物质的摩尔质量 B.水的离子积
C.气体摩尔体积 D.化学平衡常数
【答案】A
【解析】A.单位物质的量的物质具有的质量为物质的摩尔质量,与温度无关,改变温度摩尔质量不变,
故A符合题意;B.升高温度促进水的电离,水电离出的氢离子和氢氧根离子浓度增大,根据
K=c(H+)c(OH-),水的离子积增大,则改变温度,影响水的离子积大小,故B不符合题意;C.气体摩尔体
w积为单位物质的量的气体所占的体积,数值的大小决定于气体所处的温度和压强。其它条件不变,改变温
度,气体摩尔体积数值一定变化,故C不符合题意;D.在一定温度下,当一个可逆反应达到平衡状态时,
各生成物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次幂的乘积的比值是个常数,这个常
数即为化学平衡常数,平衡常数只与温度有关,温度改变,平衡常数一定改变,故D不符合题意;答案选
A。
10.(2020·福建莆田市·高三一模)已知: 、锌和稀硫酸反应会生成 、硫酸锌和水。现将
含 的试样和锌、稀硫酸混合恰好完全反应,将生成的 缓慢通过热玻璃管中, 完
全分解冷却后得到 固体。下列有关说法错误的是
A.试样中 的质量分数为
B.参与反应的锌失去电子的物质的量为
C.分解产生的氢气在标准状况下体积为
D.若硫酸的物质的量浓度为 ,则消耗稀硫酸的体积为
【答案】B
【解析】根据已知,AsO、锌和稀硫酸反应的方程式为AsO+6Zn+6HSO=2AsH+6ZnSO+3HO,AsH 分解的
2 3 2 3 2 4 3 4 2 3
方程式为2AsH 2As+3H↑,AsH 后得到3mgAs,则4.0mg试样中含AsO 的质量为 ×3mg=3.96mg,
3 2 3 2 3
n(AsO)= =2 10-5mol。
2 3
A.根据以上分析,试样中AsO 的质量分数为 100%=99%,故A正确;B.反应中As元素化合价
2 3
由AsO 中+3价降低为AsH 中-3价,Zn中锌元素化合价由0价升高为+2价,根据得失电子守恒,锌失去电
2 3 3子的物质的量为2 10-5 2 6=2.4 10-4mol,故B错误;C.由方程式2AsH 2As+3H↑可知,生成氢气的
3 2
物质的量为2 10-5mol 2 =6 10-5mol,在标准状况下体积为6 10-5mol 22.4L/
mol=0.001344L=1.344mL,故C正确;D.由方程式AsO+6Zn+6HSO=2AsH+6ZnSO+3HO可知,消耗硫酸的
2 3 2 4 3 4 2
物质的量为2 10-5mol =1.2 10-4mol,则消耗稀硫酸的体积为 =10-3L=1mL,故D正确;答
案选B。
11.(2021·上海崇明区·高三一模)由H、Cl、O 组成的混合气体,在一定条件下恰好完全反应生成盐
2 2 2
酸(无气体剩余)则原混合气体中H,Cl,O 的物质的量之比可能是
2 2 2
A.3:2:1 B.6:1:2 C.5:3:1 D.7:4:1
【答案】C
【解析】物质间的反应分别为:2H+O 2HO、H+Cl 2HCl,一定条件下恰好完全反应生成盐酸,
2 2 2 2 2
说明这三种气体都没有剩余,设氢气的物质的量xmol,氯气的物质的量ymol,氧气的物质的量zmol,氢
气和氯气反应后,剩下氢气(x-y)和氧气(z)恰好反应的比例为2:1,(x-y):z=2:1,
A.如果H、Cl、O 的体积比为3:2:1,则(x-y):z=(3-2):1=1:1,不符合,故A错误;B.如果
2 2 2
H、Cl、O 的体积比为6:1:2,则(x-y):z=(6-1):2=5:2,不符合,故B错误;C.如果H、Cl、
2 2 2 2 2
O 的体积比为5:3:1,则(x-y):z=(5-3):1=2:1,符合条件,故C正确;D.如果H、Cl、O 的体
2 2 2 2
积比为7:4:1,则(x-y):z=(7-4):1=3:1,不符合,故D错误;故选C。
12.(2020·江西南昌市·南昌十中高一月考)将a g氯酸钾(M=122.5)充分加热分解(同时加入少量
MnO),得到b L气体,残留物充分溶解后所得溶液中共有c个溶质离子。则阿伏加德罗常数(N)一定可
2 A
表示为
A. B. C. D.
【答案】D
【解析】氯酸钾分解生成氯化钾和氧气,二氧化锰是催化剂且不溶于水,所以溶液中的溶质是氯化钾;氧气的体积不一定是在标准状况下,因此不能确定氧气的物质的量;氯酸钾的物质的量是 mol,根据氯
原子守恒可知,生成物氯化钾的物质的量也是 mol,残留物充分溶解后所得溶液中共有c个溶质离子,
所以N(KCl)=0.5c;则根据n= 可知,N= = = ,答案选D。
A
13.(2020·广东广州市·高三开学考试)海水提溴过程中发生反应:3Br +6NaCO +3HO =5NaBr
2 2 3 2
+NaBrO +6NaHCO,下列说法正确的是
3 3
A.标准状况下 2 mol HO的体积约为 44.8 L
2
B.1L 0.1 mol·L− 1NaCO 溶液中 CO2−的物质的量为 0.1 mol
2 3 3
C.反应中消耗 3 mol Br 转移的电子数约为 5×6.02×1023
2
D.反应中氧化产物和还原产物的物质的量之比为 5∶1
【答案】C
【解析】反应3Br +6NaCO +3HO =5NaBr +NaBrO +6NaHCO 中,Br 一部分被还原成NaBr,一部分被氧化
2 2 3 2 3 3 2
成NaBrO,Br 既是氧化剂又是还原剂。
3 2
A.标准状况下HO不是气体,不能用22.4L/mol计算2mol水的体积,A错误;B.CO2-在溶液中会水解,
2 3
导致其物质的量小于0.1mol,B错误;C.每消耗3 mol Br,其中有0.5 mol Br 被氧化成NaBrO,有2.5
2 2 3
mol Br 被还原成NaBr,整个过程中转移电子的物质的量为5 mol,数目约为 5×6.02×1023,C正确;D.
2
氧化产物是NaBrO,还原产物是NaBr,由化学计量数可知氧化产物与还原产物物质的量之比为1:5,D错
3
误;答案选C。
14.清末成书的《化学鉴原》中有一段描述:“各原质(元素)化合所用之数名曰‘分剂数’。养气(氧
气)以八分为一分剂(即分剂数为八),……一分剂轻气(氢气)为一,……并之即水,一分剂为九”。
其中与“分剂数”一词最接近的现代化学概念是( )
A.摩尔质量 B.物质的量 C.化合价 D.质量分数
【答案】A
【解析】根据“各原质(元素)化合所用之数名曰‘分剂数’”。氧气八分为一分剂,氢气一分为一分剂,
水九分为一分剂,则氧气的分剂数为八,氢气的分剂数为一,水的分剂数为九,即8份氧气与一份氢气化合生成九份水,满足O+2H=2HO中的质量守恒,因此与“分剂数”一词最接近的现代化学概念为摩尔质量,
2 2 2
故选A。
15.(2020·海南高三一模)多硫化钙可用于防治农作物、果树的白粉病、锈病等病害。CaS 中钙硫质量
x
比为5:16,则CaS 可表示为( )
x
A.CaS B.CaS C.CaS D.CaS
2 3 4
【答案】D
【解析】CaS 中钙硫质量比为5:16,根据元素的质量比等于元素的相对原子质量和原子的个数乘积之比,
x
可以得到40:32x=5:16,解得x=4,CaS 可表示为CaS,答案选D。
x 4
16.(2020·天水市第一中学高三模拟)下列说法不正确的是( )
A.把7.2g纯铁粉加入40mL浓度未知的HNO 溶液中,充分反应后剩余固体1.6g,产生NO 和NO的混合气
3 2
体0.08mol,若不考虑NO 的存在,则原HNO 溶液的物质的量浓度为7.0mol/L
2 4 3
B.将质量分数为a%,物质的量浓度为cmol/L的稀HSO 溶液蒸发掉一定量的水,使之质量分数为2a%,
1 2 4
此时物质的量浓度为cmol/L,则c和c的数值关系是c>2c
2 1 2 2 1
C.将标准状况下的aLHCl气体溶于1000mL水中,得到的盐酸溶液密度为bg/mL,则该盐酸溶液的物质的
量浓度为 mol/L
D.VLFe(SO) 溶液中含Fe3+mg,则溶液中 的物质的量浓度为 mol/L
2 4 3
【答案】C
【解析】A.把7.2g纯铁粉投入到40mL某HNO 溶液中,充分反应后剩余固体1.6g,说明生成硝酸亚铁,
3
硝酸完全反应,参加反应的Fe的质量为:m(Fe)=7.2g−1.6g=5.6g,其物质的量为:n(Fe)=
=0.1mol,则生成硝酸亚铁的物质的量为:n[Fe(NO)]=n (Fe)=0.1mol,
3 2
反应中硝酸起氧化剂、酸性作用,起酸性作用的硝酸生成硝酸亚铁,起氧化剂作用的硝酸生成NO和NO,
2
根据N元素守恒可知该硝酸溶液中含有硝酸的总物质的量为:
n(HNO)=2n[Fe(NO)]+n(NO+NO)=0.1mol×2+0.08mol=0.28mol,所以原HNO 溶液的物质的量浓度为:
3 3 2 2 3c(HNO)= =7.0mol/L,故A正确;B.设将溶质质量分数为a%的硫酸溶液密度为ρ,则
3 1
mol/L= mol/L,设将溶质质量分数为2a%的硫酸溶液密度为ρ,则
2
mol/L= mol/L,所以c:c= mol/L: mol/L =ρ:2ρ,即 ,硫酸溶液的浓
1 2 1 2
度越大密度也越大,所以ρ>ρ 所以 >2,即c>2c,故B正确;C.标况下,aLHCl溶于1000mL
2 1, 2 1
水中,所得溶液中n(HCl)= mol,溶液体积为V=
L,因此则该盐酸溶液的物质的量浓度
mol/L,故C错误;D.VL Fe(SO) 溶液中含Fe3+mg,则溶液中
2 4 3
mol/L,由Fe(SO) 化学式以及其在水中会发生完全电离可知, 浓度
2 4 3
为Fe3+浓度1.5倍,则溶液中 的物质的量浓度为 × mo1/L = mo1/L,故D正确;答案选C。
二、主观题(共5小题,共52分)
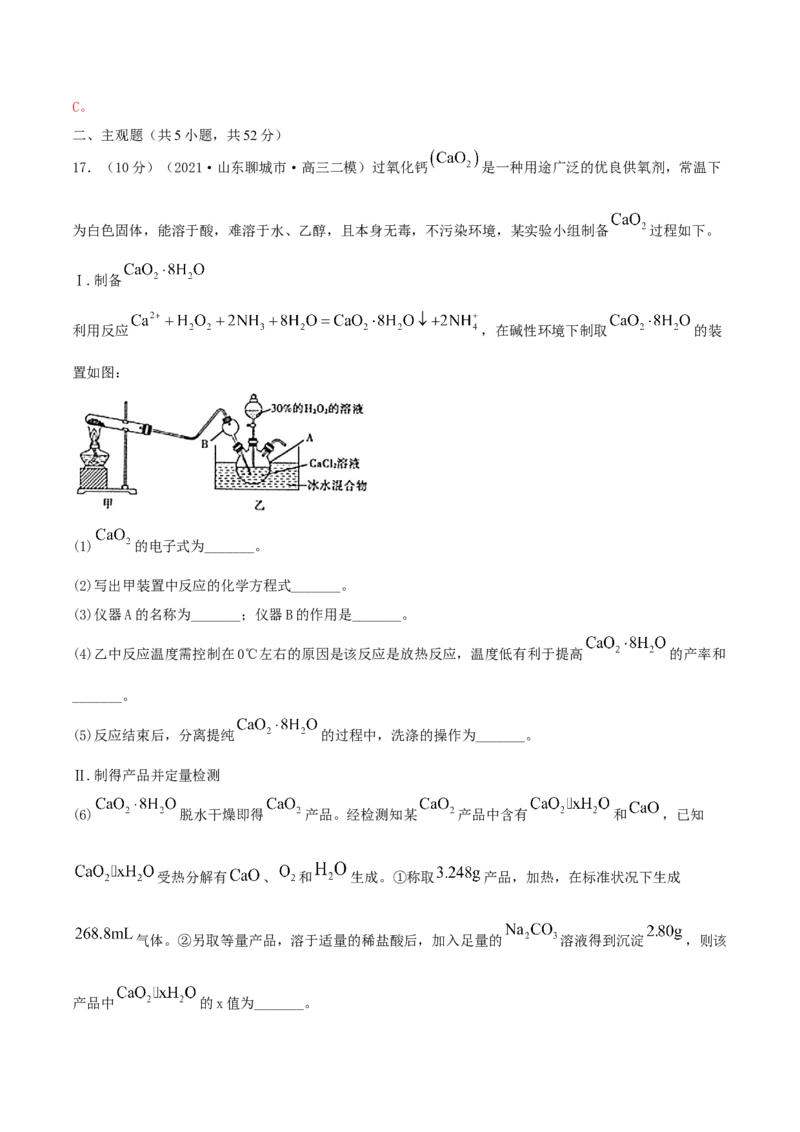
17.(10分)(2021·山东聊城市·高三二模)过氧化钙 是一种用途广泛的优良供氧剂,常温下
为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
Ⅰ.制备
利用反应 ,在碱性环境下制取 的装
置如图:
(1) 的电子式为_______。
(2)写出甲装置中反应的化学方程式_______。
(3)仪器A的名称为_______;仪器B的作用是_______。
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高 的产率和
_______。
(5)反应结束后,分离提纯 的过程中,洗涤的操作为_______。
Ⅱ.制得产品并定量检测
(6) 脱水干燥即得 产品。经检测知某 产品中含有 和 ,已知
受热分解有 、 和 生成。①称取 产品,加热,在标准状况下生成
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀 ,则该
产品中 的x值为_______。【答案】(1) (1分)(2) (2分)(3) 三颈烧瓶(1
分) 防倒吸(1分) (4)过氧化氢的利用率(1分) (5) 向过滤器中加入蒸馏水浸没沉淀,待水自然流
出后,重复操作2—3次(2分) (6) 3 (2分)
【解析】由实验装置图可知,装置甲中氯化铵固体和氢氧化钙共热反应制备氨气,装置乙中,在冰水浴的
条件下,三颈烧瓶中发生的反应为氯化钙、过氧化氢和氨气反应生成八水过氧化钙和氯化铵,氨气极易溶
于水,长颈漏斗在实验中起防倒吸的作用。
(1)过氧化钙是由钙离子和过氧根离子形成的离子化合物,电子式为 ,故答案为:
;
(2) 甲装置中发生的反应为氯化铵固体和氢氧化钙共热反应生成氯化钙、氨气和水,反应的化学方程式为
,故答案为: ;
(3)由分析可知,装置乙中仪器A的名称为三颈烧瓶,装置B为长颈漏斗,用于防止因实验时氨气极易溶于
水产生倒吸,故答案为:三颈烧瓶;防倒吸;
(4) 乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低,可以降低八水过氧化钙,便于
晶体析出,通过八水过氧化钙的产率,同时也能减少过氧化氢分解,提高过氧化氢的利用率,故答案为:
过氧化氢的利用率;
(5)洗涤八水过氧化钙的操作为向过滤器中加入蒸馏水浸没沉淀,待水自然流出后,重复操作2—3次即可,
故答案为:向过滤器中加入蒸馏水浸没沉淀,待水自然流出后,重复操作2—3次;
(6)由①可得:2CaO▪xHO—O,266.8mL氧气的物质的量为 =0.012mol,则CaO▪xHO的物质的
2 2 2 2 2
量为0.012mol×2=0.024mol;由②可知,反应生成2.80g碳酸钙的物质的量为 =0.028mol,则样
品中CaO▪xHO和CaO的物质的量之和为0.028mol,则CaO的物质的量为0.028mol—0.024mol=0.004mol;
2 2
由样品的质量为3.248g可得:0.024mol×(72+18x)g/mol+ 0.004mol×56g/mol=3.248g,解得x=3,故答
案为:3。
18.(12分)(2021·黑龙江哈尔滨市·哈尔滨三中高三一模)碱式碳酸铜又名孔雀石,主要成分为
Cu(OH)CO,呈绿色,是一种具有广泛用途的化工产品。某化学小组探究制备碱式碳酸铜的反应条件并制
2 2 3备少量碱式碳酸铜。
试剂:0.25 mol·L-1 NaCO 溶液、0.5 mol·L-1 NaOH溶液、0.5 mol·L-1 Cu(NO) 溶液各100mL
2 3 3 2
实验1:探究Cu(NO) 与NaOH和NaCO 溶液配比
3 2 2 3
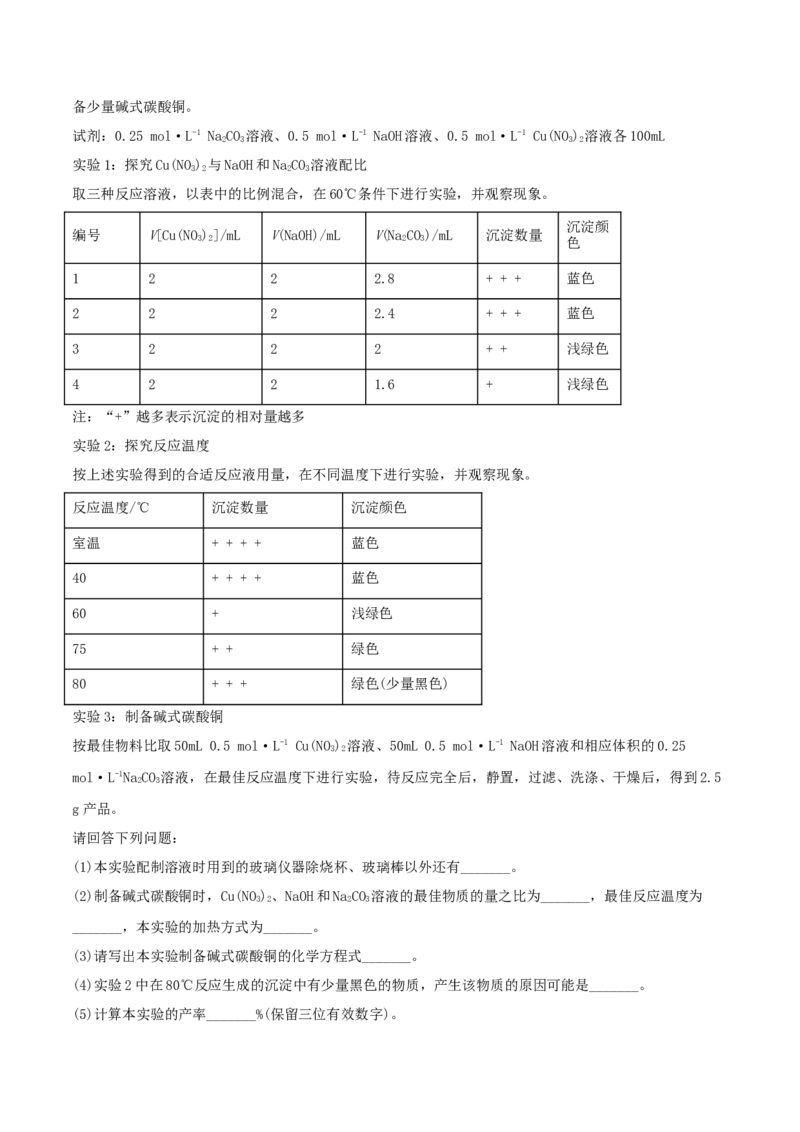
取三种反应溶液,以表中的比例混合,在60℃条件下进行实验,并观察现象。
沉淀颜
编号 V[Cu(NO)]/mL V(NaOH)/mL V(NaCO)/mL 沉淀数量
3 2 2 3 色
1 2 2 2.8 + + + 蓝色
2 2 2 2.4 + + + 蓝色
3 2 2 2 + + 浅绿色
4 2 2 1.6 + 浅绿色
注:“+”越多表示沉淀的相对量越多
实验2:探究反应温度
按上述实验得到的合适反应液用量,在不同温度下进行实验,并观察现象。
反应温度/℃ 沉淀数量 沉淀颜色
室温 + + + + 蓝色
40 + + + + 蓝色
60 + 浅绿色
75 + + 绿色
80 + + + 绿色(少量黑色)
实验3:制备碱式碳酸铜
按最佳物料比取50mL 0.5 mol·L-1 Cu(NO) 溶液、50mL 0.5 mol·L-1 NaOH溶液和相应体积的0.25
3 2
mol·L-1NaCO 溶液,在最佳反应温度下进行实验,待反应完全后,静置,过滤、洗涤、干燥后,得到2.5
2 3
g产品。
请回答下列问题:
(1)本实验配制溶液时用到的玻璃仪器除烧杯、玻璃棒以外还有_______。
(2)制备碱式碳酸铜时,Cu(NO)、NaOH和NaCO 溶液的最佳物质的量之比为_______,最佳反应温度为
3 2 2 3
_______,本实验的加热方式为_______。
(3)请写出本实验制备碱式碳酸铜的化学方程式_______。
(4)实验2中在80℃反应生成的沉淀中有少量黑色的物质,产生该物质的原因可能是_______。
(5)计算本实验的产率_______%(保留三位有效数字)。【答案】(1)100mL 容量瓶、胶头滴管 (2分)
(2)2:2:1(2分) 75℃ (1分) 水浴加热 (1分)
(3)2NaOH+NaCO+2Cu(NO) = Cu(OH)CO+4NaNO(2分)
2 3 3 2 2 2 3 3
(4)碱式碳酸铜受热分解生成黑色的氧化铜(2分)
(5)90.1 (2分)
【解析】(1)本实验配制溶液时用到的玻璃仪器除烧杯、玻璃棒以外还有100mL 容量瓶、胶头滴管;
(2)由实验1表格数据可知,当Cu(NO)、NaOH和NaCO 溶液的体积均为2mL时,生成碱式碳酸铜最多,又
3 2 2 3
Cu(NO)、NaOH和NaCO 溶液的浓度分别为0.5 mol·L-1、0.5 mol·L-1、0.25 mol·L-1,则制备碱式碳酸
3 2 2 3
铜时,Cu(NO)、NaOH和NaCO 溶液的最佳物质的量之比为2:2:1;由实验2表格数据可知,当温度为
3 2 2 3
75℃时,生成碱式碳酸铜最多,则最佳反应温度为75℃,故本实验的加热方式为水浴加热;
(3)制备碱式碳酸铜的化学方程式为2NaOH+NaCO+2Cu(NO) = Cu(OH)CO+4NaNO;
2 3 3 2 2 2 3 3
(4)实验2中在80℃反应生成的沉淀中有少量黑色的物质,产生该物质的原因可能是碱式碳酸铜受热分解
生成黑色的氧化铜;
(5)由反应方程式可知,理论上生成碱式碳酸铜的物质的量为 ,质量为 ,
则本实验的产率为 。
19.(10分)(2021·浙江宁波市·高三二模)硫粉和 溶液反应可以生成多硫化钠( ),离子
反应为: 、 …
(1)在 溶液中加入 硫粉,只发生 ,反应后溶液中 和 无剩余,则原
_______ 。
(2)在一定体积和浓度的 溶液中加入 硫粉,控制一定条件使硫粉完全反应,反应后溶液中的阴
离子有 、 、 (忽略其他阴离子),且物质的量之比为 。则反应后溶液中的_______ 。(写出计算过程)
【答案】(1)0.25 (2) 0.1
【解析】(1) 硫粉的物质的量为 =0.025mol,只发生 ,则
, 0.25 ;
(2) , ,根据 , ,
,
, 。
20.(10分)(2021·浙江衢州市·高三二模)混合碱(NaCO 与NaHCO,或NaCO 与NaOH的混合物)的成
2 3 3 2 3
分及含量可用双指示剂法测定。步骤如下:取混合碱溶液25.00 mL,滴加2滴酚酞为指示剂,用0.2000
mol·L−1的盐酸滴定液滴定至溶液呈微红色,记下消耗盐酸体积为22.50 mL;再滴加2滴甲基橙,继续滴
定至溶液由黄色变为橙色,记下第二次滴定消耗盐酸的体积12.50 mL。(已知:HCO 的K =4.3×10-7;
2 3 a1
K =5.6× 10-11)
a2
请计算:
(1)混合碱成分及物质的量之比为___________。
(2)混合碱溶液中NaCO 的浓度为___________mol·L−1.(写出计算过程)
2 3
【答案】(1)5:4 (2)0.1000 mol·L−1
【解析】滴酚酞为指示剂,发生的反应为:OH-+H+=HO,CO +H+=HCO ,或只发生CO +H+=HCO ,甲基橙
2
为指示剂时,发生HCO +H+=HO+CO ↑。由于两次消耗的酸的体积不相同,且第一次多于第二次,混合碱
2 2
成分是NaCO 与NaOH。
2 3
(1)由分析可知:混合碱成分是NaCO 与NaOH及物质的量之比为12.50 mL:(22.50 mL-12.50 mL)=5:4。
2 3
故答案为:5:4;
(2)n(NaCO)+n(NaOH)=0.2000mol·L−1×22.50mL=4.5×10-3mol,n(NaCO)= 4.5×10-3mol=2.5×10-
2 3 2 33mol, 混合碱溶液中NaCO 的浓度为 =0.1000 mol·L−1。故答案为:0.1000 mol·L−1。
2 3
21.(10分)(2020·浙江台州市·高三一模)某Al-Zn合金镀层铁片样品(无氧化膜)质量为9.320g,单
侧面积为 ,将样品投入足量浓NaOH溶液中,充分反应后,收集到标准状况下气体448 mL,将剩余
固体滤出、洗涤、干燥、称量,得固体质量为8.725g。已知: ,样品表面的Al-
Zn合金镀层密度为 ,合金镀层厚度国家标准为25~35um( ),请计算:
(1)该合金镀层中Al的物质的量分数为(保留3位有效数字)_______。
(2)通过计算,判断该样品镀层厚度是否符合国家标准(列式计算并判断)_______。
【答案】(1)66.7%或0.667 (2)符合
【解析】由题意可知,铝和锌与氢氧化钠溶液反应,而铁不反应,根据固体减少的质量可知铝和锌的总质
量,结合反应生成氢气的体积可计算出铝和锌的物质的量,进一步可求出合金镀层中Al的物质的量分数及
镀层厚度,从而判断是否符合国家标准。
(1)Al、Zn与氢氧化钠溶液反应:2Al+2OH-+2HO=2Al +3H↑、 ,Fe不参加反
2 2
应,则Al、Zn的总质量为9.320g-8.725g=0.595g,设合金镀层中含Al、Zn的物质的量分别为x、y,则有
①27x+65y=0.595,反应生成氢气的物质的量为 =0.02mol,由得失电子守恒关系可得
②3x+2y=0.02 2,联立①②,解得x=0.01mol,y=0.005mol,则合金镀层中Al的物质的量分数为:
100%=66.7%,故答案为:66.7%或0.667。
(2) 样品表面的Al-Zn合金镀层金属的总质量为0.595g,镀层密度为 ,单侧面积为 ,
则镀层厚度= =0.002975cm 30 m,故符合国家标准,故答案为:符合。