文档内容
第二章 化学物质及其变化
测试卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 N 14 O16 Na 23 S 32 K 39 Ca 40 Ag 108
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2023·上海崇明·统考一模)在 的含有 、 、 三种阳离子的溶液中,
可能存在的阴离子是 ( )
① ② ③ ④
A.①② B.②③ C.③④ D.①③
【答案】D
【解析】pH=1,c(H + )=0.1mol·L -1 。①与H + 不能共存的阴离子有:OH - ,弱酸根离子
(S 2- )及弱酸的酸式酸根离子;②H + 存在时, 具有强氧化性,将Fe 2+ 氧化。所以
存在的阴离子为①③,故答案为D。
2.(2023·重庆万州·重庆市万州第二高级中学校考模拟预测)某无色溶液中可能含有
①Na+、②Ba2+、③Cl-、④Br-、⑤SO 、⑥SO 、⑦Fe2+中的几种离子,依次进行下列
实验,且每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
Ⅰ 用pH试纸检验 溶液的pH大于7
Ⅱ 向溶液中滴加氯水,再加入CCl ,振荡,静置 CCl 层呈橙红色
4 4
Ⅲ 取Ⅱ的上层溶液,加入Ba(NO ) 溶液和稀硝酸 有白色沉淀产生
3 2
Ⅳ 将Ⅲ过滤,向滤液中加入AgNO 溶液和稀硝酸 有白色沉淀产生
3
下列结论正确的是( )
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑤⑦
C.可能含有的离子是①②⑥
D.不能确定的离子是①③⑥
【答案】A
【解析】根据步骤Ⅰ,该溶液呈碱性,则该溶液是强碱弱酸盐溶液,所以一定存在SO ,
则一定不存在Ba2+;在碱性的无色溶液中,一定不存在Fe2+;溶液呈电中性,所以溶液中
的阳离子只能是Na+;步骤Ⅱ说明该溶液中一定存在Br-,氯气与Br-反应生成溴单质,溴单
质在四氯化碳中的颜色是橙红色;步骤Ⅲ不能说明有SO 存在,因为该溶液中一定存在SO ,加入氯水后SO 被氧化为SO ,与Ba(NO ) 反应生成BaSO 沉淀;步骤Ⅳ不能确
3 2 4
定原溶液中Cl-是否存在,因为加入的氯水中含有Cl-。因此一定存在的离子是①④⑤,一
定不存在的离子是②⑦,不能确定的离子是③⑥。答案选A。
3.(2023·全国·模拟预测)下列离子方程式书写不正确的是
A.将过量SO 气体通入NaClO溶液中:SO +HO+ClO-=SO +Cl-+2H+
2 2 2
B.标准状况下将112 mL氯气通入10 mL 1 mol·L-1溴化亚铁溶液中:2Fe2++4Br-
+3Cl=2Br +2Fe3++6Cl-
2 2
C.向FeSO 溶液中滴加NaHCO 溶液和稀氨水:Fe2++HCO +NH·H O=FeCO↓+NH +
4 3 3 2 3
HO
2
D.明矾溶液中滴加Ba(OH) 溶液至沉淀的物质的量最大:2Al3++ 3SO + 3Ba2++6OH- =
2
2Al(OH) ↓+3BaSO ↓
3 4
【答案】B
【解析】A.ClO-具有强氧化性,能将SO 氧化成SO ,则其离子方程式为:SO +HO+
2 2 2
ClO-=SO +Cl-+2H+,故A正确;B.标况下,112mL氯气的物质的量为
,10 mL 1 mol·L-1溴化亚铁溶液中
, 、 , 需消
耗0.005 , 需消耗0.01mol , 量不足,由于亚铁离子还原性强于溴离
子,所以该离子方程式为:2Fe2++Cl=2Fe3++2Cl-,故B错误;C.FeSO 为强酸弱碱盐,其
2 4
溶液因亚铁离子水解呈酸性,而NaHCO 溶液和稀氨水均呈碱性,所以向FeSO 溶液中滴
3 4
加NaHCO 溶液和稀氨水的离子方程式为:Fe2++HCO +NH·H O=FeCO↓+NH +HO,故
3 3 2 3 2
C正确;D.明矾溶于水后会电离出铝离子,所以向明矾溶液中滴加Ba(OH) 溶液,使沉淀
2
的物质的量最大时,则生成的氢氧化铝未溶解,则其离子方程式为:2Al3++ 3SO + 3Ba2+
+6OH- = 2Al(OH) ↓+3BaSO ↓,故D正确;故选:B
3 4
4.(2023·陕西榆林·统考模拟预测)下列各组离子在指定溶液中能大量共存的是
A.0.1 mol·L−1 NaHCO 溶液中:H+、Mg2+ 、Cl-、
3
B.0. 1 mol·L−1 FeCl 溶液中:Fe2+、 、I-、
3
C.0. 1 mol·L−1 HCl溶液中:Fe2+、 、Br-、
D.0.1 mol·L−1 NaOH溶液中:K+、Ba2+、 、Br-
【答案】C
【解析】A.0.1 mol·L−1 NaHCO 溶液中不能大量存在H+,否则会反应产生二氧化碳和水,
3
选项A错误;B.0. 1 mol·L−1 FeCl 溶液中,Fe3+与I-因发生氧化还原反应而不能大量共存,
3选项B错误;C.0. 1 mol·L−1 HCl溶液中,H+、Cl-、Fe2+、 、Br-、 各离子之间
相互不反应,能大量共存,选项C正确;D.Ba2+与 因发生反应生成硫酸钡沉淀而不
能大量共存,选项D错误;答案选C。
5.(2023·辽宁·校联考一模)中国画中以墨色为主,以丹青色彩为辅,这样的水墨丹青画
一般画在绢、纸上。下列说法错误的是
A.丹指朱砂,也叫辰砂,是 的天然矿石
B.青指石青,即蓝铜矿,主要成分 ,该物质属于盐
C.墨的主要原料是炭黑、松烟、胶等,通过砚用水研磨可以产生用于毛笔书写的墨汁,
墨汁属于胶体
D.常见绢、纸的主要成分都是纤维素,纤维素属于天然高分子
【答案】D
【解析】A.丹指丹砂、朱砂、辰砂,是硫化汞 的天然矿石,A正确;B.青指石青,
主要成分 ,属于碱式碳酸盐,B正确;C.墨汁、墨水均属于胶体,C正
确;D.绢指丝织品,主要成分为蛋白质,纸的主要成分都是纤维素,蛋白质和纤维素属
于天然高分子,D错误;故选D。
6.(2023·河南开封·统考二模)我国传统文化蕴含着丰富的化学知识。下列说法正确的是
A.“凡酸坏之酒,皆可蒸烧”,该过程利用了物质的溶解性不同
B.“青蒿一握,以水二升渍,绞取汁”,青蒿素的提取过程涉及化学变化
C.“风干日曝咸味加,始灌潮波塯成卤”,该过程涉及的操作方法是蒸发结晶
D.“凡石灰,经火焚炼为用 ……火力用后,烧酥石性,置于风中,久自吹成粉”中的
“粉”为CaO
【答案】C
【解析】A.“凡酸坏之酒,皆可蒸烧”,蒸烧的实验方法是利用物质的沸点不同,控制
温度使乙酸与乙醇分离,选项A错误;B.“青蒿一握,以水二升渍,绞取汁”,句中体
现的对青蒿素的提取,没有生成新物质,属于物理变化,选项B错误;C.“风干日曝咸
味加,始灌潮波增成卤”指将水蒸发得到盐,该过程涉及的操作方法是蒸发结晶,选项C
正确;D.碳酸钙煅烧生成氧化钙,氧化钙久置生成氢氧化钙,氢氧化钙吸收二氧化碳生
成碳酸钙,所以凡石灰经火焚,火力到后,烧酥石性,置于风中久自吹化成粉”中的
“粉”为 碳酸钙,选项D错误;答案选C。
7.(2023·河北·模拟预测)原始瓷是中国乃至世界出现最早且初步具有瓷器特征的一种器
物。考古工作者对某原始瓷文物分析发现,其中含有石英颗粒,还有一定量的莫来石(
, )等。下列说法正确的是
A.石英的主要成分 由大量的硅氧四面体基本单元构成
B.瓷器质地均匀,硬度高,是纯净物C.莫来石的主要成分为氧化物
D.瓷器烧制前后颜色不同的现象称为“窑变”,“窑变”属于物理变化
【答案】A
【解析】A.石英的主要成分二氧化硅晶体由大量的硅氧四面体基本单元构成,选项A正
确;B.瓷器为多种硅酸盐的混合物,不是纯净物,选项B错误;C.莫来石的主要成分为
铝硅酸盐,选项C错误;D.“窑变”过程中发生复杂的化学变化和物理变化,选项D错
误;答案选A。
8.(2023·山东泰安·统考二模)“绿蚁新醅酒,红泥小火炉”、“酥暖薤白酒,乳和地黄
粥”是唐代诗人白居易的著名诗句。下列说法错误的是
A.红泥的颜色主要来自氧化铁 B.乳和粥的分散质是蛋白质
C.酿酒发酵时有二氧化碳生成 D.酒在人体内被氧化释放能量
【答案】B
【解析】A.氧化铁为红色,红泥中含有氧化铁,A项正确;B.乳分散质为蛋白质,粥分
散质为淀粉,B项错误;C.酿酒的反应为 ,C项正确;
D.乙醇在酶的作用下被氧化为乙酸和乙醛,最终代谢为CO 和HO释放能量,D项正确;
2 2
故选B。
9.(2023·上海松江·统考二模)工业上以铜阳极泥(主要成分是 )为原料提取碲(第五
周期VIA族),涉及反应:
① ②
以下说法正确的是
A. 中 元素的化合价是 价
B.氧化性强弱顺序为:
C.反应②中氧化剂是SO ,氧化产物是HSO
2 2 4
D.每制备 理论上共转移12mol电子
【答案】D
【解析】A.碲为第五周期VIA族,最低负化合价为 价,根据化合价的正负化合价为
0, 中 元素的化合价是 价,A错误;B.已知反应:
,氧化剂的氧化性强于氧化产物,所以氧化
性: ,在反应 中, 为氧化剂, 为还
原剂,所以氧化性 ,所以氧化性: ,B错误;C.根据化合价
的升降, ,硫元素的化合价升高,被氧化, 为还原剂, 为氧化产
物,C错误;D.制备 ,反应①消耗 ,转移 ,反应②,转移 ,共转移 ,D正确;
故选D。
10.(2023·浙江绍兴·统考二模)关于反应
,下列说法正确的是
A.消耗 ,转移 电子
B.在此条件下,氧化性:
C. 既是氧化剂又是还原剂
D.氧化产物和还原产物的物质的量比为21∶8
【答案】B
【分析】在反应 中,Cr元素化合价
从+3价升高为+6价,I元素化合价从-1价升高为+5价,Cl元素化合价从+1降低为-1价,
则 为还原剂,ClO-为氧化剂, 为氧化产物,Cl-为还原产物;反应中共转移
电子数为42。
【解析】A.据分析可知,消耗 ,转移 电子,A错误;B.氧化剂的氧化
性大于氧化产物,则在此条件下,氧化性: ,B正确;C.据分析可知, 是
还原剂,C错误;D.据分析可知,氧化产物和还原产物的物质的量比为8∶21,D错误;
故选B。
11.(2023·北京海淀·统考二模)某同学进行如下兴趣实验:
反应原理:①
②
③
现象:立即产生橙红色沉淀,几秒钟后溶液颜色变为蓝色
下列说法不正确的是
A.反应①中 表现氧化性
B.反应后混合液的 减小
C.该实验条件下,反应速率:③>②
D.若用 溶液代替 溶液进行上述实验,现象相同
【答案】D
【解析】A.反应①中 中I元素为+5价,生成物I-中I元素为-1价, 为氧化剂,表
现氧化性,A项正确;B.反应①生成的I-和H+的物质的量之比为1∶3,而反应②消耗的I-和H+的物质的量之比为5∶6,且反应③也消耗I-,所以总的来说H+生成的数量大于消
耗的数量,H+数量增多,pH减少,B项正确;C.先产生了橙红色沉淀后溶液颜色变蓝,
说明反应速率③>②,C项正确;D.若用 溶液代替 溶液,则没有生成反
应②所需的H+,反应②难以发生,现象应该不同,D项错误。答案选D。
12.(2023·湖南邵阳·统考三模)利用空气催化氧化法除掉电石渣浆(含CaO)上层清液中的
S2-并制取石膏(CaSO•2H O)的过程如图:
4 2
下列说法错误的是
A.CaSO•2H O属于盐类和纯净物
4 2
B.过程I中氧化剂与还原剂的物质的量之比为1∶2
C.过程II中,反应的离子方程式为4MnO +2S2-+9H O=SO +4MnO(OH)↓+10OH-
2 2 2
D.将10L上层清液中的S2-(S2-浓度为480mg•L-1)转化为SO ,理论上共需要0.15molO
2
【答案】D
【解析】A.CaSO•2H O有确定的化学式,属于纯净物,能够电离出金属阳离子和酸根,
4 2
所以为盐类物质,A正确;B.过程I中氧化剂为氧气,变成水,1个氧气分子转移4个电
子,还原剂为Mn(OH)2转化为 ,转移2个电子,发生反应时电子守恒,所以氧化剂
与还原剂的物质的量之比为1∶2,B正确;C.过程II中,反应的离子方程式为4MnO
+2S2-+9H O=SO +4MnO(OH)↓+10OH-,电子守恒,原子守恒,电荷守恒,同时生成物在
2 2 2
碱性条件下存在,故生产氢氧根,C正确;D.设转移电子数为xmol,消耗氧气的物质的
量为ymol,则
,x=1.2mol, , ,消耗氧气的物质的量为0.3mol,D错
误;故答案选D。
13.(2023·湖南长沙·湖南师大附中校考二模)某同学研究浓硝酸与KSCN溶液的反应,
在通风橱中进行如下实验:已知: 能被氧化为黄色的 , 可聚合为红色的 。下列分析错误的
是
A. 被氧化为 的过程中,S的化合价升高
B.分析①②③知, 聚合为 的速率大于其被硝酸氧化的速率
C.取少量③中的溶液加入 溶液,产生白色沉淀,不能证明最终有 生成,沉淀
可能是碳酸钡
D.①中改用溶有 的浓硝酸重复上述实验,溶液先变红后迅速褪色并产生大量红棕色
气体,可能是 气体对反应的进行起了催化作用
【答案】C
【解析】A.在SCN-被氧化为(SCN) 过程中,S元素的化合价由SCN-中的-2价升高为
2
(SCN) 中的-1价,A正确;B.根据溶液颜色变化及反应时间的长短,可知(SCN) 聚合为
2 2
(SCN) 的速率大于其被硝酸氧化的速率,B正确;C.③中的溶液显强酸性,取少量③中的
x
溶液加入BaCl 溶液,产生白色沉淀,在强酸性溶液中加入BaCl 溶液产生的白色沉淀只能
2 2
是BaSO,可证明SCN-最终被氧化有SO 生成,C错误;D.①中改用溶有NO 的浓硝酸
4 2
重复上述实验,溶液先变红后迅速褪色并产生大量红棕色气体,可能是NO 气体对反应的
2
进行起了催化作用,D正确;故选C。
14.(2023·湖南郴州·统考三模)硫化钠在造纸工业中用作纸张的蒸煮剂,在制药工业中
用于生产解热药,还可用于制备硫代硫酸钠、多硫化钠等。久置的 固体会潮解、变质、
颜色变黄。某实验小组为探究 固体在空气中变质后的固体成分进行了如下实验。下列
说法正确的是
实验
实验操作 实验现象
步骤
①一份加入 搅拌后,固体表面的少量淡黄色固体消
溶解 失
操作 取适量久置于空气中的
I 固体,分为两份 搅拌后,固体完全溶解,得到略带黄色
②另一份加
的溶液。取略带黄色的溶液,滴加稀硫
水溶解
酸,产生淡黄色浑浊M操作 向②中固体溶解得到的略带黄色的溶液
得到灰黑色悬浊液
II 中加入过量的 溶液
操作 离心管底部出现深褐色沉淀,溶液中出
将灰黑色悬浊液离心分离
III 现淡黄色浑浊
操作 向上述离心分离获得的溶液中加入足量
产生大量白色沉淀
IV 的氯化钡溶液
过滤,用无水乙醇洗涤;然后加入稀盐
操作
酸,将产生的气体通入少量酸性高锰酸 固体部分溶解,酸性高锰酸钾溶液褪色
V
钾溶液中
已知:硫化钠溶液能溶解单质硫,生成多硫化钠( )。。多硫化物的溶液颜色通常为黄
色。 与酸反应生成S和 。
A.①中黄色固体和②中黄色溶液的化学成分相同
B.②中现象淡黄色浑浊M不一定是 与稀硫酸反应产生
C.操作II中发生反应的离子方程式为
D.实验室可用稀硝酸和硫化亚铁反应制备硫化氢
【答案】B
【解析】A.①中黄色固体为S,②中固体完全溶解得到略带黄色的溶液为 溶液,A
错误;B.根据实验现象可知久置于空气中的 固体可能被氧化为 ,因此②中
取略带黄色的溶液,滴加稀硫酸,产生淡黄色浑浊M可能发生
不一定是 与酸反应生成的S,B正确;C.操作Ⅱ
中发生反应的离子方程式为 ,C错误;D.实验室可用稀
硫酸或稀盐酸和硫化亚铁反应制备硫化氢,D错误;故选B。
15.(2023·河南安阳·安阳一中校考模拟预测)如图所示,纵轴表示导电能力,横轴表示
所加溶液的量,下列说法正确的是A.曲线A表示NaOH溶液中滴加稀盐酸
B.曲线B表示CHCOOH溶液中滴加KOH溶液
3
C.曲线C表示Ba(OH) 溶液中滴加稀硫酸
2
D.曲线D表示Cu(OH) 悬浊液中滴加 溶液
2
【答案】C
【解析】A.稀盐酸和NaOH溶液混合时反应生成NaCl,溶液的体积增大,溶液中离子浓
度减小,溶液导电性降低,应该用D表示,故A错误;B.醋酸是弱电解质,醋酸中加入
KOH溶液生成强电解质醋酸钾,溶液中离子浓度增大,溶液导电性增强,应该用A表示,
故B错误;C.氢氧化钡和稀硫酸反应生成硫酸钡沉淀和水,当二者完全反应时溶液中离
子浓度最小,导电性最弱,继续加入稀硫酸,溶液中离子浓度增大,溶液导电性增强,应
该用C表示,故C正确;D.氢氧化铜是弱电解质,溶液中离子浓度较小,加入 溶
液后生成强电解质硝酸铜,离子浓度增大,溶液导电性增强,应该用A表示,故D错误;
故选C。
16.(2022·内蒙古赤峰·模拟预测)三氧化二铬(CrO) 是一种深绿色的固体,熔点很高,
2 3
难溶于水,其化学性质类似于Al O,水溶液中Cr(+3)具有还原性。下列关于Cr O 的说法
2 3 2 3
错误的是
A.与稀硫酸反应: Cr O+ 3H SO = Cr(SO )+ 3H O
2 3 2 4 2 4 3 2
B.与NaOH溶液反应: Cr O+ 4OH- = 2 +2H O
2 3 2
C.碱性条件下被HO 氧化为Cr(+6): Cr O+ 3H O+ 4OH- =2 + 5H O
2 2 2 3 2 2 2
D.由于金属性铝强于铬,且铬的熔点较高,故可用铝热法还原Cr O 制取金属铬
2 3
【答案】B
【解析】A.Cr O 呈碱性氧化物的性质,与酸反应生成盐Cr O
2 3 2 3
+3H SO =Cr (SO )+3H O,A项正确;B.Cr O 与碱反应呈现出酸性氧化物,反应产生
2 4 2 4 3 2 2 3
,方程式为 ,题目中B项方程式未配平,B项错误;C.与
HO 发生氧化还原反应,Cr O 碱性条件下氧化为 ,而HO 还原为HO,离子方程为
2 2 2 3 2 2 2
,C项正确;D.较活泼的金属可用热还原法制备金属
单质,同时Al活泼性强于Cr可以制备,D项正确;故选B。二、主观题(共5小题,共52分)
17.(10分)银及其化合物在制造钱币、电子工业、医药等方面具有广泛用途。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag O为原料冶炼银的化学方程式为__。
2
(2)电解精炼银的工作原理如图所示,___(填“a”或“b”)极为含有杂质的粗银,若b极有
少量红棕色气体生成,则生成该气体的电极反应式为___。
Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式__。
(4)在光照条件下,AgNO 可分解为Ag、O 和某种氮的氧化物。称取34g AgNO 固体,充
3 2 3
分光照使其完全分解,测得反应后生成O 的体积(折合成标准状况)为2.24L,反应过程
2
中转移电子的物质的量为__。
(5)纳米硫化(Ag S)应用广泛。Ag S溶于浓HNO 后,产生淡黄色固体及无色气体,该气体
2 2 3
遇空气迅速变为红棕色。写出反应的化学方程式__。
【答案】(除标注外,每空2分)(1)2Ag O 4Ag+O↑
2 2
(2)a(1分) NO +e-+2H+=NO +H O
2 2
(3) AgCl+Br-=AgBr+Cl-(1分)
(4)0.4mol
(5)3Ag S+8HNO (浓)=6AgNO+3S↓+2NO↑+4H O
2 3 3 2
【解析】(1)Ag的金属活泼性比较弱,用热分解法冶炼金属Ag。以Ag O为原料冶炼银的
2
化学方程式为2Ag O 4Ag+O↑;答案为:2Ag O 4Ag+O↑;
2 2 2 2
(2)由图可知,电极a与电源正极相连,作阳极。电极b与电源负极相连,作阴极。根据电
解原理,可知粗银作阳极,即a极为含有杂质的粗银。红棕色气体为NO 气体,b极有该
2
气体生成,说明NO 得到电子发生还原反应,电极反应式为:NO +e-+2H+=NO +H O;
2 2
答案为:a;NO +e-+2H+=NO +H O;
2 2
(3)AgBr为淡黄色沉淀,说明反应中AgCl转化为AgBr,反应的离子方程式为:AgCl+Br-=
AgBr+Cl-;答案为:AgCl+Br-=AgBr+Cl-;
(4)34gAgNO 的物质的量= ,生成的O 的物质的量=
3 2,NO 中O元素的化合价由-2价变为0价,每生成1molO 转移4mol
2
电子,则生成0.1molO 转移0.4mol电子。答案为:0.4mol;
2
(5)由题可知,Ag S溶于浓HNO 后,生成S单质和NO气体,根据电子转移以及原子守恒
2 3
等规律,可知反应方程式为:3Ag S+8HNO (浓)=6AgNO+3S↓+2NO↑+4H O;答案为:
2 3 3 2
3Ag S+8HNO (浓)=6AgNO+3S↓+2NO↑+4H O。
2 3 3 2
18.(10分)亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还原性。由于NaNO 有
2
毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排
放。处理方法之一如下:
___NaNO +___KI+_____→___NO↑+___I +___K SO +___Na SO +______
2 2 2 4 2 4
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:______________________;
(3)用上述反应来处理NaNO 并不是最佳方法,其原因是______________________。从
2
环保角度来讲,要处理NaNO ,所用的物质的______(填“氧化性”或“还原性”)应该
2
比KI更________(填“强”或“弱”)。
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并
用单线桥表示其电子转移的方向和数目_____________________________。
【答案】(除标注外,每空2分)(1)2 2 2H SO 2 1 1 1
2 4
2HO
2
(2)2 +2I-+4H+ = 2NO↑ +I +2H O
2 2
(3)生成物中含有大气污染物NO 还原性(1分) 强(1分)
(4)
【解析】(1)在反应___NaNO +___KI+_____→___NO↑+___I +___K SO +___Na SO +______
2 2 2 4 2 4
中,NaNO 中N元素化合价降低,NaNO 是氧化剂,KI中I元素化合价升高,KI是还原剂,
2 2
依据得失电子守恒和原子守恒,确定方程式为2NaNO +2KI+
2
2HSO =2NO↑+I +K SO +Na SO +2H O;
2 4 2 2 4 2 4 2
(2)将化学方程式2NaNO +2KI+ 2H SO =2NO↑+I +K SO +Na SO +2H O中的NaNO 、
2 2 4 2 2 4 2 4 2 2
HSO 、KSO 、NaSO 改写成离子形式,并删去方程式两边相同数目的相同离子,得上述
2 4 2 4 2 4
反应的离子反应方程式为2 +2I-+4H+ = 2NO↑ +I +2H O;
2 2
(3)在上述反应中,生成物中含有大气污染物NO,所以用此法来处理NaNO 并不是最佳方
2
法;从环保角度来讲,要处理NaNO ,所用的物质的还原性应该比KI更强;
2
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,该反应的化学方程式为:
NaNO +NHCl=NaCl+N ↑+2H O,用单线桥表示电子转移的方向和数目时,箭头应从NH Cl
2 4 2 2 4
中的N元素指向NaNO 中的N元素,数目为转移电子总数(3e-),表示为:
2。
19.(2022·江苏扬州·模拟预测)(12分)硫化氢的转化是资源利用和环境保护的重要研
究课题。
(1)工业上利用克劳斯法将 转化为硫单质回收。该法首先将部分 燃烧转化为 ,
然后再将 与剩余的 混合。为实现硫的最大回收,用于燃烧的 和剩余的 的
物质的量之比为_______。
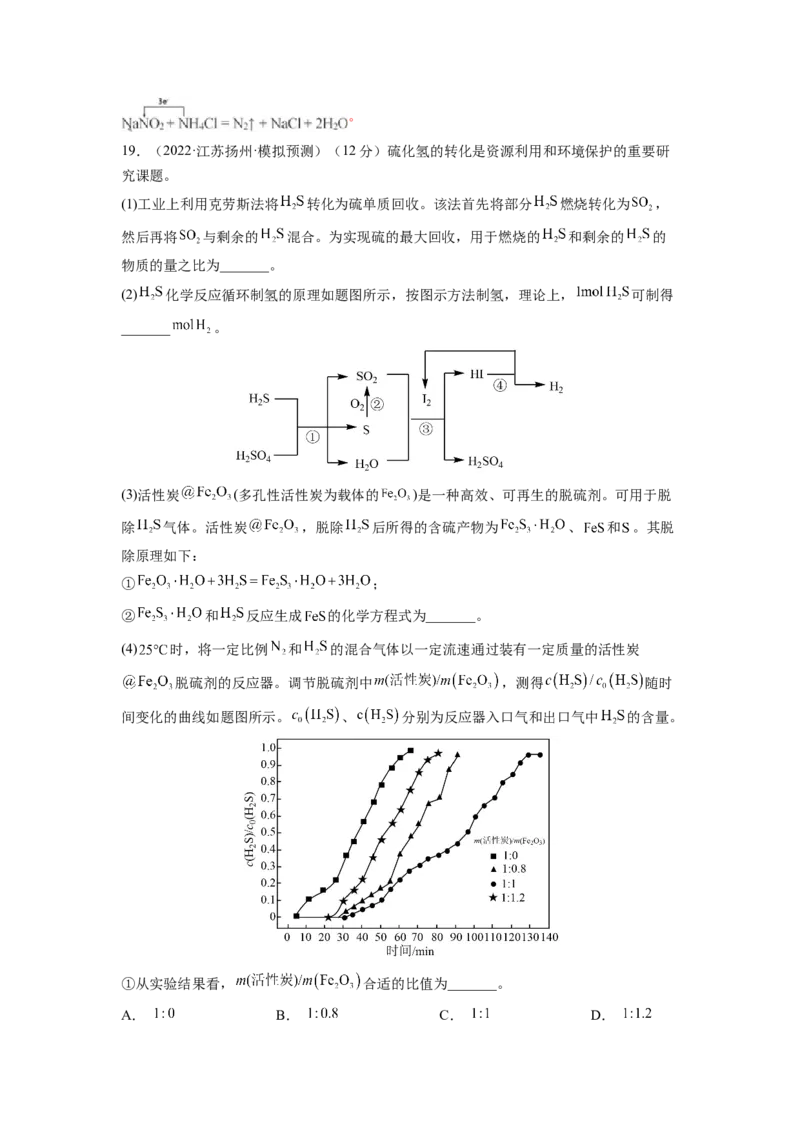
(2) 化学反应循环制氢的原理如题图所示,按图示方法制氢,理论上, 可制得
_______ 。
(3)活性炭 (多孔性活性炭为载体的 )是一种高效、可再生的脱硫剂。可用于脱
除 气体。活性炭 ,脱除 后所得的含硫产物为 、 和 。其脱
除原理如下:
① ;
② 和 反应生成 的化学方程式为_______。
(4) 时,将一定比例 和 的混合气体以一定流速通过装有一定质量的活性炭
脱硫剂的反应器。调节脱硫剂中 ,测得 随时
间变化的曲线如题图所示。 、 分别为反应器入口气和出口气中 的含量。
①从实验结果看, 合适的比值为_______。
A. B. C. D.②当脱硫剂中含有 时, 内, 均为0的原因是_______。
③当 时,测得 时所用的时间为 ;当
时,测得 时所用的时间为 ; 小于
的原因可能是_______。
【答案】(每空2分)(1)1:2
(2)2
(3)
(4)①C
②活性炭吸附 ; 与 反应,通入的 气体被活性炭 完全吸收
③活性炭质量减少,吸附的 的量减少; 的量增多,与 反应的 的量增加,
且前者的影响大于后者。与 反应的 的量增加,导致生成的 、 、
的质量增多,覆盖在脱硫剂表面,影响反应的进一步进行,也影响活性炭的吸附性能。
(“堵塞活性炭的管道,降低了活性炭的吸附能力”也可)
【解析】(1)根据反应2HS+3O 2SO +2H O,2HS+SO=3S+2H O,假设第一反应生成二
2 2 2 2 2 2 2
氧化硫为2mol,则在第二反应中消耗硫化氢4mol,故整个过程第一反应消耗硫化氢为
2mol,即燃烧消耗2mol,剩余4mol,物质的量之比为1:2,故答案为1:2;
(2)根据流程中总反应为HS+O+2H O==2H +H SO ,故每消耗1mol硫化氢生成氢气是
2 2 2 2 2 4
2mol,故答案为2;
(3)根据元素原子守恒及元素化合价升降守恒配平得: ;
(4)①在反应30分钟后, 的比值为1:1时,出来的硫化氢与进入的硫化
氢比值最小,故选择C。
②当脱硫剂中含有 时, 内,活性炭吸附 ; 与 反应,通入的
气体被活性炭 完全吸收,故答案为:活性炭吸附 ; 与 反应,通
入的 气体被活性炭 完全吸收;
③ 变为 时,活性炭质量减少,吸附的
的量减少; 的量增多,与 反应的 的量增加,且前者的影响大于后者。
与 反应的 的量增加,导致生成的 、 、 的质量增多,覆盖在脱硫
剂表面,影响反应的进一步进行,也影响活性炭的吸附性能,故答案为:活性炭质量减少,
吸附的 的量减少; 的量增多,与 反应的 的量增加,且前者的影响大于
后者。与 反应的 的量增加,导致生成的 、 、 的质量增多,覆盖在脱硫剂表面,影响反应的进一步进行,也影响活性炭的吸附性能。
20.(10分)氧化还原法、沉淀法等是常用于治理水体污染的重要化学方法。
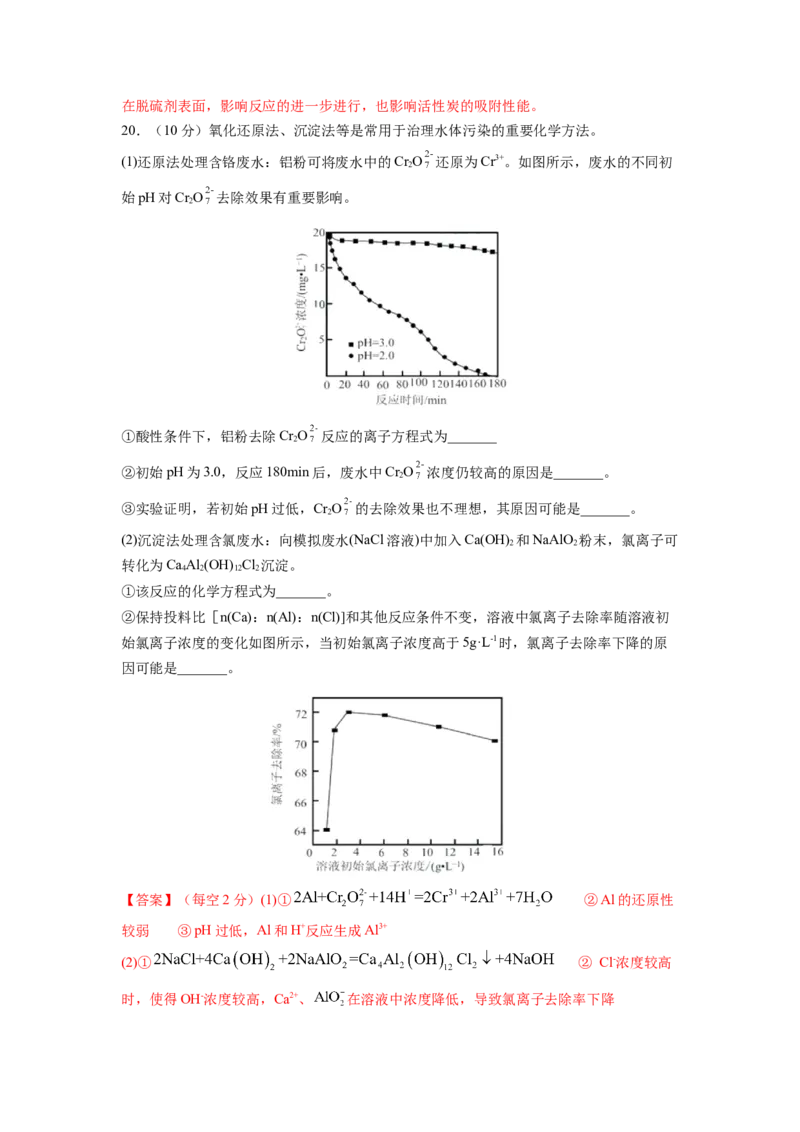
(1)还原法处理含铬废水:铝粉可将废水中的Cr O 还原为Cr3+。如图所示,废水的不同初
2
始pH对Cr O 去除效果有重要影响。
2
①酸性条件下,铝粉去除Cr O 反应的离子方程式为_______
2
②初始pH为3.0,反应180min后,废水中Cr O 浓度仍较高的原因是_______。
2
③实验证明,若初始pH过低,Cr O 的去除效果也不理想,其原因可能是_______。
2
(2)沉淀法处理含氯废水:向模拟废水(NaCl溶液)中加入Ca(OH) 和NaAlO 粉末,氯离子可
2 2
转化为Ca Al (OH) Cl 沉淀。
4 2 12 2
①该反应的化学方程式为_______。
②保持投料比[n(Ca):n(Al):n(Cl)]和其他反应条件不变,溶液中氯离子去除率随溶液初
始氯离子浓度的变化如图所示,当初始氯离子浓度高于5g·L-1时,氯离子去除率下降的原
因可能是_______。
【答案】(每空2分)(1)① ②Al的还原性
较弱 ③pH过低,Al和H+反应生成Al3+
(2)① ② Cl-浓度较高
时,使得OH-浓度较高,Ca2+、 在溶液中浓度降低,导致氯离子去除率下降【解析】(1)①酸性条件下,铝粉可将废水中的Cr O 还原为Cr3+,化学方程式为:
2
;
②pH为3.0,Al的还原性较弱;
③pH过低,溶液中H+含量较高,Al和H+反应生成Al3+,导致Cr O 的去除效果不理想;
2
(2)①NaCl溶液、Ca(OH) 和NaAlO 反应生成Ca Al (OH) Cl 沉淀,化学方程式为:
2 2 4 2 12 2
;
②保持投料比[n(Ca):n(Al):n(Cl)] 和其他反应条件不变,当初始氯离子浓度高于5g·L-1
时, ,Cl-浓度较高时,
使得OH-浓度较高,Ca2+、 在溶液中浓度降低,导致氯离子去除率下降。
21.(10分)(2023·江苏·模拟预测) 和氮氧化物(NOx)都是空气污染物,科学处理及
综合利用是环境科学研究的热点。
(1)某科研小组研究不同条件下0.4molL-1(NH )S溶液常压下吸收SO 烟气的吸收率。
4 2 2
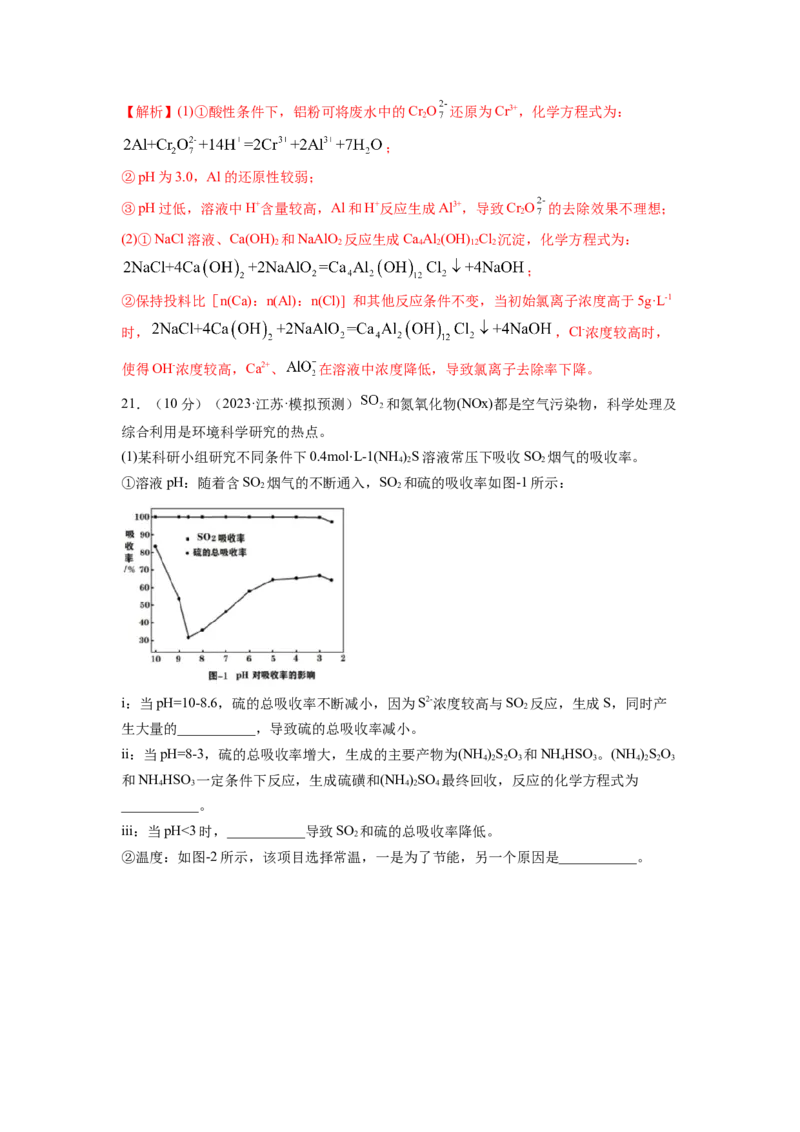
①溶液pH:随着含SO 烟气的不断通入,SO 和硫的吸收率如图-1所示:
2 ⋅ 2
i:当pH=10-8.6,硫的总吸收率不断减小,因为S2-浓度较高与SO 反应,生成S,同时产
2
生大量的___________,导致硫的总吸收率减小。
ii:当pH=8-3,硫的总吸收率增大,生成的主要产物为(NH )SO 和NH HSO 。(NH )SO
4 2 2 3 4 3 4 2 2 3
和NH HSO 一定条件下反应,生成硫磺和(NH )SO 最终回收,反应的化学方程式为
4 3 4 2 4
___________。
iii:当pH<3时,___________导致SO 和硫的总吸收率降低。
2
②温度:如图-2所示,该项目选择常温,一是为了节能,另一个原因是___________。(2)联合脱硫脱硝技术,是一种工业工艺技术,采用“35%的氯酸(HClO3)同时脱硫脱氮技
术”,处理烟气(含SO 、NO)可获得HSO 、HCl、HNO 副产品,通过实验发现,当氯酸
2 2 4 3
的浓度小于35%时,SO 和NO的脱除率几乎不变,但生成HNO 的量远小于理论值,可能
2 3
的原因是___________。
【答案】(每空2分)(1)①i 气体
ii
iii吸收剂消耗完全, 饱和逸出
②常温时硫的吸收率已经很高了,升高温度吸收率变化不大
(2)NO可能被氧化成 及其他含氮化合物
【解析】(1)①由图可知当 时,硫的总吸收率不断减小;当 ,硫的总吸收
率增大;当 时, 和硫的总吸收率降低。当 时, 浓度较高与 反应,
生成硫单质和硫化氢气体,导致硫的总吸收率减小;由题目可知, 和
一定条件下反应,生成硫磺和 ,故反应的化学方程式为:
;当 时,吸收剂消耗完全, 饱
和逸出,导致 和硫的总吸收率降低。故答案为: 气体;
;吸收剂消耗完全, 饱和逸出。
②由图二可看出,温度对吸收率的影响不大,说明常温时硫的吸收率已经很高了,升高温
度吸收率变化不大;
(2)采用“35%的氯酸 同时脱硫脱氮技术”,处理烟气,因为烟气中含有 、
NO,故可能导致NO被氧化成 及其他含氮化合物,故答案为:NO可能被氧化成
及其他含氮化合物。