文档内容
第3讲 氧化还原反应基础
【2020·备考】
最新考纲:1.了解氧化还原反应的本质是电子的转移。2.了解常见的氧化还原反应。
核心素养:1.证据推理与模型认知:建立氧化还原的观点,通过分析、推理等方法
认识氧化还原反应的特征和实质,建立氧化还原反应计算、配平的思维模型。2.科
学探究与创新意识:认识科学探究是进行科学解释和发现、创造和应用的科学实
践活动;能从氧化还原反应的角度,设计探究方案,进行实验探究,加深对物质氧
化性、还原性的理解。
考点一 氧化还原反应的相关概念及表示方法
(频数:★☆☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 氧
化还原反应的有关概念属于基础理论知识,双线桥法是串联各概念的有效途径,
是后面方程式配平和计算的基础。
1.氧化还原反应本质和特征
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
有化合价变化的反应一定是氧化还原反应,但有单质参与的反应不一定属于氧化
还原反应,如O 和O 的转化。
2 3
2.相关概念及其关系示例:在Fe O +3CO=====2Fe+3CO 的反应中Fe O 是氧化剂,CO 是还原剂;C
2 3 2 2 3
元素被氧化,Fe 元素被还原;Fe O 具有氧化性,CO具有还原性;CO 是氧化产物,
2 3 2
Fe 是还原产物。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
氧化还原反应概念的“三大误区”(学生举出反例)
误区1.某元素由化合态变为游离态时,该元素一定被还原。
误区2.在氧化还原反应中,非金属单质一定只作氧化剂。
误区3.在氧化还原反应中,若有一种元素被氧化,则一定有另一种元素被还原。
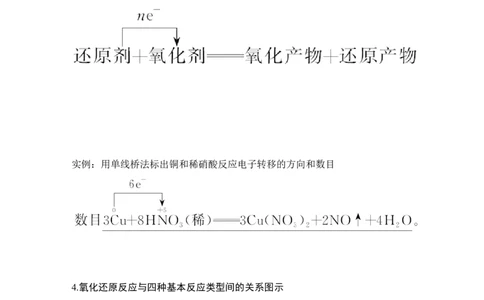
3.氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价,②画箭头,③算数目,④说变化。
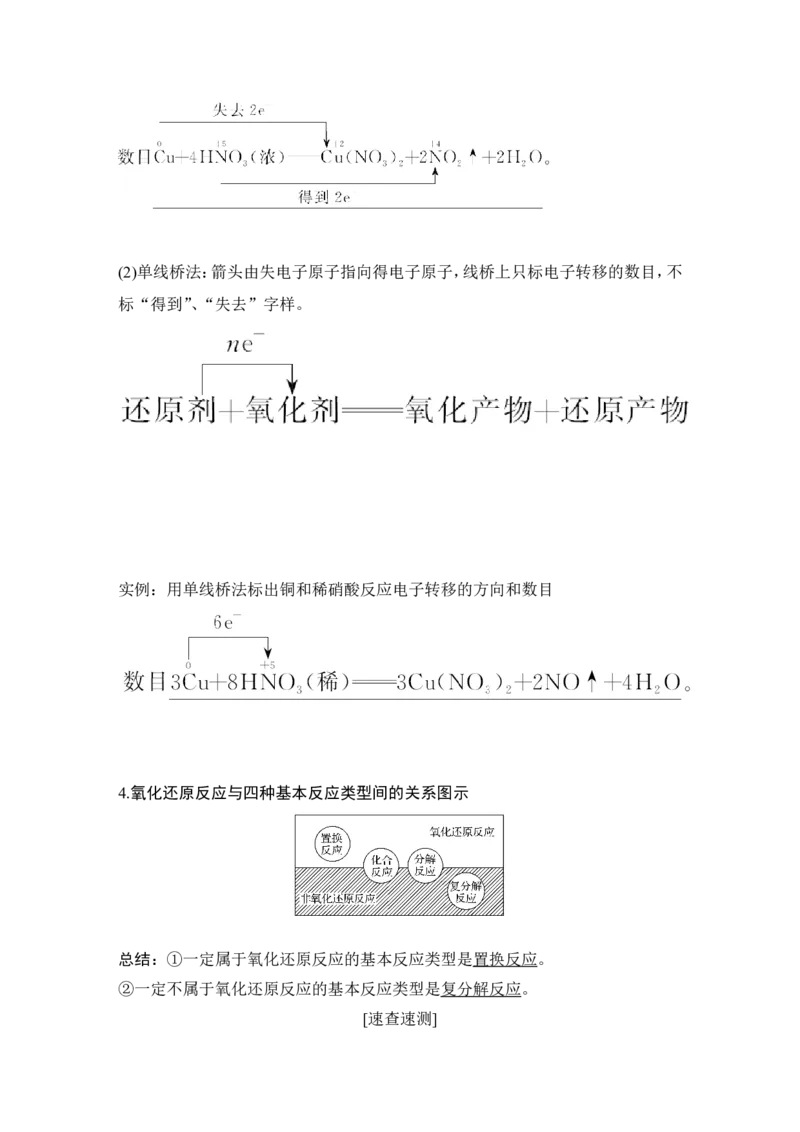
实例:用双线桥法标出铜和浓硝酸反应电子转移的方向和数目(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不
标“得到”、“失去”字样。
实例:用单线桥法标出铜和稀硝酸反应电子转移的方向和数目
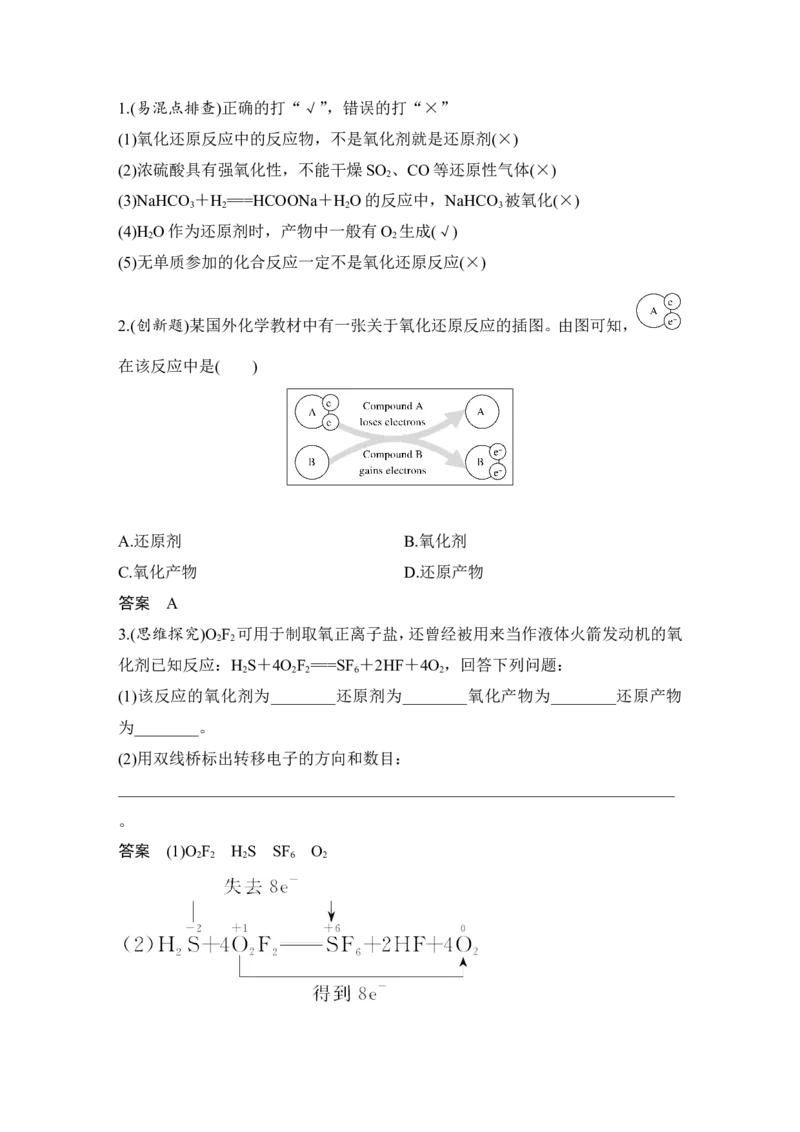
4.氧化还原反应与四种基本反应类型间的关系图示
总结:①一定属于氧化还原反应的基本反应类型是置换反应。
②一定不属于氧化还原反应的基本反应类型是复分解反应。
[速查速测]1.(易混点排查)正确的打“√”,错误的打“×”
(1)氧化还原反应中的反应物,不是氧化剂就是还原剂(×)
(2)浓硫酸具有强氧化性,不能干燥SO 、CO等还原性气体(×)
2
(3)NaHCO +H ===HCOONa+H O的反应中,NaHCO 被氧化(×)
3 2 2 3
(4)H O作为还原剂时,产物中一般有O 生成(√)
2 2
(5)无单质参加的化合反应一定不是氧化还原反应(×)
2.(创新题)某国外化学教材中有一张关于氧化还原反应的插图。由图可知,
在该反应中是( )
A.还原剂 B.氧化剂
C.氧化产物 D.还原产物
答案 A
3.(思维探究)O F 可用于制取氧正离子盐,还曾经被用来当作液体火箭发动机的氧
2 2
化剂已知反应:H S+4O F ===SF +2HF+4O ,回答下列问题:
2 2 2 6 2
(1)该反应的氧化剂为________还原剂为________氧化产物为________还原产物
为________。
(2)用双线桥标出转移电子的方向和数目:
_____________________________________________________________________
。
答案 (1)O F H S SF O
2 2 2 6 2INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·福建省德化一中、永安一中、漳平一中学联考)分析生产生活中的下列过
程,不涉及氧化还原反应的是( )
A.铜制品、铁制品在潮湿的空气中生锈
B.缺铁性贫血服用补铁剂时,需与维生维C同时服用
C.将氯气通入冷的消石灰中制漂白粉
D.从海水中提取氯化镁
解析 A.铜制品、铁制品在潮湿的空气中生锈,单质转化为化合物,是氧化还原反
应;B.缺铁性贫血服用补铁剂时,需与维生素C同时服用,维C是强还原剂,可以
把氧化性较强的+3价铁还原为+2价铁;C.将氯气通入冷的消石灰中制漂白粉,
氯气转化为化合物,是氧化还原反应;D.从海水中提取氯化镁的方法是先用碱把
海水中的镁离子沉淀富集镁,再用盐酸溶解沉淀得氯化镁溶液,然后蒸发浓缩、降
温结晶得氯化镁晶体,接着在氯化氢气流中脱水得无水氯化镁,这个过程中没有
氧化还原反应。
答案 D
2.下列表示电子转移方向和数目正确的是( )答案 D
3.(2018·黑龙江、吉林两省六校期中)已知在相同条件下进行下列反应:①Cl +
2
2KBr===2KCl+Br ;② KClO +6HCl===3Cl ↑+KCl+3H O;③ 2KBrO +
2 3 2 2 3
Cl ===Br +2KClO 。下列说法正确的是( )
2 2 3
A.上述三个反应都有单质生成,所以都是置换反应
B.反应①和反应③中均生成Br ,溴元素发生的变化相同
2
C.反应②中被氧化与被还原物质的物质的量之比为6∶1
D.③中1 mol还原剂反应,则氧化剂得到电子的物质的量为10 mol
解析 反应②中生成物有单质,但反应物没有单质,所以不是置换反应,故A错误;
反应①Cl +2KBr===2KCl+Br 中溴元素的化合价由-1价升高为0价,被氧化,
2 2
反应③2KBrO +Cl ===Br +2KClO 中溴元素的化合价由+5价降低为0价,被
3 2 2 3
还原,故 B 错误;反应② KClO +6HCl===3Cl ↑+KCl+3H O 中,氧化剂是
3 2 2
KClO ,还原剂是HCl,但只有的HCl被氧化,所以还原剂和氧化剂的物质的量之
3
比是5∶1,故C错误;反应③中还原剂是Cl ,氧化剂是KBrO ,该反应中1 mol还
2 3
原剂反应,则氧化剂得到电子的物质的量为2×(5-0)mol=10 mol,故D正确。
答案 D【练后归纳】
化合价的判定方法
1.有机物中碳的化合价判定方法:
有机物中氧元素的化合价为-2,氢元素的化合价为+1。利用元素化合价代数和
为零的规则确定碳元素的化合价。乙酸(C H O )中满足2x+(+1)×4+(-2)×2=
2 4 2
0,则x=0。
2.近几年高考中一些特殊物质中元素化合价判定
[B组 考试能力过关]
4.(2018·北京理综,9)下列实验中的颜色变化,与氧化还原反应无关的是( )
A B C D
NaOH溶液滴入 石蕊溶液滴入氯 Na S溶液滴入 热铜丝插入稀硝
实验 2
FeSO 溶液中 水中 AgCl浊液中 酸中
4
产生白色沉淀, 溶液变红,随后 沉淀由白色逐渐 产生无色气体,
现象
随后变为红褐色 迅速褪色 变为黑色 随后变为红棕色
解析 NaOH溶液滴入FeSO 溶液中,发生反应:2NaOH+FeSO ===Fe(OH) ↓+
4 4 2
Na SO ,生成白色沉淀Fe(OH) ,Fe(OH) 不稳定,迅速被空气中的氧气氧化为红褐
2 4 2 2
色的Fe(OH) :4Fe(OH) +O +2H O===4Fe(OH) ,后一过程发生了氧化还原反应,
3 2 2 2 3
A项不符合题意;氯水中含有HCl和HClO,溶液呈酸性,能使石蕊溶液变红,次氯
酸具有强氧化性,能将红色物质氧化,溶液红色褪去,该过程发生了氧化还原反应,
B项不符合题意;Na S溶液滴入AgCl浊液中,发生了沉淀的转化:Na S+2AgCl
2 2
Ag S+2NaCl,此过程中不涉及氧化还原反应,C项符合题意;将铜丝插入
2
稀硝酸中,发生反应:3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O,生成无色
3 3 2 2
气体NO,但NO能与空气中的氧气发生反应:2NO+O ===2NO ,这两步反应都
2 2
是氧化还原反应,D项不符合题意。
答案 C
5.(2017·天津理综,3)下列能量转化过程与氧化还原反应无关的是( )A.硅太阳能电池工作时,光能转化成电能
B.锂离子电池放电时,化学能转化成电能
C.电解质溶液导电时,电能转化成化学能
D.葡萄糖为人类生命活动提供能量时,化学能转化成热能
解析 A项,硅太阳能电池工作时,发生光电效应,使光能转化成电能,与氧化还
原反应无关;B项,锂离子电池放电时,正极和负极分别发生还原反应和氧化反应
使化学能转化成电能;C项,电解质溶液导电时,阴极和阳极分别发生还原反应和
氧化反应,使电能转化成化学能;D项,葡萄糖在酶的作用下发生氧化还原反应等
一系列反应的同时为人类生命活动提供能量,使化学能转化成热能。
答案 A
6.(课标全国卷)(1)次磷酸(H PO )是一种精细磷化工产品,具有较强还原性,回答下
3 2
列问题:
H PO 及NaH PO 均可将溶液中的Ag+还原为银,从而可用于化学镀银。
3 2 2 2
①H PO 中,P元素的化合价为________。
3 2
②利用H PO 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则
3 2
氧化产物为_____________________________________________________(填化学
式)。
(2)(2015·课标全国Ⅰ)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加
MnO 和H SO ,即可得到I 。该反应的还原产物为________。
2 2 4 2
答案 (1) ①+1 ②H PO (2)MnSO
3 4 4
考点二 氧化剂与还原剂
(频数:★★☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 常
见的氧化剂与还原剂属于氧化还原反应有关概念的延伸,是基本理论之一,复习时应掌握好常见的氧化剂和还原剂及其强弱比较方法。
1.常见的氧化剂、还原剂
(1)常见氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
(2)常见还原剂
常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、
非金属单质及其氢化物等。如:
(3)具有中间价态的物质既有氧化性,又有还原性
具有中间价态的物质 氧化产物 还原产物
Fe2+ Fe 3 + Fe
SO SO S
H O O H O
2 2 2 2
2.氧化性、还原性及其强弱比较
(1)氧化性、还原性的判断
(2)氧化性、还原性的强弱比较
Ⅰ.依据反应原理判断氧化性强弱:氧化剂>氧化产物
还原性强弱:还原剂>还原产物
实例:有以下反应:
①H SO +I +H O===2HI+H SO ;
2 3 2 2 2 4
②2FeCl +2HI===2FeCl +I +2HCl;
3 2 2
③3FeCl +4HNO ===2FeCl +NO↑+2H O+Fe(NO ) 。
2 3 3 2 3 3
还原性 氧化性
从反应①可知 H SO >I - I >H SO
2 3 2 2 4
从反应②可知 I - >Fe 2 + Fe 3 + >I
2
从反应③可知 Fe 2 + >NO HNO >Fe 3 +
3
还原性:H SO >I - >Fe 2 + >NO
2 3
总的强弱顺序
氧化性:HNO >Fe 3 + >I >H SO
3 2 2 4
Ⅱ.根据与同一物质反应情况(反应条件、剧烈程度)判断
F +H =====2HF
2 2
Cl +H =====2HCl
2 2
氧化性F >Cl
2 2
③根据原电池电极反应判断
还原性Zn>Fe
Ⅲ.根据物质浓度、溶液酸碱性或温度判断
氧化性:浓HNO >稀HNO
3 3
还原性:浓盐酸>稀盐酸INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.常用的物质氧化性、还原性强弱顺序为
氧化性:MnO>Cl >Br >Fe3+>I ,
2 2 2
还原性:S2->SO(或H SO )>I->Fe2+>Br->Cl-。
2 3
2.H O 中氧元素尽管处于中间价态,但 H O 主要表现为氧化性,其还原产物是
2 2 2 2
H O,故H O 又被称为绿色氧化剂。
2 2 2
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)强氧化剂与强还原剂混合不一定能发生氧化还原反应(√)
(2)元素的非金属性越强,其氧化性越强,相应单质越活泼(×)
(3)难失电子的物质一定易得电子(×)
(4)NO 和NH 之间可能发生反应产生N (√)
2 3 2
(5)含硫化合物X、Y的转化关系S+NaOH→X+Y+H O中,硫单质的化合价最低
2
(×)
2.(教材改编题)(RJ必修1·P 5改编)下列叙述正确的是( )
38
A.氧化还原反应的本质是化合价发生变化
B.氧化剂在化学反应中失去电子
C.还原剂在反应中发生还原反应
D.反应中同一反应物可能既发生氧化反应又发生还原反应
答案 D
3.(思维探究题)物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的
浓度和反应温度等有关。下列各组物质:①Cu与HNO 溶液 ②Cu与FeCl 溶液
3 3
③Zn与H SO 溶液 ④Fe与FeCl 溶液 ⑤Cl 和NaOH溶液 ⑥Fe和HNO
2 4 3 2 3
溶液 ⑦Fe和H SO 溶液 ⑧Na和O
2 4 2
(1)由于浓度不同而发生不同氧化还原反应的是①③⑥⑦。
(2)由于温度不同而发生不同氧化还原反应的是⑤⑥⑦⑧。
(3)氧化还原反应不受浓度、温度影响的是②④。INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·湖南郴州质监)在下列变化:①大气固氮,②硝酸银分解,③实验室制取氨
气。按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列正确的是( )
A.①②③ B.②①③
C.③②① D.③①②
解析 大气固氮发生的反应为N +O =====2NO,氮元素被氧化;硝酸银分解的
2 2
化学方程式为2AgNO =====2Ag+2NO ↑+O ↑,氮元素被还原;实验室制取氨
3 2 2
气的化学方程式为2NH Cl+Ca(OH) =====CaCl +2NH ↑+2H O,该反应属于
4 2 2 3 2
非氧化还原反应,氮元素既不被氧化也不被还原,故正确答案是A。
答案 A
2.(2018·吉林长春实验中学模拟)已知NH CuSO 与足量的3 mol/L硫酸混合微热,
4 3
产生下列现象:①有红色金属生成;②产生刺激气味的气体;③溶液呈现蓝色。据
此判断下列说法正确的是( )
A.反应中硫酸作氧化剂
B.NH CuSO 中硫元素被氧化
4 3
C.刺激性气味的气体是氨气
D.1 mol NH CuSO 完全反应转移0.5 mol电子
4 3
解析 反应方程式为:2NH CuSO +4H+===Cu+Cu2++2SO ↑+2H O+2NH由
4 3 2 2
方程式知反应中只有Cu元素的化合价发生变化、硫酸根反应前后未变,反应中
H SO 表现酸性,不做氧化剂,A错误;反应生成的红色固体是Cu,蓝色溶液是Cu2
2 4
+,刺激性气味气体是SO ,S元素化合价没变,所以B、C错误。
2答案 D
3.(2018·浙江联考)在室温下,发生下列几种反应:
①16H++10Z-+2XO===2X2++5Z +8H O
2 2
②2A2++B ===2A3++2B-
2
③2B-+Z ===B +2Z-
2 2
根据上述反应,判断下列结论错误的是( )
A.要除去含有A2+、Z-和B-混合溶液中的A2+,而不氧化Z-和B-,应加入Z
2
B.还原性强弱顺序为A2+>B->Z->X2+
C.X2+是XO的还原产物,B 是B-的氧化产物
2
D.在溶液中可能发生反应:8H++5A2++XO===X2++5A3++4H O
2
解析 氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,反应①16H++
10Z-+2XO===2X2++5Z +8H O中,氧化性:XO>Z ;反应②2A2++B ===
2 2 2 2
2A3++2B-中,氧化性:B >A3+;反应③2B-+Z ===B +2Z-中,氧化性:Z >B ,则
2 2 2 2 2
氧化性强弱顺序是XO>Z >B >A3+,所以要除去含有A2+、Z-和B-混合溶液中的
2 2
A2+,而不氧化Z-和B-,应加入B ,故A错误;还原剂的还原性强于还原产物的
2
还原性,由反应①②③中还原性的比较可知,还原性强弱顺序为A2+>B->Z->X2
+,故B正确;反应①中X元素的化合价降低,则XO为氧化剂,X2+是XO的还原
产物,反应③中B-发生氧化反应生成B ,即B 是B-的氧化产物,故C正确;根据
2 2
A项中的分析,氧化性强弱顺序是XO>Z >B >A3+,所以XO能氧化A2+,发生的
2 2
反应为8H++5A2++XO===X2++5A3++4H O,故D正确。
2
答案 A
【方法技巧】[B组 考试能力过关]
4.(2017·北京理综)下列变化中,气体被还原的是( )
A.二氧化碳使Na O 固体变白
2 2
B.氯气使KBr溶液变黄
C.乙烯使Br 的四氯化碳溶液褪色
2
D.氨气使AlCl 溶液产生白色沉淀
3
解析 A.二氧化碳使Na O 固体变白,发生反应2CO +2Na O ===O +2Na CO ,
2 2 2 2 2 2 2 3
CO 中元素的化合价没有发生改变;B.氯气使KBr溶液变黄,发生反应2KBr+
2
Cl ===2KCl+Br ,Cl 中氯元素化合价降低,被还原,符合题意;C.乙烯使Br 的四
2 2 2 2
氯化碳溶液褪色,是乙烯与溴发生了加成反应;D.氨气使AlCl 溶液产生白色沉淀
3
氢氧化铝,化合价没有改变。
答案 B
5.(海南化学)化学与生活密切相关。下列应用中利用了物质氧化性的是( )
A.明矾净化水 B.纯碱去油污
C.食醋除水垢 D.漂白粉漂白织物
解析 A项,明矾净水是利用Al3+水解生成的氢氧化铝胶体具有吸附能力,错误;B项,纯碱去油污是利用碳酸钠水解溶液呈碱性,错误;C项,食醋除水垢是利用
醋酸的酸性,能与碳酸钙反应而除去,错误;D项,因漂白粉具有强氧化性而用于
漂白织物,正确。
答案 D
6.(2016·北京理综,10)K Cr O 溶液中存在平衡:Cr O(橙色)+H O2CrO(黄色)
2 2 7 2 2
+2H+。用K Cr O 溶液进行下列实验:
2 2 7
结合实验,下列说法不正确的是( )
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr O被C H OH还原
2 2 5
C.对比②和④可知K Cr O 酸性溶液氧化性强
2 2 7
D.若向④中加入70%H SO 溶液至过量,溶液变为橙色
2 4
解析 A项,①中在平衡体系中滴加70%H SO 溶液,平衡向左移动,c(Cr O)增大,
2 4 2
橙色加深,③中滴加30%NaOH溶液,平衡向右移动,c(CrO)增大,溶液变黄,正确
B项,②中重铬酸钾氧化乙醇,反应中重铬酸钾被乙醇还原,正确;C项,②是酸性
溶液,④是碱性溶液,酸性溶液中能氧化乙醇,而碱性溶液中不能氧化乙醇,说明
K Cr O 在酸性溶液中氧化性强,正确;D项,若向④溶液中加入70%的H SO 溶液
2 2 7 2 4
至过量,溶液由碱性变为酸性,K Cr O 在酸性溶液中氧化性强,可以氧化乙醇,溶
2 2 7
液变绿色,错误。
答案 D
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.(2018·河北邢台期末,4)中国传统文化对人类文明贡献巨大,《本草纲目》中有如下记载:“(火药)乃焰消(KNO )、硫黄、杉木炭所合,以为烽燧铳机诸药者”,其中
3
利用的KNO 的性质是( )
3
A.自燃性 B.稳定性
C.还原性 D.氧化性
解析 火药爆炸的反应原理为2KNO +S+3C INCLUDEPICTURE "F:\\方正文
3
件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\反应点燃.TIF"
\* MERGEFORMATINET K S+N ↑+3CO ↑,反应中N元素化合价降低,
2 2 2
KNO 为氧化剂,故反应中利用了KNO 的氧化性,D项正确。
3 3
答案 D
2.下列物质应用中,利用物质氧化性的是( )
A.SO 使品红溶液褪色
2
B.食品袋中铁粉作除氧剂
C.臭氧作自来水消毒剂
D.活性炭作冰箱里的去味剂
解析 A项,利用SO 漂白性;B项,铁粉作除氧剂,利用铁粉的还原性;C项,臭
2
氧作消毒剂,利用臭氧的强氧化性;D项,活性炭作去味剂,利用活性炭的吸附性。
本题选C。
答案 C
3.(2018·福建福州八县(市)协作体联考,6)已知反应:O +2I-+H O===O +I +
3 2 2 2
2OH-,下列说法中不正确的是( )
A.O 为还原产物
2
B.氧化性:O >I
3 2
C.H O既不是氧化剂也不是还原剂
2
D.反应生成1 mol I 时转移2 mol电子
2
解析 反应O +2I-+H O===O +I +2OH-中,O元素化合价降低,O 部分被还
3 2 2 2 3
原生成OH-,I元素化合价升高,I-被氧化生成I 。O 生成O 时没有发生化合价的
2 3 2
变化,O 不是还原产物,A项错误;该反应中I 是氧化产物,O 是氧化剂,氧化性:
2 2 3
O >I ,B项正确;H O在反应中所含元素化合价没有发生变化,所以水既不是氧化
3 2 2
剂也不是还原剂,C项正确; I元素化合价由-1价升高到0价,则反应生成1 molI 时转移2 mol电子,D项正确。
2
答案 A
4.已知几种阴离子的还原性强弱顺序为OH-I->Br->Cl->OH-,Cl 最后氧化Br-,本题选A。
2
答案 A
5.(2018·广东深圳三校联考)已知下列反应:
反应Ⅰ:Co O +6HCl(浓)===2CoCl +Cl ↑+3H O
2 3 2 2 2
反应Ⅱ :5Cl +I +6H O===10HCl+2HIO
2 2 2 3
下列说法正确的是( )
A.反应Ⅰ中HCl是氧化剂
B.反应Ⅱ中Cl 发生氧化反应
2
C.氧化性:Co O >Cl >HIO
2 3 2 3
D.还原性:CoCl >HCl>I
2 2
解析 反应Ⅰ中Cl元素的化合价升高,则HCl为还原剂,故A项错误;反应Ⅱ中
Cl元素的化合价降低,则Cl 发生还原反应,故B项错误;由氧化剂的氧化性强于
2
氧化产物的氧化性可知,反应Ⅰ中氧化性:Co O >Cl ,反应Ⅱ中氧化性:
2 3 2
Cl >HIO ,则氧化性:Co O >Cl >HIO ,故C项正确;由还原剂的还原性强于还原
2 3 2 3 2 3
产物的还原性,反应Ⅰ中还原性:HCl>CoCl ,反应Ⅱ中还原性:I >HCl,故还原性:
2 2
I >HCl>CoCl ,D项错误。
1 2
答案 C
6.铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发
生:① Tl3++2Ag===Tl++2Ag+,② Ag++Fe2+===Ag+Fe3+,③ Fe+2Fe3+
===3Fe2+,下列离子氧化性比较顺序正确的是( )
A.Tl3+>Fe3+>Ag+
B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+D.Tl3+>Ag+>Fe3+
解析 在氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性。
答案 D
7.(2019·安徽亳州质量检测,6)Cl 是纺织工业常用的漂白剂,Na S O 可作为漂白
2 2 2 3
布匹后的“脱氯剂”。S O和Cl 反应的产物之一为SO。下列说法中不正确的是(
2 2
)
A.该反应中还原剂是S O
2
B.H O参与该反应,且作氧化剂
2
C.根据该反应可判断氧化性:Cl >SO
2
D.该反应中,每生成1 mol SO,可脱去2 mol Cl
2
解析 反应的离子方程式为:S O+4Cl +10OH-===2SO+8Cl-+5H O。反应中S
2 2 2
元素的化合价升高被氧化,则S O为还原剂,A项正确;反应中H O为产物,B项
2 2
错误;根据氧化剂的氧化性大于氧化产物的氧化性可知,氧化性:Cl >SO,C项正
2
确;由离子方程式可知,每生成1 mol SO,可脱去2 mol Cl ,D项正确。
2
答案 B
8.化学反应的发生往往遵循着相应的反应规律,下表中列举了三类反应,根据相应
反应得出的结论正确的是( )
氧化还原反应 复分解反应 热分解反应
4NaClO
INCLUDEPICTURE "F:\
\方正文件\\2019文件\\课
件\\2020版 创新设计 高
考总复习 化学 人教版\
\反应三角.TIF" \*
2HSCN+K CO === MERGEFORMATINET
2 3
2Co(OH) +6HCl===2CoCl
3 2 2KSCN+CO ↑+H O 3NaCl+NaClO
+Cl ↑+6H O 2 2 4
2 2
KCN+CO +H O=== NaClO
2FeCl +Cl ===2FeCl 2 2 4
2 2 3 INCLUDEPICTURE "F:\
HCN+KHCO
3 \方正文件\\2019文件\\课
件\\2020版 创新设计 高
考总复习 化学 人教版\
\反应三角.TIF" \*
MERGEFORMATINET
NaCl+2O ↑
2
A.氧化性:FeCl >Co(OH) >Cl
3 3 2B.还原性:HCl>CoCl >FeCl
2 2
C.热稳定性:NaCl>NaClO>NaClO
4
D.酸性:HSCN>H CO >HCN
2 3
解析 根据氧化还原反应中氧化剂的氧化性强于氧化产物,还原剂的还原性强于
还原产物,所以氧化性:Co(OH) >Cl >FeCl ,A错误;还原性:HCl>CoCl ,由所给
3 2 3 2
方程式不能推出CoCl 与FeCl 的还原性强弱,B错误;根据在热分解反应中稳定
2 2
性弱的物质容易分解生成相对稳定性强的物质,则热稳定性顺序为
NaCl>NaClO >NaClO,C错误;根据在复分解反应中强酸制取弱酸的原则,酸性:
4
HSCN>H CO >HCN,D正确。
2 3
答案 D
9.水是一种重要的资源,它同时在化学反应中担任着重要的角色,既可作为反应物
又可作为生成物,如图中和水相连的物质都能和水发生反应,则有关说法正确的
是( )
A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①和⑦中都有氧气生成,且生成1 mol O 转移的电子数相同
2
C.①④⑧反应中水都既不作氧化剂也不作还原剂
D.⑦中水作氧化剂,②中水作还原剂
解析 先写出这8个反应的化学方程式,然后分析这8个反应,其中化合价没有变
化的有③⑤⑥,其余的都属于氧化还原反应,A错;①中2Na O +2H O===4NaOH
2 2 2
+O ,生成1 mol O 转移2 mol e-,⑦中2F +2H O===4HF+O ,生成1 mol O 转
2 2 2 2 2 2
移4 mol e-,B错;①④⑧三个反应都属于氧化还原反应中的歧化反应,Cl 、Na O
2 2 2
和NO 在反应中都是既作氧化剂又作还原剂,水都既不作氧化剂也不作还原剂,C
2
正确;⑦中水作还原剂,②中水作氧化剂,D错。
答案 C
10.按要求填空。
(1)在Fe、Fe2+、Fe3+、H+中,①只有氧化性的是________,
②只有还原性的是________,
③既有氧化性又有还原性的是________。
(2)某同学写出以下三个化学方程式(未配平)
①NO+HNO →N O +H O
3 2 3 2
②NH +NO→HNO +H O
3 2 2
③N O +H O→HNO +HNO
2 4 2 3 2
在②、③反应中一定不可能实现的是________;在反应①中氧化剂是________,还
原性最强的是________,若该物质消耗30 g,转移电子________mol。
解析 (2)若含有同种元素不同价态的两种物质发生氧化还原反应时,生成物中该
元素的价态应介于两种反应物价态之间。②式反应物中的氮元素化合价分别为-
3价和+2价,生成物中为+3价,-3价与+2价之间的价态应为0价或+1价,不
可 能 出 现 + 3 价 的 氮 , 所 以 ② 式 不 能 实 现 。 在 反 应
中,根据元素的化合价变化可知HNO 为氧
3
化剂,NO为还原剂(还原性最强),当有30 g NO(即1 mol)消耗时,转移电子的物质
的量为1 mol×1=1 mol。
答案 (1)①Fe3+、H+ ②Fe ③Fe2+ (2)② HNO NO 1
3
11.为验证氧化性Cl >Fe3+>SO ,某小组用下图所示装置进行实验(夹持仪器和A
2 2
中加热装置已略,气密性已检验)。
实验过程:
Ⅰ.打开弹簧夹K ~K ,通入一段时间N ,再将T形导管插入B中,继续通入N ,
1 4 2 2
然后关闭K 、K 、K 。
1 3 4
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。Ⅲ.当B中溶液变黄时,停止加热,关闭K 。
2
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K 和活塞c,加入70%的硫酸,一段时间后关闭K 。
3 3
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是___________________________________________________。
(2)棉花中浸润的溶液为________。
(3)A中发生反应的化学方程式:_______________________________________。
(4)若将制取的 SO 通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为
2
___________________________________________________________________。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一
定能够证明氧化性Cl >Fe3+>SO 的是________(填“甲”“乙”或“丙”)。
2 2
过程ⅣB溶液中含有的离子 过程ⅥB溶液中含有的离子
甲 有Fe3+无Fe2+ 有SO
乙 既有Fe3+又有Fe2+ 有SO
丙 有Fe3+无Fe2+ 有Fe2+
解析 (5)甲、乙、丙在过程ⅣB溶液中都可确定含有Fe3+,则可证明氧化性Cl >
2
Fe3+;甲在过程ⅣB溶液中如果含有Cl ,可把SO 氧化成SO,无法证明氧化性Fe3
2 2
+>SO ,故甲不合理;由乙在过程ⅣB溶液中含有的离子可知溶液中无Cl ,通过Ⅵ
2 2
B溶液中含有SO可证明Fe3+>SO ,故乙合理;在丙中ⅥB溶液中含有Fe2+可知
2
在此过程发生还原反应,由Fe3+→Fe2+可推知SO →SO,氧化性
2
Fe3+>SO ,故丙合理。
2
答案 (1)排出装置中的空气,防止干扰
(2)NaOH溶液
(3)MnO +4HCl(浓)=====MnCl +Cl ↑+2H O
2 2 2 2
(4)2MnO+5SO +2H O===2Mn2++5SO+4H+
2 2
(5)乙、丙
[B级 拔高选做题]
12.过氧化钠具有强氧化性,遇亚铁离子可将其氧化为一种常见的高效水处理剂,
化学方程式为2FeSO +6Na O ===2Na FeO +2Na O+2Na SO +O ↑。下列说法
4 2 2 2 4 2 2 4 2
不正确的是( )A.氧化性:Na O >Na FeO >FeSO
2 2 2 4 4
B.FeSO 只作还原剂,Na O 既作氧化剂,又作还原剂
4 2 2
C.由反应可知每3 mol FeSO 完全反应时,反应中共转移12 mol电子
4
D.Na FeO 处理水时,不仅能杀菌消毒,还能起到净水的作用
2 4
解 析 A 项 , 由 氧 化 剂 的 氧 化 性 强 于 氧 化 产 物 可 知 , 氧 化 性 :
Na O >Na FeO >FeSO ,正确;B项,由反应方程式可知,铁元素的化合价由+2升
2 2 2 4 4
高到+6,氧元素的化合价部分由-1降低到-2,部分由-1升高到0,所以FeSO
4
只作还原剂,Na O 既作氧化剂又作还原剂,正确;C项,由反应方程式可知,2 mol
2 2
FeSO 完全反应时,转移10 mol 电子,所以每3 mol FeSO 完全反应时,共转移15
4 4
mol 电子,错误;D项,Na FeO 处理水时,Na FeO 可以氧化杀死微生物,生成的还
2 4 2 4
原产物氢氧化铁又具有吸附作用,可以起到净水的作用,正确。
答案 C
13.环保督察不是“一阵风”,环保部对大气污染、水体污染等高度重视。氰化物是
污染水体的重要物质,该类物质剧毒,特别是HCN具有挥发性,毒害更大。一般可
采用次氯酸钠法进行处理,该处理方法的原理可分两步:
步骤①:NaCN与NaClO反应,生成NaOCN和NaCl;
步骤②:NaOCN与NaClO反应,生成Na CO 、CO 、NaCl和N 。
2 3 2 2
下列有关判断正确的是( )
A.NaCN与NaOCN中C、N的化合价分别相等
B.步骤①可在酸性条件下进行
C.步骤②的氧化产物是CO 、Na CO 、N
2 2 3 2
D.步骤②生成标准状况下5.6 L气体时,转移0.75 mol 电子
解析 NaCN与NaOCN中Na的化合价均为+1,NaOCN中含有O,O的化合价不
是0,故该两种化合物中C、N的化合价至少有一种不相等,A项错误;HCN易挥
发且有毒,而酸性条件下CN-易与H+结合生成HCN,故不能在酸性条件下进行
步骤①,B项错误;步骤②的离子方程式为2OCN-+3ClO-===CO ↑+CO+3Cl-
2
+N ↑,氧化剂是NaClO,还原剂是NaOCN,氧化产物只有N ,还原产物是NaCl,
2 2
C项错误;根据离子方程式可知,生成1 mol N 转移的电子的物质的量为6 mol,
2
N 的体积占气体总体积的,生成标准状况下5.6 L气体时,n(e-)=6××=0.75
2
mol,D项正确。答案 D
14.(原创题)2018年5月15日是我国第25个“防治碘缺乏病日”。关于“食盐加
碘”的问题一直以来被广大医疗专家、沿海居民热议,在社会上引起广泛关注。某
地市场销售的某种食用精制盐配料为食盐、碘酸钾、抗结剂,某学生为了测定其中
的碘含量,设计步骤如下:
a.准确称取 g食盐,加适量蒸馏水使其完全溶解;
w
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO 与KI反应完全;
3
c.以淀粉溶液为指示剂,逐渐加入物质的量浓度为2.0×10-3mol/L的Na S O 溶液
2 2 3
10.0 mL,恰好反应完全。
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数
填于空白处):
________KIO +________KI+________H SO ===________K SO +________I +
3 2 4 2 4 2
________H O
2
(2)向碘的四氯化碳溶液中加入足量Na SO 稀溶液,将I 还原,以回收四氯化碳。
2 3 2
Na SO 稀 溶 液 与 I 反 应 的 离 子 方 程 式 是
2 3 2
_____________________________________________________________________。
(3)①上述c反应常用于定量测定碘的含量。I 与Na S O 溶液反应的离子方程式
2 2 2 3
是_________________________________________________________。
② 判 断 c 中 反 应 恰 好 完 全 所 依 据 的 现 象 是
____________________________________________________________________。
③b中反应所产生的I 的物质的量是________mol。
2
解析 (1)KIO 中I元素的化合价由+5价降低为0价,KIO 为氧化剂,KI中I元素
3 3
的化合价由-1价升高到0价,KI为还原剂,由得失电子守恒及质量守恒定律可
知,反应方程式为KIO +5KI+3H SO ===3K SO +3I +3H O。
3 2 4 2 4 2 2
(2)Na SO 稀溶液与I 反应,Na SO 具有还原性,被氧化为Na SO ,I 具有氧化性,
2 3 2 2 3 2 4 2
被还原为I-,结合反应的电荷守恒和原子守恒写出并配平离子方程式:I +SO+
2
H O===2I-+SO+2H+。(3)碘遇淀粉变蓝色,所以溶液呈蓝色,随反应 I +
2 2
2S O===2I-+S O的进行,溶液中I 完全转化为I-,溶液由蓝色变为无色,说明反
2 4 2
应到达终点,判断c中反应恰好完全所依据的现象是滴最后一滴溶液,由蓝色恰好变为无色,且半分钟内不变色。根据反应I +2S O===2I-+S O可得:
2 2 4
n(I )=n(S O)==1.0×10-5mol。
2 2
答案 (1)1 5 3 3 3 3
(2)I +SO+H O===2I-+SO+2H+
2 2
(3)①I +2S O===2I-+S O ②滴最后一滴溶液,由蓝色恰好变为无色,且半分钟
2 2 4
内不变色 ③1.0×10-5